Identification des attributs de qualité critiques dans les produits pharmaceutiques : la clé pour garantir des traitements sûrs et efficaces
Dans la fabrication de médicaments, aucune erreur n'est tolérée. Chaque décision, de la formulation initiale à la mise sur le marché, doit garantir que le produit est sûr, efficace et homogène.
Au cœur de ce processus se trouvent les attributs de qualité critiques (CQA), ces propriétés mesurables qui déterminent si un médicament répond aux normes requises.
Dans cet article, nous analysons le rôle des CQA dans le développement des produits biologiques et expliquons comment l'analyse avancée des particules permet d'obtenir des informations plus approfondies, de prendre des décisions plus tôt et d'assurer une continuité du développement jusqu'au contrôle qualité.
Que sont les attributs de qualité essentiels ?
Un paramètre de qualité (CQA) désigne toute propriété physique, chimique, biologique ou microbiologique qui doit rester dans une fourchette définie afin de garantir la qualité du produit.
Les CQA se répartissent généralement en trois catégories :
- Caractéristiques physiques :elles comprennent des aspects tels que la taille et la forme du produit pharmaceutique.
- Propriétés chimiques :elles englobent des éléments tels que le niveau de pH et la concentration du médicament.
- Attributs biologiques :il s'agit de facteurs tels que la stérilité et les niveaux de charge microbienne dans le produit.
Le processus d'identification des CQA est une étape essentielle dans le processus de développement d'un médicament, car il garantit que le produit final est cohérent, efficace et sûr pour les patients.2 Toutécart peut influencer l'efficacité d'un médicament et potentiellement entraîner des effets néfastes pour le patient.
De plus, la reconnaissance des CQA n'est pas seulement une bonne pratique, c'est une obligation réglementaire. Les autorités réglementaires, notamment la FDA et l'Agence européenne des médicaments (EMA), exigent l'identification des CQA dans le cadre du processus de développement des médicaments.3 Celagarantit que les médicaments répondent aux normes de qualité requises et peuvent être consommés en toute sécurité.4
Critères de qualité (CQA) et « Quality by Design »
Les CQA constituent le fondement du « Quality by Design » (QbD), un cadre qui met l'accent sur l'intégration de la qualité dans un produit dès le début, plutôt que sur des tests de contrôle à la fin.
Le QbD repose sur une compréhension approfondie des processus, l'identification des facteurs de risque et des stratégies de contrôle directement liées aux CQA. Dans la pratique, cela signifie que les CQA doivent être mesurés avec précision et cohérence à chaque étape du développement, et pas seulement au moment de la mise sur le marché.
Le défi : les particules invisibles à l'œil nu, un paramètre de qualité critique
L'un des critères de qualité critiques (CQA) les plus complexes dans le domaine des produits biologiques concerne les particules invisibles à l'œil nu.
Ces particules ont souvent une taille supérieure ou égale à 10 µm et peuvent :
- Réduire la stabilité et raccourcir la durée de conservation
- Provoquer des réactions immunitaires ou des effets indésirables
Because of this, they are closely monitored throughout development and in QC environments. Subvisible particle analysis is also central to meeting compendial requirements, such as USP <788> and USP <789>, which define limits for particulate matter in injectable drug products and set expectations for particle counting and size classification.
Malgré leur importance, les méthodes traditionnelles ont du mal à fournir des informations exploitables, en particulier lors des premières phases de développement et lorsque les volumes sont faibles. Il en résulte une lacune dans le flux de travail, avec une visibilité limitée sur le développement, des méthodes différentes requises pour le contrôle qualité et des ensembles de données disjoints tout au long du cycle de vie du produit.
Combler le fossé grâce à l'analyse avancée des particules
Le site Aura Particle Analysis System comble cette lacune en permettant une caractérisation des particules en haute résolution, du développement au contrôle qualité, pour diverses thérapies, notamment les produits biologiques, les AAV, les LNP et les thérapies cellulaires.
Utilisation de Imagerie par membrane en arrière-plan (BMI) et la microscopie à membrane à fluorescence (FMM), Aura permet de déterminer avec précision le nombre de particules, leur distribution granulométrique, leur morphologie et leur identification.
Il est important de noter qu'Aura prend en charge les deux :
- Analyse de petits volumes à partir de seulement 5 µL pour les travaux préliminaires
- Des flux de travail à haut débit prenant en charge plus de 500 µL par échantillon afin de répondre aux exigences en matière de contrôle qualité
Cela permet aux équipes de générer plus tôt des données CQA pertinentes, d'appliquer une méthode unique à toutes les étapes et de constituer un ensemble de données continu, de la formulation jusqu'à la mise sur le marché.
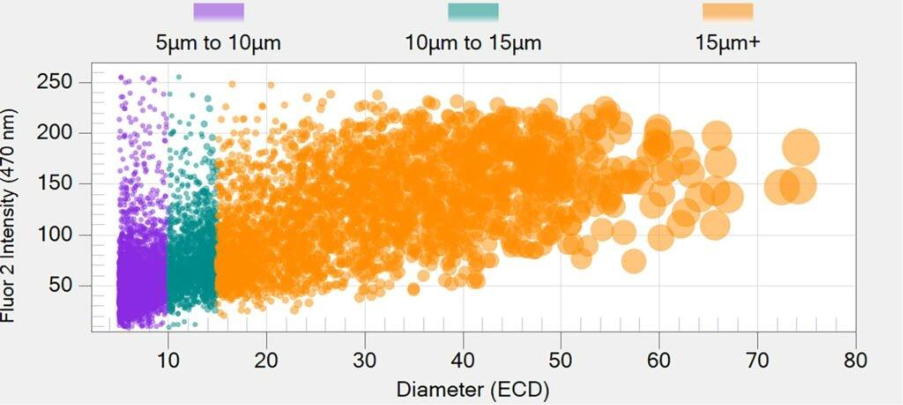
Une vision plus complète des CQA
En offrant une meilleure visibilité sur les particules submicroniques, l'un des critères de qualité critiques les plus complexes, le système Aura permet de détecter plus tôt les instabilités ou les agrégats, de mieux distinguer les différents types de particules et de prendre des décisions plus éclairées tout au long du processus de développement.
Au lieu de réagir tardivement aux défaillances du CQA, les équipes peuvent en tenir compte dès le début de la conception.
Conclusion
Les AQC constituent le fondement de la qualité des médicaments, mais leur utilité dépend de la manière dont elles sont comprises et maîtrisées.
À mesure que les produits biologiques gagnent en complexité, le besoin de technologies capables de fournir des informations précises, cohérentes et couvrant toutes les phases de développement ne cesse de croître.
Grâce à l'analyse avancée des particules, il est désormais possible de passer de processus de travail fragmentés à une vision unique et continue des critères de qualité critiques tout au long du processus de développement.
Références
- https://www.linkedin.com/pulse/benefits-identifying-critical-quality-attributes-cqas-mo-heidaran-2e/
- Département américain de la Santé et des Services sociaux, Administration des aliments et des médicaments, Centre d'évaluation et de recherche sur les médicaments (CDER). Lignes directrices à l'intention de l'industrie : Q8(R2) Développement pharmaceutique. Novembre 2009.
Sujets populaires
ACQUITY QDa (17) bioanalyse (12) produits biologiques (17) biopharmacie (50) produits biopharmaceutiques (59) biothérapies (24) étude de cas (20) chromatographie (14) intégrité des données (23) analyse alimentaire (12) HPLC (15) informatique (12) LC-MS (27) chromatographie en phase liquide (LC) (25) détection de masse (16) spectrométrie de masse (MS) (61) développement de méthodes (14) analyse des particules (21)


