识别药品中的关键质量属性:确保治疗安全有效的关键
在药品生产中,绝不容许出现任何差错。从早期配方研发到最终放行,每一个决策都必须确保产品安全、有效且质量稳定。
这一过程的核心是关键质量属性(CQAs),即用于判定药物是否符合规定标准的可量化特性。
在本篇博客中,我们将深入解析CQAs在生物制剂开发中的作用,以及先进的颗粒分析技术如何助力获得更深入的洞察、更早的决策,并确保从开发到质量控制(QC)的全流程连续性。
什么是关键质量属性?
关键质量属性(CQA)是指任何必须保持在规定范围内以确保产品质量的物理、化学、生物或微生物特性。
质量保证专员通常分为三类:
- 物理特性:包括药品的尺寸和形状等方面
- 化学性质:包括药物pH值和浓度等要素
- 生物学属性:涉及产品中的无菌性、生物负荷水平等因素
确定关键质量属性(CQAs)的过程是药物研发过程中至关重要的一步,它确保最终药物产品在患者使用时具有一致性、有效性和安全性。任何偏差都可能影响药物的疗效,进而对患者产生潜在危害。
此外,关键质量属性的确认不仅是最佳实践,更是法规强制要求。包括美国食品药品监督管理局(FDA)和欧洲药品管理局(EMA)在内的监管机构,均要求在药物研发过程中明确关键质量属性。³这确保了药品符合必要的质量标准且安全可供使用。⁴
关键质量属性(CQAs)与基于设计的质量(QbD)
关键质量属性(CQAs)是“基于设计的质量”(QbD)的基础。QbD 是一种强调从产品开发初期就将质量融入其中,而非在最终阶段通过检测来确保质量的框架。
QbD 依赖于对工艺的深入理解、风险因素的识别,以及与关键质量属性直接相关的控制策略。在实践中,这意味着关键质量属性必须在开发过程的每个阶段都得到准确、一致的测量,而不仅仅是在产品放行时。
挑战:亚可见颗粒作为关键质量属性
在生物制剂领域,亚可见颗粒是具有挑战性的关键质量属性之一。
这些颗粒的尺寸通常在≥10微米范围内,并且可能:
- 降低稳定性并缩短保质期
- 引发免疫反应或不良反应
Because of this, they are closely monitored throughout development and in QC environments. Subvisible particle analysis is also central to meeting compendial requirements, such as USP <788> and USP <789>, which define limits for particulate matter in injectable drug products and set expectations for particle counting and size classification.
尽管传统方法至关重要,但在提供可操作的洞察方面却举步维艰,尤其是在早期阶段和样本量较小的情况下。这导致工作流程中存在断层:研发环节的洞察有限,质量控制环节需要采用不同的方法,且产品生命周期各阶段的数据集之间缺乏关联。
借助先进的颗粒分析技术缩小差距
ǞǞǞ Aura Particle Analysis System 该技术通过实现从研发到质量控制阶段的高分辨率颗粒表征,弥补了这一空白,适用于多种疗法——包括生物制剂、腺相关病毒(AAV)、脂质纳米颗粒(LNP)和细胞疗法。
使用 背景膜成像(BMI) 以及荧光膜显微镜(FMM), Aura 可精确测定颗粒数量、粒径分布、形态及颗粒识别。
重要的是,Aura 同时支持以下两种:
- 仅需5 µL即可进行小样本分析,适用于早期研究
- 支持单样本超过 500 µL的大容量工作流程,以满足质量控制要求
这使团队能够更早地生成有价值的CQA数据,在各个阶段保持一致的方法,并从配方开发到产品放行构建一个连续的数据集。
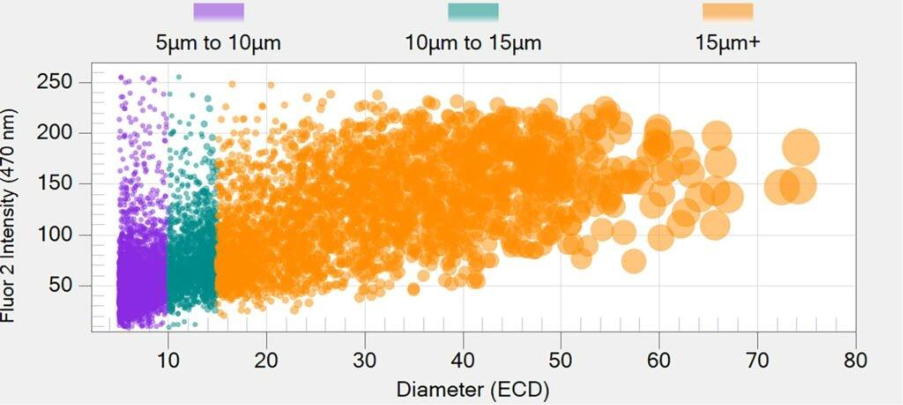
对关键质量属性(CQAs)的更全面认识
通过深入监测亚可见颗粒(这是最复杂的CQA之一),Aura系统能够更早地检测到不稳定性或聚集现象,更准确地区分不同类型的颗粒,并在整个开发过程中为决策提供更充分的信息依据。
团队不必等到CQA出现故障后再做出反应,而是可以从一开始就针对这些问题进行设计。
总结
关键质量属性(CQAs)是药品质量的基础,但其价值取决于对其理解和控制的程度。
随着生物制剂日益复杂,人们对能够提供准确、一致且贯穿各个研发阶段的洞察力的技术的需求也在不断增加。
借助先进的颗粒分析技术,如今我们能够摆脱分散的工作流程,在整个开发过程中对关键质量属性(CQAs)形成统一、连贯的认知。
参考文献
- https://www.linkedin.com/pulse/benefits-identifying-critical-quality-attributes-cqas-mo-heidaran-2e/
- 美国卫生与公众服务部,食品药品监督管理局,药品评价与研究中心(CDER)。《行业指南:Q8(R2) 药品研发》。2009年11月。


