Identificación de los atributos críticos de calidad en los medicamentos: la clave para garantizar terapias seguras y eficaces.
En la fabricación de medicamentos, no hay margen para el error. Cada decisión, desde la formulación inicial hasta la comercialización final, debe garantizar que el producto sea seguro, eficaz y homogéneo.
En el centro de este proceso se encuentran los atributos críticos de calidad (CQA), las propiedades cuantificables que determinan si un medicamento cumple con los estándares exigidos.
En este blog, analizamos el papel de los CQA en el desarrollo de productos biológicos y cómo el análisis avanzado de partículas permite obtener una visión más profunda, tomar decisiones en una fase más temprana y garantizar la continuidad desde el desarrollo hasta el control de calidad.
¿Qué son los atributos críticos de calidad?
Un CQA es cualquier propiedad física, química, biológica o microbiológica que debe mantenerse dentro de un rango definido para garantizar la calidad del producto.
Las CQA suelen clasificarse en tres categorías:
- Características físicas:incluyen aspectos como el tamaño y la forma del producto farmacéutico.
- Propiedades químicas:estas abarcan elementos como el nivel de pH y la concentración del fármaco.
- Atributos biológicos:estos incluyen factores como la esterilidad y los niveles de carga biológica en el producto.
El proceso de identificación de los CQA es un paso esencial en el proceso de desarrollo de fármacos, ya que garantiza que el producto farmacéutico final sea consistente, eficaz y seguro para su uso por parte de los pacientes.2 Cualquierdesviación puede influir en la eficacia de un fármaco, lo que podría provocar efectos nocivos para el paciente.
Además, el reconocimiento de los CQA no es solo una buena práctica, sino una obligación reglamentaria. Las autoridades reguladoras, entre ellas la FDA y la Agencia Europea de Medicamentos (EMA), exigen la identificación de los CQA como parte del proceso de desarrollo de medicamentos.³ Estogarantiza que los productos farmacéuticos cumplan con los estándares de calidad necesarios y sean seguros para el consumo.⁴
Atributos clave de calidad (CQA) y Calidad por Diseño
Los CQA son fundamentales para el «Quality by Design» (QbD), un marco que hace hincapié en integrar la calidad en un producto desde el principio, en lugar de comprobarla al final.
El QbD se basa en un profundo conocimiento de los procesos, la identificación de los factores de riesgo y estrategias de control directamente vinculadas a los CQA. En la práctica, esto significa que los CQA deben medirse de forma precisa y coherente en todas las fases del desarrollo, y no solo en el momento de la comercialización.
El reto: las partículas subvisibles como parámetro crítico de control de calidad
Uno de los parámetros de control de calidad más complejos en los productos biológicos son las partículas invisibles a simple vista.
Estas partículas suelen tener un tamaño de ≥10 µm y pueden:
- Reducir la estabilidad y acortar la vida útil
- Provocar respuestas inmunitarias o efectos adversos
Because of this, they are closely monitored throughout development and in QC environments. Subvisible particle analysis is also central to meeting compendial requirements, such as USP <788> and USP <789>, which define limits for particulate matter in injectable drug products and set expectations for particle counting and size classification.
A pesar de su importancia, los métodos tradicionales han tenido dificultades para proporcionar información útil, especialmente en las primeras fases del desarrollo y en condiciones de bajo volumen. Esto genera una brecha en el flujo de trabajo, con una visión limitada del desarrollo, la necesidad de utilizar diferentes métodos en el control de calidad y conjuntos de datos inconexos a lo largo del ciclo de vida del producto.
Reducir la brecha gracias al análisis avanzado de partículas
El Aura Particle Analysis System subsana esta carencia al permitir la caracterización de partículas en alta resolución, desde la fase de desarrollo hasta el control de calidad, en diversas terapias, entre las que se incluyen los productos biológicos, los vectores AAV, los LNP y las terapias celulares.
Uso de Imágenes de membrana en segundo plano (BMI) y la microscopía de membrana fluorescente (FMM), Aura proporciona datos precisos sobre el recuento de partículas, la distribución del tamaño, la morfología y la identificación de partículas.
Es importante destacar que Aura es compatible con ambas opciones:
- Análisis de pequeños volúmenes con tan solo 5 µL para trabajos en fase inicial
- Flujos de trabajo de gran volumen que admiten más de 500 µl por muestra para cumplir con los requisitos de control de calidad
Esto permite a los equipos generar datos de CQA significativos en una fase más temprana, mantener un único método en todas las etapas y crear un conjunto de datos continuo desde la formulación hasta la comercialización.
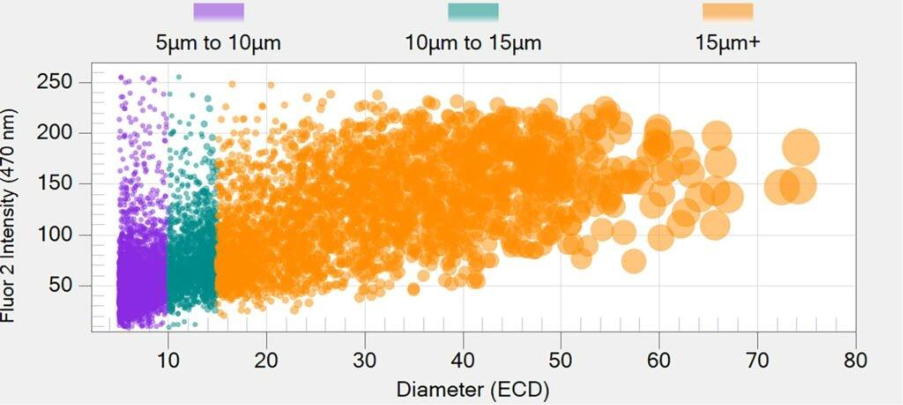
Una visión más completa de los CQA
Al ofrecer una mayor visibilidad de las partículas submicroscópicas —uno de los parámetros de control de calidad más complejos—, el sistema Aura permite detectar antes la inestabilidad o la agregación, diferenciar mejor entre los distintos tipos de partículas y tomar decisiones más fundamentadas a lo largo de todo el proceso de desarrollo.
En lugar de reaccionar tardíamente ante los fallos de CQA, los equipos pueden tenerlos en cuenta desde el principio.
Conclusión
Los CQA son la base de la calidad de los medicamentos, pero su valor depende de hasta qué punto se comprenden y controlan adecuadamente.
A medida que los productos biológicos se vuelven más complejos, sigue aumentando la necesidad de tecnologías capaces de proporcionar información precisa, coherente y que abarque todas las fases.
Gracias al análisis avanzado de partículas, ahora es posible pasar de flujos de trabajo fragmentados a una visión única y continua de los parámetros de control de calidad a lo largo de todo el proceso de desarrollo.
Referencias
- https://www.linkedin.com/pulse/benefits-identifying-critical-quality-attributes-cqas-mo-heidaran-2e/
- Departamento de Salud y Servicios Humanos de los Estados Unidos, Administración de Alimentos y Medicamentos, Centro para la Evaluación e Investigación de Medicamentos (CDER). Guía para la industria: Q8(R2) Desarrollo farmacéutico. Noviembre de 2009.
Temas populares
ACQUITY QDa (17) bioanálisis (12) productos biológicos (17) biofarmacia (50) biofarmacéutico (59) bioterapéuticos (24) estudio de caso (20) cromatografía (14) integridad de los datos (23) análisis de alimentos (12) HPLC (15) informática (12) LC-MS (27) cromatografía líquida (LC) (25) detección de masas (16) espectrometría de masas (MS) (61) desarrollo de métodos (14) análisis de partículas (21)


