Identification des attributs de qualité critiques dans les produits pharmaceutiques : la clé pour garantir des traitements sûrs et efficaces
Dans la fabrication de médicaments, il n'y a pas de place pour l'erreur. Chaque étape et chaque processus doivent être gérés avec soin afin de garantir que le produit final soit à la fois sûr et efficace. Les attributs qualitatifs critiques (CQA), qui constituent le fondement du contrôle qualité (CQ), jouent un rôle essentiel à cet égard.

Dans cet article, nous examinons ce que sont les attributs de qualité critiques, leur rôle essentiel dans le développement des médicaments, et nous soulignons comment notre technologie de pointe en matière d'analyse des particules contribue à l'identification et à l'analyse de ces attributs.
Comprendre les CQA des produits biologiques
Que sont les CQA ? Une CQA est une propriété physique, chimique, biologique ou microbiologique, ou une caractéristique clé, qui doit se situer dans une limite, une plage ou une distribution appropriée afin de garantir la qualité souhaitée du produit.1
Les CQA se répartissent généralement en trois catégories :
- Caractéristiques physiques :elles comprennent des aspects tels que la taille et la forme du produit pharmaceutique.
- Propriétés chimiques :elles englobent des éléments tels que le niveau de pH et la concentration du médicament.
- Attributs biologiques :il s'agit de facteurs tels que la stérilité et les niveaux de charge microbienne dans le produit.
Le processus d'identification des CQA est une étape essentielle dans le processus de développement d'un médicament, car il garantit que le produit final est cohérent, efficace et sûr pour les patients.2 Toutécart peut influencer l'efficacité d'un médicament et potentiellement entraîner des effets néfastes pour le patient.
De plus, la reconnaissance des CQA n'est pas seulement une bonne pratique, c'est une obligation réglementaire. Les autorités réglementaires, notamment la FDA et l'Agence européenne des médicaments (EMA), exigent l'identification des CQA dans le cadre du processus de développement des médicaments.3 Celagarantit que les médicaments répondent aux normes de qualité requises et peuvent être consommés en toute sécurité.4
Le rôle des CQA dans la qualité par la conception (QbD)
Les CQA sont au cœur de l'approche QbD dans le développement pharmaceutique. La QbD est une stratégie qui commence par des objectifs prédéfinis et met l'accent sur la compréhension des produits et des processus basée sur les connaissances scientifiques et la gestion des risques liés à la qualité. En substance, les CQA jouent un rôle essentiel dans la mise en œuvre réussie d'une approche QbD. Elles contribuent à garantir que le produit pharmaceutique final est à la fois inoffensif et efficace pour les patients, et qu'il satisfait aux normes de qualité requises par les organismes de réglementation.
L'impact de la technologie d'analyse des particules dans l'identification des CQA
Dans l'industrie pharmaceutique, la technologie est devenue un outil puissant pour détecter et analyser les CQA dans les produits pharmaceutiques. L'une des CQA importantes dans les produits pharmaceutiques qui a toujours posé des défis est l'identification précise des particules subvisibles. D'une taille d'environ 10 µm, la présence de ces particules peut avoir des conséquences désastreuses, allant du raccourcissement de la durée de conservation d'un produit pharmaceutique à l'obstruction des capillaires, en passant par des réactions immunitaires potentiellement mortelles.
Les méthodes traditionnelles d'analyse des particules invisibles ont eu du mal à identifier ces particules avec précision, laissant les particules invisibles non contrôlées et la sécurité des patients en danger. Cependant, grâce à la Aura Particle Analysis Système, ce casse-tête est en passe de devenir rapidement une chose du passé.
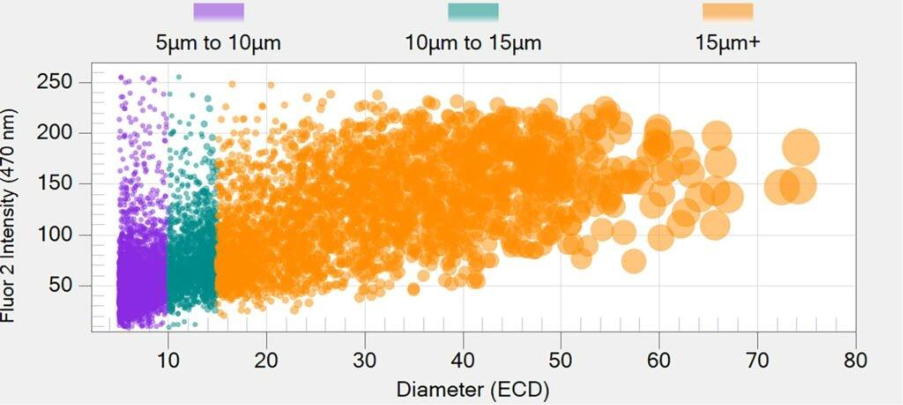
La plateforme Aura utilise une imagerie haute résolution entièrement automatisée pour obtenir des images détaillées des particules présentes dans un échantillon. Elle permet la détection et la quantification de particules subvisibles de 1 à 100 µm, qui sont des CQA dans divers produits biologiques tels que les vaccins, les thérapies géniques et les anticorps monoclonaux (mAbs).
En utilisant des technologies telles que Backgrounded Membrane Imaging (BMI) et Microscopie à membrane fluorescente (FMM)Les systèmes Aura révèlent des données essentielles sur les particules invisibles, notamment leur nombre, leur taille et leur identification. Cela permet d'obtenir des résultats plus précis et une meilleure compréhension du produit pharmaceutique.
Conclusion
Comprendre et surveiller les CQA des produits pharmaceutiques n'est pas seulement un aspect bénéfique de la fabrication pharmaceutique, c'est une nécessité. Ce processus clé garantit que le produit pharmaceutique final dépasse les exigences de base en matière d'efficacité et assure les normes les plus élevées de sécurité et de qualité pour les patients.
À mesure que la technologie continue de progresser, des outils tels que la technologie révolutionnaire d'analyse des particules de Waters joueront un rôle de plus en plus important dans l'identification et l'analyse de ces attributs essentiels.
Références
- https://www.linkedin.com/pulse/benefits-identifying-critical-quality-attributes-cqas-mo-heidaran-2e/
- Département américain de la Santé et des Services sociaux, Administration des aliments et des médicaments, Centre d'évaluation et de recherche sur les médicaments (CDER). Lignes directrices à l'intention de l'industrie : Q8(R2) Développement pharmaceutique. Novembre 2009.
Sujets populaires
ACQUITY QDa (17) bioanalyse (12) produits biologiques (17) biopharmacie (49) biopharmaceutique (58) biothérapeutiques (21) étude de cas (18) chromatographie (14) conformité (12) intégrité des données (23) analyse alimentaire (12) HPLC (15) LC-MS (26) chromatographie liquide (LC) (24) détection de masse (16) spectrométrie de masse (MS) (58) développement de méthodes (13) analyse des particules (19)


