Obtenir la bonne formulation de nanoparticules lipidiques pour garantir une administration efficace du médicament
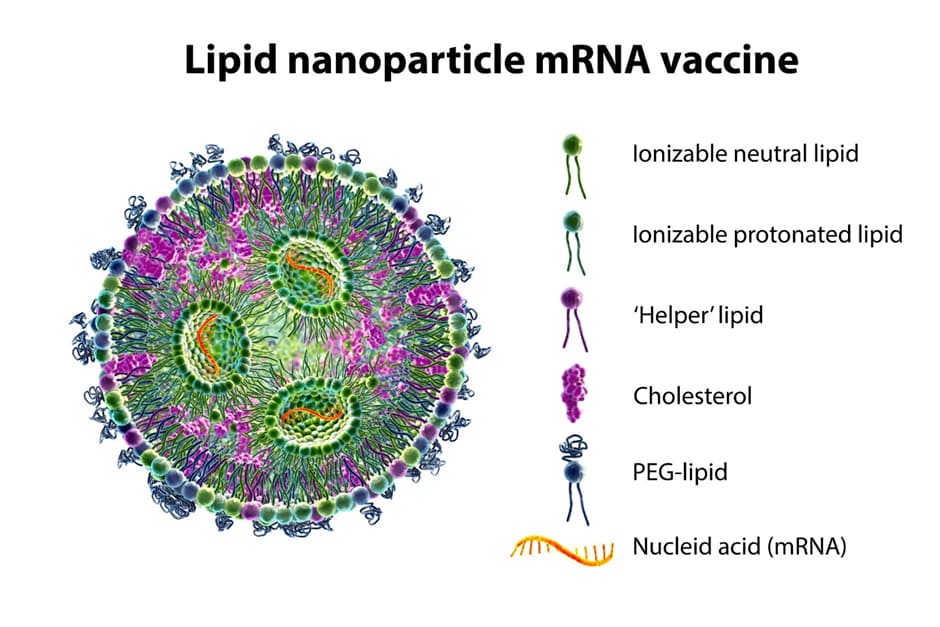
Dans la lutte contre la COVID-19, une technologie a discrètement transformé la manière dont nous combattons ce virus mortel : les nanoparticules lipidiques (LNP).
Ces minuscules vésicules constituent un vecteur idéal pour le matériel génétique, qu'elles encapsulent et transportent directement dans nos cellules. Elles agissent comme un bouclier pour l'ARNm, le protégeant de la dégradation dans l'organisme tout en assurant son acheminement vers le bon endroit dans nos cellules.

Dans le contexte des vaccins contre la COVID-19, l'ARNm transporté par les LNP ordonne à nos cellules de produire la protéine Spike présente sur le virus SARS-CoV-2. Ce processus déclenche une réponse immunitaire sans provoquer de maladie, préparant ainsi notre organisme à combattre le virus réel s'il venait à se présenter.
Cette utilisation innovante des formulations LNP a joué un rôle déterminant dans le développement des vaccins à ARNm contre la COVID-19 par Moderna et Pfizer. Les raisons de leur popularité sont claires :
- Ils encapsulent le matériel génétique dans des vésicules lipidiques de taille inférieure au micromètre.
- Ils peuvent transporter d'importantes charges utiles biologiques.
- Ils présentent une faible immunogénicité, ce qui réduit le risque de réactions immunitaires indésirables.
- Ils sont compatibles avec les processus de fabrication à grande échelle, ce qui permet une production rapide de vaccins.
Cependant, comme tous les produits biologiques, les formulations LNP peuvent être physiquement instables, s'agglomérer et former subvisible particles (SVPs). Par conséquent, une formulation et une évaluation adéquates du LNP sont nécessaires pour garantir sa stabilité physique et chimique.
La stabilité des LNP fait référence à la capacité des nanoparticules à base de lipides à conserver leur intégrité structurelle et à empêcher leur dégradation ou leur agrégation au fil du temps. Ces nanoparticules, composées de lipides tels que des phospholipides et du cholestérol, sont largement utilisées dans divers domaines, notamment l'administration de médicaments, la thérapie génique et le diagnostic. Il est essentiel d'assurer la stabilité des LNP afin de garantir leur efficacité et leur sécurité dans ces applications. La stabilité des LNP peut être influencée par des facteurs tels que la composition lipidique, la taille des particules, la charge superficielle et les conditions environnementales. Les chercheurs étudient en permanence de nouvelles stratégies pour améliorer la stabilité, notamment l'utilisation d'agents stabilisants, l'optimisation des paramètres de formulation et les techniques de modification de surface. Il est impératif de comprendre et d'améliorer la stabilité des LNP pour développer des nanomédicaments et des technologies biomédicales efficaces et fiables.
Redéfinir la formulation LNP : la puissance de l'imagerie membranaire en arrière-plan
Les tests USP 787 et USP 788 sur les particules subvisibles constituent un processus clé dans l'évaluation des formulations LNP. Cependant, la méthode 1 des tests USP 788, connue sous le nom d'obscurcissement lumineux (LO), est considérée comme inadaptée à la mesure de solutions complexes telles que les suspensions liposomales et colloïdales. Cette limitation résulte de l'incapacité du LO à traiter efficacement les matrices complexes. Par conséquent, l'USP 788 recommande la microscopie à membrane (méthode 2 de la pharmacopée) pour mesurer les formulations liposomales.
L'imagerie par membrane en arrière-plan (BMI), une forme contemporaine de microscopie membranaire, se distingue par son efficacité dans la caractérisation des particules subvisibles à haut débit et faible volume. Aura System utilise cette méthode, tirant parti des capacités du BMI pour une caractérisation complète et efficace des particules.
Comprendre les effets de la formulation LNP et du stress sur la stabilité du produit
Les facteurs de stress, notamment les variations de température, de pH et les forces mécaniques, peuvent avoir un impact significatif sur la stabilité des produits biopharmaceutiques, ce qui peut entraîner une agrégation des protéines et compromettre l'efficacité et la sécurité d'un produit.
Par exemple, un stress thermique important peut décomposer une formulation liposomale, augmentant ainsi la solubilité des LNP et réduisant par conséquent le nombre de particules insolubles capturées sur la membrane. À l'inverse, la congélation-décongélation produit davantage d'agrégats LNP insolubles, augmentant ainsi le nombre de particules subvisibles, comme le montre l'IMG, et présentant un comportement similaire à l'agrégation induite par la chaleur dans la plupart des formulations protéiques.
Dans un récent study, nous avons analysé deux échantillons de LNP, chacun formulé dans des tampons différents. Ces échantillons ont ensuite été soumis à des contraintes de température et de congélation-décongélation à l'aide de Système Aura GT et SYBR™ Gold Assay (ThermoFisher Scientific) pour aider à caractériser la fuite d'acide nucléique dans les échantillons LNP soumis à un stress et analyser quantitativement leur stabilité et leur pureté.
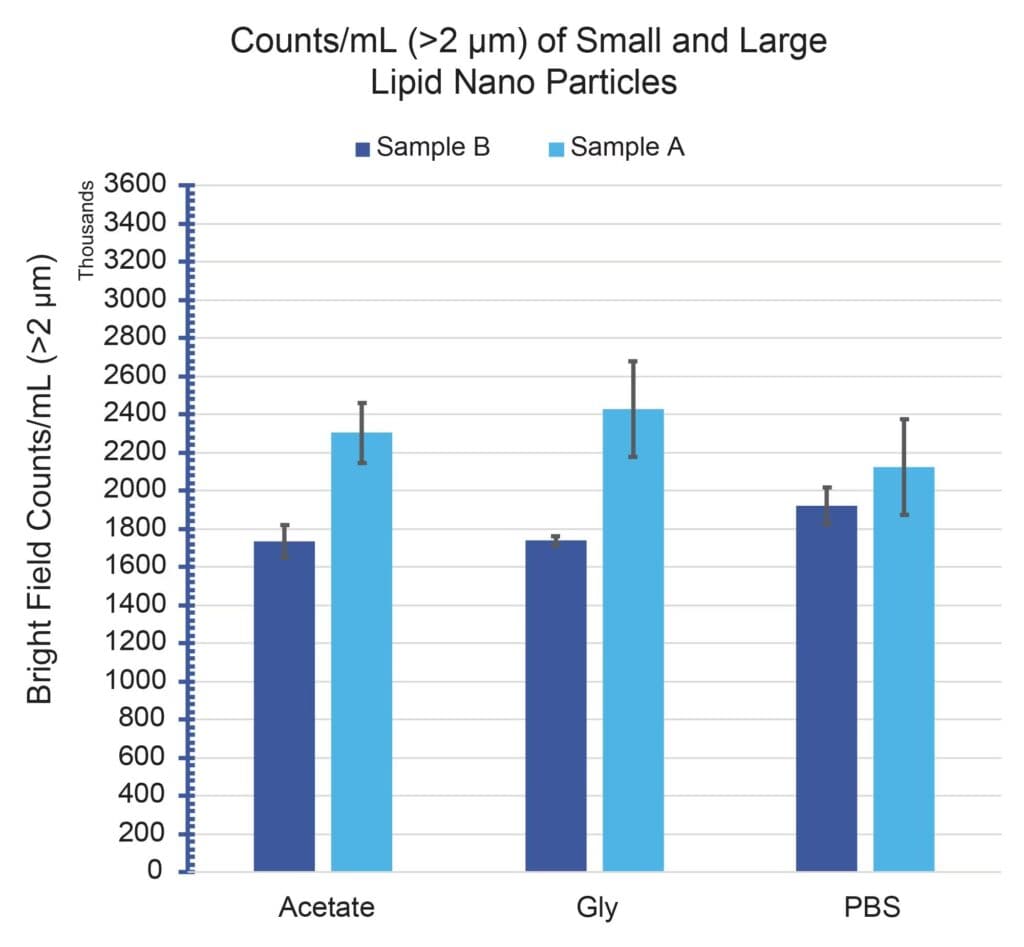
Figure 1 shows the >2 μm/mL subvisible particle concentrations for Sample A and Sample B formulated in three separate buffers: acetate, glycine and PBS. All particle measurements showed significant particle concentrations (>1.5E6/mL) across all conditions, with good repeatability (CVs <15%). In addition, both samples exhibited subvisible particle formation that remained consistent and did not vary beyond measurement uncertainty with buffer type.
Le lien entre la libération d'acide nucléique et la couverture des échantillons soumis à un stress
Il peut être difficile de prédire avec précision la qualité des médicaments LNP, même en utilisant des échantillons provenant de développeurs commerciaux renommés. Chaque formulation a son propre profil particulaire, et les formulations LNP ne font pas exception. Il s'agit d'un thème récurrent dans la stabilité des particules subvisibles.
En tirant parti du test SYBR Gold via la microscopie à membrane fluorescente (FMM), le système Aura GT résout ce problème en évaluant à la fois la stabilité et la pureté des échantillons dans le cadre de tests à haut débit et à faible volume, ce qui permet une caractérisation précise des LNP à un stade précoce, depuis le développement initial jusqu'à la mise sur le marché du produit final.
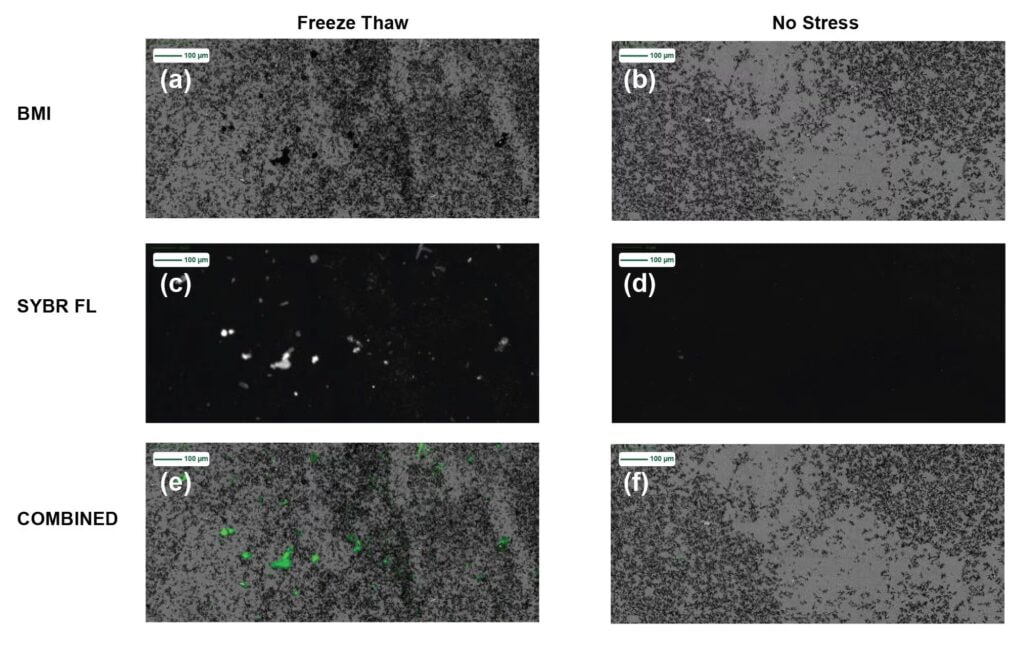
Dans la figure 2, nous examinons plus en détail les images des particules subvisibles pour l'échantillon A avant l'application d'une contrainte et après congélation-décongélation. Les images de la membrane après congélation-décongélation sont présentées dans trois modes d'imagerie : (2a) BMI, (2c) fluorescence SYBR Gold Assay et (2e) image combinée BMI et fluorescence SYBR Gold Assay, tandis que les images de l'échantillon non soumis à des contraintes sont présentées dans les modes (2b) BMI, (2d) fluorescence SYBR Gold Assay et (2f) image combinée BMI et fluorescence SYBR Gold Assay.
Les deux séries d'images de membrane BMI montrent une formation significative de particules invisibles à l'œil nu pour les types non stressés et stressés. Après coloration des échantillons non stressés et congelés-décongelés avec le test SYBR Gold, l'échantillon stressé présente des zones importantes de forte fluorescence au test SYBR Gold, indiquant la présence d'échantillons insolubles recouverts de matière nucléique, tandis qu'aucun signal de fluorescence n'est visible dans l'échantillon non stressé.
Importance d'une formulation LNP adéquate
Les cycles de congélation-décongélation peuvent augmenter considérablement la formation de particules subvisibles, tandis que le stress thermique peut réduire considérablement la concentration de particules subvisibles dans les deux échantillons. Comparé aux formulations protéiques, cet effet du stress thermique peut sembler inhabituel. Cependant, compte tenu de la composition des LNP et après avoir examiné de plus près la littérature, nous sommes en mesure de comprendre ce phénomène et de conclure qu'un stress thermique important peut décomposer une formulation liposomale, augmentant ainsi la solubilité des LNP et réduisant par conséquent le nombre de particules insolubles capturées sur la membrane.
D'autre part, la congélation-décongélation produit davantage d'agrégats insolubles, augmentant ainsi le nombre de particules subvisibles, comme le montre le BMI, et présentant un comportement similaire à l'agrégation des LNP induite par la chaleur dans la plupart des formulations protéiques. Un thème récurrent dans la stabilité des particules subvisibles est que chaque formulation présente son propre profil de particules, et les LNP ne font pas exception. Un autre point intéressant est que les LNP congelées-décongelées ont présenté une coloration SYBR Gold Assay significative, contrairement aux LNP non soumises à des contraintes, ce qui indique un comportement unique de fuite ou de rupture d'acide nucléique pour ce type de contrainte.
Conclusion
L'utilisation des LNP comme technologie d'administration de médicaments est un processus sophistiqué qui nécessite la meilleure formulation possible, associée à une évaluation minutieuse afin de garantir que leur efficacité ne soit pas compromise.
Les mesures de particules subvisibles à faible volume doivent être effectuées avec précision afin d'évaluer correctement la stabilité des LNP. Cependant, les méthodes traditionnelles peuvent ne pas vous offrir la précision, la rapidité ou la flexibilité dont vous avez besoin.
Aura GT Le système résout ces problèmes en fournissant une solution pour l'analyse des particules subvisibles des LNP, depuis leur conception initiale jusqu'à leur mise sur le marché.
Références
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9238147/
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8604799/
- https://www.nature.com/articles/s41422-022-00647-5
- https://www.waters.com/nextgen/global/library/application-notes/2025/accurate-particles-characterization-in-lipid-nanoparticle-therapies.html
- https://www.sciencedirect.com/science/article/abs/pii/S0022354921005001
Sujets populaires
ACQUITY QDa (17) bioanalyse (12) produits biologiques (17) biopharmacie (50) produits biopharmaceutiques (58) biothérapies (21) étude de cas (18) chromatographie (14) conformité (12) intégrité des données (23) analyse alimentaire (12) HPLC (15) LC-MS (26) chromatographie en phase liquide (LC) (24) détection de masse (16) spectrométrie de masse (MS) (58) développement de méthodes (13) analyse des particules (19)


