Obtenga la formulación adecuada de nanopartículas lipídicas para garantizar una administración eficaz del fármaco.
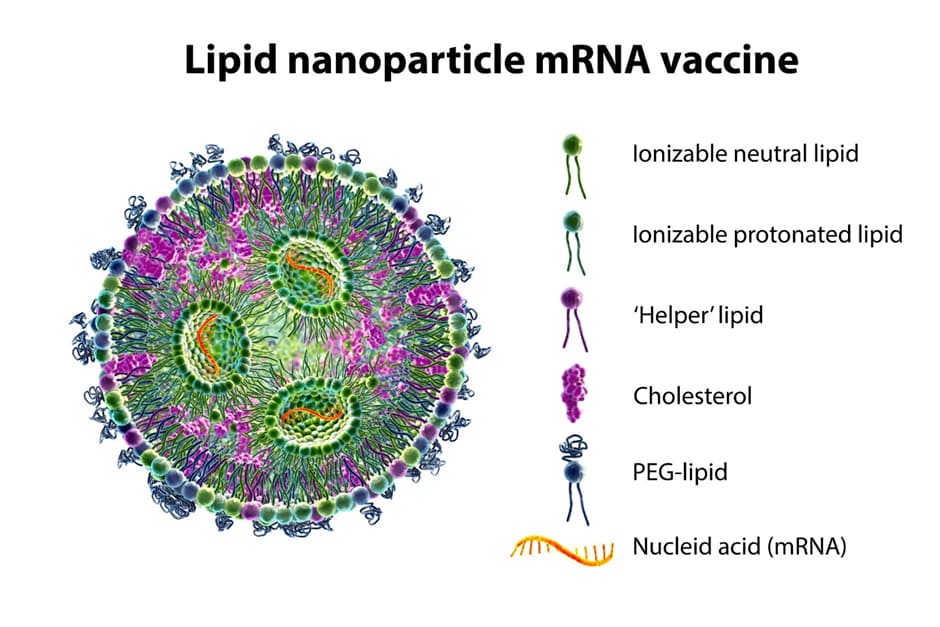
En la lucha contra la COVID-19, una tecnología ha transformado silenciosamente la forma en que combatimos este virus mortal: las nanopartículas lipídicas (LNP).
Estas diminutas vesículas sirven como vehículo ideal para el material genético, encapsulándolo y transportándolo directamente a nuestras células. Actúan como un escudo para el ARNm, protegiéndolo de la degradación en el organismo y garantizando su entrega en el lugar adecuado de nuestras células.

En el contexto de las vacunas contra la COVID-19, el ARNm transportado por las LNP instruye a nuestras células para que produzcan la proteína espicular que se encuentra en el virus SARS-CoV-2. Este proceso desencadena una respuesta inmunitaria sin causar la enfermedad, preparando así a nuestro organismo para combatir el virus real si se encuentra con él.
Este uso innovador de las formulaciones LNP ha sido fundamental en el desarrollo de las vacunas de ARNm contra la COVID-19 de Moderna y Pfizer. Las razones de su popularidad son evidentes:
- Encapsulan material genético dentro de vesículas lipídicas de tamaño submicrométrico.
- Pueden transportar grandes cargas biológicas.
- Presentan una baja inmunogenicidad, lo que reduce el riesgo de reacciones inmunitarias adversas.
- Son compatibles con procesos de fabricación a gran escala, lo que permite una rápida producción de vacunas.
Sin embargo, al igual que todos los productos biológicos, las formulaciones de LNP pueden ser físicamente inestables, agregarse y formar subvisible particles (SVPs). Como resultado, se requiere una formulación y evaluación adecuadas de la LNP tanto para la estabilidad física como química.
La estabilidad de las LNP se refiere a la capacidad de las nanopartículas basadas en lípidos para mantener su integridad estructural y evitar la degradación o la agregación de las LNP con el paso del tiempo. Estas nanopartículas, compuestas por lípidos como fosfolípidos y colesterol, se utilizan ampliamente en diversos campos, como la administración de fármacos, la terapia génica y el diagnóstico. Lograr la estabilidad de las LNP es fundamental para garantizar su rendimiento eficiente y seguro en estas aplicaciones. La estabilidad de las LNP puede verse influida por factores como la composición lipídica, el tamaño de las partículas, la carga superficial y las condiciones ambientales. Los investigadores estudian constantemente nuevas estrategias para mejorar la estabilidad, como el uso de agentes estabilizadores, la optimización de los parámetros de formulación y las técnicas de modificación de la superficie. Comprender y mejorar la estabilidad de las LNP es imprescindible para el desarrollo de nanomedicamentos y tecnologías biomédicas eficaces y fiables.
Redefiniendo la formulación LNP: el poder de la imagen de membrana en segundo plano
Las pruebas de partículas subvisibles USP 787 y USP 788 son un proceso clave en la evaluación de las formulaciones de LNP. Sin embargo, el método 1 de las pruebas USP 788, conocido como oscurecimiento de la luz (LO), se considera inadecuado para medir soluciones complejas, como suspensiones liposomales y coloidales. Esta limitación se debe a la incapacidad del LO para manejar matrices complejas de manera eficaz. Por lo tanto, la USP 788 recomienda el microscopio de membrana (método 2 de la farmacopea) para medir las formulaciones liposomales.
La imagen de membrana con fondo (BMI), una forma contemporánea de microscopía de membrana, destaca por su eficacia en la caracterización de partículas subvisibles con alto rendimiento y bajo volumen. Aura System utiliza este método, aprovechando las capacidades del BMI para la caracterización completa y eficiente de partículas.
Comprensión de los efectos de la formulación de LNP y el estrés sobre la estabilidad del producto
Los factores de estrés, incluidos los cambios de temperatura, pH y fuerzas mecánicas, pueden afectar significativamente a la estabilidad de los productos biofarmacéuticos, lo que puede provocar la agregación de proteínas y comprometer la eficacia y la seguridad de un producto.
Por ejemplo, un estrés térmico significativo puede descomponer una formulación liposomal, aumentando la solubilidad de las LNP y, por lo tanto, reduciendo la cantidad de partículas insolubles capturadas en la membrana. Por el contrario, la congelación-descongelación produce más agregados de LNP insolubles, lo que aumenta el recuento subvisible, como se muestra en el IMC, y presenta un comportamiento similar al de la agregación inducida por el calor en la mayoría de las formulaciones proteicas.
En un reciente study, analizamos dos muestras de LNP, cada una formulada en diferentes tampones. A continuación, estas muestras se sometieron a estrés térmico y de congelación-descongelación utilizando Sistema Aura GT y SYBR™ Gold Assay (ThermoFisher Scientific) para ayudar a caracterizar el escape de ácido nucleico en muestras de LNP sometidas a estrés y analizar cuantitativamente su estabilidad y pureza.
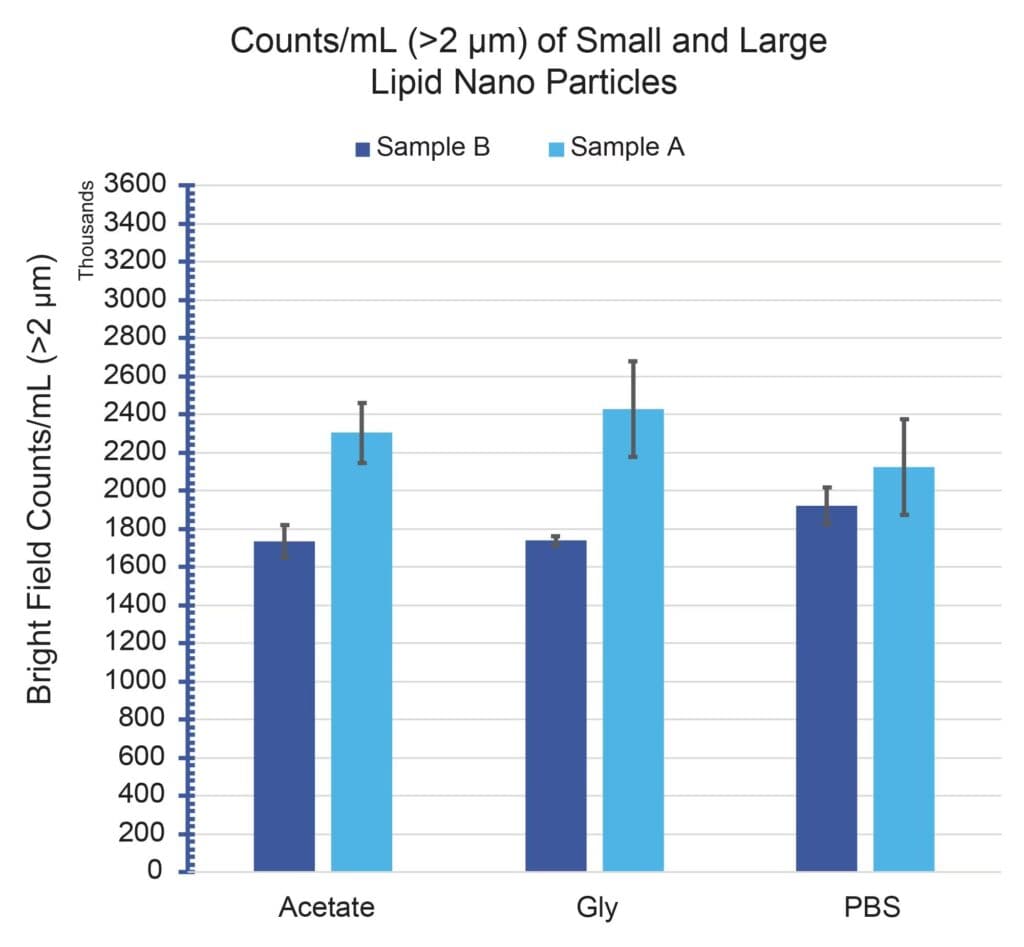
Figure 1 shows the >2 μm/mL subvisible particle concentrations for Sample A and Sample B formulated in three separate buffers: acetate, glycine and PBS. All particle measurements showed significant particle concentrations (>1.5E6/mL) across all conditions, with good repeatability (CVs <15%). In addition, both samples exhibited subvisible particle formation that remained consistent and did not vary beyond measurement uncertainty with buffer type.
La relación entre la liberación de ácido nucleico y la cobertura de muestras sometidas a estrés
Puede resultar difícil predecir con precisión la calidad de los fármacos LNP, incluso cuando se utilizan muestras de desarrolladores comerciales conocidos. Cada formulación tiene su propio perfil de partículas, y las formulaciones LNP no son una excepción. Este es un tema común en la estabilidad de las partículas subvisibles.
Aprovechando el ensayo SYBR Gold mediante microscopía de membrana fluorescente (FMM), el sistema Aura GT resuelve este problema evaluando tanto la estabilidad como la pureza de las muestras en pruebas de alto rendimiento y bajo volumen, lo que permite una caracterización precisa de las LNP en etapas más tempranas, desde el desarrollo inicial hasta el lanzamiento final del producto.
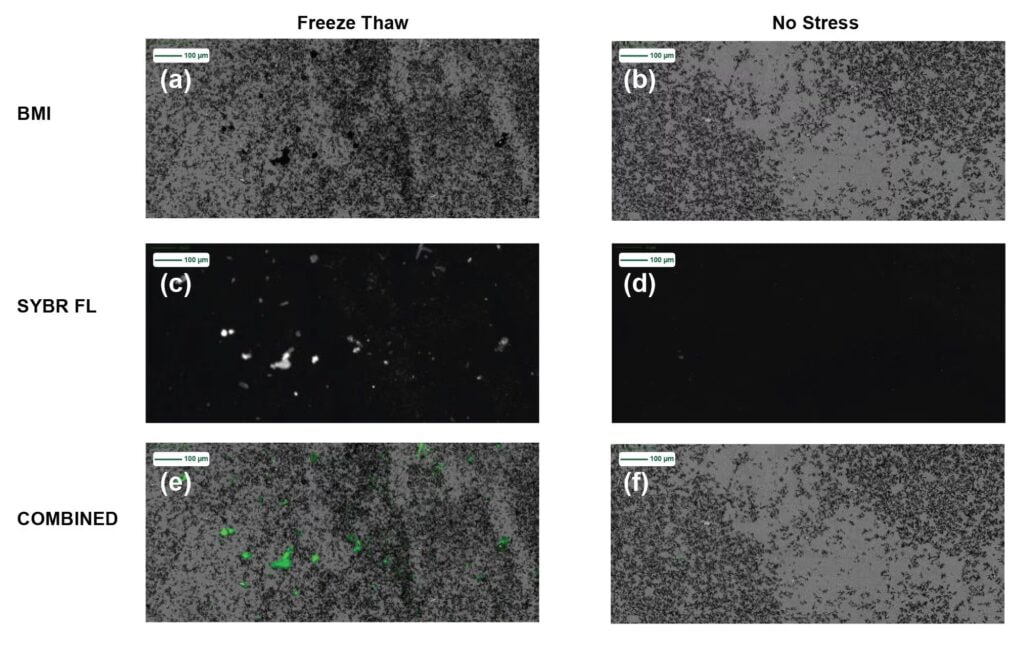
En la figura 2, analizamos más detenidamente las imágenes de partículas subvisibles de la muestra A antes de aplicar tensión y después de la congelación-descongelación. Las imágenes de la membrana descongelada se muestran en tres modos de imagen: (2a) BMI, (2c) fluorescencia del ensayo SYBR Gold y (2e) imagen combinada de BMI y fluorescencia del ensayo SYBR Gold, mientras que las imágenes de la muestra sin tensión se muestran en (2b) BMI, (2d) fluorescencia del ensayo SYBR Gold y (2f) imágenes combinadas de BMI y fluorescencia del ensayo SYBR Gold.
Ambos conjuntos de imágenes de membrana BMI muestran una formación significativa de partículas subvisibles para los tipos sin estrés y con estrés. Tras teñir tanto las muestras sin estrés como las congeladas y descongeladas con SYBR Gold Assay, la muestra con estrés muestra áreas significativas con una fuerte fluorescencia SYBR Gold Assay, lo que indica muestras insolubles recubiertas de material de ácido nucleico, mientras que en la muestra sin estrés no se aprecia ninguna señal de fluorescencia.
Importancia de una formulación adecuada de LNP
Los ciclos de congelación-descongelación pueden aumentar significativamente la formación de partículas subvisibles, mientras que el estrés térmico puede reducir significativamente la concentración de partículas subvisibles en ambas muestras. En comparación con las formulaciones proteicas, este efecto del estrés térmico puede parecer poco convencional. Sin embargo, teniendo en cuenta la composición de las LNP y tras examinar más detenidamente la bibliografía, podemos comprender este fenómeno y concluir que un estrés térmico significativo puede descomponer una formulación liposomal, aumentando la solubilidad de las LNP y, por lo tanto, dando lugar a menos partículas insolubles capturadas en la membrana.
Por otro lado, la congelación-descongelación produce más agregados insolubles, lo que aumenta los recuentos subvisibles, como se muestra en el BMI, y presenta un comportamiento similar al de la agregación de LNP inducida por el calor, como ocurre en la mayoría de las formulaciones proteicas. Un tema recurrente en la estabilidad de las partículas subvisibles es que cada formulación presenta su propio perfil de partículas, y las LNP no son una excepción. Otro dato interesante es que las LNP congeladas y descongeladas mostraron una tinción significativa en el ensayo SYBR Gold, mientras que las LNP sin estrés no lo hicieron, lo que indica un comportamiento único de fuga o ruptura del ácido nucleico para este tipo de estrés.
Conclusión
El uso de LNP como tecnología de administración de fármacos es un proceso sofisticado y requiere la mejor formulación, junto con una evaluación minuciosa para garantizar que su eficacia no se vea comprometida.
Las mediciones de partículas subvisibles de bajo volumen deben realizarse con precisión para evaluar adecuadamente la estabilidad de las LNP. Sin embargo, es posible que los métodos tradicionales no le proporcionen la precisión, la velocidad o la flexibilidad que necesita.
Aura GT El sistema resuelve estos retos, proporcionando una solución para el análisis de partículas subvisibles de LNP, desde la fase inicial hasta el lanzamiento del producto.
Referencias
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9238147/
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8604799/
- https://www.nature.com/articles/s41422-022-00647-5
- https://www.waters.com/nextgen/global/library/application-notes/2025/accurate-particles-characterization-in-lipid-nanoparticle-therapies.html
- https://www.sciencedirect.com/science/article/abs/pii/S0022354921005001
Temas populares
ACQUITY QDa (17) bioanálisis (12) productos biológicos (17) biofarmacia (50) biofarmacéutico (58) bioterapéuticos (21) estudio de caso (18) cromatografía (14) cumplimiento normativo (12) integridad de los datos (23) análisis de alimentos (12) HPLC (15) LC-MS (26) cromatografía líquida (LC) (24) detección de masas (16) espectrometría de masas (MS) (58) desarrollo de métodos (13) análisis de partículas (19)


