Décrypter la contamination des cultures cellulaires – Une analyse approfondie
La contamination des cultures cellulaires est le cauchemar de tous les laboratoires. Elle peut être physique, chimique ou biologique, et aller de problèmes mineurs à des catastrophes.
Les solutions à la contamination vont du respect des bonnes pratiques de laboratoire au maintien de normes élevées de propreté et d'entretien des milieux de culture, en passant par des nettoyages efficaces et l'utilisation de technologies telles que Aura+ System détecter et caractériser les contaminants, et éventuellement la source de contamination et d'autres remèdes.
Cette analyse examinera l'importance du contrôle de la contamination, les types de contamination, les tests d'identification de la contamination particulaire et diverses méthodes de détection et de contrôle.
Aperçu de la culture cellulaire
La culture cellulaire, qui consiste à cultiver et à maintenir des cellules vivantes dans un environnement artificiel en laboratoire, est l'une des techniques les plus importantes en biologie cellulaire et moléculaire. Les cultures cellulaires permettent aux chercheurs de découvrir la biologie, la chimie, la physiologie et les processus métaboliques des cellules sauvages, malades et modifiées.
Les cellules cancéreuses immortelles ont permis aux chercheurs de comprendre comment le cancer se développe (et peut être traité ou prévenu), et les cellules souches provenant de personnes atteintes de maladies héréditaires sont devenues des plateformes précieuses pour étudier les bases moléculaires de la maladie, le tout dans une boîte de Petri. Les cultures cellulaires sont également utilisées pour tester l'efficacité et la toxicité de nouveaux composés médicamenteux sur certaines cellules et sont indispensables pour développer des tissus régénératifs, des vaccins et des thérapies géniques et cellulaires.
Contrôle de la contamination des cultures cellulaires
Selon le contaminant en question, la Food and Drug Administration (FDA) et l'American Type Cell Collection (ATCC)estiment que jusqu'à 30 % de toutes les cultures cellulaires sontcontaminées (au moins par des mycoplasmes).
Les conséquences de la contamination des cultures cellulaires comprennent des retards dans les expériences et la croissance cellulaire, des pertes financières liées à l'achat de nouvelles cellules, de milieux de culture, de sérums et de boîtes/récipients, ainsi que des coûts de main-d'œuvre liés à la nécessité de recommencer les expériences et de développer de nouvelles cultures.
Dans le domaine du développement de médicaments, les contaminants cachés peuvent altérer la croissance et le fonctionnement de vos cellules, ainsi que leur capacité à produire des thérapies biologiques et des vaccins. Ces produits sont souvent rendus inutilisables et ne respectent pas les réglementations et normes en matière de sécurité des médicaments.
Il n'est peut-être pas possible d'empêcher totalement la contamination des cultures cellulaires, mais les particules et les contaminants physiques peuvent être réduits au minimum grâce à la mise en place de stratégies et d'outils appropriés visant à prévenir les pertes de cultures, d'expériences et de production. Ce type de contaminant peut être considéré comme le plus préoccupant, car il peut mettre les patients en danger, voire entraîner leur décès.
For biotherapeutic production, USP <788> standards set biopharmaceutical lot release guidelines and the proper limits of subvisible particles of no more than 12 particles per ml at least 10 µm and no more than two particles per ml that are at least 25 µm. In biotherapeutics, these particles are usually protein or other molecular fragments. The Aura System est un outil précieux pour identifier et caractériser les particules invisibles à l'œil nu responsables de certaines contaminations des cultures cellulaires.
Évaluation des risques de contamination
Pour déterminer le risque de contamination de votre culture cellulaire, il est essentiel d'évaluer minutieusement les propriétés de votre culture. Ces propriétés sont intrinsèques (quels sérums et milieux utilisez-vous, et quelles sont les propriétés des cellules après modification génétique) et extrinsèques (quel est le risque d'infection par des agents pathogènes, d'autres particules protéiques, voire de contamination croisée par d'autres cellules cultivées (HeLa, par exemple)).
Certaines cultures présentent des risques plus élevés que d'autres :
- Risque réduit— utilisation de lignées cellulaires continues non humaines ou non primates, ou de lignées cellulaires continues humaines bien caractérisées.
- Risque moyen— utilisation de cellules mammifères mal caractérisées.
- Risque élevé— utilisation de cellules primaires provenant de tissus et/ou de sang humains ou primates. Les cellules à haut risque sont également celles qui contiennent des agents pathogènes endogènes.
Vous devrez également procéder à un examen approfondi de vos procédures de laboratoire afin de vous assurer que les bonnes pratiques de laboratoire (BPL) sont respectées, que des désinfectants appropriés sont utilisés régulièrement, que les cultures cellulaires sont inspectées afin de détecter toute infection/contamination éventuelle et que les outils appropriés permettant de détecter et de quantifier les agents invisibles ou subvisibles sont en place.
Types de contamination
La contamination peut provenir de nombreuses sources différentes. Pour la plupart des chercheurs et des développeurs, les bactéries et les champignons sont généralement les premiers contaminants qui viennent à l'esprit. D'autres types peuvent inclure les virus, les produits chimiques et les particules macromoléculaires.
- Contaminants microbiens: ils sont généralement clairement visibles, avec une turbidité rapide et des changements de couleur dans les milieux. Il s'agit notamment des bactéries, des champignons et des levures. D'autres intrus, tels que les mycoplasmes, ne sont pas aussi faciles à détecter.
- Les virussont parmi les contaminants les plus difficiles à détecter. Ils peuvent provenir du patient ou de l'animal hôte, et certaines lignées cellulaires issues de la biotechnologie contiennent des rétrovirus endogènes.
- Contamination chimique: contaminant non vivant, notamment les radicaux libres, les ions métalliques, les résidus de désinfectants et de détergents, ou les endotoxines bactériennes résiduelles. Pour les développeurs de produits biothérapeutiques et de vaccins, ces agents contaminants peuvent également inclure des fragments de protéines et d'autres molécules plus grosses qui accompagnent la fabrication de médicaments/vaccins à base de protéines et constituent un problème important pour les développeurs de produits biologiques.

Analyse de la contamination par des traces de produits chimiques et de métaux
En fonction du type de contamination et de la culture cellulaire utilisée, l'analyse de la contamination peut faire appel à plusieurs techniques et outils. Ces outils détectent, identifient et caractérisent la contamination et les matières étrangères présentes dans la culture cellulaire. Les outils d'analyse peuvent aller de l'inspection visuelle à la microscopie, en passant par la spectroscopie, l'analyse physique/chimique et l'analyse élémentaire. Une détection et une analyse rapides sont essentielles.
Alors que la microscopie (optique, à balayage laser confocal, électronique) peut fournir des informations sur la forme, la taille et les surfaces des contaminants, la spectroscopie et d'autres techniques microscopiques (microscopie électronique à balayage et spectroscopie à dispersion d'énergie par rayons X) permettent de déterminer la composition chimique d'un contaminant. La spectroscopie Raman, la microscopie à fluorescence, la spectroscopie optique et la spectroscopie ATR-FTIR fournissent la composition moléculaire des matières organiques, tandis que la spectroscopie à plasma inductif permet de détecter les métaux à l'état de traces.
Analyse de la contamination — Tests d'identification
Il peut être difficile de déterminer la contamination chimique et inorganique, car ces contaminants sont plus difficiles à détecter que les contaminants biologiques. Pour les tests d'identification, commencez par examiner les changements survenus dans le laboratoire plusieurs semaines avant l'apparition du problème, en particulier les changements au niveau des équipements, des fournitures, des solutions et des milieux. Réfléchissez avec le personnel du laboratoire et déterminez la meilleure direction à prendre pour poursuivre l'évaluation. Il est également important d'essayer de déterminer ce qui pourrait se produire, en particulier compte tenu des risques liés à votre culture cellulaire.
L'identification peut commencer par l'enregistrement de toute odeur ou saveur inhabituelle (le cas échéant), de tout problème de couleur ou de toute particule étrangère. Éliminez (si possible) les contaminants résultant d'un stockage ou d'une manipulation inappropriés, ou de matières premières de mauvaise qualité. Vous pouvez ensuite commencer à utiliser des outils permettant d'identifier un contaminant chimique, physique ou biologique.
Analyse de la contamination particulaire
Les particules, en particulier les particules subvisibles (2 à 100 µm), peuvent être courantes dans les injections et perfusions biopharmaceutiques et sont étroitement liées à l'immunogénicité, et donc à l'altération ou à l'échec du produit.
USP <788> and FDA standards and regulations establish lot release guidelines and limits for these particles. USP <788> describes two methods for particulate analysis—light obscuration and membrane microscopy. Membrane microscopy is recommended over light obscuration when working with complex, viscous and low-volume samples (a large proportion of biopharmaceutical drugs under development).
Une fois les particules microscopiques identifiées, vous pouvez alors isoler les phases particulaires des dépôts et agrégats de production et déterminer les sources des contaminants. Ces particules peuvent être des fragments de protéines, mais aussi des particules étrangères qui apparaissent sous forme de taches noires, des résidus chimiques provenant du nettoyage et de l'entretien, des particules visibles après dissolution, l'abrasion ou la corrosion métallique des tuyaux, pompes ou conteneurs, des particules provenant des équipements de traitement, des fragments de verre provenant du délaminage ou de la rupture, des minéraux ou divers plastiques, caoutchouc, silicone ou autres polymères.
Techniques d'analyse de la contamination
Le choix du meilleur analyseur de particules dépend des exigences spécifiques de l'application, telles que le type d'échantillon, la gamme de tailles et les objectifs d'analyse. Il n'existe pas de solution universelle. Cependant, les analyseurs de particules les plus courants utilisent souvent la diffraction laser, la diffusion dynamique de la lumière (DLS) ou des techniques basées sur la microscopie. The Aura Systems suite of analyzers peut fournir une analyse plus détaillée des particules que la DLS ou la microscopie pour les particules ≥ 1 µm, en proposant les techniques BMI et FMM pour détecter et caractériser davantage de particules, y compris les particules subvisibles qui, autrement, passeraient inaperçues.
Analyse granulométrique
Presque tous les produits biothérapeutiques contiennent des particules subvisibles (dont le diamètre est compris entre 2 et 100 µm). La propriété la plus importante des échantillons particulaires est la taille des particules, qui peut être cruciale pour la réussite de votre produit final. La plupart des particules varient en volume et en forme. Comprendre la distribution granulométrique de votre produit peut vous aider à faire des prévisions concernant sa fabricabilité, son efficacité, sa qualité, sa biodisponibilité et sa durée de conservation. La distribution granulométrique peut avoir un impact sur la porosité et la surface spécifique de votre produit thérapeutique : des tailles de particules inappropriées peuvent nuire à la production, au rendement et aux bénéfices.
Méthodes de détection
Diffraction laser— Également connue sous le nom de diffusion statique de la lumière laser, cette méthode mesure indirectement la taille en détectant les distributions d'intensité de la lumière laser diffusée par les particules. L'évaluation de la forme n'est pas possible (elle suppose que toutes les particules sont sphériques) et sa faible résolution et sensibilité constituent des inconvénients. Elle n'est pas aussi efficace dans les échantillons polydispersés.
Réaction en chaîne par polymérase (PCR)— Cette technique très répandue peut être utilisée pour déterminer les espèces de contaminants biologiques, tels que les mycoplasmes, les virus ou les bactéries.
DLS— Dans cette méthode, les particules passent devant une caméra et sont analysées en temps réel. La DLS permet d'examiner des millions de particules en quelques minutes et de fournir divers paramètres relatifs à leur taille et à leur forme. Actuellement, la DLS est la méthode la plus couramment utilisée pour l'analyse de la distribution granulométrique des particules biothérapeutiques.
Imagerie (microscopie, MEB)— Ici, les particules sont mesurées en comparant leur taille à une grille de lignes et en les comptant. Cependant, des millions de particules doivent être mesurées pour obtenir une analyse statistiquement valide. L'analyse automatisée des micrographies électroniques permet de surmonter cette difficulté. Cette méthode est utile pour les particules dont la taille est comprise entre 0,2 et 100 µm.
IMC/FMM—Backgrounded membrane imaging (BMI), combiné avec microscopie à membrane fluorescente (FMI), constituent la base du Système d'analyse des particules de l'aura. Le BMI, une technique d'imagerie à contraste élevé, permet d'obtenir des images claires des particules présentes dans un échantillon. Il ne nécessite que 5 µl d'échantillon et peut fournir des résultats en une minute. Le FMM marque les particules à l'aide de colorants fluorescents ou d'anticorps spécifiques, ce qui permet une identification simple et définitive.
Comparaison des méthodes
La microscopie(optique, électronique, diffraction des rayons X) permet de visualiser la taille et la forme des contaminants, mais peut ne pas être en mesure de détecter les particules invisibles à l'œil nu. La PCR est sensible, mais ne permet pas de détecter les fragments de protéines ou les contaminants chimiques/physiques. Le BMI, associé au FMM et à l'imagerie par membrane à éclairage latéral (SIMI), qui constituent la base du système Aura, permet de distinguer facilement, rapidement et précisément les particules dans les thérapies cellulaires, géniques et protéiques.
BMI— Apporte de la clarté aux risques liés à la formulation qui étaient auparavant difficiles à détecter. Cette technique trouve ses origines dans la microscopie membranaire, mais a considérablement évolué. Une image de fond de la membrane est d'abord prise avant que les échantillons ne soient filtrés et les particules capturées. La même membrane est à nouveau photographiée, avec les particules à sa surface. Ensuite, l'image de fond est soustraite afin d'éliminer la texture de fond et de révéler les particules.
FMM— Fonctionne avec BMI pour un niveau d'analyse inédit dans les autres systèmes d'analyse de particules. Marquez vos cibles avec des colorants fluorescents ou des anticorps spécifiques, soit sur la membrane elle-même, soit en solution. Commencez par imager les membranes avec BMI pour localiser les particules, puis utilisez FMM pour caractériser les particules elles-mêmes.
SIMI — Fonctionnede concert avec BMI et FMM en détectant la diffusion de la lumière, en particulier les particules à indice de réfraction élevé, y compris celles qui dépassent de la surface de la membrane. Les particules qui diffusent la lumière indiquent la présence de matières inorganiques dépassant de la membrane, telles que du verre ou du plastique. Les particules qui absorbent la lumière indiquent la présence de particules métalliques, telles que des résidusde DynabeadsTM, et d'huiles absorbantes qui dépassent également de la membrane.
Une étude de cas diagnostique
Récemment, les scientifiques de Waters ont utilisé le Aura+ System pour détecter et caractériser les particules à l'aide des méthodes BMI, FMM et SIMI, démontrant ainsi que le système Aura+ était supérieur aux autres méthodes pour distinguer les particules subvisibles dans les thérapies cellulaires. Cela est devenu encore plus important dans le développement thérapeutique à la lumière d'une récente publication par la FDA du formulaire 483 concernant la contamination des thérapies cellulaires Kymriah® par du bois, de la cellulose, du laiton et de l'acier, qui auraient pénétré dans les sacs de cryoconservation.
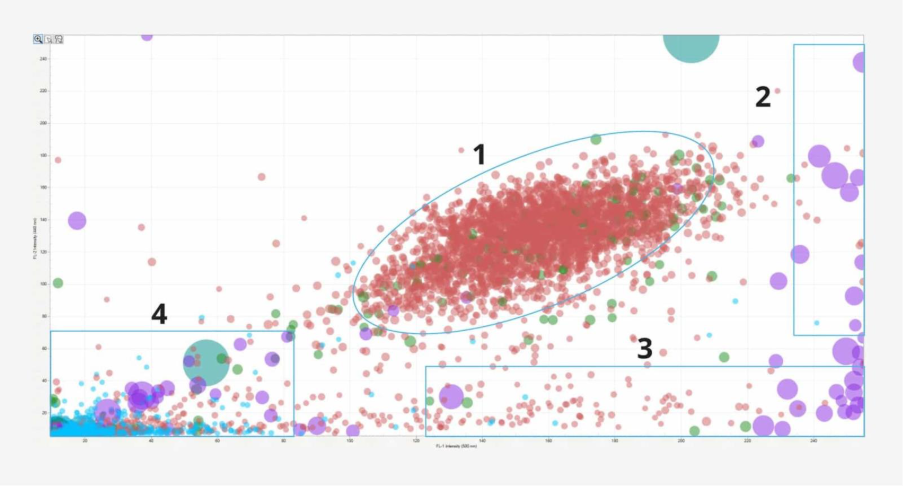
Les chercheurs ont mélangé des cellules Car-T avec des particules standard du NIST, de la cellulose et des particules métalliques. Les cellules Car-T mélangées à des Dynabeads ont été analysées à l'aide du mode SIMI sur le système Aura+. Ensemble, les modes BMI, FMM et SIMI ont permis une analyse complète des particules dans le mélange complexe de particules et de cellules. Les chercheurs ont identifié quatre sous-types de particules : plastique, cellules non viables, cellules viables et agrégats protéiques.
Contrôle de la contamination et décontamination
Heureusement, les bonnes pratiques de laboratoire (BPL) contribuent grandement à gérer la fréquence et le degré de contamination des cultures. Il est important de gérer activement vos cultures afin de réduire les problèmes et de conserver des registres précis pendant au moins un mois pour tout problème qui survient, aussi minime soit-il.
D'autres méthodes éprouvées pour éviter la contamination comprennent :
- De bonnes techniques d'asepsie: créer une barrière entre vos cellules et l'environnement.
- Réduire les accidents— réduire les déversements, les bris ou les fuites.
- Maintenir un laboratoire proprepermet de réduire la pénétration de particules biologiques, chimiques et même physiques.
- Surveillance régulière: consignez tout problème qui survient.
- Évitez les antibiotiques— combattez les souches bactériennes résistantes
Cependant, une utilisation appropriée des antiseptiques (dans le cadre du nettoyage de votre laboratoire) peut être bénéfique pour prévenir la contamination.
Normes de laboratoire, contrôles qualité
Standards for laboratory practice fall under GLP methods, and quality controls are dictated by FDA standards, based on USP <788>.
USP <788>: Specifically outlines the requirements for particle size limits (between 10 and 25 µm) and methods of particulate matter determination in injections for various dosage forms.
BPL: Aux États-Unis, ces pratiques sont régies par la norme 21 CFR partie 58. La Communauté européenne et les principaux pays d'Asie, d'Afrique, d'Amérique et du Moyen-Orient suivent également ces normes. Selon la FDA, les BPL fournissent un cadre pour la conduite d'études bien contrôlées :
- Garantit la qualité et l'intégrité des données
- Facilite la reconstruction des études
- Assure la responsabilité globale
- La sécurité des nouveaux composés est d'abord testée dans le cadre d'études non cliniques.
Détection de contamination avec les systèmes Aura
La gamme d'analyseurs de détection de particules Aura Systems utilise une combinaison d'imagerie en champ clair et par fluorescence, ainsi que la diffusion de la lumière pour identifier et quantifier spécifiquement les contaminants des cultures cellulaires, en utilisant des échantillons plus petits que les autres méthodes et en fournissant des lectures plus précises et plus exactes de votre culture cellulaire. La gamme Aura Systems comprend :
- Aura+ System: Biothérapies interdisciplinaires réunies dans un seul et même système.
- Aura CL System: Pour la thérapie cellulaire, permet d'identifier les agrégats cellulaires et de réaliser des tests cellulaires.
- Aura GT System: Pour la thérapie génique, permet d'identifier les agrégats de capside, de détecter les fuites d'ADN et de réaliser des tests immunologiques.
- Aura PTx System: Pour l'immunothérapie (anticorps), identifie le polysorbate et réalise des tests immunologiques.
Références
Culture cellulaire : cultiver des cellules comme systèmes modèles in vitrohttps://www.ncbi.nlm.nih.gov/pmc/articles/PMC7149418/#:~:text=Cell%20culture%20is%20one%20of,type%20cells%20and%20diseased%20cells.
FDA et BPLhttps://www.fda.gov/media/165993/download
USP <788> https://www.uspnf.com/sites/default/files/usp_pdf/EN/USPNF/revisionGeneralChapter788.pdf
Contaminations virales des cultures cellulaireshttps://rdcu.be/dMCh0
DynabeadsTM est une marque déposée de Thermo Fisher Scientific.
Sujets populaires
ACQUITY QDa (17) bioanalyse (12) produits biologiques (17) biopharmacie (50) produits biopharmaceutiques (58) biothérapies (21) étude de cas (18) chromatographie (14) conformité (12) intégrité des données (23) analyse alimentaire (12) HPLC (15) LC-MS (26) chromatographie en phase liquide (LC) (24) détection de masse (16) spectrométrie de masse (MS) (58) développement de méthodes (13) analyse des particules (19)


