Descifrando la contaminación del cultivo celular: un análisis en profundidad
La contaminación de los cultivos celulares es la pesadilla de todos los laboratorios. Puede ser física, química o biológica, y abarca desde problemas menores hasta catástrofes.
Las soluciones a la contaminación van desde observar buenas prácticas de laboratorio, mantener altos estándares de limpieza y cuidado de los medios de cultivo, realizar limpiezas eficaces y utilizar tecnologías como Aura+ System detectar y caracterizar los contaminantes, y potencialmente la fuente de contaminación y otras soluciones.
Este análisis revisará la importancia del control de la contaminación, los tipos de contaminación, las pruebas de identificación de la contaminación por partículas y diversos métodos de detección y control.
Descripción general del cultivo celular
El cultivo celular, es decir, la práctica de cultivar y mantener células vivas en un entorno artificial de laboratorio, es una de las técnicas más importantes en biología celular y molecular. Los cultivos celulares permiten a los investigadores descubrir la biología, la química, la fisiología y los procesos metabólicos de células de tipo salvaje, enfermas y modificadas.
Las células cancerosas inmortales han mostrado a los investigadores cómo se desarrolla el cáncer (y cómo se puede tratar o prevenir), y las células madre derivadas de personas con trastornos hereditarios se han convertido en valiosas plataformas para estudiar la base molecular de la enfermedad, todo ello en una placa de Petri. Los cultivos celulares también se utilizan para seleccionar nuevos compuestos farmacológicos en función de su eficacia y toxicidad en determinadas células, y son muy valiosos para el desarrollo de tejidos regenerativos, vacunas y terapias genéticas y celulares.
Control de la contaminación en cultivos celulares
Dependiendo del contaminante en cuestión, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) y la Colección Americana de Cepas de Cultivo (ATCC)estiman que hasta el 30 % de todos los cultivos celulares estáncontaminados (al menos con micoplasma).
Las consecuencias de la contaminación de los cultivos celulares incluyen retrasos en los experimentos y en el crecimiento celular, pérdidas económicas por tener que comprar nuevas células, medios de cultivo, sueros y placas/recipientes, y costes laborales por tener que volver a preparar los experimentos y desarrollar nuevos cultivos.
En el desarrollo de fármacos, los contaminantes ocultos pueden alterar el crecimiento y la función de las células, así como su capacidad para producir terapias biológicas y vacunas. Estos productos suelen quedar inutilizados y incumplen las normas y estándares de seguridad de los medicamentos.
Puede que no sea posible prevenir totalmente la contaminación de los cultivos celulares, pero las partículas y los contaminantes físicos pueden reducirse al mínimo con las estrategias y herramientas adecuadas para evitar pérdidas de cultivos, experimentos y producción. Este tipo de contaminantes puede considerarse la mayor preocupación, ya que podrían poner en riesgo a los pacientes o incluso causarles la muerte.
For biotherapeutic production, USP <788> standards set biopharmaceutical lot release guidelines and the proper limits of subvisible particles of no more than 12 particles per ml at least 10 µm and no more than two particles per ml that are at least 25 µm. In biotherapeutics, these particles are usually protein or other molecular fragments. The Aura System es una herramienta invaluable para identificar y caracterizar las partículas subvisibles responsables de la contaminación de algunos cultivos celulares.
Evaluación del riesgo de contaminación
Determinar el riesgo de contaminación de su cultivo celular depende de una evaluación exhaustiva de las propiedades de su cultivo. Estas propiedades son intrínsecas (qué sueros y medios utiliza y qué propiedades tienen las células tras las modificaciones genéticas) y extrínsecas (cuál es la posibilidad de infección por patógenos, otras partículas proteicas e incluso contaminación cruzada de otras células cultivadas, como las HeLa, por ejemplo).
Algunas culturas presentan riesgos más elevados que otras:
- Menor riesgo: uso de líneas celulares continuas no humanas o no primates, o líneas celulares continuas humanas bien caracterizadas.
- Riesgo medio: uso de células mamíferas mal caracterizadas.
- Alto riesgo: uso de células primarias procedentes de tejido y/o sangre humana o de primates. Las células de alto riesgo son también aquellas que contienen patógenos endógenos.
También querrá realizar una revisión exhaustiva de los procedimientos de su laboratorio para asegurarse de que se siguen las buenas prácticas de laboratorio (BPL), se utilizan desinfectantes adecuados con regularidad, se inspeccionan los cultivos celulares para detectar posibles infecciones o contaminaciones y se dispone de las herramientas adecuadas para detectar y cuantificar agentes invisibles o subvisibles.
Tipos de contaminación
La contaminación puede provenir de muchas fuentes diferentes. Para la mayoría de los investigadores y desarrolladores, las bacterias y los hongos suelen ser los primeros contaminantes que les vienen a la mente. Otros tipos pueden incluir virus, sustancias químicas y partículas macromoleculares.
- Contaminantes microbianos: suelen ser claramente visibles, con cambios rápidos en la turbidez y el color de los medios. Entre ellos se incluyen bacterias, hongos y levaduras. Otros intrusos, como el micoplasma, no son tan fáciles de detectar.
- Los virusson algunos de los contaminantes más difíciles de detectar. Los virus pueden provenir del paciente o del animal huésped, y algunas líneas celulares biotecnológicas contienen retrovirus endógenos.
- Contaminación química: contaminante no vivo, incluidos radicales libres, ionenes metálicos, residuos de desinfectantes y detergentes, o restos de endotoxinas bacterianas. Para los desarrolladores de productos bioterapéuticos y vacunas, estos agentes contaminantes también pueden incluir fragmentos de proteínas y otras moléculas más grandes que acompañan a la fabricación de medicamentos/vacunas basados en proteínas y que suponen un problema importante para los desarrolladores de productos biológicos.

Análisis de contaminación de trazas químicas y metales
Dependiendo del tipo de contaminación y del cultivo celular utilizado, el análisis de la contaminación puede emplear varias técnicas y herramientas. Estas herramientas detectan, identifican y caracterizan la contaminación y las materias extrañas en el cultivo celular. Las herramientas analíticas pueden abarcar desde la inspección visual, la microscopía, la espectroscopia, la investigación física/química y el análisis de elementos. La detección y el análisis rápidos son fundamentales.
Mientras que la microscopía (óptica, láser confocal de barrido, electrónica) puede proporcionar información sobre la forma, el tamaño y las superficies de los contaminantes, la espectroscopia y otras técnicas microscópicas (microscopía electrónica de barrido y espectroscopia de rayos X de dispersión de energía) permiten determinar la composición química de un contaminante. La espectroscopia Raman, la microscopía de fluorescencia, la espectroscopia óptica y la espectroscopia ATR-FTIR proporcionan la composición molecular de los materiales orgánicos, mientras que la espectroscopia de plasma acoplado inductivamente puede detectar trazas de metales.
Análisis de contaminación: pruebas de identificación
Determinar la contaminación química e inorgánica puede resultar difícil, ya que estos contaminantes son más difíciles de detectar que los contaminantes biológicos. Para realizar pruebas de identificación, comience por observar cualquier cambio que haya ocurrido en el laboratorio semanas antes de que surgiera el problema, especialmente cambios en el equipo, los suministros, las soluciones y los medios. Haga una lluvia de ideas con el personal del laboratorio y determine la mejor dirección para una evaluación más profunda. También es importante intentar averiguar qué podría haber ocurrido, especialmente teniendo en cuenta los riesgos de su cultivo celular.
La identificación puede comenzar registrando cualquier olor o sabor extraño (si procede), problemas de color anómalo o partículas extrañas. Descarte (si es posible) los contaminantes derivados de un almacenamiento y manipulación inadecuados, o de materias primas de mala calidad. A continuación, puede empezar a utilizar herramientas que permitan identificar contaminantes químicos, físicos o biológicos.
Análisis de contaminación por partículas
Las partículas en suspensión, especialmente las partículas subvisibles (de 2 a 100 µm), pueden ser comunes en las inyecciones e infusiones biofarmacéuticas y están estrechamente relacionadas con la inmunogenicidad y, por lo tanto, con el deterioro o el fallo del producto.
USP <788> and FDA standards and regulations establish lot release guidelines and limits for these particles. USP <788> describes two methods for particulate analysis—light obscuration and membrane microscopy. Membrane microscopy is recommended over light obscuration when working with complex, viscous and low-volume samples (a large proportion of biopharmaceutical drugs under development).
Una vez identificadas las partículas microscópicas, se puede proceder a aislar las fases particuladas de los depósitos y agregados de producción y determinar las fuentes de los contaminantes. Estas partículas pueden ser fragmentos de proteínas, pero también pueden ser partículas extrañas que aparecen como motas negras, residuos químicos de limpieza y mantenimiento, partículas visibles tras la disolución, abrasión o corrosión metálica de tuberías, bombas o contenedores, partículas de equipos de proceso, fragmentos de vidrio procedentes de delaminación o rotura, minerales o diversos plásticos, caucho, silicona u otros polímeros.
Técnicas de análisis de contaminación
La elección del mejor analizador de partículas depende de los requisitos específicos de la aplicación, como el tipo de muestra, el rango de tamaño y los objetivos del análisis. No existe una solución única para todos los casos. Sin embargo, los analizadores de partículas más populares suelen utilizar técnicas basadas en la difracción láser, la dispersión dinámica de luz (DLS) o la microscopía. The Aura Systems suite of analyzers Puede proporcionar un análisis de partículas más detallado que el DLS o la microscopía para partículas ≥1 µm, ofreciendo BMI y FMM para encontrar y caracterizar más partículas, incluidas las partículas subvisibles que de otro modo pasarían desapercibidas.
Análisis del tamaño de las partículas
Casi todos los productos bioterapéuticos contienen partículas subvisibles (entre 2 y 100 µm de diámetro). La propiedad más importante de las muestras de partículas es el tamaño de las mismas, que puede ser crucial para el éxito de su producto final. La mayoría de las partículas varían en volumen y forma. Comprender la distribución del tamaño de las partículas en su producto puede ayudarle a hacer predicciones sobre su fabricabilidad, eficacia, calidad, biodisponibilidad y vida útil. La distribución del tamaño puede influir en la porosidad y la superficie de su producto terapéutico: un tamaño de partícula inadecuado puede interferir en la producción, el rendimiento y los beneficios.
Métodos de detección
Difracción láser: también conocida como dispersión estática de luz láser, este método mide el tamaño de forma indirecta mediante la detección de las distribuciones de intensidad de la luz láser dispersada por las partículas. No permite evaluar la forma (asume que todas las partículas son esféricas) y presenta desventajas como su baja resolución y sensibilidad. No es tan eficaz en muestras polidispersas.
Reacción en cadena de la polimerasa (PCR): esta técnica muy utilizada puede emplearse para determinar las especies de contaminantes biológicos, como micoplasmas, virus o bacterias.
DLS: en este método, las partículas pasan por delante de una cámara y se analizan en tiempo real. El DLS puede examinar millones de partículas en cuestión de minutos y proporcionar información sobre diversos parámetros relacionados con el tamaño y la forma. Actualmente, el DLS es el método más utilizado para el análisis de la distribución del tamaño de las partículas en productos bioterapéuticos.
Imágenes (microscopía, SEM): aquí, las partículas se miden comparando su tamaño con una cuadrícula de líneas y contándolas. Sin embargo, es necesario medir millones de partículas para obtener un análisis estadísticamente válido. El análisis automatizado de micrografías electrónicas ayuda a superar esta barrera. Este método es útil para tamaños de partículas entre 0,2 y 100 µm.
IMC/FMM—Backgrounded membrane imaging (BMI), combinado con microscopía de membrana fluorescente (FMI), son la base de la Sistema de análisis de partículas Aura. El BMI, una técnica de imagen de alto contraste, genera imágenes nítidas de las partículas presentes en una muestra. Solo requiere 5 µl de muestra y puede ofrecer resultados en un minuto. El FMM marca las partículas utilizando tintes fluorescentes o anticuerpos específicos, lo que permite una identificación sencilla y definitiva.
Comparación de métodos
La microscopía(óptica, electrónica y de difracción de rayos X) puede mostrar el tamaño y la forma de los contaminantes, pero es posible que no detecte partículas invisibles. La PCR es sensible, pero no puede detectar fragmentos de proteínas ni contaminantes químicos o físicos. El BMI, combinado con el FMM y la imagen de membrana con iluminación lateral (SIMI), la base del sistema Aura, puede distinguir de forma fácil, rápida y precisa las partículas en terapias celulares, genéticas y proteicas.
BMI: aporta claridad a los riesgos de formulación que antes eran difíciles de detectar. Tiene sus raíces en la microscopía de membrana, pero con avances significativos. Primero se toma una imagen de fondo de la membrana antes de filtrar las muestras y capturar las partículas. Se vuelve a tomar una imagen de la misma membrana, con las partículas en la superficie. A continuación, se resta la imagen de fondo para eliminar la textura de fondo y revelar las partículas.
FMM: funciona con BMI para ofrecer un nivel de análisis que no se encuentra en otros sistemas de análisis de partículas. Etiquete sus objetivos con tintes fluorescentes o anticuerpos específicos, ya sea en la propia membrana o en solución. Primero, obtenga imágenes de las membranas con BMI para localizar las partículas y, a continuación, utilice FMM para caracterizar las partículas.
SIMI: funcionaen conjunto con BMI y FMM mediante la detección de la dispersión de la luz, concretamente de partículas con un índice de refracción elevado, incluidas aquellas que sobresalen de la superficie de la membrana. Las partículas que dispersan la luz indican la presencia de materia inorgánica que sobresale de la membrana, como vidrio o plástico. Las partículas que absorben la luz son indicativas de partículas metálicas, comoDynabeadsTM residuales, y aceites absorbentes que también sobresalen de la membrana.
Un estudio de caso diagnóstico
Recientemente, los científicos de Waters utilizaron el Aura+ System para detectar y caracterizar partículas utilizando BMI, FMM y SIMI, lo que demostró que el sistema Aura+ era superior a otros métodos para distinguir partículas subvisibles en terapias celulares. Esto ha cobrado mayor importancia en el desarrollo terapéutico a la luz de la reciente publicación por parte de la FDA del formulario 483 relativo a la contaminación de las terapias celulares Kymriah® con madera, celulosa, latón y acero, que se cree que entraron a través de bolsas de crioconservación.
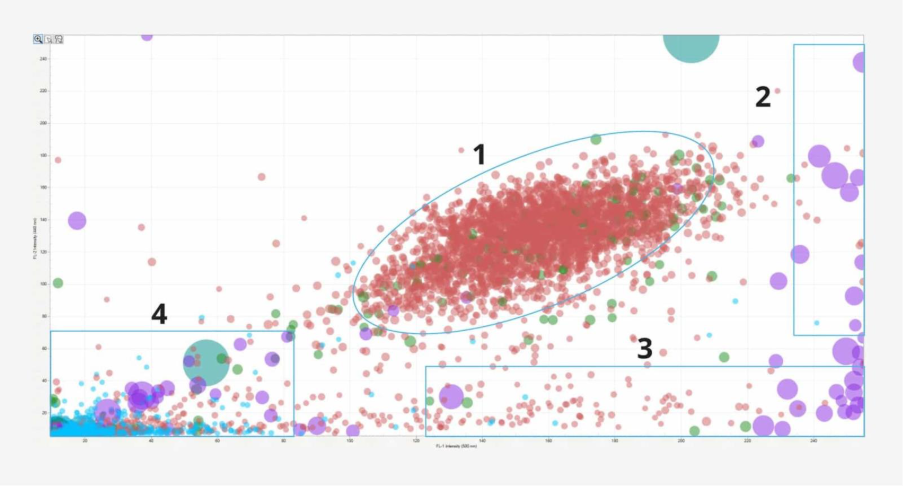
Los investigadores mezclaron células Car-T con estándares de partículas del NIST, celulosa y partículas metálicas. Las células Car-T mezcladas con Dynabeads se analizaron utilizando el modo SIMI en el sistema Aura+. En conjunto, BMI, FMM y SIMI permitieron el análisis total de las partículas en la compleja mezcla de partículas y células; los investigadores encontraron cuatro subtipos de partículas: plástico, células no viables, células viables y agregados proteicos.
Control de la contaminación y descontaminación
Afortunadamente, las buenas prácticas de laboratorio (BPL) contribuyen en gran medida a controlar la frecuencia y el grado de contaminación de los cultivos. Es importante gestionar activamente los cultivos para reducir los problemas y mantener registros precisos durante al menos un mes de cualquier problema que surja, por pequeño que sea.
Otros métodos probados y comprobados para evitar la contaminación incluyen:
- Buenas técnicas asépticas: proporcionar una barrera entre las células y el entorno.
- Reducir los accidentes: garantizar menos derrames, roturas o fugas.
- Mantener un laboratorio limpio: reduce la entrada de partículas biológicas, químicas e incluso físicas.
- Control rutinario: mantenga registros de cualquier problema que surja.
- Evite los antibióticos: combata las cepas resistentes de bacterias.
Sin embargo, el uso adecuado de antisépticos (parte de la limpieza de su laboratorio) puede ser beneficioso para evitar la contaminación.
Normas de laboratorio, controles de calidad
Standards for laboratory practice fall under GLP methods, and quality controls are dictated by FDA standards, based on USP <788>.
USP <788>: Specifically outlines the requirements for particle size limits (between 10 and 25 µm) and methods of particulate matter determination in injections for various dosage forms.
GLP: En Estados Unidos, estas prácticas se rigen por la norma 21 CFR parte 58. La Comunidad Europea y los principales países de Asia, África, América y Oriente Medio también siguen estas normas. Según la FDA, las GLP proporcionan un marco para la realización de estudios bien controlados:
- Garantiza la calidad y la integridad de los datos.
- Facilita la reconstrucción del estudio.
- Proporciona responsabilidad general.
- Los nuevos compuestos se someten primero a pruebas de seguridad mediante estudios no clínicos.
Detección de contaminación con Aura Systems
La familia de analizadores de detección de partículas de Aura Systems utiliza una combinación de imágenes de campo claro y fluorescentes, así como la dispersión de la luz, para identificar y cuantificar específicamente los contaminantes de los cultivos celulares, utilizando muestras más pequeñas que otros métodos y proporcionando lecturas más precisas y exactas de su cultivo celular. La familia de Aura Systems incluye:
- Aura+ System: Bioterapéuticos interdisciplinarios, todo en un solo sistema.
- Aura CL System: Para la terapia celular, puede identificar agregados celulares y realizar ensayos celulares.
- Aura GT System: Para la terapia génica, puede identificar agregados de cápsides, detectar fugas de ADN y realizar inmunoensayos.
- Aura PTx System: Para la terapia inmunológica (anticuerpos), identifica el polisorbato y realiza inmunoensayos.
Referencias
Cultivo celular: cultivo de células como sistemas modelo in vitrohttps://www.ncbi.nlm.nih.gov/pmc/articles/PMC7149418/#:~:text=El%20cultivo%20celular%20es%20uno%20de,células%20normales%20y%20células%20enfermas.
FDA yGLPhttps://www.fda.gov/media/165993/download
USP <788> https://www.uspnf.com/sites/default/files/usp_pdf/EN/USPNF/revisionGeneralChapter788.pdf
Contaminaciones víricas de cultivoscelulareshttps://rdcu.be/dMCh0
DynabeadsTM es una marca comercial de Thermo Fisher Scientific.
Temas populares
ACQUITY QDa (17) bioanálisis (12) productos biológicos (17) biofarmacia (50) biofarmacéutico (59) bioterapéuticos (24) estudio de caso (20) cromatografía (14) integridad de los datos (23) análisis de alimentos (12) HPLC (15) informática (12) LC-MS (27) cromatografía líquida (LC) (25) detección de masas (16) espectrometría de masas (MS) (61) desarrollo de métodos (14) análisis de partículas (21)