L'importance de la caractérisation des AAV pour garantir le développement sûr des thérapies géniques
Les capside des virus adéno-associés (AAV) se sont imposées comme les favorites pour l'administration de gènes in vivo grâce à leur profil de sécurité unique et à leur capacité à assurer une expression génique à long terme. Avec l'utilisation de multiples sérotypes de vecteurs AAV recombinants dans divers programmes de thérapie génique, ce domaine connaît une croissance sans précédent.
En avril 2020, 244 essais cliniques actifs impliquant des AAV étaient en cours dans le monde, dont 24 en phase III. Cependant, le développement d'analyses AAV complètes pour le développement de processus et l'évaluation finale des médicaments n'est pas sans obstacles.
Précis AAV characterization est crucial pour garantir l'efficacité des thérapies géniques. Visible et particule subvisible (SVP) L'analyse joue un rôle clé dans ce processus. Cependant, lorsqu'elle est appliquée aux thérapies géniques basées sur les AAV, elle présente un défi unique en raison de la disponibilité limitée du matériel pour les tests. Les méthodes actuelles de caractérisation des AAV comprennent la diffusion dynamique de la lumière (DLS) et la chromatographie d'exclusion stérique (SEC), qui sont couramment utilisées pour caractériser les populations d'AAV solubles et submicroniques. Bien que très informatives, ces techniques ne fournissent pas une image complète, car elles se concentrent principalement sur les AAV solubles et stables. Il est tout aussi essentiel d'étudier les AAV insolubles et instables afin d'identifier les vulnérabilités ou les irrégularités potentielles et de garantir leur utilisation sûre et efficace.
Des techniques telles que l'obscurcissement de la lumière (LO) et l'imagerie de flux (FI) sont utilisées pour caractériser les populations de particules insolubles dans les formulations AAV, fournissant des informations sur les espèces plus grandes et hétérogènes. Cependant, elles nécessitent de grands volumes de matière, peuvent être coûteuses et prendre beaucoup de temps, ce qui crée des goulots d'étranglement dans le développement et la fabrication des thérapies géniques.

Approches analytiques traditionnelles et novatrices pour caractériser les AAV
La garantie d'une qualité constante des thérapies géniques AAV dépend de la capacité à caractériser rapidement les attributs de qualité critiques (CQA). Cela inclut la mesure du titre viral, du contenu de la capside et de l'agrégation, qui ont tous un impact sur la puissance, la pureté et la sécurité des AAV. Malheureusement, les méthodes existantes de caractérisation des AAV pour mesurer ces attributs prennent souvent beaucoup de temps ou ne fonctionnent pas bien pour le développement de processus, mais de nouvelles méthodes d'analyse des AAV rapides et à haut débit sont en cours de développement.
Dans uneétuderécemment publiée dansScience Direct, des chercheurs ont examiné les techniques conventionnelles et émergentes permettant de mesurer les attributs de qualité des AAV recombinants (rAAV).
Les rAAV sont des vecteurs prometteurs pour la thérapie génique, mais leurs caractéristiques qualitatives doivent être soigneusement analysées afin d'en garantir la sécurité et l'efficacité. Les analyses traditionnelles et les tests de contrôle qualité des AAV prennent beaucoup de temps et peuvent ne pas convenir à des délais de développement de produits rapides. Les méthodes d'analyse rapide et à haut débit des AAV peuvent fournir rapidement des résultats exploitables, mais leur développement et leur mise en œuvre peuvent s'avérer difficiles en raison des quantités limitées d'échantillons et des effets de matrice.
Malgré ces défis, des progrès significatifs ont été réalisés dans le développement de méthodes d'analyse rapides et à haut débit pour la caractérisation des rAAV, en particulier pour trois CQA potentiels : le titre de capside, le rapport de contenu et la teneur en agrégats. Les méthodes basées sur la chromatographie et la diffusion de la lumière peuvent désormais être utilisées pour caractériser ces CQA directement ou en ligne, ce qui permet une surveillance et un contrôle du processus en temps réel.
Selon les auteurs de l'article, voici quelques-uns des principaux avantages des méthodes d'analyse rapides et à haut débit pour la caractérisation des rAAV :
- Développement plus rapide des produits: les méthodes d'analyse rapides peuvent contribuer à accélérer le développement des produits en fournissant des informations en temps opportun sur les performances des processus et la qualité des produits.
- Réduction des coûts: les méthodes d'analyse rapides peuvent contribuer à réduire les coûts en diminuant le temps et les ressources nécessaires aux tests de contrôle qualité.
- Amélioration de la qualité des produits :les méthodes d'analyse rapides peuvent contribuer à améliorer la qualité des produits en permettant la surveillance et le contrôle des processus en temps réel.
Cependant, des défis subsistent :
- Quantités d'échantillons limitées :la production de rAAV ne permet généralement d'obtenir que de petits volumes de produit purifié, ce qui peut limiter la quantité d'échantillons disponibles pour l'analyse.
- Effets matriciels : laprésence d'autres molécules dans l'échantillon de rAAV, telles que des tampons, de l'ADN ou des protéines résiduels, ou des sels ioniques, peut interférer avec les mesures analytiques.
- Développement de méthodes :Le développement de méthodes analytiques rapides, à haut débit, précises, fiables et reproductibles peut s'avérer difficile.
Les auteurs ont conclu que le développement de méthodes analytiques AAV capables de prendre en charge des délais courts et un débit élevé dans le développement des processus, tout en conservant la reproductibilité et la spécificité, sera essentiel.
Au-delà des méthodes traditionnelles de caractérisation des AAV : mieux comprendre les échantillons grâce à Aura
Il est essentiel de caractériser l'agrégation et la stabilité des AAV à des volumes ultra-faibles pour garantir la pureté du produit et prévenir les fuites ou la contamination de l'ADN. Les progrès technologiques ont ouvert de nouvelles possibilités dans ce domaine, de sorte qu'il est désormais possible de dépister rapidement l'instabilité et de caractériser l'agrégation des AAV à des volumes ultra-faibles, ce qui est pertinent pour le développement de thérapies géniques. Grâce à la technologie SIMI (Side Illumination Membrane Imaging) et FMM (Fluorescence Membrane Microscopy) d'Aura System, combinée aux capacités d'indice de réfraction de BMI, vous pouvez acquérir une compréhension plus approfondie des échantillons afin d'identifier les contenus protéiques ou non protéiques ainsi que les éléments intrinsèques ou extrinsèques, ce que les analyseurs de particules traditionnels basés sur le flux ne pouvaient pas fournir. Cela permet une meilleure protection contre les rappels coûteux dus à une contamination particulaire invisible.
Contrairement à l'imagerie de flux, qui nécessite plusieurs millilitres d'échantillon, Aura Systems peut caractériser rapidement et facilement les vecteurs viraux et d'autres types de thérapies géniques à partir d'un échantillon de seulement 5 µL. Cela est possible grâce à l'analyse des échantillons par microscopie à membrane, qui nécessite des quantités minimes tout en conservant une efficacité d'échantillonnage de 100 %.
Aura GT System’s technology also allows for AAV characterization with high throughput (<1 min/sample), quickly revealing insights into their stability. The system helps to ensure that a gene therapy’s most important stability characteristic — its SVP concentration — can be monitored throughout process development and through quality control testing.
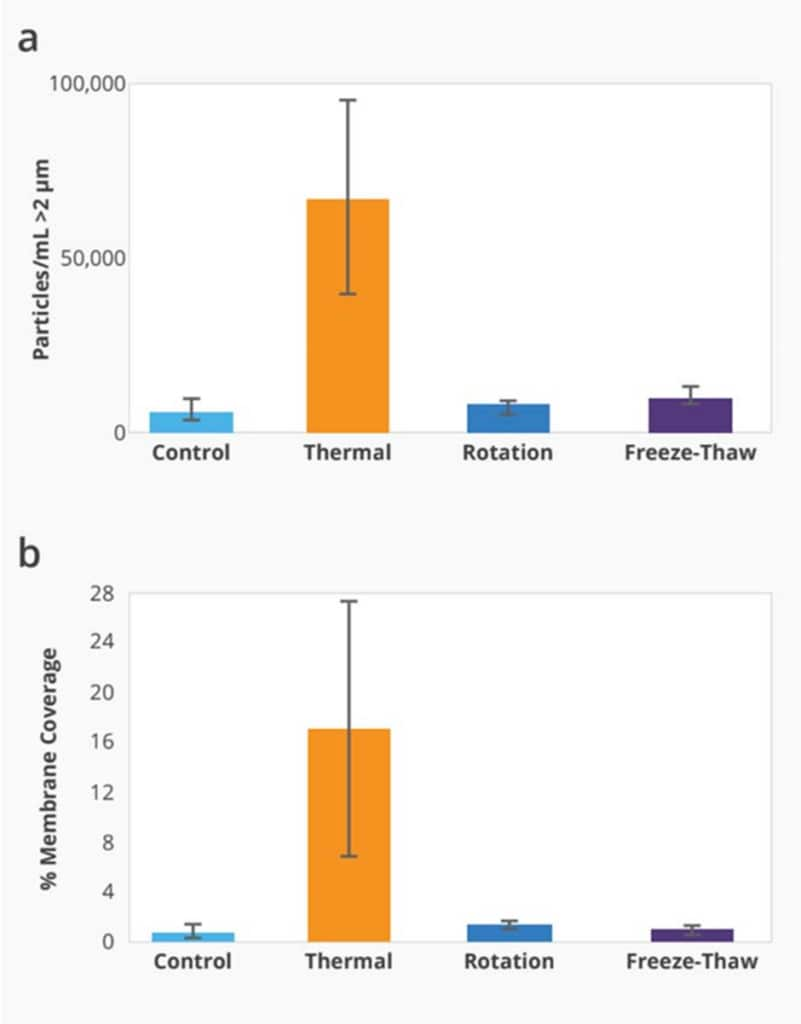
Utiliser plusieurs méthodes d'analyse AAV
En mettant en œuvre une méthode d'analyse rapide pour la caractérisation des AAV, vous pouvez commencer le criblage et la sélection des candidats beaucoup plus tôt dans le développement, ce qui vous apporte la confiance nécessaire pour commercialiser votre thérapie génique.
Références
- McIntosh, N.L., Berguig, G.Y., Karim, O.A. et al. (2021). Caractérisation et quantification complètes des vecteurs associés à l'adénovirus par chromatographie d'exclusion stérique et diffusion de la lumière multi-angle. Scientific Reports, 11, 3012.https://doi.org/10.1038/s41598-021-82599-1
- Cole, L., Fernandes, D., Hussain, M.T., Kaszuba, M., Stenson, J., & Markova, N. (2021). Caractérisation des virus adéno-associés recombinants (rAAV) pour la thérapie génique à l'aide de techniques orthogonales. Pharmaceutics, 13(4), 586.https://doi.org/10.3390/pharmaceutics13040586
- Gimpel, A.L., Katsikis, G., Sha, S., Maloney, A.J., Hong, M.S., Nguyen, T.N.T., Wolfrum, J., Springs, S.L., Sinskey, A.J., Manalis, S.R., Barone, P.W., & Braatz, R.D. (2021). Méthodes analytiques pour la caractérisation des processus et des produits des thérapies géniques à base de virus adéno-associés recombinants. Molecular Therapy – Methods & Clinical Development, 20, 740-754.https://doi.org/10.1016/j.omtm.2021.02.010
Sujets populaires
ACQUITY QDa (17) bioanalyse (12) produits biologiques (17) biopharmacie (49) biopharmaceutique (58) biothérapeutiques (21) étude de cas (18) chromatographie (14) conformité (12) intégrité des données (23) analyse alimentaire (12) HPLC (15) LC-MS (26) chromatographie liquide (LC) (24) détection de masse (16) spectrométrie de masse (MS) (58) développement de méthodes (13) analyse des particules (19)


