Polysorbate 80 : étude de son impact sur la stabilité des IgG

Avec le renforcement des réglementations en matière de sécurité des médicaments, les fabricants doivent s'assurer que leurs formulations, comme le polysorbate 80, sont exemptes de particules visibles et contiennent un nombre limité de particules subvisibles supérieures à 10 µm (conformément aux exigences de la FDA). Ces particules ne sont pas seulement dues à l'instabilité du processus, mais aussi à la dégradation des excipients de la formulation.
Les contraintes mécaniques exercées pendant la fabrication peuvent provoquer une agrégation des protéines, ce qui nuit à la qualité et à la sécurité du produit. L'agrégation résulte souvent d'interactions faibles entre des zones hydrophobes exposées de protéines partiellement ou totalement dépliées. Diverses conditions, telles que les variations de pH, les températures élevées et les contraintes mécaniques supplémentaires, peuvent induire le dépliage des protéines, favorisant ainsi la formation d'agrégats protéiques.
Par conséquent, il est essentiel de mettre au point des formulations robustes qui limitent le dépliement et l'agrégation des protéines afin de garantir la qualité des médicaments protéiques.
Les polysorbates : un élément clé dans la prévention de l'agrégation des protéines
Pour empêcher l'agrégation, on utilise fréquemment des polysorbates. Ces tensioactifs non ioniques sont principalement composés d'esters d'acides gras de sorbitane polyoxyéthylène (POE). La fonction protectrice des polysorbates dans les formulations protéiques a fait l'objet de nombreuses études, qui ont permis d'identifier deux mécanismes principaux : (1) les polysorbates agissent comme des chaperons pour les sites hydrophobes sujets à l'agrégation à la surface des protéines, soutenant ainsi la structure repliée, et (2) les polysorbates entrent en compétition avec les protéines au niveau des interfaces, réduisant ainsi l'exposition de celles-ci.
Le polysorbate 80 (mono-oléate de sorbitane POE, PS80) est un tensioactif couramment utilisé dans les formulations biopharmaceutiques disponibles dans le commerce en raison de son efficacité à prévenir l'adsorption et l'agrégation des protéines. Cependant, il y a un hic : la qualité du PS80, en particulier lors des processus générant des contraintes mécaniques, peut influencer considérablement la stabilité des protéines, notamment des IgG.
De plus, le stockage à long terme du polysorbate à basse température peut entraîner la formation de particules d'acides gras libres, ce qui peut compromettre l'efficacité du médicament. Les méthodes d'analyse traditionnelles telles que l'obscurcissement lumineux (LO) et l'imagerie de flux (FI) ont du mal à identifier les sources de dégradation. Au fil du temps, elles peuvent devenir sensibles à l'hydrolyse enzymatique par les protéines des cellules hôtes (HCP), ce qui entraîne la formation de particules visibles et subvisibles qui pourraient compromettre l'efficacité d'un médicament.
Il a été difficile de réaliser des analyses à haut débit, sensibles et spécifiques des particules de polysorbate en raison de leur composition chimique complexe et de leur faible concentration dans les formulations, ce qui en fait un véritable problème de l'aiguille dans une botte de foin.
Imagerie par membrane en arrière-plan utilisée pour explorer la fonctionnalité du polysorbate 80
Le rôle du PS80 dans la stabilité des protéines fait l'objet d'un débat continu. De plus, l'impact du PS partiellement dégradé sur l'agrégation des protéines n'est pas encore bien compris. Cela a conduit les chercheurs à mener une étude sur la fonctionnalité du PS80.
Dans cetteétude, un anticorps monoclonal (mAb), IgG, a été soumis à trois conditions de contrainte mécanique différentes en présence de PS80 de qualité multicompendiale (MC) et de qualité pharmacopée chinoise (ChP). Les formulations d'IgG ont été complétées par du PS80 partiellement hydrolysé afin d'étudier l'effet de ses produits de dégradation sur la stabilité des protéines.
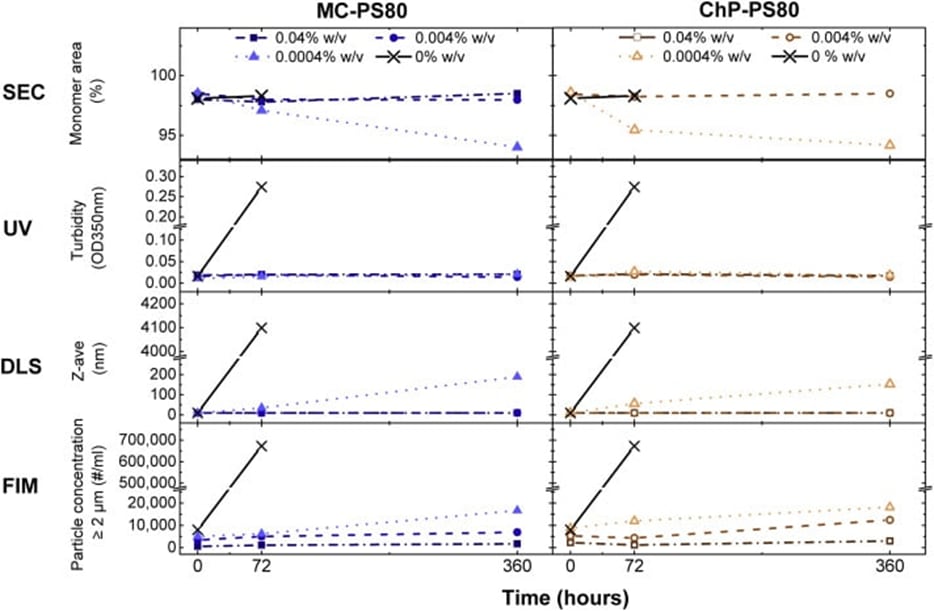
La fonctionnalité du PS80 a été évaluée en mesurant l'agrégation des protéines et la formation de particules induites lors d'un stress mécanique à l'aide de plusieurs méthodes analytiques. Celles-ci comprenaient : la chromatographie d'exclusion stérique (SEC), la diffusion dynamique de la lumière (DLS), la microscopie à imagerie de flux (FIM) et l'imagerie membranaire en arrière-plan (BMI).
Les chercheurs ont utilisé le Aura Système permettant d'effectuer un BMI pour la caractérisation et la quantification de particules de taille micrométrique. Dans des conditions de flux d'air laminaire, 30 μL de l'échantillon ont été transférés sur une plaque de filtration à membrane en polycarbonate à 96 puits (Waters) avec une taille de pores de 0,4 μm. Un vide de 350 mbar a été appliqué après le remplissage de six puits afin de permettre l'écoulement du liquide à travers la membrane et le piégeage des particules. Ensuite, 90 μL d'eau hautement purifiée ont été utilisés pour laver chaque puits après le transfert de l'échantillon afin d'éliminer toute matière soluble. Chaque échantillon a été mesuré en trois exemplaires.1
L'étude n'a révélé aucune différence significative dans la fonctionnalité du PS80 entre les grades MC et ChP lors des tests de résistance. Cependant, à mesure que le degré d'hydrolyse du PS80 augmentait, un nombre plus élevé de particules subvisibles a été mesuré après la résistance. De plus, des niveaux plus élevés de dégradants du PS80 à une concentration constante de PS80 peuvent déstabiliser l'IgG. Les chercheurs ont conclu que les grades MC et ChP du PS80 offraient une protection équivalente, mais que les dégradants du PS80 compromettaient la stabilité de l'IgG.
Identification à haut débit des particules de polysorbate à l'aide du test Aura
La dégradation du polysorbate produit trois acides gras distincts : l'acide laurique, l'acide myristique et l'acide palmitique. Ces acides créent des particules aux caractéristiques morphologiques uniques qui peuvent être identifiées à l'aide des capacités d'étiquetage et d'imagerie du système Aura. Grâce à l'application du BODIPY™ FLC16 ( Thermo Fisher Scientific), un colorant à haute affinité, les chercheurs peuvent identifier avec précision les AGL.
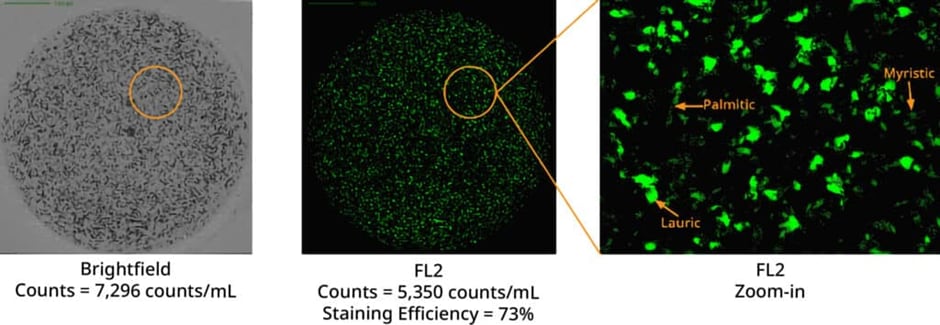
Le test de dégradation des polysorbates d'Aura System rationalise le processus de détection des excipients dégradés dans les formulations protéiques à concentrations élevées. Cette méthode est adaptable, capable de gérer un large éventail de volumes d'échantillons allant de 5 µL à 10 mL, et peut analyser simultanément jusqu'à 96 échantillons pour détecter la présence de particules d'acide libre. Cette efficacité réduit considérablement le temps et les efforts nécessaires.
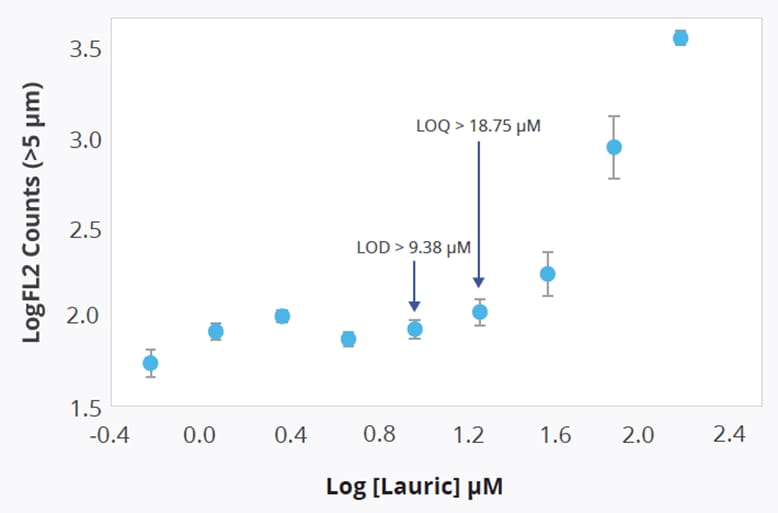
Il est important de noter que le test au polysorbate du système Aura est suffisamment sensible pour identifier les acides gras libres (AGL) à des concentrations relatives à l'acide laurique supérieures à 9,38 µM (ce qui correspond à plus de 2183 comptes/mL) et peut les quantifier à des niveaux supérieurs à 18,75 µM, soit plus de 2976 comptes/mL.
Conclusion
Aura Le système simplifie la détection et la distinction des composants dégradés dans les échantillons à base de protéines à n'importe quel stade du processus de production des médicaments. Ne nécessitant que 5 µL d'échantillon, cette méthode est à la fois spécifique et sensible, capable d'analyser 96 échantillons en quelques heures, surpassant ainsi les techniques alternatives.
De plus, cette technologie avancée permet d'identifier et de différencier les particules dégradées cruciales issues de la formulation du polysorbate en fonction de leur forme, de leur apparence et de leur marquage unique avec du BODIPY FLC16, ce qui en fait un outil indispensable.
Références
Sujets populaires
ACQUITY QDa (17) bioanalyse (12) produits biologiques (17) biopharmacie (49) biopharmaceutique (58) biothérapeutiques (21) étude de cas (18) chromatographie (14) conformité (12) intégrité des données (23) analyse alimentaire (12) HPLC (15) LC-MS (26) chromatographie liquide (LC) (24) détection de masse (16) spectrométrie de masse (MS) (58) développement de méthodes (13) analyse des particules (19)


