Progrès dans les techniques de quantification des exosomes
L'étudedes exosomes asuscité un intérêt considérable ces dernières années en raison de leur potentiel significatif dans le domaine du diagnostic, des applications thérapeutiques et en tant que biomarqueurs pour diverses maladies.Les exosomes, qui sont des vésicules extracellulaires (EV) dont la taille varie entre 30 et 150 nm lorsqu'elles sont stables et en solution, sont sécrétées par diverses cellules et transportent des signaux moléculaires tels que des protéines, des lipides et des ARN vers les cellules réceptrices. Cette fonction rend les exosomes essentiels dans la communication intercellulaire, la progression des maladies et la modulation immunitaire.
En conséquence, les exosomes sont désormais considérés comme des acteurs clés dans le développement de médicaments thérapeutiques et de méthodes de détection des maladies. Cependant, pour que les chercheurs et les entreprises pharmaceutiques puissent exploiter pleinement le potentiel des exosomes, il est essentielde quantifier avec précisionces vésicules. Qu'il s'agisse de développer de nouvelles stratégies thérapeutiques ou de détecter des biomarqueurs spécifiques à une maladie, la capacité à mesurer avec précision la concentration et le contenu des exosomes est essentielle.
Ce blog explore le dernières avancées en matière de techniques de quantification des exosomes, en détaillant leur impact sur la recherche et le développement pharmaceutiques, les diagnostics et l'administration des médicaments. Nous mettrons en avant les principaux outils utilisés pour l'analyse des exosomes, en nous concentrant sur les technologies émergentes telles que the Aura System, qui offre de nouveaux niveaux de sensibilité et de précision dans la quantification des exosomes.
Que sont les exosomes ?
Les exosomes sont de petites vésicules libérées par les cellules dans l'espace extracellulaire, qui jouent un rôle importantdans la communication intercellulaire. Ils proviennent de la voie endosomale et sont formés par le bourgeonnement interne de corps multivésiculaires. Lorsque ces corps fusionnent avec la membrane cellulaire, les exosomes sont sécrétés dans l'environnement extracellulaire. En raison de leur biogenèse unique, les exosomes sont équipés de biomolécules provenant de leurs cellules mères, notamment :
- Protéines: protéines membranaires, enzymes et molécules de signalisation.
- Lipides: cholestérol, phospholipides et céramides.
- Acides nucléiques: ARN, y compris l'ARN messager (ARNm) et le microARN (miARN).
Les exosomes peuvent être isolés à partir de divers fluides corporels, tels que le sang, l'urine, le liquide céphalo-rachidien et la salive, ce qui les rend accessibles à des fins cliniques et de recherche. Leurs rôles biologiques sont variés, allant de la modulation immunitaire à la facilitation de la progression du cancer par le transfert d'oncogènes entre les cellules. Leur capacité à transporter des signaux moléculaires les rend précieuxen tant que biomarqueurs pourdiverses maladies, notamment le cancer, les troubles neurodégénératifs et les maladies cardiovasculaires.
Pourquoi la quantification des exosomes est-elle importante ?
Une quantification précise des exosomes est essentielle pour garantir la cohérence, la reproductibilité et l'efficacité de la recherche et du développement thérapeutique. Qu'ils soient utilisés à des fins diagnostiques ou thérapeutiques, la concentration et le contenu des exosomes doivent être soigneusement mesurés afin d'obtenir des données significatives.
- Développement thérapeutique: dans le domaine du développement de médicaments, les exosomes sont étudiés comme systèmes de délivrance de molécules thérapeutiques telles que les petits ARN interférents (siRNA) et les protéines. Une quantification précise garantit un dosage exact, ce qui est essentiel pour la sécurité des patients et l'efficacité du traitement.
- Applications diagnostiques: les exosomes sont également utilisés comme biomarqueurs pour la détection précoce des maladies. Par exemple, les exosomes provenant de cellules cancéreuses transportent des protéines et des ARN spécifiques à la tumeur qui peuvent être détectés dans le sang, ce qui permet un diagnostic non invasif du cancer. Une quantification précise des exosomes est essentielle dans le domaine du diagnostic afin d'améliorer la sensibilité et la spécificité de ces tests.
- Reproductibilité: une quantification précise et cohérente des exosomes garantit la reproductibilité des données de recherche entre différentes expériences et différents laboratoires. Cela est particulièrement important lors du transfert des résultats de recherche issus d'études précliniques vers des applications cliniques.
Techniques de quantification des exosomes
À mesure que l'importance des exosomes dans la recherche et la médecine continue de croître, la demande pour des méthodes de quantification plus fiables et plus sensibles augmente également. Actuellement, plusieurs techniques établies sont largement utilisées pour mesurer la concentration et les caractéristiques des exosomes. Chaque méthode présente des avantages et des limites qui lui sont propres, en fonction de l'application de recherche.
Analyse par suivi des nanoparticules (NTA)
L'analyse par suivi des nanoparticules (NTA) est l'une des méthodes les plus couramment utilisées pour la quantification des exosomes. Cette technique permet aux chercheurs de mesurer à la foisla distributiongranulométriqueet la concentration desparticules dans un échantillon en suivant le mouvement des exosomes dans une suspension liquide. Les exosomes se déplacentselon un mouvement brownien, et la vitesse de leur mouvement est utilisée pour calculer la taille des particules.
Avantages de la NTA :
- Mesure simultanée de la taille et de la concentration: la NTA peut fournir des informations détaillées sur la distribution de la taille des exosomes ainsi que sur leur concentration globale dans l'échantillon.
- Préparation minimale des échantillons: contrairement à certaines autres techniques, la NTA nécessite généralement moins de préparation des échantillons, ce qui réduit le risque de dégradation et de contamination des échantillons.
- Visualisation en temps réel: la NTA fournit aux chercheurs des données en temps réel sur le mouvement des particules, leur permettant ainsi d'obtenir un retour immédiat pendant les expériences.
Limites de la NTA:
- Incapacité à distinguer les différents types de particules: la NTA ne fait pas la différence entre les exosomes et d'autres particules de taille similaire, telles que les agrégats protéiques, à moins que l'échantillon ne soit soigneusement purifié.
- Problèmes de reproductibilité: la NTA peut être sensible aux changements dans les conditions expérimentales, ce qui entraîne une variabilité des résultats. Elle nécessite également un étalonnage minutieux et une certaine expérience de la part de l'opérateur.
Malgré ses limites, la NTA reste l'une des méthodes les plus couramment utilisées pour la quantification des exosomes en raison de sa capacité à mesurer simultanément la taille et la concentration. Cependant, les chercheurs doivent s'assurer que les échantillons sont bien préparés afin d'éviter toute contamination par d'autres particules.
Cytométrie en flux
La cytométrie en flux est une autre méthode largement utiliséepour la détection et la quantification des exosomes. Cette technique consiste à marquer les exosomes avec des anticorps fluorescents qui se lient à des marqueurs de surface spécifiques, tels queCD63, CD9 et CD81. Les exosomes marqués sont ensuite passés à travers un faisceau laser, et les signaux fluorescents résultants sont mesurés afin de quantifier le nombre d'exosomes dans l'échantillon.
Avantages de la cytométrie en flux :
- Débit élevé: la cytométrie en flux permet l'analyse rapide d'un grand nombre d'exosomes, ce qui la rend idéale pour les études qui nécessitent une collecte de données à haut débit.
- Analyse multiparamétrique: les chercheurs peuvent utiliser différents marqueurs fluorescents pour analyser simultanément plusieurs marqueurs de surface, ce qui leur permet d'obtenir un profil détaillé des sous-populations d'exosomes.
- Spécificité: grâce à l'utilisation d'anticorps ciblant des marqueurs spécifiques aux exosomes, la cytométrie en flux offre un degré de spécificité supérieur à celui de techniques telles que la NTA.
Cytométrie en flux Limites :
- Limites de détection de taille: les cytomètres en flux traditionnels ont du mal à détecter les petites particules telles que les exosomes, ce qui réduit leur sensibilité pour les particules inférieures à 100 nm.
Bien que la cytométrie en flux soit un outil puissant pour la quantification des exosomes, elle est souvent utilisée en association avec d'autres techniques afin de pallier ses limites en termes de sensibilité.
Microscopie électronique à transmission (MET)
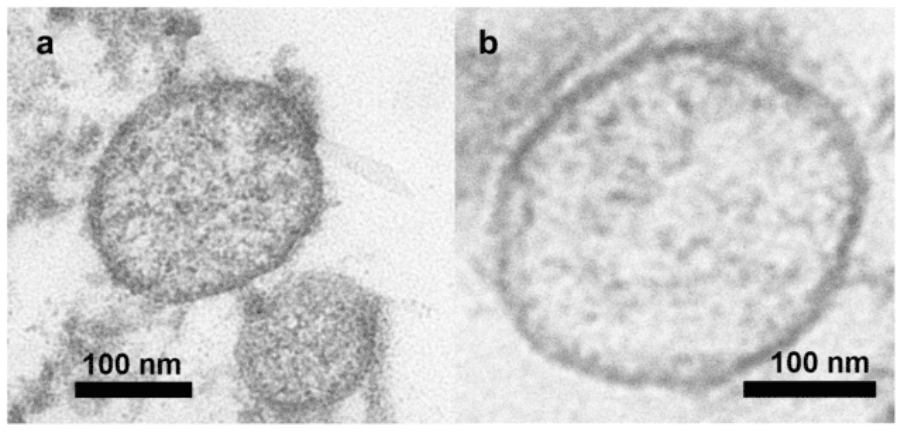
La microscopie électronique à transmission (MET)est souvent utiliséepour confirmer visuellement la présence d'exosomes dans un échantillon. La MET fournit des images haute résolution qui permettent aux chercheurs d'évaluer la morphologie et l'intégrité structurelle des exosomes. Bien qu'il ne s'agisse pas principalement d'une technique de quantification, la MET est précieuse pour vérifier la qualité des exosomes isolés.
Avantages du TEM :
- Imagerie haute résolution: le TEM offre des images détaillées de la structure des exosomes, permettant aux chercheurs de confirmer la présence d'exosomes intacts.
- Évaluation morphologique: le TEM permet de détecter des anomalies structurelles, telles que des exosomes endommagés ou agrégés, fournissant ainsi des informations sur la qualité de l'échantillon.
Limites du TEM :
- Nécessite beaucoup de travail: la TEM nécessite une préparation minutieuse des échantillons et peut prendre beaucoup de temps, ce qui la rend moins pratique pour la quantification routinière des exosomes.
- Coûteux: l'équipement et l'expertise nécessaires pour utiliser le TEM sont coûteux, ce qui limite son utilisation dans de nombreux laboratoires.
Techniques émergentes dans la quantification des exosomes
À mesure que la recherche sur les exosomes progresse, de nouvelles technologies sont développées pour pallier les limites des méthodes traditionnelles. L'une de ces technologies émergentes est la Aura System, qui combine analyse à haut débit avec détection de particules sans marquage.
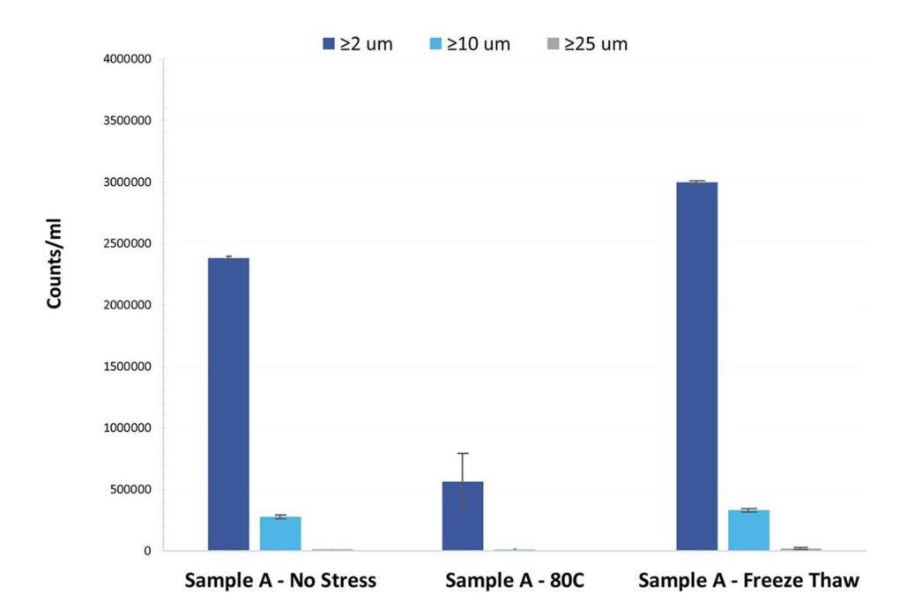
Le système Aura estconçu pour fournir une quantification plus sensible et plus précise des exosomes en détectant non seulement les exosomes solubles et stables, mais aussiles agrégats d'exosomes. La stabilité des exosomes est essentielle dans les applications thérapeutiques, et la détection des agrégats peut aider à garantir que seuls des exosomes fonctionnels et stables sont utilisés dans les processus en aval.
Avantages du système Aura :
- Volume d'échantillon ultra-faible: contrairement aux techniques traditionnelles qui nécessitent de grands volumes d'échantillon, le système Aura peut quantifier les exosomes à partir d'un échantillon de seulement 5 μL.
- Détection des agrégats: La détection des agrégats d'exosomes est essentielle pour maintenir la stabilité et la qualité des thérapies à base d'exosomes. Le système Aura excelle dans ce domaine, fournissant des données plus complètes sur la qualité des échantillons.
- Capacités à haut débit: le système Aura est conçu pour le criblage à haut débit, ce qui le rend idéal pour les études à grande échelle ou les applications industrielles où le temps et l'efficacité des échantillons sont essentiels.
Analyse et détection des exosomes
Si une quantification précise est essentielle, il est tout aussi important de comprendre la composition moléculaire des exosomes. Les exosomes transportent toute une sériede biomolécules, notamment des protéines, des lipides et des acides nucléiques, qui peuvent fournir des informations précieuses sur leur fonction biologique.
Marqueurs exosomes pour la détection
Les marqueurs de surface spécifiques aux exosomes sont utilisés pour détecter et caractériser les exosomes dans les échantillons biologiques. Ces marqueurs sontgénéralement des protéines, notamment :
- CD63, CD9 et CD81: membres de la famille des tétraspanines, ces protéines sont très concentrées à la surface des exosomes et sont couramment utilisées comme marqueurs dans la recherche sur les exosomes.
- Alix et TSG101: ces protéines interviennent dans la biogenèse des exosomes et sont fréquemment utilisées pour confirmer la présence d'exosomes dans un échantillon.
En ciblant ces marqueurs spécifiques, les chercheurs peuvent isoler et étudier les exosomes provenant d'une grande variété de fluides biologiques, tels que le sang, l'urine et la salive. La capacité à détecter les exosomes dans ces fluides en fait des candidats intéressants pour le diagnostic non invasif et la découverte de biomarqueurs.
Détection par immunoaffinité
L'une des méthodes les plus spécifiques et précises pour la détection des exosomesest celle basée sur l'immunoaffinité. Ces méthodes utilisent des anticorps qui se lient spécifiquement aux protéines de surface des exosomes, telles que les tétraspanines. Les anticorps capturent les exosomes d'intérêt, ce qui permet une quantification et une analyse plus précises.
Détection par immunoaffinité Avantages :
- Haute spécificité: en ciblant des marqueurs spécifiques aux exosomes, les méthodes d'immunoaffinité permettent d'isoler sélectivement les exosomes à partir d'échantillons biologiques complexes.
- Sensibilité: les techniques d'immunoaffinité améliorent la sensibilité de la détection des exosomes en se concentrant uniquement sur les vésicules exprimant des protéines de surface spécifiques.
Détection par immunoaffinité Limites :
- Limité aux marqueurs connus: la détection par immunoaffinité est limitée aux exosomes présentant des marqueurs bien caractérisés. Cela peut exclure les populations d'exosomes qui n'expriment pas les protéines ciblées.
- Préparation des échantillons: comme pour la cytométrie en flux, ces méthodes nécessitent une manipulation et une préparation minutieuses des échantillons, ce qui peut introduire une variabilité.
Cette technique est particulièrement utile dans les études visant à isoler les exosomes provenant de tissus ou de maladies spécifiques, tels que le cancer ou les troubles neurodégénératifs, où les sous-types d'exosomes jouent un rôle clé dans la progression de la maladie.
Défis et limites de la quantification des exosomes
Bien que des progrès significatifs aient été réalisés dans la quantification des exosomes, plusieurs défis et limites subsistent, notamment en matière de préparation des échantillons et de précision technique.
Défis liés à la préparation des échantillons
L'un des principaux obstacles à la recherche sur les exosomes est de garantir la pureté des échantillons d'exosomes. Les échantillons biologiques contiennent souvent un mélange de vésicules extracellulaires, d'agrégats protéiques et d'autres particules qui peuvent interférer avec la quantification des exosomes. Si ces contaminants ne sont pas éliminés efficacement, ils peuvent fausser les résultats et conduire à des mesures inexactes.
Les méthodes courantes d'isolement des exosomes, telles que l'ultracentrifugation etla chromatographie d'exclusion stérique, sont fréquemment utilisées pour purifier les échantillons. Cependant, ces méthodes sont longues et peuvent ne pas éliminer complètement les contaminants. De plus, les petits volumes d'échantillons peuvent compliquer le processus d'isolement.
Meilleures pratiques en matière de préparation d'échantillons :
- Utilisation de protocoles d'isolement optimisés: l'utilisation de protocoles et de kits validés pour l'isolement des exosomes peut contribuer à réduire la contamination et à améliorer la précision de la quantification.
- Plusieurs cycles de purification: dans certains cas, les chercheurs peuvent avoir besoin d'utiliser plusieurs techniques d'isolement, telles que la combinaison de l'ultracentrifugation et de la capture par immunoaffinité, afin d'améliorer la pureté des échantillons.
Limitations techniques
Plusieurs limitations techniques entravent également la quantification précise des exosomes, notamment en termes de reproductibilité et de sensibilité des techniques actuelles. Par exemple,la NTA peineà fournir des résultats cohérents entre différents laboratoires en raison des variations dans la manipulation des échantillons, l'étalonnage des instruments et l'expertise des opérateurs.
De plus, ces méthodes traditionnelles ont souvent des difficultés à détecter les populations d'exosomes plus petites ou plus hétérogènes, en particulier lorsque la concentration en exosomes est faible.
Comment le système Aura surmonte les défis techniques :
Le site Aura System répond à bon nombre de ces limitations techniques. Contrairement aux méthodes traditionnelles, le système Aura nécessite des volumes d'échantillons minimes et offre une sensibilité élevée, ce qui le rend idéal pour détecter les exosomes à faible abondance dans des échantillons complexes. De plus, sa capacité à détecter agrégats d'exosomes ajoute une couche supplémentaire d'analyse, garantissant que les chercheurs travaillent avec des exosomes stables et fonctionnels.
Applications de la quantification des exosomes
La quantification précise des exosomes trouve de nombreuses applications dans la recherche et la pratique clinique. Du diagnostic à la thérapie, la capacité à mesurer la concentration et le contenu des exosomes peut faire considérablement progresser le développement de nouveaux traitements et outils de surveillance des maladies.
Quantification des exosomes dans le domaine du diagnostic
L'une des applications les plus prometteuses de la quantification des exosomes se trouve dans le domainedu diagnostic. Les exosomes transportent les signatures moléculaires de leurs cellules mères, ce qui en fait des outils précieux pour détecter les biomarqueurs de maladies. Par exemple, les exosomes isolés à partir de cellules cancéreuses contiennentdes protéines oncogèneset des ARN quipeuvent être détectés dans le sang, ce qui permet un diagnostic précoce des tumeurs.
Les exosomes sont particulièrement utiles dans le diagnostic de maladies telles que :
- Cancer: les exosomes dérivés de tumeurs transportent des protéines et des ARN spécifiques qui peuvent être utilisés comme biomarqueurs pour la détection précoce et la surveillance du cancer.
- Maladies neurodégénératives: les exosomes présents dans le liquide céphalo-rachidien des patients atteints de la maladie d'Alzheimer ou de la maladie de Parkinson transportent des protéines spécifiques à la maladie qui peuvent fournir des informations sur la progression de celle-ci.
- Maladies cardiovasculaires: les exosomes libérés par les tissus cardiaques endommagés transportent des signaux moléculaires qui peuvent être détectés dans les échantillons sanguins, offrant ainsi des méthodes non invasives pour diagnostiquer les maladies cardiaques.
Une quantification précise des exosomes dans ces fluides est essentielle pour mettre au point des tests diagnostiques sensibles capables de détecter les maladies à un stade précoce, lorsqu'elles sont le plus faciles à traiter.
Avantages des diagnostics basés sur les exosomes :
- Prélèvement non invasif: les exosomes peuvent être isolés à partir de liquides biologiques facilement accessibles, tels que le sang et l'urine, ce qui réduit le recours aux biopsies invasives.
- Surveillance en temps réel: comme les exosomes sont constamment libérés par les cellules, ils peuvent être utilisés pour surveiller en temps réel la progression d'une maladie ou la réponse à un traitement.
Quantification des exosomes dans le développement thérapeutique

Dans le domainethérapeutique, les exosomes sont étudiés comme vecteurs potentiels pour l'administration de médicaments. Grâce à leur capacité naturelle à transporter et à délivrer des charges à des cellules spécifiques, les exosomes sont particulièrement adaptés à l'administration de molécules thérapeutiques, telles que les petits ARN interférents (siRNA), les protéines et les médicaments.
Une quantification précise des exosomes est essentielle dans le développement thérapeutique afin de garantir l'administration de la dose appropriée.L'administration de médicaments à base d'exosomes offreplusieurs avantages par rapport aux systèmes d'administration traditionnels, notamment :
- Biocompatibilité: les exosomes étant d'origine naturelle, ils sont moins susceptibles d'être immunogènes ou toxiques que les nanoparticules synthétiques.
- Spécificité de la cible: les exosomes peuvent être conçus pour transporter des charges thérapeutiques vers des types de cellules ou des tissus spécifiques, améliorant ainsi l'efficacité du traitement.
Les exosomes font également l'objet de recherches en vue d'une utilisationdans la thérapie génique. En chargeant les exosomes avec du matériel génétique, tel quedes composants siRNA ou CRISPR, les chercheurs peuvent modifier de manière sélective les gènes dans les cellules cibles. Cette précision dans l'administration des gènes fait des exosomes un outil puissant dans le développement de la médecine personnalisée.
Orientations futures en matière de quantification des exosomes
Le domaine de la quantification des exosomes évolue rapidement, avec le développement constant de nouvelles techniques et de nouveaux outils visant à améliorer la sensibilité, la spécificité et le débit. À mesure que les chercheurs continuent d'explorer le potentiel thérapeutique et diagnostique des exosomes, la demande pour des méthodes de quantification plus précises et évolutives ne fera que croître.
L'une des tendances les plus prometteuses dans la recherche sur les exosomes est l'intégrationde l'apprentissage automatiqueet de l'intelligence artificielle (IA) dans l'analyse des données. En exploitant les algorithmes d'IA, les chercheurs peuvent analyser de grands ensembles de données issus d'études sur les exosomes et identifier des schémas qui ne sont pas visibles à l'œil nu. Ces informations pourraient mener à la découverte de nouveaux biomarqueurs ou cibles thérapeutiques liés aux exosomes.
De plus, les progrèsréalisés dans le domaine des technologies microfluidiques devraientrévolutionner l'isolation et la quantification des exosomes. Les dispositifs microfluidiques permettent de manipuler avec précision de petits volumes de fluide, ce qui facilite l'isolation rapide et efficace des exosomes à partir d'échantillons biologiques. À mesure que ces technologies deviendront plus accessibles, elles joueront probablement un rôle central dans les futures recherches sur les exosomes.
Conclusion
La quantification des exosomes est un domaine en pleine expansion qui joue un rôle essentiel dans les applications diagnostiques et thérapeutiques. La mesure précise de la concentration, de la taille et du contenu des exosomes est essentielle pour garantir la reproductibilité, la cohérence et la sécurité dans la recherche et le développement de médicaments. Si les méthodes traditionnelles telles quel'analyse par suivi des nanoparticules (NTA)et la cytométrie en flux restentpopulaires, les technologies émergentes telles que le système Aura offrent une détection orthogonale avec une sensibilité et une efficacité optimales, en particulier pour détecter les agrégats d'exosomes et ne nécessitent qu'un volume d'échantillon minimal. Les développeurs doivent être conscients de la stabilité biophysique de leurs thérapies à base d'exosomes afin de garantir la sécurité des patients et l'efficacité des médicaments.
Les exosomes recèlent un immense potentiel dans la médecine moderne, offrant des outils de diagnostic non invasifs et des systèmes d'administration de médicaments hautement spécifiques. Cependant, pour exploiter ce potentiel, il est nécessaire d'adopter des techniques et des outils de quantification avancés. En tirant parti des dernières avancées, les chercheurs et les sociétés pharmaceutiques peuvent repousser les limites de la recherche sur les exosomes et développer de nouvelles thérapies qui transformeront les soins de santé.
À mesure que le domaine continue d'évoluer, les innovations en matière de quantification des exosomes conduiront sans aucun doute à de nouvelles avancées dans le domaine du dépistage des maladies, de la médecine personnalisée et des thérapies ciblées. Les chercheurs et les développeurs pharmaceutiques qui adoptent ces technologies seront bien placés pour mener la prochaine vague d'avancéesdans le domaine des biothérapies.
Références
- Zhang Y, et al. Cell Biosci. 2019;9:19. doi: 10.1186/s13578-019-0282-2.
- Lai JL , et al. Adv Sci (Weinh). 2022;9(15):2103222. doi: 10.1002/advs.202103222.
Sujets populaires
ACQUITY QDa (17) bioanalyse (12) produits biologiques (17) biopharmacie (49) biopharmaceutique (58) biothérapeutiques (21) étude de cas (18) chromatographie (14) conformité (12) intégrité des données (23) analyse alimentaire (12) HPLC (15) LC-MS (26) chromatographie liquide (LC) (24) détection de masse (16) spectrométrie de masse (MS) (58) développement de méthodes (13) analyse des particules (19)


