获取正确的脂质纳米颗粒配方,确保有效的药物递送
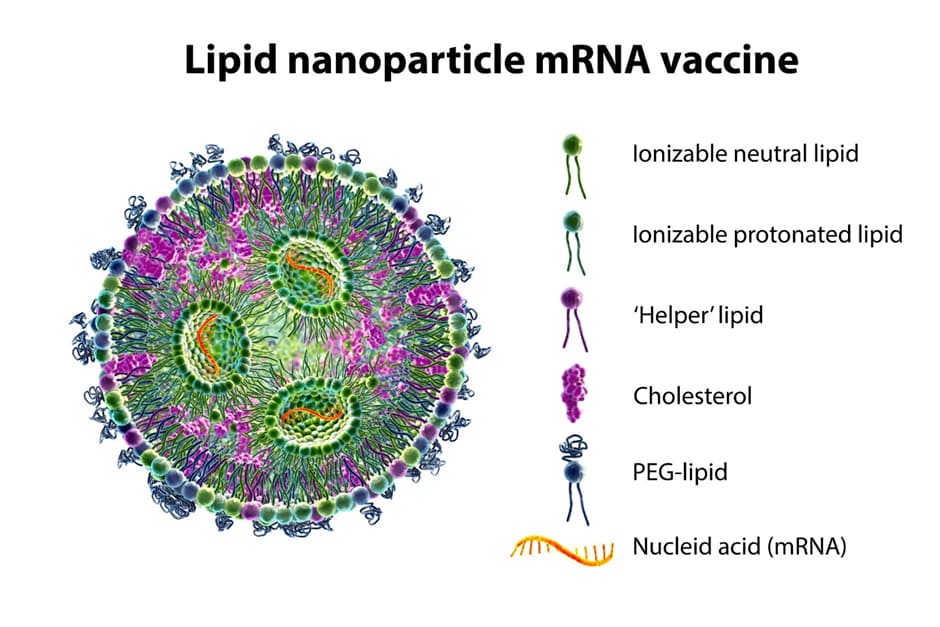
在抗击新冠肺炎的斗争中,一项技术正悄然改变着我们对抗这种致命病毒的方式——脂质纳米颗粒(LNPs)。
这些微小的囊泡是遗传物质的理想载体,能够将其包裹并直接运送至细胞内部。它们如同保护屏障,既能防止信使RNA在体内降解,又能确保其精准递送至细胞内的特定位置。

在COVID-19疫苗的背景下,由脂纳米颗粒(LNPs)携带的信使RNA(mRNA)会指导人体细胞产生冠状病毒(SARS-CoV-2)表面的刺突蛋白。这一过程能触发免疫反应而不引发疾病,从而使人体在遭遇真实病毒时做好防御准备。
这种对纳米脂质体(LNP)制剂的创新应用,已成为莫德纳和辉瑞公司开发mRNA新冠疫苗的关键技术。其广受欢迎的原因显而易见:
- 它们将遗传物质封装在亚微米级大小的脂质囊泡内。
- 它们能够运送大型生物有效载荷。
- 它们具有低免疫原性,可降低不良免疫反应的风险。
- 它们适用于大规模生产工艺,能够实现疫苗的快速生产。
然而,与所有生物制剂一样,LNP制剂可能存在物理不稳定性,形成聚集体并产生沉淀。 subvisible particles (SVPs)因此,需要对LNP进行适当的配方设计,并对其物理和化学稳定性进行评估。
脂质纳米颗粒(LNP)的稳定性指其在时间推移中维持结构完整性、防止降解或聚集的能力。这类由磷脂、胆固醇等脂质构成的纳米颗粒广泛应用于药物递送、基因治疗及诊断等领域。确保LNP稳定性对保障其在这些应用中的高效安全性能至关重要。 LNP的稳定性受脂质组成、粒径、表面电荷及环境条件等因素影响。研究人员正持续探索增强稳定性的新策略,包括使用稳定剂、优化配方参数及表面修饰技术。理解并提升LNP稳定性,对开发高效可靠的纳米药物和生物医学技术具有重要意义。
重新定义LNP配方:背景化膜成像的强大功能
美国药典787和788标准中的亚可见颗粒检测是评估脂质纳米颗粒制剂的关键流程。然而,788标准中的方法1(即光遮蔽法)被认为不适用于测量脂质体和胶体悬浮液等复杂溶液。该局限源于光遮蔽法无法有效处理复杂基质。 因此,USP 788建议采用膜显微镜法(药典方法2)来测量脂质体制剂。
背景膜成像(BMI)作为膜显微镜技术的现代形式,以其在高通量、小体积条件下表征亚可见颗粒的卓越效能而备受瞩目。 Aura System 采用该方法,利用BMI在全面高效的颗粒表征方面的能力。
理解脂质纳米颗粒配方与应力对产品稳定性的影响
应力因素(包括温度、pH值及机械力的变化)会显著影响生物制药产品的稳定性,可能导致蛋白质聚集,从而损害产品的疗效与安全性。
例如,显著的热应力会破坏脂质体制剂的结构,增加脂质纳米颗粒(LNP)的溶解度,从而导致膜上捕获的不溶性颗粒减少。相反,冻融过程会产生更多不溶性LNP聚集物,增加BMI检测中的亚可见物计数,其行为与大多数蛋白质制剂中热诱导聚集类似。
在最近的一次 study我们分析了两个脂质纳米颗粒样本,每个样本分别配制在不同的缓冲液中。随后,这些样本被置于温度和冻融应力条件下进行测试。 奥拉GT系统 并采用SYBR™ Gold Assay(赛默飞世尔科技)来表征应力作用下脂质纳米颗粒样品中的核酸逃逸现象,并定量分析其稳定性和纯度。
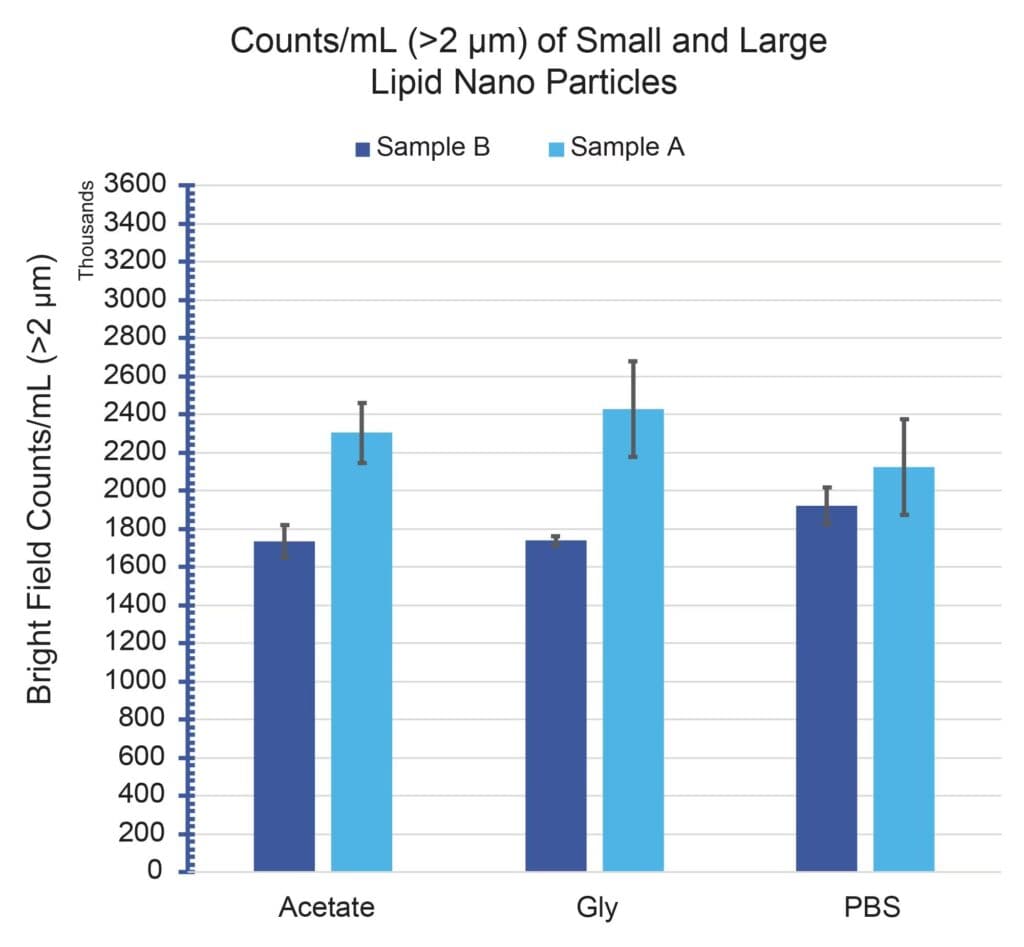
Figure 1 shows the >2 μm/mL subvisible particle concentrations for Sample A and Sample B formulated in three separate buffers: acetate, glycine and PBS. All particle measurements showed significant particle concentrations (>1.5E6/mL) across all conditions, with good repeatability (CVs <15%). In addition, both samples exhibited subvisible particle formation that remained consistent and did not vary beyond measurement uncertainty with buffer type.
核酸释放与应力样本覆盖率之间的关联
即使使用知名商业开发商的样品,准确预测脂质纳米颗粒(LNP)药物的质量也颇具挑战。每种配方都有其独特的颗粒分布特征,LNP配方也不例外。这在亚可见颗粒的稳定性研究中是一个普遍现象。
通过荧光膜显微镜(FMM)技术应用SYBR Gold检测试剂,Aura GT系统在高通量、小体积检测中同时评估样本的稳定性和纯度,从而解决这一难题。该系统能够在更早阶段实现精确的脂纳米颗粒表征,覆盖从初期研发直至最终产品放行的全过程。
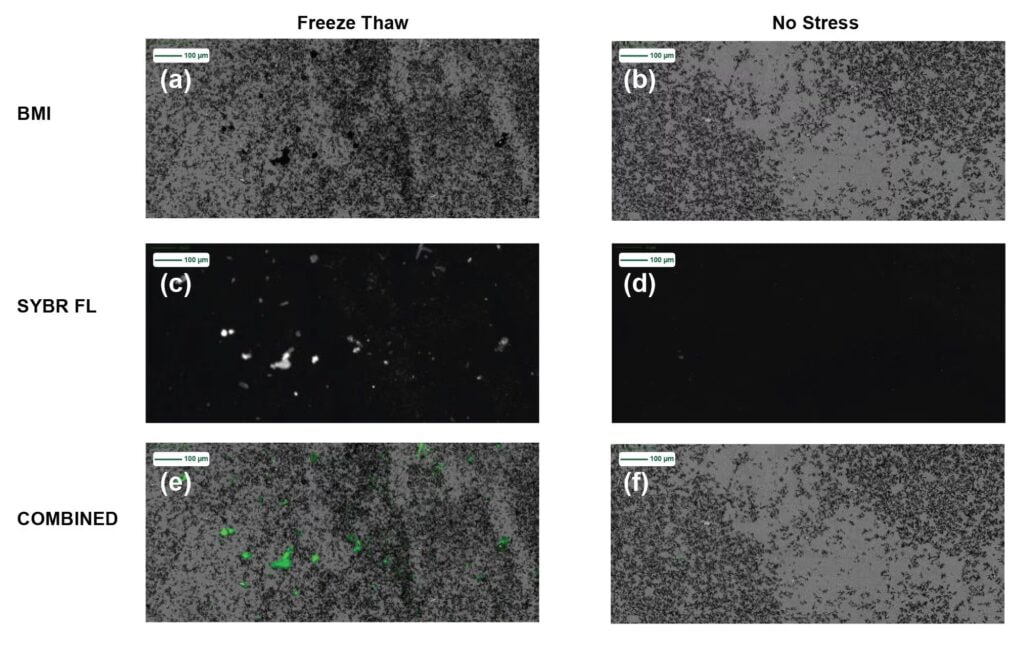
在图2中,我们深入观察了样品A在施加应力前及冷冻-解冻后的亚可见粒子图像。 经冻融处理的膜样本图像以三种成像模式呈现:(2a)BMI成像、(2c)SYBR Gold检测荧光成像以及(2e)BMI与SYBR Gold检测荧光的复合图像;而未受应力样本的图像则分别以(2b)BMI成像、(2d)SYBR Gold检测荧光成像以及(2f)BMI与SYBR Gold检测荧光的复合图像形式展示。
两组BMI膜图像均显示未受应力和受应力类型存在显著的亚可见颗粒形成。使用SYBR Gold试剂对未受应力和冷冻解冻样本进行染色后,受应力样本呈现大面积强荧光信号,表明存在被核酸物质包覆的不溶性样本;而未受应力样本则未见荧光信号。
正确LNP制剂的重要性
冻融循环会显著增加亚可见颗粒的形成,而热应力则能显著降低两种样本中的亚可见颗粒浓度。相较于蛋白质制剂,这种热应力效应看似非传统。但考虑到脂质纳米颗粒(LNP)的组成,并结合文献研究,我们得以理解这一现象:强烈的热应力会破坏脂质体制剂结构,提高LNP溶解度,从而减少膜上捕获的不溶性颗粒。
另一方面,冻融过程会产生更多不溶性聚集体,从而增加亚可见颗粒计数(如BMI所示),其行为与大多数蛋白质制剂中热诱导的LNP聚集体相似。 亚可见颗粒稳定性的核心规律在于:每种制剂均呈现独特的颗粒特征,脂质纳米颗粒亦不例外。另一关键数据点是:经冻融处理的脂质纳米颗粒在SYBR Gold染色检测中呈现显著信号,而未受应力的样本则无此现象,表明此类应力条件下存在独特的核酸渗漏或破裂行为。
总结
利用脂质纳米颗粒作为药物递送技术是一个精密的过程,需要最佳配方配合严谨评估,以确保其疗效不受影响。
低体积、亚可见粒子的测量必须精确进行,才能正确评估脂质纳米粒子的稳定性。然而,传统方法可能无法满足您所需的精度、速度或灵活性。
Aura GT 该系统解决了这些难题,为脂质纳米颗粒(LNPs)的亚可见颗粒分析提供了从早期研发到产品放行的完整解决方案。
参考文献
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9238147/
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8604799/
- https://www.nature.com/articles/s41422-022-00647-5
- https://www.waters.com/nextgen/global/library/application-notes/2025/accurate-particles-characterization-in-lipid-nanoparticle-therapies.html
- https://www.sciencedirect.com/science/article/abs/pii/S0022354921005001


