Identificación de los atributos críticos de calidad en los medicamentos: la clave para garantizar terapias seguras y eficaces.
En la fabricación de medicamentos, no hay margen para el error. Cada paso y cada proceso deben gestionarse cuidadosamente para garantizar que el producto farmacéutico final sea seguro y eficaz. Un concepto clave que desempeña un papel fundamental es el de los atributos críticos de calidad (CQA), la base del control de calidad (QC).

En este blog, analizamos qué son los atributos críticos de calidad, su papel fundamental en el desarrollo de fármacos, y destacamos cómo nuestra tecnología de análisis de partículas de vanguardia contribuye a identificar y analizar estos atributos.
Comprensión de los CQA de los productos biológicos
¿Qué son los CQA? Un CQA es una propiedad física, química, biológica o microbiológica, o una característica clave, que debe estar dentro de un límite, rango o distribución adecuados para garantizar la calidad deseada del producto.1
Las CQA suelen clasificarse en tres categorías:
- Características físicas:incluyen aspectos como el tamaño y la forma del producto farmacéutico.
- Propiedades químicas:estas abarcan elementos como el nivel de pH y la concentración del fármaco.
- Atributos biológicos:estos incluyen factores como la esterilidad y los niveles de carga biológica en el producto.
El proceso de identificación de los CQA es un paso esencial en el proceso de desarrollo de fármacos, ya que garantiza que el producto farmacéutico final sea consistente, eficaz y seguro para su uso por parte de los pacientes.2 Cualquierdesviación puede influir en la eficacia de un fármaco, lo que podría provocar efectos nocivos para el paciente.
Además, el reconocimiento de los CQA no es solo una buena práctica, sino una obligación reglamentaria. Las autoridades reguladoras, entre ellas la FDA y la Agencia Europea de Medicamentos (EMA), exigen la identificación de los CQA como parte del proceso de desarrollo de medicamentos.³ Estogarantiza que los productos farmacéuticos cumplan con los estándares de calidad necesarios y sean seguros para el consumo.⁴
El papel de los CQA en la calidad por diseño (QbD)
Los CQA son el núcleo del enfoque QbD en el desarrollo farmacéutico. El QbD es una estrategia que parte de objetivos predefinidos y hace hincapié en la comprensión del producto y el proceso basándose en el conocimiento científico y la gestión de riesgos de calidad. En esencia, los CQA desempeñan un papel fundamental en la ejecución de un enfoque QbD exitoso. Contribuyen a garantizar que el producto farmacéutico final sea inocuo y eficaz para los pacientes, y que cumpla con los estándares de calidad necesarios estipulados por los organismos reguladores.
El impacto de la tecnología de análisis de partículas en la identificación de los CQA
En la industria farmacéutica, la tecnología se ha convertido en una poderosa herramienta para detectar y analizar los CQA en los productos farmacéuticos. Una CQA significativa en los productos farmacéuticos que históricamente ha planteado retos es la identificación precisa de partículas subvisibles. Con un tamaño aproximado de 10 µm, la presencia de estas partículas puede causar estragos, desde acortar la vida útil de un producto farmacéutico y obstruir los capilares hasta provocar reacciones inmunitarias potencialmente mortales.
Los métodos tradicionales de análisis de partículas subvisibles han tenido dificultades para identificar con precisión estas partículas, lo que ha dejado partículas invisibles sin controlar y ha puesto en peligro la seguridad de los pacientes. Sin embargo, gracias al Aura Particle Analysis Sistema, este dolor de cabeza pronto será cosa del pasado.
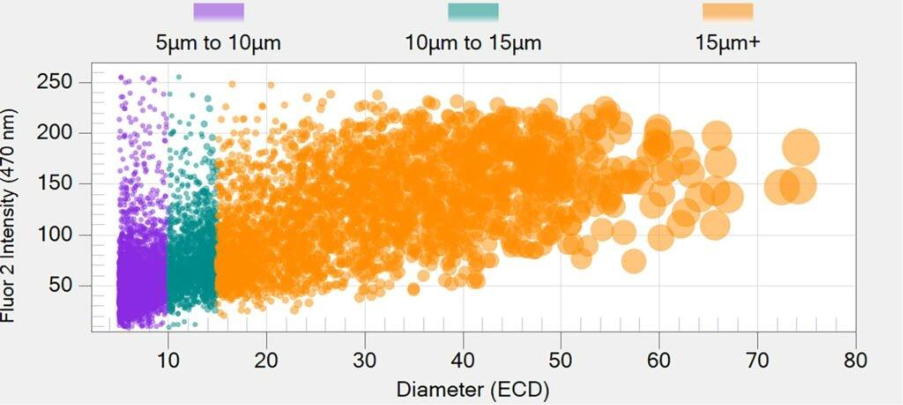
La plataforma Aura aprovecha la imagenología de alta resolución totalmente automatizada para obtener imágenes detalladas de las partículas dentro de una muestra. Permite la detección y cuantificación de partículas subvisibles que oscilan entre 1 y 100 µm, que son CQA en diversos productos biológicos, como vacunas, terapias génicas y anticuerpos monoclonales (mAbs).
Mediante el uso de tecnologías como Backgrounded Membrane Imaging (BMI) y Microscopía de membrana fluorescente (FMM)Aura Systems revela datos críticos sobre partículas subvisibles, incluyendo su recuento, tamaño e identificación. Esto permite obtener resultados más precisos y comprender mejor el medicamento.
Conclusión
Comprender y supervisar los CQA de los medicamentos no solo es beneficioso para la fabricación farmacéutica, sino que es una necesidad. Este proceso clave garantiza que el medicamento final supere los requisitos básicos de eficacia y asegura los más altos estándares de seguridad y calidad para los pacientes.
A medida que la tecnología sigue avanzando, herramientas como la revolucionaria tecnología de análisis de partículas de Waters desempeñarán un papel cada vez más importante en la identificación y el análisis de estos atributos críticos.
Referencias
- https://www.linkedin.com/pulse/benefits-identifying-critical-quality-attributes-cqas-mo-heidaran-2e/
- Departamento de Salud y Servicios Humanos de los Estados Unidos, Administración de Alimentos y Medicamentos, Centro para la Evaluación e Investigación de Medicamentos (CDER). Guía para la industria: Q8(R2) Desarrollo farmacéutico. Noviembre de 2009.
Temas populares
ACQUITY QDa (17) bioanálisis (12) productos biológicos (17) biofarmacéutica (49) biofarmacéutica (58) bioterapéuticos (21) estudio de caso (18) cromatografía (14) cumplimiento normativo (12) integridad de los datos (23) análisis de alimentos (12) HPLC (15) LC-MS (26) cromatografía líquida (LC) (24) detección de masas (16) espectrometría de masas (MS) (58) desarrollo de métodos (13) análisis de partículas (19)


