USP<787>: Tailored Guidance for Better Biologics

Understanding US<787> and its Impact on Pharmaceutical Quality with Tailored Guidance for Biologics
In the world of pharmaceuticals, quality is paramount. Ensuring the safety and efficacy of medications is not only a regulatory requirement but also a moral obligation to patients. To achieve this, regulatory bodies like the United States Pharmacopeia (USP) lay down guidelines and standards that pharmaceutical companies must adhere to. Two such standards, USP<787> and USP<788>, play a crucial role in maintaining the quality of pharmaceutical products, particularly in relation to particulate matter. Let’s delve into what these standards entail and how they compare.
What is USP<787>?
USP<787>, titled “Subvisible Particulate Matter in Therapeutic Protein Injections,” provides guidelines for assessing the presence of subvisible particulate matter in protein-based pharmaceutical products. These particulates, though not visible to the naked eye, can potentially impact product safety and efficacy. USP<787> outlines specific testing methods and acceptance criteria for detecting and quantifying these particulates, helping manufacturers ensure the quality of their protein injections.
Key Components of USP<787>:
- Testing Methods: USP<787> details various analytical techniques for detecting subvisible particulate matter, including light obscuration, microscopy, and flow imaging analysis. Each method has its advantages and limitations, allowing manufacturers to choose the most suitable approach based on their product characteristics.
- Criterios de aceptación:La norma establece criterios de aceptación para las partículas en suspensión basados en el tamaño y la naturaleza de las partículas. Estos criterios son fundamentales para determinar si un producto cumple con los estándares de calidad o si requiere una investigación más profunda y, potencialmente, medidas correctivas.
- Risk Assessment: USP<787> emphasizes the importance of risk assessment in evaluating the impact of particulate matter on product safety and efficacy. Manufacturers are encouraged to conduct thorough risk assessments to identify potential risks associated with particulate contamination and implement appropriate mitigation strategies.
Comparison with USP<788>:
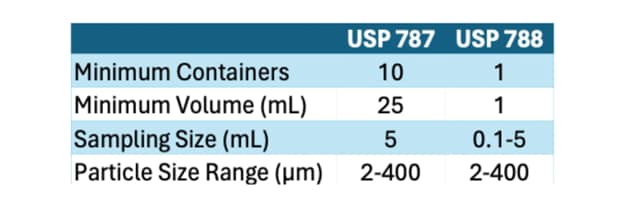
While USP<787> focuses specifically on protein-based pharmaceuticals, USP<788> addresses particulate matter in injections as a whole, encompassing both protein and non-protein formulations. The key differences between the two standards lie in their scope and application:
- Scope: USP<788> is broader in scope, covering all injectable products, including both small-molecule drugs and biologics, whereas USP<787> specifically targets therapeutic protein injections.
- Testing Methods: While both standards prescribe similar testing methods for particulate matter analysis, USP<787> may have additional considerations specific to protein formulations, such as protein aggregation and particle morphology.
- Acceptance Criteria: The acceptance criteria outlined in USP<788> are generally applicable to all injectable products, whereas USP<787> may have more tailored criteria considering the unique characteristics of protein-based formulations.
An important emphasis of USP<787> is that it acknowledges the limitations of light obscuration for protein-based particles and encourages additional methods like microscopy and image analysis for comprehensive characterization.
La importancia del cumplimiento normativo
Adherence to standards like USP<787> and USP<788> is not just about regulatory compliance; it’s about ensuring patient safety and maintaining the reputation of pharmaceutical products. By following these guidelines, manufacturers can mitigate the risks associated with particulate contamination and uphold the quality of their products throughout the manufacturing process.
USP<787> plays a vital role in ensuring the quality and safety of therapeutic protein injections by providing comprehensive guidelines for detecting and assessing subvisible particulate matter. While similar in essence, USP<788> covers a broader spectrum of injectable products, highlighting the importance of understanding the specific requirements applicable to each product type. Ultimately, compliance with these standards is indispensable for pharmaceutical manufacturers committed to delivering safe and effective medications to patients worldwide.
How to Perform USP<787>
In the realm of pharmaceutical quality assurance, the ability to accurately detect and characterize subvisible particulate matter is paramount. One of the primary methods prescribed by USP<787> for this purpose is light microscopy. Let’s explore how light microscopy serves as a vital tool in the analysis of therapeutic protein injections and why its utilization is crucial for pharmaceutical manufacturers.
Ventajas clave de la microscopía óptica
- Caracterización de partículas:La microscopía óptica proporciona información valiosa sobre las características de las partículas, como su tamaño, forma y morfología. Esta información es esencial para evaluar el impacto potencial de las partículas en la seguridad y eficacia del producto.
- Alta resolución: Los microscopios ópticos modernos ofrecen capacidades de imagen de alta resolución, lo que permite examinar con detalle partículas individuales. Este nivel de detalle es crucial para distinguir entre diferentes tipos de partículas y determinar su origen.
- Análisis en tiempo real:a diferencia de otras técnicas analíticas, la microscopía óptica facilita la observación en tiempo real de las partículas, lo que permite tomar decisiones inmediatas durante el proceso de análisis. Este rápido ciclo de retroalimentación es muy valioso para garantizar una detección eficiente y precisa de los contaminantes particulados.
Retos y consideraciones
Aunque la microscopía óptica es una herramienta muy eficaz para el análisis de partículas, presenta ciertas limitaciones y retos que deben abordarse:
- Preparación de muestras:Una preparación adecuada de las muestras es esencial para obtener resultados fiables con el microscopio óptico. Se debe tener cuidado para garantizar que las muestras estén correctamente dispersas y montadas, a fin de facilitar la obtención de imágenes nítidas.
- Habilidades del operador: La interpretación deimágenes microscópicas requiere un cierto nivel de conocimientos y experiencia. Se necesitan operadores capacitados para identificar y caracterizar con precisión las partículas, minimizando el riesgo de interpretaciones erróneas.
- Calibración de instrumentos:Es necesario realizar calibraciones y mantenimientos periódicos de los equipos de microscopía para garantizar mediciones precisas y un rendimiento fiable a lo largo del tiempo.
Microscopía óptica automatizada moderna con sistemas Aura
Con Aura PTx Sistema, todos estos retos y consideraciones quedan resueltos. Sistemas Aura are based on membrane/filter microscopy and are USP<787> compliant. Utilizing high-contrast imaging techniques, Background Membrane Imaging (BMI) and Fluorescence Membrane Imaging (FMM), drug manufacturers can detect, count, and size particulate matter with high confidence and reproducibility:
- Alto rendimiento:reduzca los riesgos de preparación de muestras analizando múltiples muestras. Los sistemas Aura tardan 1 minuto por ensayo.
- Totalmente automatizado con soporte CFR Software: Elimine los errores y sesgos del operador. Los sistemas Aura están totalmente automatizados y capturan datos sin necesidad de que el operador tenga conocimientos especializados. Además, el software Particle Vue identifica, mide y cuenta automáticamente las partículas de una muestra.
- Instrumentación robusta y fiable:los sistemas Aura son instrumentos fiables y de bajo mantenimiento. Para aquellos que requieren mayor atención y servicios, Waters ofrece una variedad de programas de servicio/mantenimiento y cualificación de la instalación/cualificación operativa (IQ/OQ).
The Role of Light Microscopy in USP<787> Compliance
In accordance with USP<787> guidelines, pharmaceutical manufacturers rely on light microscopy as a key tool for assessing the presence of subvisible particulate matter in therapeutic protein injections. By leveraging the capabilities of light microscopy, manufacturers can effectively identify and quantify particulate contaminants, garantizando así el cumplimiento de las normas reglamentarias y manteniendo la calidad de sus productos.
In conclusion, light microscopy and Aura PTx Systems play a pivotal role in USP<787> analysis, offering pharmaceutical manufacturers a reliable means of detecting and characterizing subvisible particulate matter in therapeutic protein injections. Despite its challenges, the benefits of using light microscopy for particulate analysis far outweigh the drawbacks, making it an indispensable tool in the quest for pharmaceutical quality assurance.
Temas populares
ACQUITY QDa (17) bioanálisis (12) productos biológicos (17) biofarmacia (50) biofarmacéutico (59) bioterapéuticos (24) estudio de caso (20) cromatografía (14) integridad de los datos (23) análisis de alimentos (12) HPLC (15) informática (12) LC-MS (27) cromatografía líquida (LC) (25) detección de masas (16) espectrometría de masas (MS) (61) desarrollo de métodos (13) análisis de partículas (21)