Polisorbato 80: análisis de su impacto en la estabilidad de la IgG

A medida que se intensifican las regulaciones sobre seguridad de los medicamentos, los fabricantes deben garantizar que sus formulaciones, como el polisorbato 80, estén libres de partículas visibles y contengan un número limitado de partículas subvisibles de más de 10 µm (según los requisitos de la FDA). Estas partículas no solo se deben a la inestabilidad del proceso, sino también a la degradación de los excipientes de la formulación.
El estrés mecánico durante la fabricación puede provocar la agregación de proteínas, lo que afecta negativamente a la calidad y la seguridad del producto. La agregación suele ser el resultado de interacciones débiles entre zonas hidrofóbicas expuestas de proteínas parcial o totalmente desplegadas. Diversas condiciones, como cambios en el pH, temperaturas elevadas y estrés mecánico adicional, pueden provocar el despliegue de las proteínas, lo que favorece la formación de agregados proteicos.
Por lo tanto, desarrollar fórmulas sólidas que limiten el desdoblamiento y la agregación de las proteínas es clave para garantizar la calidad de los medicamentos proteicos.
Los polisorbatos: un elemento clave en la prevención de la agregación de proteínas
Para evitar la agregación, se utilizan con frecuencia polisorbatos. Estos tensioactivos no iónicos consisten principalmente en ésteres de ácidos grasos de polioxietileno (POE) de sorbitán. La función protectora de los polisorbatos en las formulaciones proteicas ha sido ampliamente estudiada, y se han identificado dos mecanismos principales: (1) los polisorbatos actúan como chaperonas para los sitios hidrofóbicos propensos a la agregación en las superficies proteicas, lo que favorece la estructura plegada, y (2) los polisorbatos compiten con las proteínas en las interfaces, lo que reduce la exposición de estas.
El polisorbato 80 (monooleato de sorbitán POE, PS80) es un tensioactivo muy utilizado en las formulaciones biofarmacéuticas disponibles en el mercado debido a su eficacia para prevenir la adsorción y la agregación de proteínas. Sin embargo, hay un inconveniente: el grado y la calidad del PS80, especialmente durante los procesos que generan estrés mecánico, pueden influir significativamente en la estabilidad de las proteínas, en particular la IgG.
Además, el almacenamiento prolongado del polisorbato a bajas temperaturas puede provocar la formación de partículas de ácidos grasos libres, lo que podría comprometer la eficacia del fármaco. Los métodos de análisis tradicionales, como la oscurecimiento de la luz (LO) y la imagen de flujo (FI), tienen dificultades para identificar las fuentes de degradación. Con el tiempo, pueden volverse susceptibles a la hidrólisis enzimática por las proteínas de las células huéspedes (HCP), lo que da lugar a la formación de partículas visibles y subvisibles que podrían comprometer la eficacia del fármaco.
La realización de análisis de alto rendimiento, sensibles y específicos de las partículas de polisorbato ha resultado difícil debido a su compleja composición química y a los entornos de formulación con bajas concentraciones, lo que lo convierte en un eterno problema de buscar una aguja en un pajar.
Imágenes de membranas en segundo plano utilizadas para explorar la funcionalidad del polisorbato 80
El papel del PS80 en la estabilidad de las proteínas es un tema de debate constante. Además, aún no se comprende bien el impacto del PS parcialmente degradado en la agregación de proteínas. Esto ha llevado a los investigadores a realizar un estudio sobre la funcionalidad del PS80.
En elestudio, se sometió un anticuerpo monoclonal (mAb), IgG, a tres condiciones diferentes de estrés mecánico en presencia de PS80 de grado farmacopea multicompound (MC) y farmacopea china (ChP). Las formulaciones de IgG se complementaron con PS80 parcialmente hidrolizado para investigar el efecto de sus degradantes sobre la estabilidad de las proteínas.
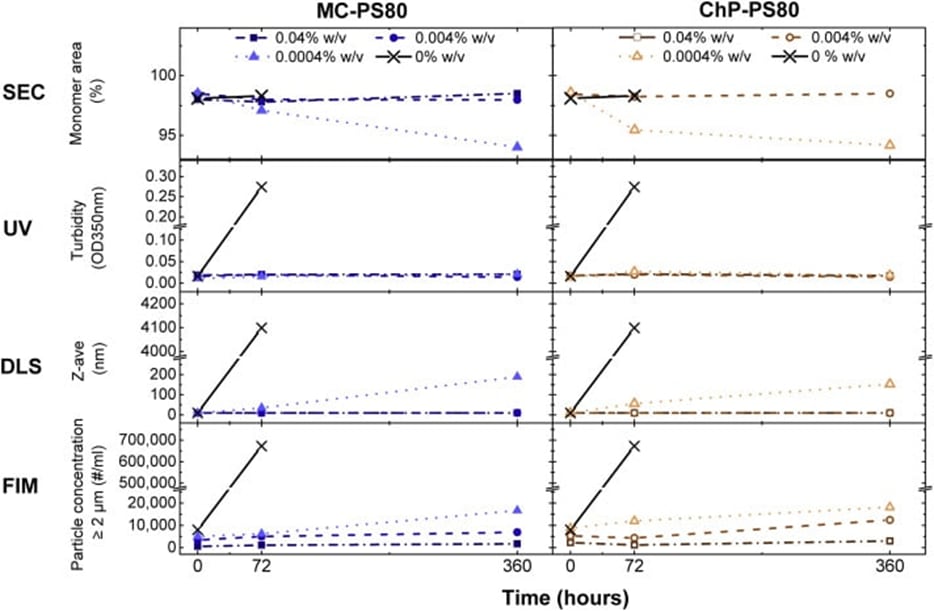
La funcionalidad del PS80 se evaluó midiendo la agregación de proteínas y la formación de partículas inducidas durante el estrés mecánico mediante varios métodos analíticos. Entre ellos se incluyeron: cromatografía de exclusión por tamaño (SEC), dispersión dinámica de luz (DLS), microscopía de imagen de flujo (FIM) e imagen de membrana con fondo (BMI).
Los investigadores utilizaron el Aura Sistema para realizar el BMI para la caracterización y cuantificación de partículas de tamaño micrométrico. En condiciones de flujo laminar de aire, se transfirieron 30 μL de la muestra a una placa de filtro de membrana de policarbonato de 96 pocillos (Waters) con un tamaño de poro de 0,4 μm. Se aplicó un vacío de 350 mbar después de llenar seis pocillos para permitir el flujo de líquido a través de la membrana y el atrapamiento de partículas. Posteriormente, se utilizaron 90 μL de agua altamente purificada para lavar cada pocillo después de la transferencia de la muestra con el fin de eliminar cualquier material soluble. Cada muestra se midió por triplicado.1
El estudio no encontró diferencias significativas en la funcionalidad del PS80 entre los grados MC y ChP en las pruebas de estrés. Sin embargo, a medida que aumentaba el grado de hidrólisis del PS80, se midieron recuentos más altos de partículas subvisibles después del estrés. Además, los niveles más altos de degradantes del PS80 a una concentración constante de PS80 pueden desestabilizar la IgG. Los investigadores concluyeron que los grados MC y ChP del PS80 ofrecían la misma protección, pero que los degradantes del PS80 comprometían la estabilidad de la IgG.
Identificación de partículas de polisorbato de alto rendimiento mediante el ensayo Aura
La degradación del polisorbato da lugar a tres ácidos grasos distintos: ácido láurico, mirístico y palmítico. Estos ácidos crean partículas con características morfológicas únicas que pueden identificarse con precisión utilizando las capacidades de etiquetado y obtención de imágenes del sistema Aura. Mediante la aplicación de BODIPY™ FLC16 ( Thermo Fisher Scientific), un colorante de alta afinidad, los investigadores pueden identificar con precisión los AGL.
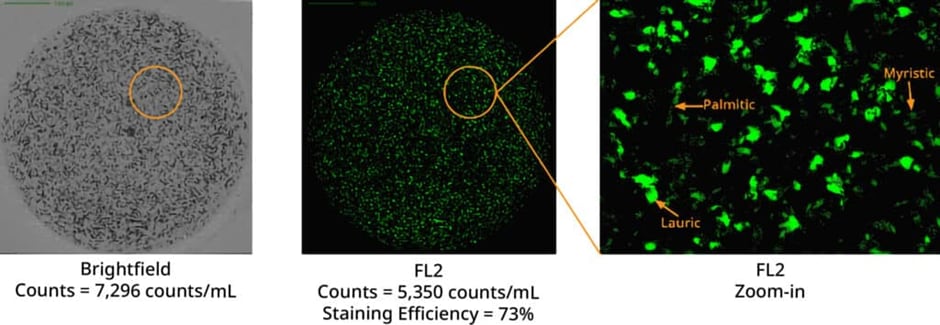
El ensayo de degradación de polisorbato de Aura System agiliza el proceso de detección de excipientes degradados en formulaciones proteicas con concentraciones elevadas. Este método es adaptable, capaz de gestionar una amplia gama de volúmenes de muestra, desde 5 µL hasta 10 mL, y puede analizar simultáneamente hasta 96 muestras para detectar la presencia de partículas de ácido libre. Esta eficiencia reduce significativamente tanto el tiempo como el esfuerzo.
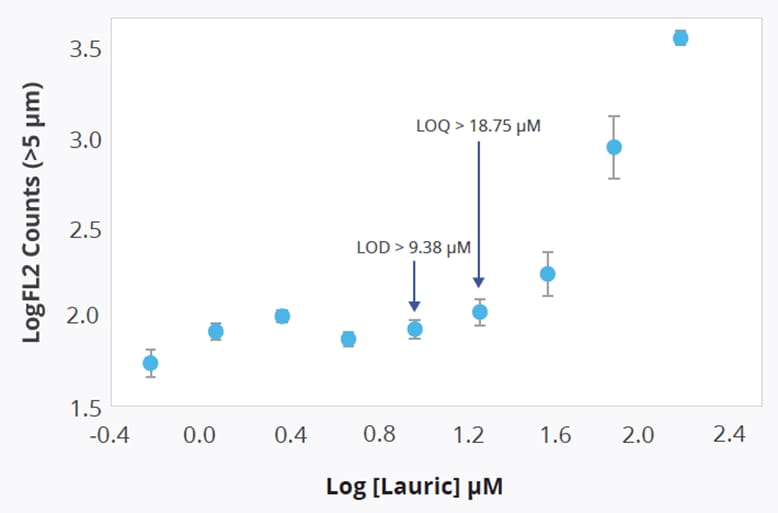
Es importante destacar que el ensayo de polisorbato del sistema Aura es lo suficientemente sensible como para identificar los ácidos grasos libres (AGL) en concentraciones relativas al ácido láurico superiores a 9,38 µM (lo que se traduce en más de 2183 recuentos/ml), y puede cuantificarlos en niveles superiores a 18,75 µM, o más de 2976 recuentos/ml.
Conclusión
Aura El sistema simplifica la detección y distinción de componentes degradados en muestras basadas en proteínas en cualquier punto del proceso de producción de medicamentos. Con solo 5 µL de muestra, este método es específico y sensible, capaz de analizar 96 muestras en cuestión de horas, superando así a otras técnicas alternativas.
Además, esta avanzada tecnología puede identificar y diferenciar partículas degradadas cruciales de la formulación de polisorbato basándose en su forma, apariencia y etiquetado único con BODIPY FLC16, lo que la convierte en una herramienta indispensable.
Referencias
Temas populares
ACQUITY QDa (17) bioanálisis (12) productos biológicos (17) biofarmacéutica (49) biofarmacéutica (58) bioterapéuticos (21) estudio de caso (18) cromatografía (14) cumplimiento normativo (12) integridad de los datos (23) análisis de alimentos (12) HPLC (15) LC-MS (26) cromatografía líquida (LC) (24) detección de masas (16) espectrometría de masas (MS) (58) desarrollo de métodos (13) análisis de partículas (19)


