La oscurecimiento de la luz puede no ser suficiente para detectar SVP en su producto farmacéutico.

¿Sabías que...? subvisible particles (SVP) son la principal causa de retirada de medicamentos del mercado? A pesar de su pequeño tamaño, estas partículas subvisibles tienen un gran impacto en las terapias biológicas, celulares y génicas, ya que no solo limitan la vida útil del producto, sino que también comprometen la seguridad del paciente. Por este motivo, los medicamentos inyectables deben cumplir requisitos estrictos para estar prácticamente libres de SVP, lo que requiere la realización de pruebas de partículas subvisibles, un método utilizado en el control de calidad farmacéutico para detectar y cuantificar partículas que no son fácilmente visibles a simple vista.
Los investigadores necesitan comprender y controlar completamente la estabilidad física en todas las etapas del proceso de fabricación. Hay una serie de factores que contribuyen a la inestabilidad y la agregación de los productos biológicos, entre ellos «el cizallamiento de las operaciones de bombeo, las temperaturas de almacenamiento subóptimas, los ciclos de congelación-descongelación, las interfaces aire-agua y la exposición a diversas sustancias químicas superficiales». Aunque los agregados pueden variar tanto en tamaño como en solubilidad, los esfuerzos actuales se han centrado en las partículas insolubles y subvisibles de entre 1 µm y 100 µm, debido principalmente al hecho de que se ha demostrado que las partículas subvisibles «pueden provocar respuestas inmunitarias indeseadas».
Recently, USP<1788> was revised to update and improve USP<788>, the primary governing standard for particle analysis of injectables. USP<788> provides an overview of two methods that can be used to determine particulate matter: light obscuration (LO) particle count test and microscopic particle count test. Now, in addition to light obscuration and membrane microscopic methods, USP<1788> provides new guidance on the use of flow microscopy for the determination of particulate matter. USP<1788> revision reinforces the idea that complementary, orthogonal tests must be paired with light obscuration when used alone.
Oscurecimiento de la luz frente a recuento de partículas microscópicas frente a microscopía de imagen de flujo dinámico
El contador de partículas LO es un instrumento que utiliza una fuente de luz y un detector para determinar el tamaño y la concentración de partículas subvisibles suspendidas en una muestra determinada. Al pasar la muestra a través de una abertura estrecha, el instrumento mide el grado de bloqueo de la luz causado por las partículas individuales.
La prueba de recuento de partículas LO es actualmente una técnica estándar común para la cuantificación de partículas con tamaños ≥ 10 µm y ≥ 25 µm, aunque también puede medir partículas de hasta 2 µm. Sin embargo, este método tiene algunas limitaciones. No puede contar con precisión las partículas en formulaciones de alta viscosidad y también tiene dificultades para evaluar la información morfológica de las partículas. A menudo, las partículas transparentes y no esféricas no oscurecen eficazmente la luz y, por lo tanto, suelen ser subestimadas por este método.

El método de recuento de partículas microscópicas se considera una técnica adecuada para la medición de partículas subvisibles con el fin de garantizar la seguridad y el control para uso clínico. Se trata de un método de recuento directo que caracteriza cada muestra en su totalidad. Sin embargo, se ha demostrado que tiene un rendimiento bajo y que produce resultados de magnitudes inferiores a los obtenidos mediante la oscurecimiento de la luz.
Un tercer método que los investigadores utilizan cada vez más para cuantificar y caracterizar las partículas subvisibles es la microscopía de imagen de flujo dinámico. Esta técnica captura imágenes dinámicas de las partículas a medida que fluyen a través de una célula y, a continuación, utiliza esas imágenes para calcular el tamaño, la forma, el recuento y otras características morfológicas basándose en un análisis píxel a píxel. Sin embargo, este método también tiene sus propias limitaciones. Los sistemas utilizados tienen un rendimiento relativamente bajo cuando se manejan manualmente, requieren un volumen de muestra elevado, entre 200 y 700 μL aproximadamente, y presentan constantemente problemas de arrastre de partículas, obstrucciones o ensuciamiento de la celda de flujo.
Debido a la importancia que tiene para los investigadores characterize protein aggregates y controlar su presencia en las agencias reguladoras, es necesario que utilicen las herramientas más eficaces para supervisar los niveles de partículas subvisibles con el fin de demostrar el control y la seguridad. Por lo tanto, existe una necesidad crítica de una técnica fiable de alto rendimiento y bajo volumen para el análisis de partículas subvisibles.
La imagen de membrana de fondo ofrece una alternativa de alto contraste.
Imágenes de membrana de fondo (BMI) se desarrolló expresamente como técnica alternativa para la medición de SVP. De forma similar a la prueba de recuento de partículas microscópicas, las partículas subvisibles de una muestra líquida se aíslan en la superficie de un filtro para su análisis mediante recuento con un microscopio. El software BMI, Particle Vue Software, obtiene una imagen de la línea de base antes del aislamiento de las partículas y, a continuación, resta esa línea de base píxel a píxel de las partículas aisladas, de modo que solo queda la información fotográfica del aislado.
Esta técnica se ha desarrollado en Aura System, el primer sistema que permite analizar las partículas tanto en las primeras fases de desarrollo como posteriormente durante el control de calidad. Con Aura System, se puede determinar si una partícula es el resultado del propio fármaco, de un ingrediente del líquido que se ha separado de la solución, de un contaminante externo o incluso de una célula. BMI reinventa la obtención de imágenes de membranas con robótica moderna, procesamiento de imágenes y óptica novedosa en un formato de placa de filtro de 96 pocillos que funciona igual que un lector de placas.
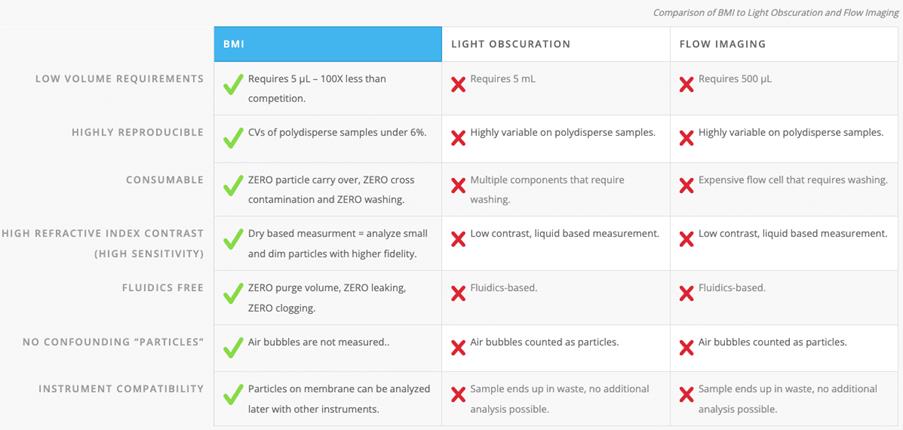
Conclusión
Al desarrollar terapias proteicas, es fundamental comprender y controlar la estabilidad física durante todas las etapas del proceso de fabricación. Los fabricantes de medicamentos no pueden basarse en estándares mínimos cuando lanzan un producto: las partículas deben caracterizarse completamente en cada paso del proceso. Y aunque LO es un método eficaz, los usuarios no deben basarse únicamente en esta técnica. El uso de BMI con LO garantizará que las terapias críticas sean más seguras y se desarrollen más rápidamente, con el fin de ayudar a los pacientes que lo necesitan.
Aura Systems generate accurate USP<788> compliant subvisible particle data, perfectly complementing light obscuration so drug producers have complete coverage of all particles of interest including subvisible particle testing.
Para obtener una caracterización completa de las partículas sin los inconvenientes del LO, cambie hoy mismo al sistema Aura. Más información sobre Aura PTx System.
Temas populares
ACQUITY QDa (17) bioanálisis (12) productos biológicos (17) biofarmacéutica (49) biofarmacéutica (58) bioterapéuticos (21) estudio de caso (18) cromatografía (14) cumplimiento normativo (12) integridad de los datos (23) análisis de alimentos (12) HPLC (15) LC-MS (26) cromatografía líquida (LC) (24) detección de masas (16) espectrometría de masas (MS) (58) desarrollo de métodos (13) análisis de partículas (19)


