Más allá de las impurezas: por qué los productos biológicos actuales necesitan un análisis de partículas más inteligente

El análisis de partículas no es solo un requisito en el desarrollo biofarmacéutico, sino que es un componente crítico que puede determinar la seguridad y la eficacia de su medicamento. Al desarrollar terapias proteicas, se deben definir y supervisar partículas como los agregados de más de 1 µm, mientras que en los sistemas de administración, incluso los propios vehículos (células o virus) se consideran partículas. Ignorar o gestionar incorrectamente este paso pone en riesgo todo, incluida la seguridad del paciente.
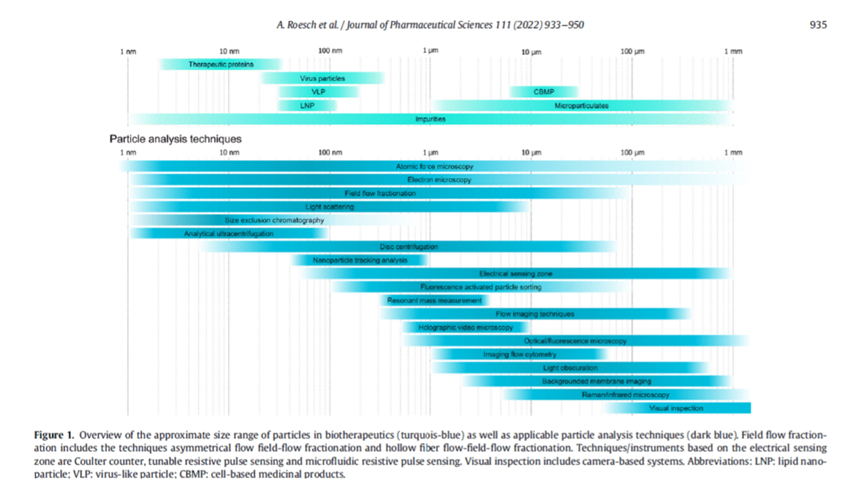
Fuente de la imagen: https://www.sciencedirect.com/science/article/pii/S0022354921006894
Técnicas analíticas en terapias proteicas
En la terapia proteica, las pruebas de liberación suelen implicar una serie de métodos analíticos. Entre ellos se incluyen el análisis de oligómeros mediante cromatografía de exclusión por tamaño (SEC), mediciones de turbidez causadas por partículas submicrónicas o autoasociación reversible, análisis de partículas subvisibles mediante oscurecimiento de la luz (LO) e inspección visual de partículas visibles. Los métodos de partículas submicrónicas se utilizan con frecuencia para la caracterización ampliada de productos y la resolución de problemas, aunque su robustez relativamente baja sigue siendo un reto en las aplicaciones de control de calidad.
Dada la naturaleza diversa de los productos biofarmacéuticos, es importante seleccionar las técnicas analíticas adecuadas. A menudo, es necesario combinar múltiples técnicas complementarias para obtener los resultados más precisos. Además, las características de estos métodos deben evolucionar con las diferentes etapas del desarrollo de los medicamentos para garantizar que se apliquen de forma adecuada en cada fase.
En las primeras fases del desarrollo, los métodos deben centrarse en un bajo consumo de muestras, un alto rendimiento y la automatización. A medida que el fármaco avanza en su desarrollo, se hace más hincapié en las propiedades indicadoras de estabilidad, la solidez y la relevancia estadística de los resultados. Cuando el fármaco alcanza la fase final de desarrollo y las pruebas de liberación, la facilidad de uso en entornos regulados se vuelve fundamental. Para las pruebas de liberación, la atención se centra en los CQA, ya que el producto ya ha sido caracterizado exhaustivamente y se han establecido estrategias de control.
Un artículopublicado recientemente ofrecía información actualizada sobre las técnicas y enfoques analíticos que han surgido en la última década. Los autores también ofrecían una visión general completa de la aplicación del análisis de partículas para los diferentes tipos de productos biofarmacéuticos, incluidas las proteínas terapéuticas y las formulaciones biofarmacéuticas particuladas, como las partículas víricas.
Superar los retos del análisis de partículas submicrométricas
El análisis de partículas ha evolucionado desde centrarse únicamente en las partículas «no deseadas» (como los agregados proteicos) hasta identificar también las partículas «deseadas», como los productos médicos basados en células (CBMP), las partículas similares a virus (VLP), las nanopartículas lipídicas (LNP) y las vacunas. Estos nuevos productos requieren métodos de identificación de partículas más precisos.
A pesar de los avances, el análisis de partículas submicrónicas, especialmente en formulaciones complejas como LNP y VLP, sigue siendo difícil. Las técnicas disponibles para este rango de tamaños son limitadas y se utilizan principalmente con fines de caracterización. A medida que los productos biofarmacéuticos se vuelven más sofisticados, el análisis de partículas debe abarcar una amplia gama de tamaños, desde nanómetros hasta micrómetros, para abordar la complejidad del producto.
Imágenes de partículas de alto contraste para análisis visibles y subvisibles
Para ayudar a superar algunos de estos retos con los métodos actuales, Waters ha desarrollado una técnica de análisis de partículas denominada «imagen de membrana de fondo» (BMI). La BMI utiliza un enfoque automatizado basado en placas de 96 pocillos para el análisis microscópico de partículas de un tamaño superior a 2 mm.
BMI utiliza sofisticadas técnicas de procesamiento de imágenes para analizar imágenes y adquirir datos sobre partículas. En primer lugar, toma una imagen de fondo de la membrana. A continuación, después de filtrar las muestras y capturar las partículas, se vuelve a tomar una imagen de la misma membrana, esta vez con las partículas en la superficie. La imagen de fondo se alinea con precisión con la imagen de la muestra y luego se resta píxel a píxel, de modo que se elimina la textura del fondo y se revelan las partículas. El contraste es 10 veces mayor que el de las mediciones realizadas en líquido, los tamaños se calibran con un microscopio electrónico y el análisis está totalmente automatizado.
Recientemente, BMI ha avanzado hacia la microscopía de membrana fluorescente, que complementa a BMI con opciones de imagen fluorescente.
Conclusión
A medida que los productos biofarmacéuticos siguen evolucionando, aumenta la complejidad del análisis de partículas. La selección de las técnicas adecuadas para el análisis de partículas ya no se limita a la detección de impurezas, sino que ahora incluye la caracterización precisa de componentes esenciales, como CBMP, partículas víricas, VLP, LNP y vacunas. Comprender cómo funcionan los diferentes métodos y elegir la combinación adecuada de técnicas es fundamental para garantizar la seguridad, la calidad y la eficacia de estas terapias avanzadas.
El método BMI de Waters ofrece una solución innovadora para muchos de los retos asociados al análisis de partículas. Al eliminar el ruido de fondo y proporcionar imágenes de alto contraste, el BMI mejora la detección de partículas visibles y subvisibles. Esta técnica automatizada, con su capacidad para manejar un alto rendimiento y proporcionar datos claros y precisos, representa un avance significativo para los desarrolladores de productos biofarmacéuticos. La incorporación del BMI a su estrategia de análisis de partículas garantiza que está utilizando las herramientas más avanzadas para salvaguardar la calidad de sus productos farmacéuticos.
Referencias
1. Partículas en formulaciones biofarmacéuticas, parte 2: Actualización sobre técnicas analíticas y aplicaciones para proteínas terapéuticas, virus, vacunas y células. Roesch, Alexandra et al. Journal of Pharmaceutical Sciences, volumen 111, número 4, 933-950.https://www.sciencedirect.com/science/article/pii/S0022354921006894
Temas populares
ACQUITY QDa (17) bioanálisis (12) productos biológicos (17) biofarmacia (50) biofarmacéutico (58) bioterapéuticos (21) estudio de caso (18) cromatografía (14) cumplimiento normativo (12) integridad de los datos (23) análisis de alimentos (12) HPLC (15) LC-MS (26) cromatografía líquida (LC) (24) detección de masas (16) espectrometría de masas (MS) (58) desarrollo de métodos (13) análisis de partículas (19)


