基于病毒载体的基因治疗药物属于大分子药物制剂,由蛋白质和核酸组分组成,原子数超过200,000个。沃特世的液相色谱(LC)技术结合光学检测(UV、MALS)和质谱分析(MS),可以从不同成分和完整分子层面,准确表征和定量分析这些异质结构及其属性,从而为稳定的病毒载体解决方案提供支持。在病毒载体解决方案工作流程中,常规测定项目包括病毒滴度、聚集体/杂质分析、病毒蛋白比率、肽图分析和修饰分析、封装效率和基因组完整性。
网络研讨会:利用电荷检测质谱(CDMS)连接创新与产业
借助生物制药工作流程专用的waters_connec应用程序和病毒载体解决方案支持完整蛋白质量数分析、序列确认、工艺监测等,加快从样品分析到决策制定的过程。
在病毒载体的分析中,为您的实验室装配Empower色谱数据系统(CDS),获得先进的实验室数据管理功能,包括数据采集、处理和报告功能。
沃特世高柱效的GTxResolve Premier SEC色谱柱可缩短分析时间并减少样品消耗量,支持测定多种属性,包括聚集体和大小异构体分析。
沃特世AEX色谱柱使用无孔的高柱效固定相(例如:Protein-Pak Hi Res Q),回收率更高,结合经过优化的盐梯度,生成一种适用于QC环境的空/满比率测定技术。
使用MaxPeak Premier BEH C4色谱柱结合DFA离子对试剂,鉴定并测定病毒蛋白的相对丰度,获得理想的LC和MS性能。
酰胺基固定相,旨在提高病毒载体、衣壳蛋白和核酸的批间重现性。通过优化应用HILIC分离,可以轻松地将氧化和磷酸化异构体与其未修饰的对应物质分离开来。
使用Waters CSH™色谱柱进行肽图分析,确认病毒蛋白的序列、翻译后修饰(PTM)或降解,这款色谱柱能够在此应用中发挥高分离度。
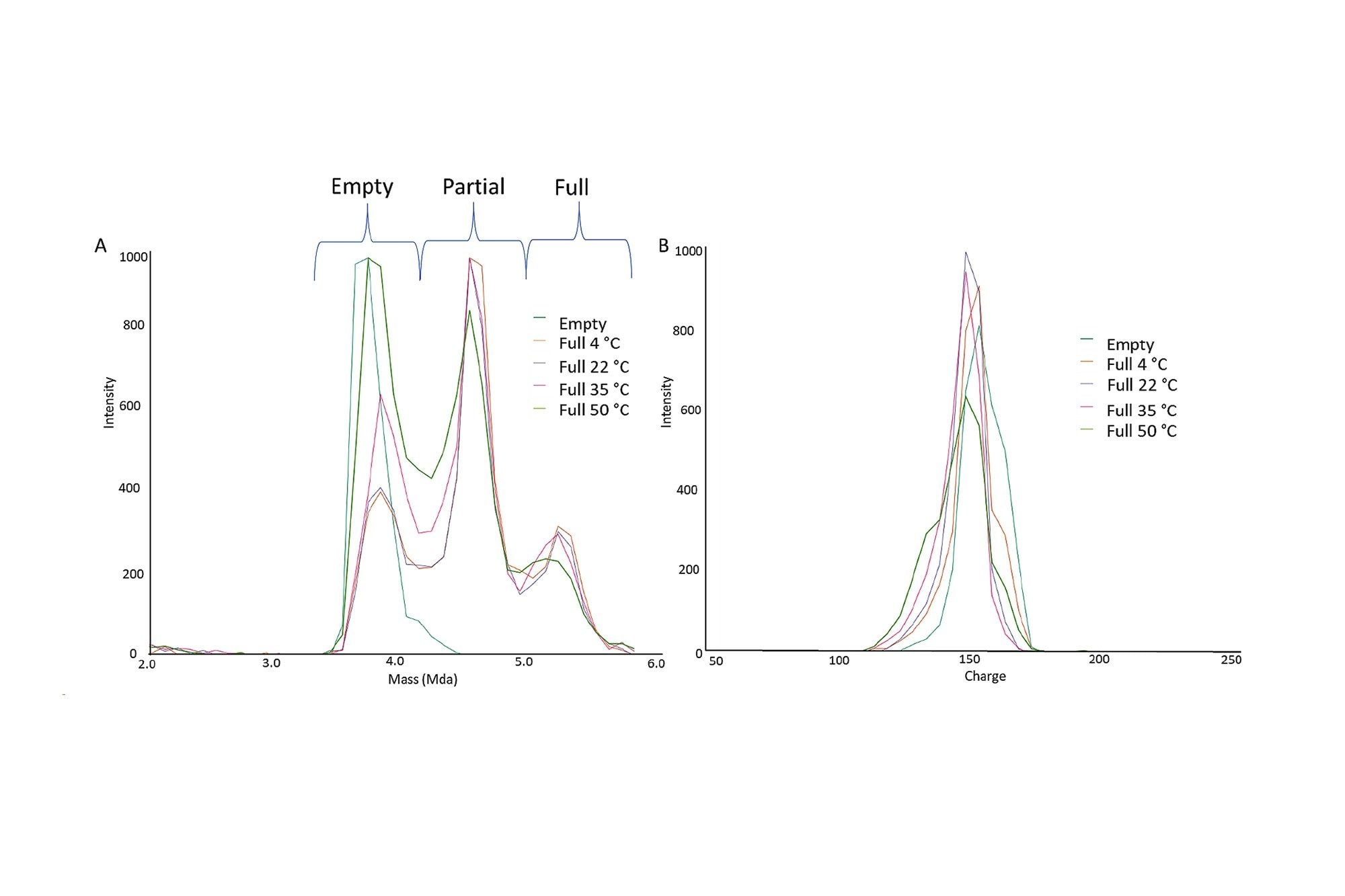
a) AAV8的叠加质谱图,放大到2.5–6 MDa质量数范围,包括100%空衣壳和经过4、22、35和50 ℃下温育30 min处理的满衣壳。b) AAV8的电荷谱图,放大到2.5–6 MDa的质量数范围,包括100%空衣壳和经过4、22、35和50 ℃下温育30 min处理的满衣壳。
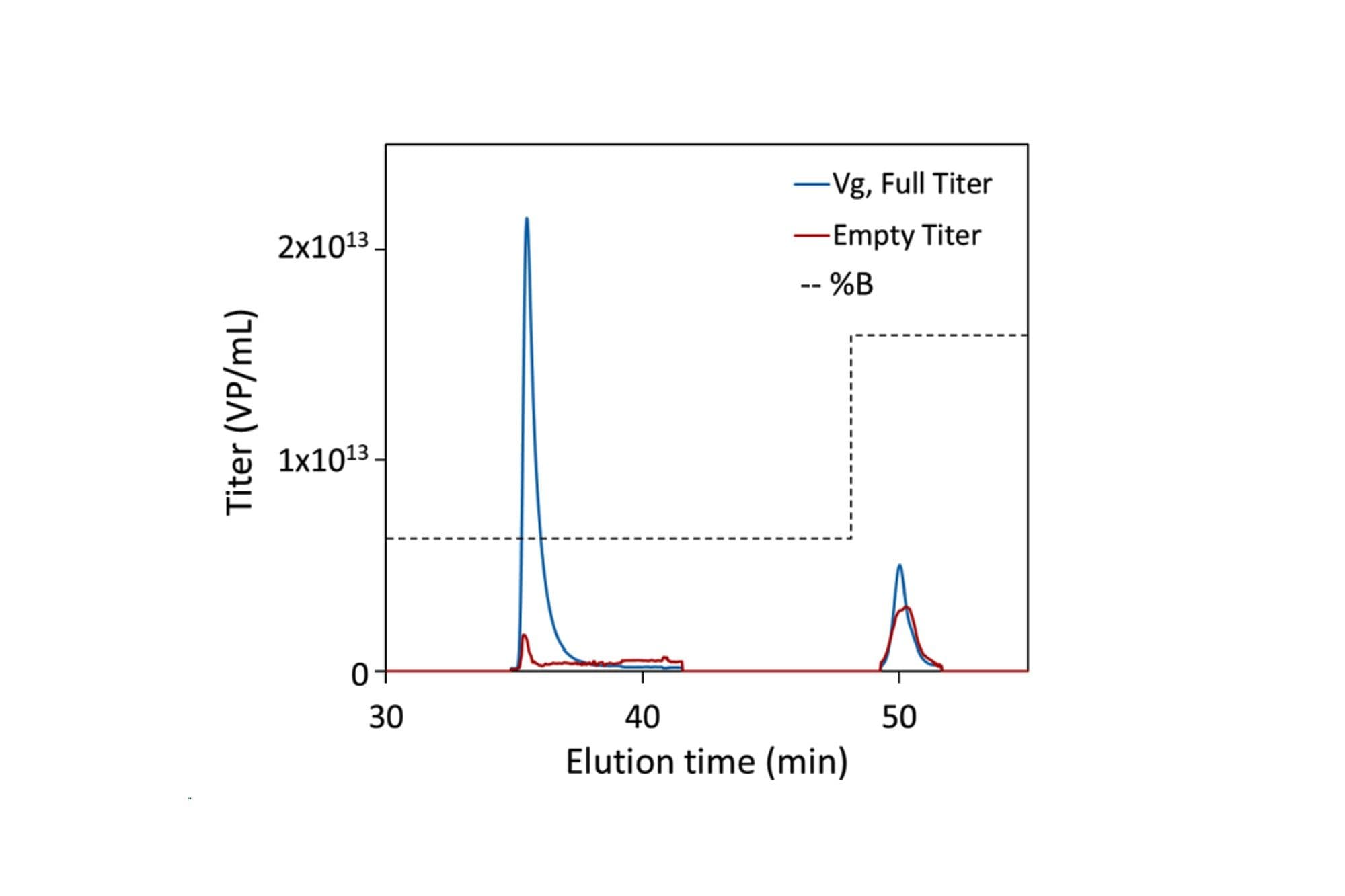
利用RT-MALS确定最终线性梯度中洗脱期间(34-48分钟)和洗脱后(>48分钟)的满衣壳滴度(蓝色)和空衣壳滴度(红色)。缓冲液离子强度用黑色虚线表示。
AAV2色谱图的放大图,分别使用不锈钢硬件(4.6 x 150 mm,5 µm颗粒,红色迹线)和MaxPeak HPS硬件(XBridge Premier GTx BEH SEC 450 Å 2.5 µm 4.6 x 150 mm色谱柱,黑色迹线)。分离使用了含有标准离子强度缓冲液(10 mM磷酸盐pH 7.4 + 200 mM KCl)的流动相。
采用(A) UV和(B) 荧光(FLR)两种光学检测方法测定VP蛋白的相对定量结果。峰注释为所检出成分的归属判定结果以及相对丰度计算结果。采用FLR检测时,VP3的S/N几乎是采用UV检测的5倍,由于UV检测的载样量是FLR的10倍,所以FLR检测使灵敏度得到近50倍的提升。
