Bei Gentherapien auf Basis viraler Vektoren handelt es sich um große Arzneimittelformulierungen, die aus Protein- und Nukleinsäurekomponenten mit über 200.000 Atomen bestehen. Die Flüssigkeitschromatographie (LC) von Waters in Kombination mit optischer Detektion (UV, MALS) und Massenspektrometrie (MS) bietet die analytischen Mittel zur genauen Charakterisierung und Quantifizierung dieser heterogenen Strukturen und ihrer Eigenschaften, sowohl auf Komponenten- als auch auf intakter Ebene, und unterstützt so robuste Lösungen für virale Vektoren. Zu den Routinemessungen in Ihren Workflows für virale Vektoren gehören Virustiter, Aggregat-/Verunreinigungsanalysen, virale Proteinverhältnisse, Peptid-Mapping und Modifikationsanalysen, Verkapselungseffizienz und Genomintegrität.
Webinar: Verbindung von Innovation und Industrie mit Ladungsdetektions-Massenspektrometrie (CDMS)
Beschleunigen Sie den Weg von der Probenanalyse bis zur Entscheidungsfindung mit waters_connect für die Analyse von Biopharmazeutika und Lösungen für virale Vektoren, mit Apps für die Analyse intakter Massen, Sequenzbestätigung, Prozessüberwachung und mehr.
Rüsten Sie Ihr Labor mit dem Empower Chromatographiedatensystem (CDS) aus und profitieren Sie von einem fortschrittlichen Labordatenmanagement für Ihre Analysen viraler Vektoren, einschließlich Aufnahme, Prozessierung und Berichtserstellung.
Gerätesteuerung, Datenerfassung, Analyse und Reporting werden von der ASTRA Software mit dem Modul für die Analyse viraler Vektoren bereitgestellt. Wir bieten eine Plattform-SEC-MALS-Methode, die speziell für die AAV-Quantifizierung entwickelt wurde und für jedes Produkt und jeden Serotyp leicht anpassbar ist.
Ermöglichen Sie die Messung mehrerer Attribute, einschließlich der Analyse von Aggregations- und Größenvarianten, mit den hocheffizienten GTxResolve Premier SEC-Säulen von Waters, die die Analysezeit verkürzen und den Probenverbrauch senken.
Verbessern Sie die Ausbeute dank Waters AEX-Chromatographie, bei der eine nicht poröse, hocheffiziente stationäre Phase (z. B.Protein-Pak Hi Res Q) in Kombination mit optimierten Salzgradienten für eine QC-freundliche Technik für Leer/Voll-Messungen zum Einsatz kommt.
Identifizieren und messen Sie die relative Abundanz von Virusproteinen mithilfe von MaxPeak Premier BEH C4-Säulen und DFA-Ionenpaarreagenz, um eine optimale LC- und MS-Leistung zu erhalten.
Stationäre Amid-Phase, die für eine hohe Batch-zu-Batch-Reproduzierbarkeit von viralen Vektoren, Kapsidproteinen und Nukleinsäuren entwickelt wurde. Oxidierte und phosphorylierte Varianten können mit einer optimal angewandten HILIC-Trennung leicht von ihren nicht modifizierten Gegenstücken getrennt werden.
Bestätigen Sie die Sequenz, die posttranslationalen Modifikationen (PTM) oder den Abbau von Virusproteinen mithilfe von Peptid-Mapping und Waters CSH™-Säulen, die eine hohe Auflösung für diese Applikation liefern.
Optimieren Sie die Produktivität und den Erfolg Ihres Labors mit Waters Global Services, um eine optimale Systemleistung aufrechtzuerhalten, Ausfallzeiten zu minimieren, Applikationsprobleme zu lösen und strenge Compliance-Anforderungen zu erfüllen.
Maximieren Sie Ihre Ressourcen und minimieren Sie das Risiko mit den Zahlungsoptionen von Waters Capital, einschließlich der Aufrüstung veralteter Geräte, der Inanspruchnahme von individuellem Support und der Bündelung von Dienstleistungen in einer monatlichen Zahlung.
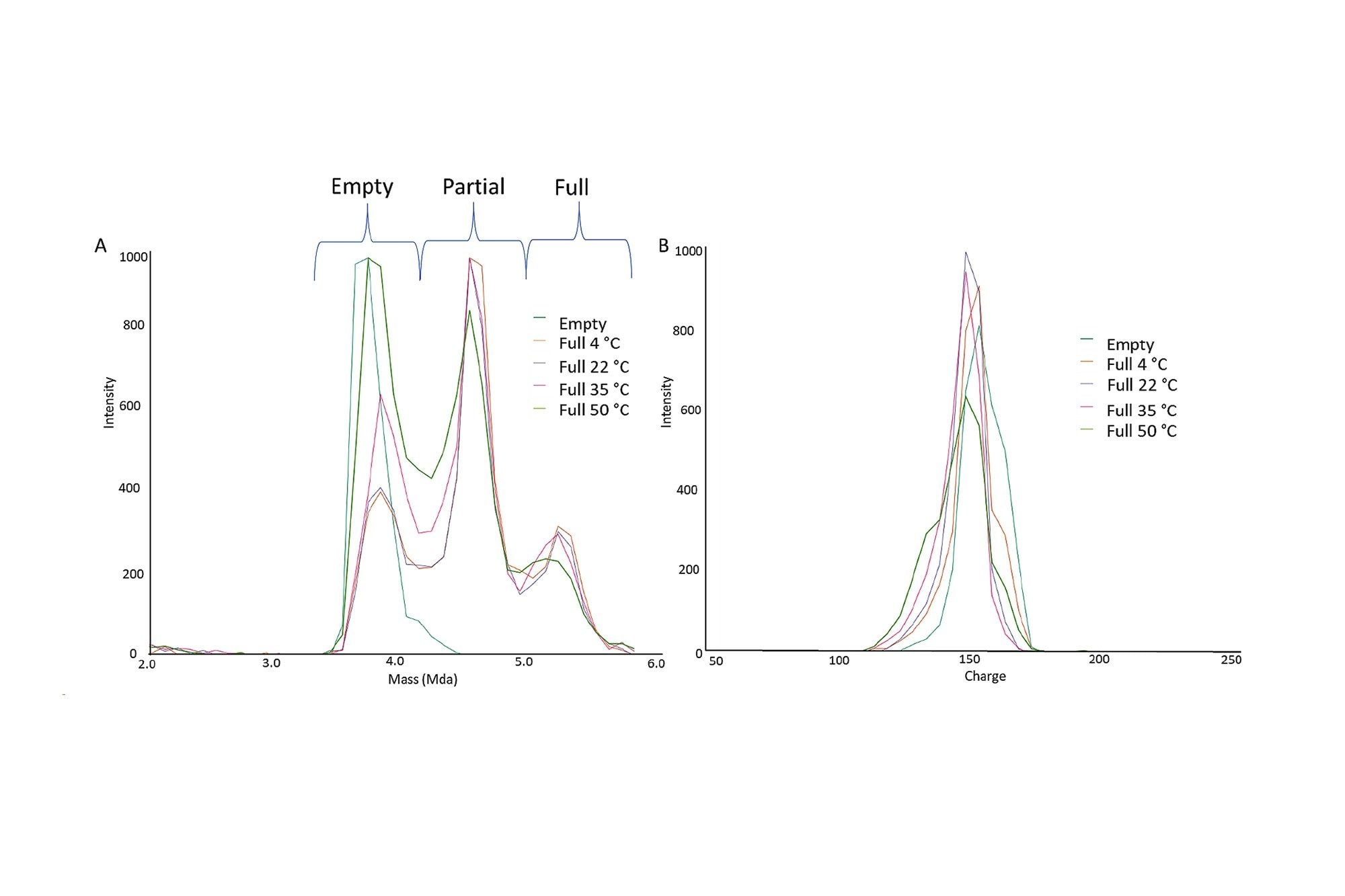
a) Überlagertes Massenspektrum von AAV8, gezoomt auf den Massenbereich von 2,5–6 MDa mit 100 % leerem und vollem Kapsid, behandelt mit 30-minütigen Inkubationen bei 4, 22, 35 und 50 °C. b) Ladungsspektrum von AAV8, gezoomt auf den Massenbereich von 2,5–6 MDa mit 100 % leerem und vollem Kapsid, behandelt mit 30-minütigen Inkubationen bei 4, 22, 35 und 50 °C.
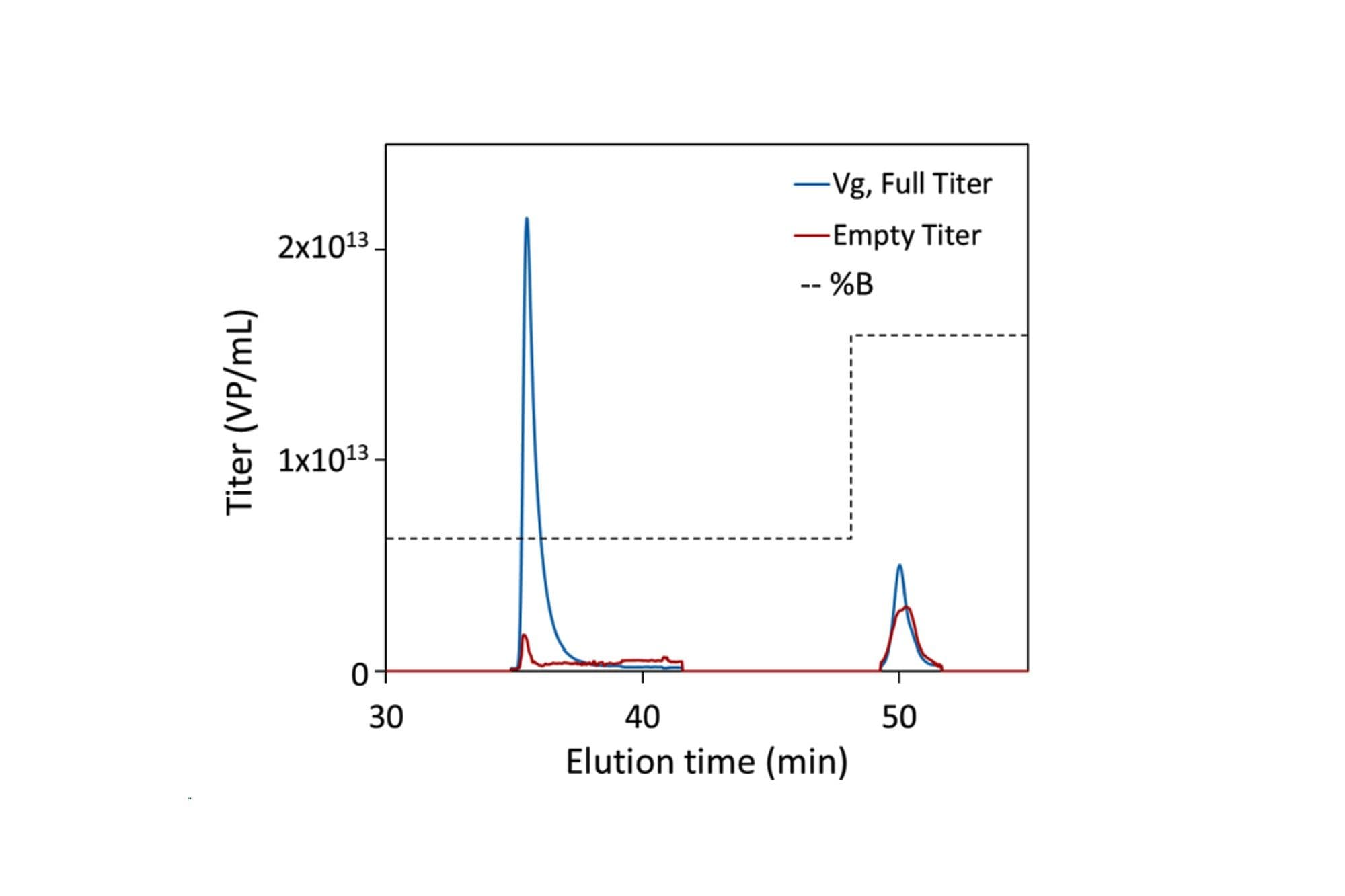
Volle (blau) und leere (rot) Titer, bestimmt durch RT-MALS während der Elution (34 – 48 Minuten) und des Strippings (> 48 Minuten) im finalen linearen Gradienten. Die Ionenstärke des Puffers wird durch die gestrichelte schwarze Linie dargestellt.
Vergrößerte Ansichten eines AAV2-Chromatogramms, das mit Edelstahlhardware (4,6 × 150 mm, 5-µm-Partikel, rote Kurve) gegenüber MaxPeak HPS-Hardware (XBridge Premier GTx BEH SEC 450 Å, 2,5 µm, 4,6 × 150 mm Säule, schwarze Kurve) erhalten wurde. Die Trennungen wurden mit einer mobilen Phase durchgeführt, die einen Puffer mit Standard-Ionenstärke (10 mM Phosphat pH 7,4 + 200 mM KCl) enthielt.
Die relative Quantifizierung der VP-Proteine wurde mittels optischer Detektion gemessen, einschließlich (A) UV und (B) Fluoreszenz (FLR). Die Peakanmerkung zeigt die Zuordnung und die berechnete relative Abundanz der erkannten Komponenten. Bei FLR-Detektion ist das S/R von VP3 fast fünfmal höher als das S/R bei der UV-Detektion mit einer 10-fach höheren Massenladung, was auf eine etwa 50-fache Verbesserung der Empfindlichkeit schließen lässt.
