自動化および標準化された Oasis™ HLB 固相抽出(SPE)アプローチを使用した、血漿からのシタグリプチンおよびパルボシクリブのバイオアナリシス
要約
バイオアナリシスラボでの使用を目的とした頑健な分析法の開発および最適化は、高感度で再現性のあるアッセイ性能を保つために重要です。固相抽出(SPE)は、バイオマトリックスからのターゲット薬物の分離が容易になる、一般的なバイオアナリシスサンプル抽出手法です。SPE 抽出は多くの場合、複雑で最適化が必要なステップが多く、メソッド開発に長時間を要することが多いと認識されています。このアプリケーションノートでは、血漿からの分析種の回収率 >90% が得られる、迅速でシンプルな SPE メソッド開発のための自動 20 ボトル逆相 SPE の最適化戦略を紹介します。このアプローチにより、医薬品シタグリプチンおよびパルボシクリブのバイオアナリシス定量に続いて LC-MS での定量に成功しました。
はじめに
バイオアナリシスは、医薬品の探索および開発における重要な構成要素です。また、ジェネリック医薬品の生物学的同等性の判定においても重要な役割を果たします。これらのラボで実施されるルーチンアッセイには、高い感度、頑健性、再現性が必要となります。これらのアッセイのメソッド開発および最適化も、シンプルで標準化されたものであることが必要です。SPE により、一般にアッセイの選択性、感度、頑健性が向上するため、複雑なマトリックスから対象の分析種を抽出するために SPE がしばしば使用されます。バイオアナリシスアッセイのもう 1 つの重要な要素は再現性です。バイオアナリシスラボでは、日間および日内のばらつきを低減し、研究者が困難な科学的問題、実験計画、データ分析に集中できるようにするために、ますます自動化が進んでいます。
逆相 SPE は、複雑な生物学的マトリックスからの低分子の抽出に適しており、さまざまな分析種について高い回収率が得られます。サンプルの前処理、洗浄、および溶出溶媒の組成を微調整することで、吸着剤ベッドの選択性を対象の分析種に対して最適化することができます。Extraction+ コネクテッドデバイスで構成した Andrew+™ ピペッティングロボットにより、既存の OneLab™ ライブラリーメソッドを使用して、手を使わずに検量線および QC サンプルの完全に自動化した作成および SPE 実行を行うことができます。今回、モデル分析種として医薬品シタグリプチンおよびパルボシクリブのバイオアナリシス定量を行いました。シタグリプチンは、2 型糖尿病の治療に、単独またはメトホルミンと併用して使用されます。パルボシクリブは、HR 陽性かつ HER2 陰性の乳がんの治療に使用される選択的 CDK4/6 阻害剤です。
実験方法
サンプル前処理
Sigma Aldrich(米国、ミズーリ州セントルイス)から入手したシタグリプチンとパルボシクリブのストック溶液(1 mg/mL)を、Sigma Aldrich(米国、ミズーリ州セントルイス)から入手した 100% メタノール中に調製しました。このストック溶液を 5% メタノール水溶液で連続希釈して、10 µg/mL の作業用ストック溶液を調製しました。この 10 µg/mL の作業用ストック溶液を使用して、ラット血漿(BioIVT、米国、ニューヨーク州ウェストベリー)中にキャリブレーションサンプルおよび品質管理(QC)サンプルを調製しました。キャリブレーションサンプル(1 ~ 1000 ng/mL)は 2 回繰り返しで調製し、低、中、高レベルの QC は、それぞれ最終濃度 7.5 ng/mL、75 ng/mL、750 ng/mL で 2 回繰り返しで調製しました。単純連続希釈メソッドを OneLab ライブラリー(単純連続希釈 - OneLab(andrewalliance.com))からダウンロードし、Andrew+ ピペッティングロボットを使用して、検量線および QC ポイントを作成しました。
SPE 抽出
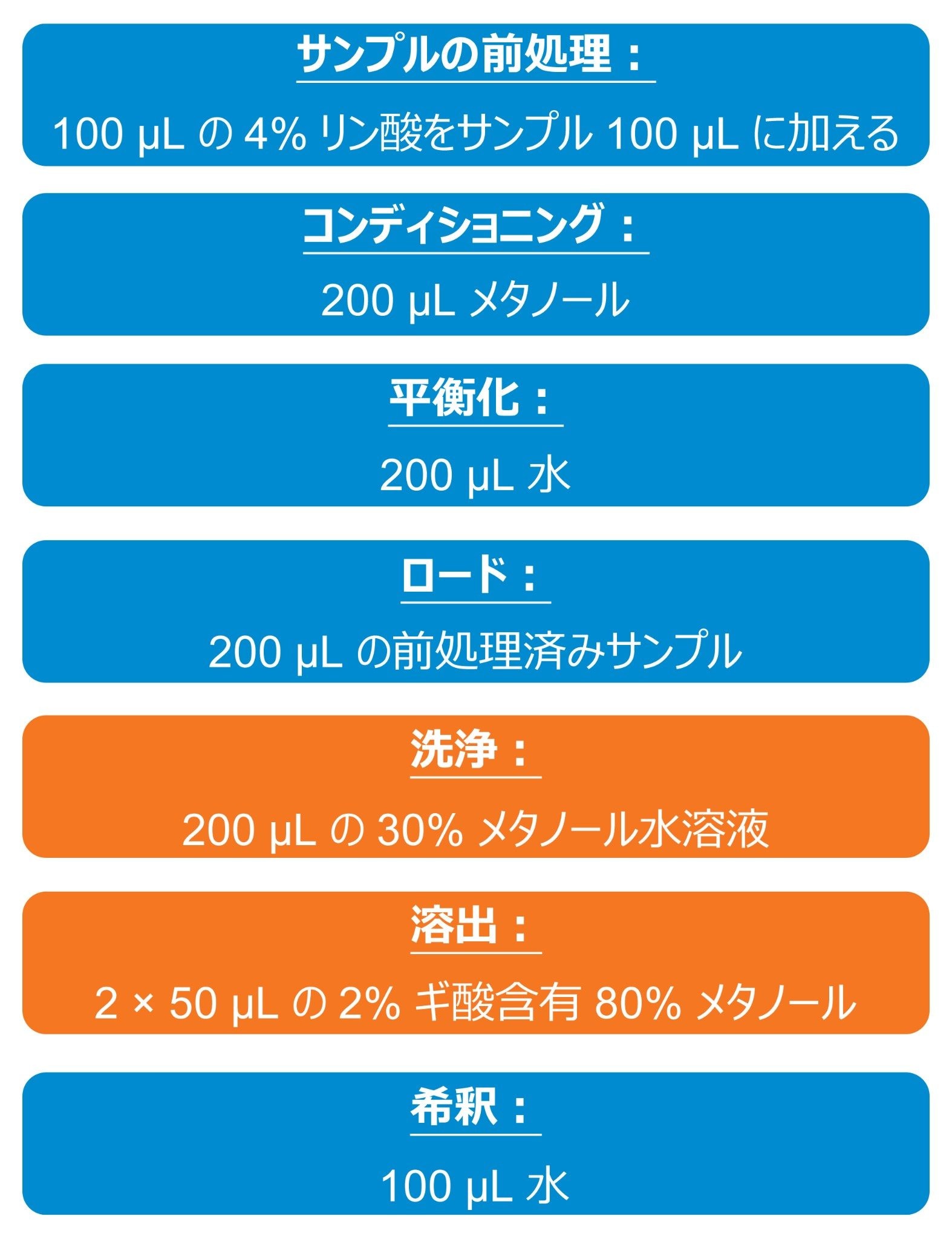
維持管理マニュアル(715000109)および以前のアプリケーションノート(720008001)に記載されている 20 ボトル Oasis HLB SPE 最適化戦略を使用して、シタグリプチンおよびパルボシクリブに最適な SPE における洗浄条件および溶出条件を迅速に評価しました。最終的な SPE プロトコルでは、シタグリプチンおよびパルボシクリブの両方について >90% の回収率が得られています(図 1)。OneLab ライブラリー(自動バイオアナリシス SPE - OneLab(andrewalliance.com))からダウンロードした標準 OneLab メソッドを使用し、Andrew+ ピペッティングロボットによって、すべての抽出ステップを完全に自動化しました。抽出したサンプルを UPLC-MS/MS システムに注入しました。
LC-MS 分析
シタグリプチンおよびパルボシクリブのクロマトグラフィー分離は、ACQUITY™ I-Class UPLC™ および ACQUITY UPLC HSS T3 C18 カラム(100Å 2.1 × 50 mm、1.7 µm)を使用し、3.5 分間で 5 ~ 95 % B(アセトニトリル中 0.1% ギ酸)の汎用グラジエントを使用して行いました。検出は、個々の分析種のマルチプルリアクションモニタリング(MRM)を使用して、Xevo™ TQ-XS 質量分析計(ESI+)で行いました。シタグリプチンおよびパルボシクリブの定量に使用した MRM トランジションは、それぞれ 408.3→174.6 および 448.2→80.5 でした。
結果および考察
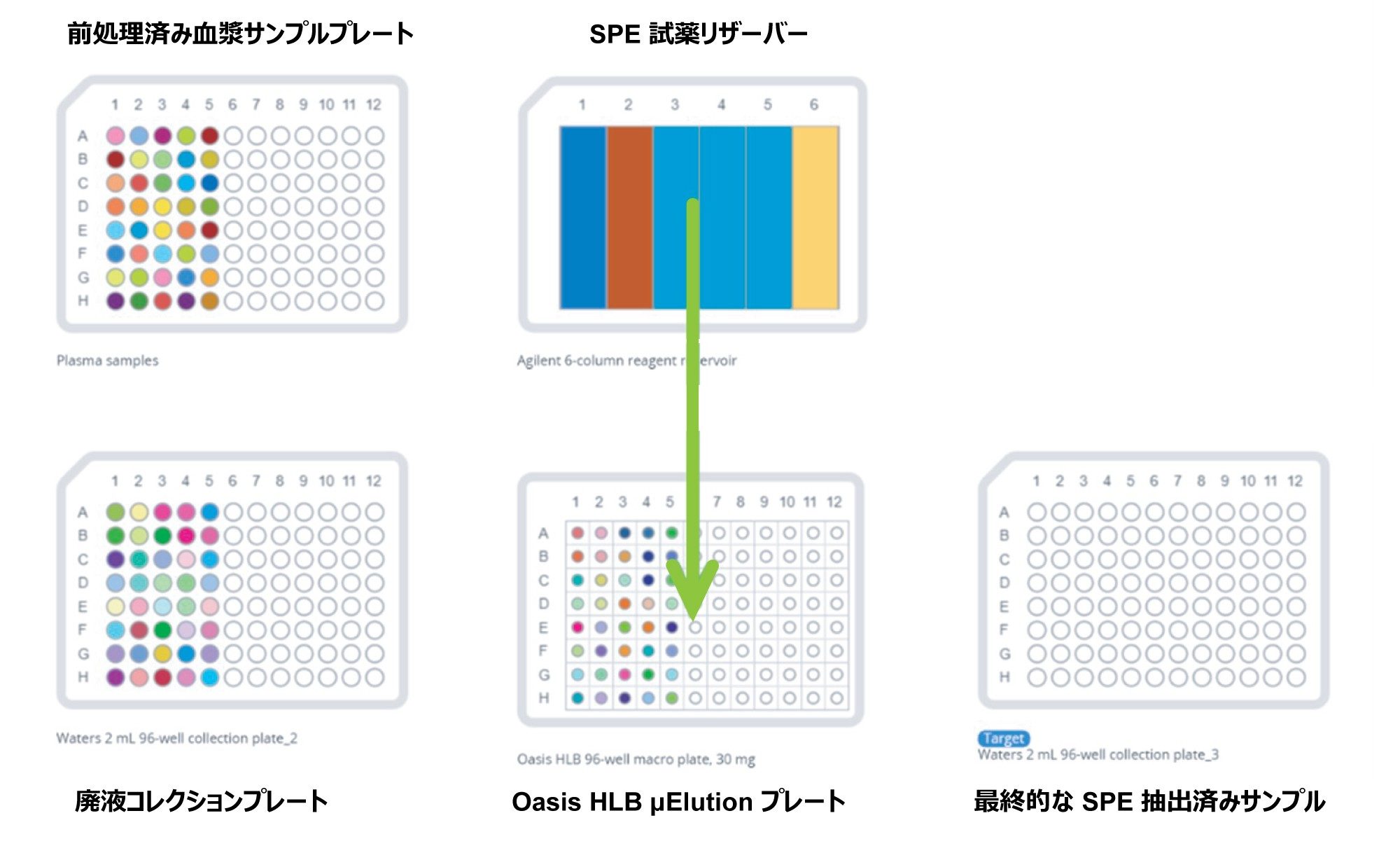
既存の OneLab ライブラリーメソッドを使用し、Extraction+ コネクテッドデバイスを装備した Andrew+ ピペッティングロボットを使用してサンプルを調製し、20 ボトル SPE の最適化および最終的な Oasis HLB SPE 血漿定量実験を行いました。この試験では、OneLab ライブラリーから単純連続希釈メソッドをダウンロードして、検量線および QC の血漿サンプルを容易に調製することができました。自動バイオアナリシス SPE メソッドをダウンロードして、自動化プラットホームで SPE を行いました(図 2)。
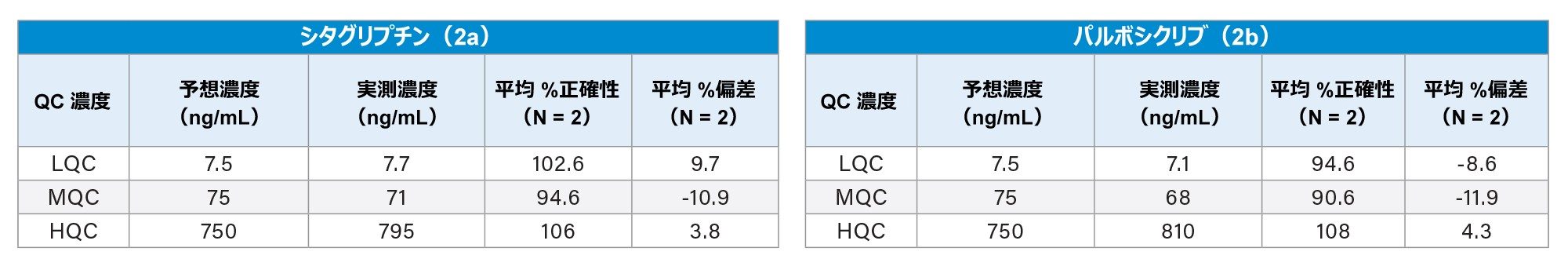
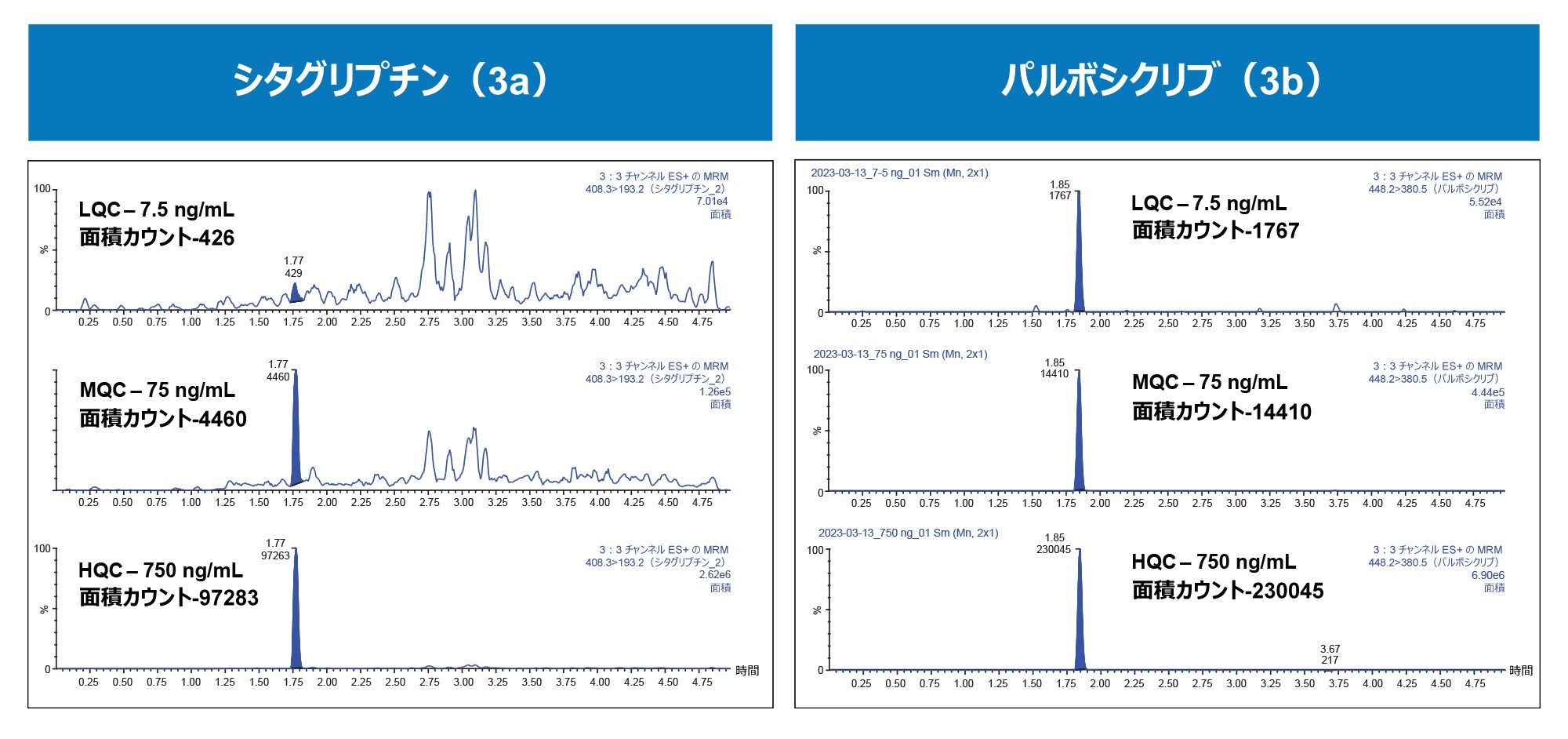
シタグリプチンおよびパルボシクリブの定量性能は、1/x 回帰でリニアダイナミックレンジ 1 ~ 1000 ng/mL(>0.99)と優れており、平均正確性はそれぞれ 92.7% および 94.5% でした。これらの結果を表 1 に示します。シタグリプチンおよびパルボシクリブの QC レベルはすべて、正確性(%)および偏差(+/-15%)というバイオアナリシスメソッドのバリデーション基準に合格していました。QC レベルの平均正確性は 90.6 ~ 108% の範囲で、平均偏差値は -11.9 ~ 9.7 % の範囲です(表 2a および 2b)。代表的な QC クロマトグラムでは、シタグリプチンおよびパルボシクリブの分析種濃度の増加に応じて、MS の面積カウントが直線的に増加していることがわかります。このような性能は、それぞれ図 3 のパネル a および b で明らかです。

結論
バイオアナリシスラボで使用する SPE サンプル抽出および LC-MS/MS 分析法の開発および最適化は、プロトコルが複雑で分析法開発に長時間かかる困難な作業と認識されています。この試験では、高速逆相 Oasis HLB SPE メソッドの最適化のための、完全に自動化した 2 つの実験アプローチに焦点を当てています。Extraction+ コネクテッドデバイスを装備した Andrew+ ピペッティングロボットを使用して、血漿からの分析種の高い回収率を優れた正確性と再現性で実現しています。ラット血漿から抽出されたシタグリプチンとパルボシクリブの定量性能は、リニアダイナミックレンジ 1 ~ 1000 ng/mL、QC 正確性 90.6 ~ 108%、RSD -11.9 ~ 9.7% と優れていました。これらの性能は、低分子 LC-MS 分析法のバリデーションの推奨ガイダンス基準を満たしています。汎用プロトコルと自動サンプル前処理の組み合わせにより、サンプル抽出が大幅に簡素化および合理化され、ラボの生産性が最大化してミスが低減して、バイオアナリシスメソッドの全般的な性能が保たれました。
720007996JA、2023 年 11 月