カラムの再現性の検討:製造時期が互いに離れている 3 つのバッチの 1.8 μm HSS T3 固定相を用いた血清中の内因性ステロイドホルモンの分析
要約
特定のアッセイのための固定相のバッチ間試験は、分析法の頑健性実験として一般的に行われています1-3。 これらの試験を成功させるためには、再現性の高いカラムが不可欠であり、アッセイの使用期間にわたる性能を保証するためにも重要になります。ウォーターズのカラムケミストリーの再現性を実証するため、5 年間にわたって製造された 3 つのバッチで ACQUITY UPLC HSS T3 で内因性ステロイドホルモンの分析を実施しました。保持時間、ピーク面積、ピーク幅、ピーク対称性の %RSD 値が低いことから、HSS T3 固定相の再現性が高く、最も古いバッチと最新のバッチの間でクロマトグラフィー性能の差がほぼ見られないことが分かります。
アプリケーションのメリット
- 製造時期が互いに離れている 3 つのバッチの HSS T3 充塡剤において、バッチ間性能が同等
- 除タンパクして固相抽出したサンプルに対する ACQUITY UPLC HSS T3 カラムでのシグナルおよび検出が向上
はじめに
質の高い製品、特に液体クロマトグラフィー(LC)固定相およびカラムを使用することで、アッセイについて生成されたデータが、時間が経過しても正確で再現性のあるものになります。LC 固定相の品質は、特定のアッセイについてのバッチ間再現性試験によって測定できます。これにより、製造された各ロットの充塡剤が同等に機能することが保証されます。ほとんどのバッチ間試験は、分析法バリデーションキット内の充塡剤など、特定の時期に製造された 3 バッチの充塡剤を使用して行われます。これらの充塡剤は良好に機能しますが、それらを使用して得られるのは、製品の全体的な品質のスナップショットのみである可能性があります。全体像を把握するには、製造時期が互いに離れているバッチをテストする必要があり、これによって製品全体の品質の範囲が改善します。
ACQUITY HSS T3 固定相は、全多孔性シリカ粒子を使用した一般的に使用される C18 結合相です。この相は、疎水性化合物の分離を損なうことなく、従来の C18 よりも極性分析種の保持が高まるように設計されています。この相は、多くのアプリケーションや論文で、剤形中の低分子医薬品からバイオ分析アプリケーションに至るまで、様々な分離に使用されています4-6。 HSS T3 充塡剤の品質を実証するために、3 本のカラムに異なるバッチの充塡剤を使用しました。これらの充塡剤は、2016 年から 2021 年までの 5 年間に製造されたものです。3 本のカラムすべてを使用して、ヒト血清中の内因性ステロイドホルモンを分離し、すべてのカラムにわたるデータの再現性を評価しました。
実験方法
サンプルの説明
ヒト血清は、固相抽出(SPE)と除タンパク(PPT)によって前処理しました。PPT はアセトニトリル(3:1 アセトニトリル:血清)を使用して行いました。サンプルをボルテックス混合して遠心分離し、上清を除いて分析に用いました。SPE は、Oasis HLB 1 cc 30 mg カートリッジ(製品番号:WAT094225)を使用して行いました。吸着剤は、メタノールでコンディショニングし、文献の記載にしたがって水で平衡化しました7。 汎用的な SPE 条件を使用し、100% アセトニトリルを用いて溶出しました。この溶出物を 60 ℃ 窒素下で蒸発乾固し、100 μL の Milli-Q 水で再溶解して分析に用いました。
LC 条件
|
LC システム: |
バイナリーソルベントマネージャー(BSM)、サンプルマネージャーフロースルーニードル(SM-FTN)、および PDA 検出器を備えた ACQUITY UPLC I-Class PLUS |
|
検出: |
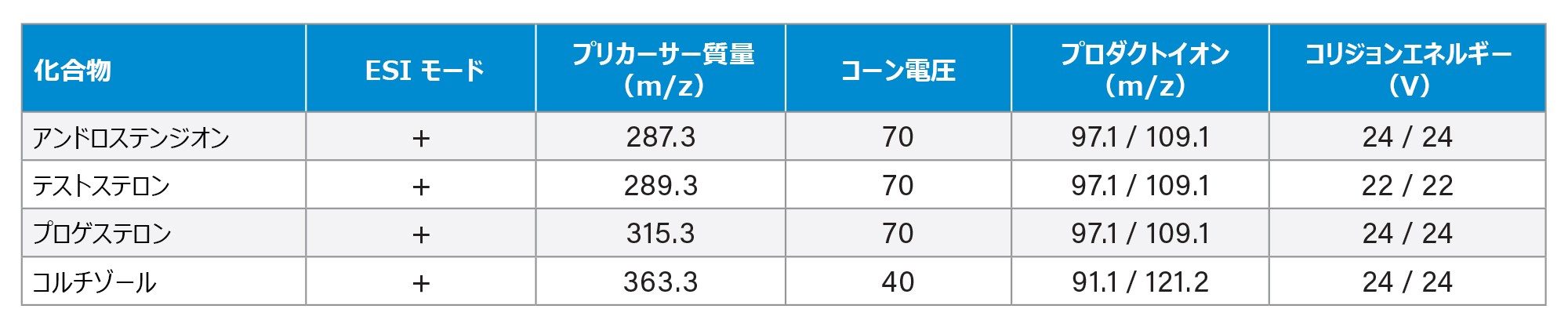
血清ホルモンの MRM は表 1 に記載 |
|
カラム: |
ACQUITY UPLC HSS T3、1.8 µm、2.1 × 50 mm(製品番号 186009467) 3 つの充塡剤バッチ: 189 – 2016 年 10 月に製造 233 – 2019 年 11 月に製造 270 – 2021 年 11 月に製造 |
|
カラム温度: |
30 ℃ |
|
サンプル温度: |
10 °C |
|
注入量: |
5.0 μL |
|
流速: |
0.6 mL/分 |
|
移動相 A: |
0.1% ギ酸含有 Milli-Q 水 |
|
移動相 B: |
0.1% ギ酸アセトニトリル溶液 |
|
グラジエントプロファイル: |
5% ~ 95% B を 5.0 分で、95% B を 0.5 分間保持。 |
MS 条件
|
MS システム: |
Xevo TQ-S micro |
|
イオン化モード: |
ESI+ |
|
取り込み範囲: |
MRM の概要を表 1 に示す |
|
キャピラリー電圧: |
3.0 kV |
|
コーン電圧: |
分析種によって異なる(表 1) |
|
脱溶媒温度: |
500 ℃ |
|
脱溶媒流量: |
500 L/時間 |
|
コーンガス流量: |
10 L/時間 |
データ管理
|
クロマトグラフィーソフトウェア: |
MassLynx v4.1 |
結果および考察
カラム試験の前に、アッセイを最適化するため、2 種類のサンプル前処理メソッドを評価しました。PPT および SPE を、ヒト血清のサンプルに対して実施しました。「実験方法」セクションで概説した Oasis HLB 1 cc 30 mg カートリッジを使用する SPE プロトコルは、この実験用に最適化しませんでした。汎用的な SPE 条件を使用して、PPT と比較した場合の SPE の有効性を実証しました。SPE プロトコルを最適化することで、シグナルが更に改善する可能性があります。単一バッチの ACQUITY UPLC HSS T3 1.8 μm、2.1 × 50 mm を使用して、両方のサンプル前処理メソッドを分析し、予想される分析種の質量分析(MS)シグナル強度を評価しました。図 1 に、血清中に検出されたステロイドホルモンについての SPE と PPT の結果の比較を示します。
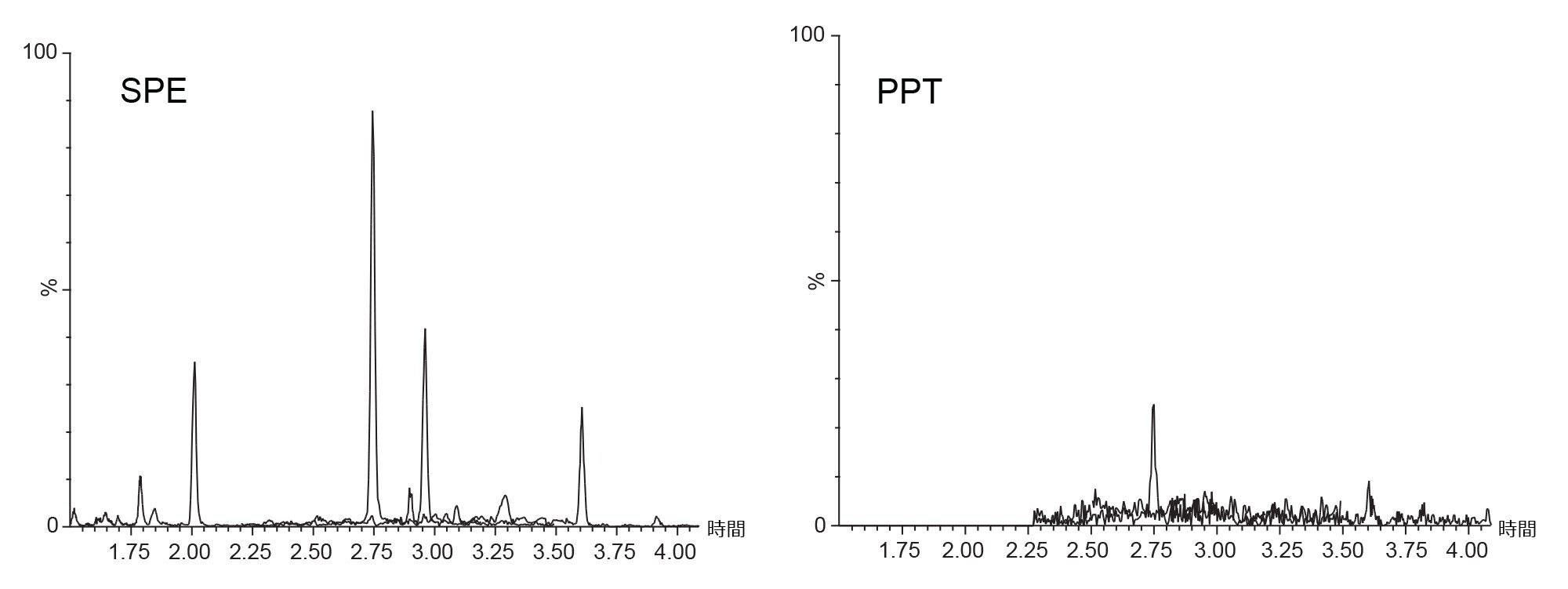
血清中のステロイド候補を試験しました8。 これらの条件下での SPE の後に、4 種類のステロイドホルモンが 1e5 を上回るシグナル強度で検出されました。他のステロイドは検出されませんでした。ピーク同定は、ステロイドの標準混合液を用い、表示した試験条件を用いて行いました。PPT 後の結果では、2 種類のステロイドホルモン(テストステロン、コルチゾール)のみが検出され、SPE と比較してかなり低いシグナルになりました。PPT 後では、アンドロステンジオンとプロゲステロンは検出されませんでした。SPE では、コルチゾールのシグナルが 5 倍に増加し、テストステロンのシグナルが約 30 倍に増加していました。これにより、ピークの検出が容易になるだけでなく、アッセイの LOD と LOQ も低くなり、SPE による回収試験のダイナミックレンジが広くなります。SPE ではまた、リン脂質その他の問題のある化合物を除去することで、より清浄なサンプルが得られます9,10。清浄なサンプルを用いることで、装置やカラムが汚れる確率が低くなるとともに、イオン化抑制やイオン化促進などのマトリックス効果が低減します。カラムの比較を進めるにあたり、今後サンプル前処理には SPE を使用します。
SPE により新たにサンプルを調製し、製造時期が互いに離れている 3 つのバッチの ACQUITY UPLC HSS T3 1.8 μm 充塡剤を評価しました。これらのバッチは 5 年間にわたって製造されたもので、最も古いバッチは 2016 年 10 月に製造および試験されています。残りのバッチは 2019 年 11 月と 2021 年 11 月に製造されたものです。図 2 に、3 本のカラムで得られた 4 種類の内因性ステロイドのクロマトグラムを示します。システムのキャリーオーバーがないことを確認するために、各カラムで血清の繰り返し注入を行い(n = 3)、前後に 2 つのブランクを注入しました。
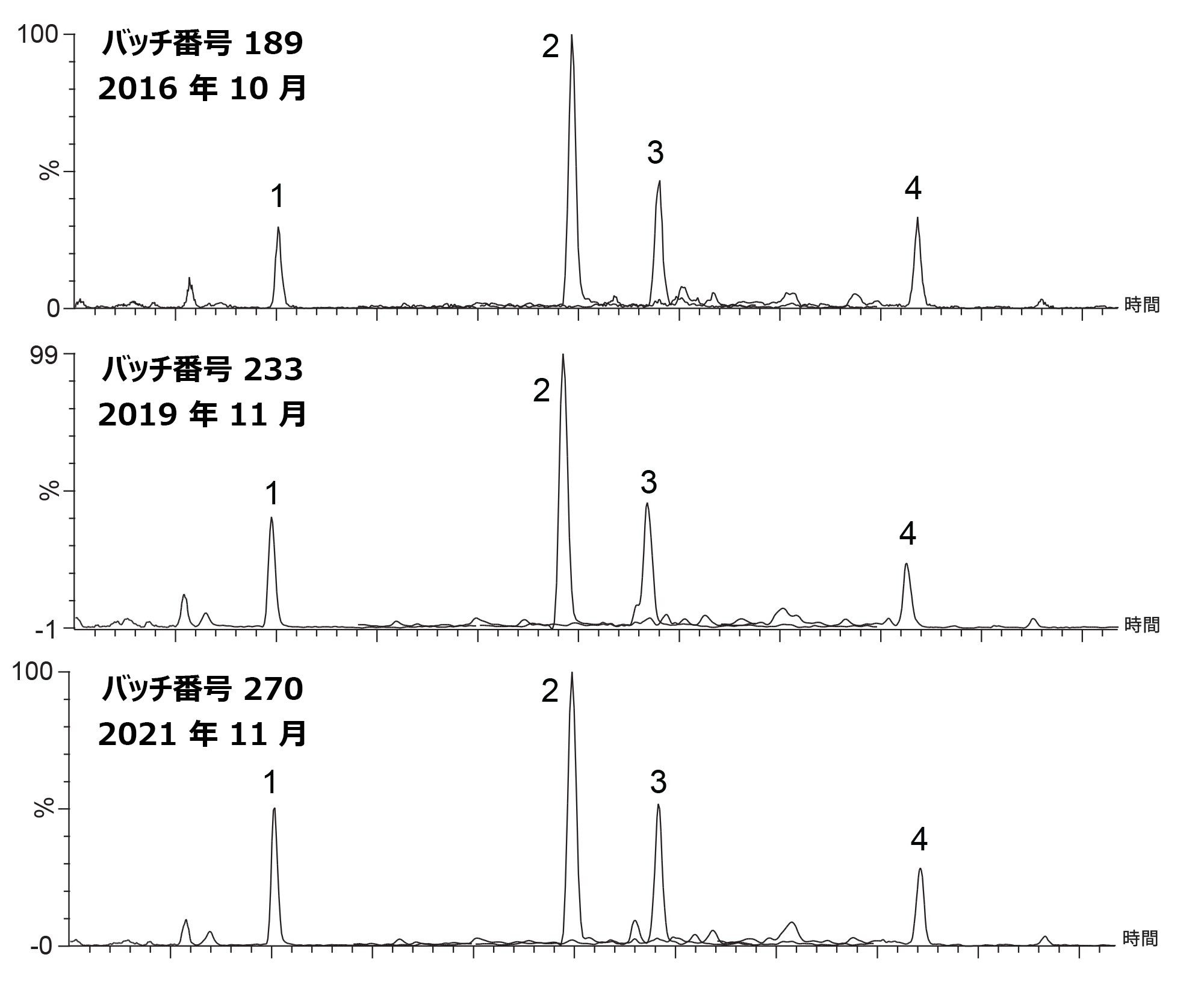
1)コルチゾール、2)テストステロン、3)アンドロステンジオン、4)プロゲステロン。
3 本のカラムすべてで、内因性ステロイドの分析において同等の結果が得られました。3 本のカラムすべて、およびプールしたデータサンプルについて、ピーク保持時間、ピーク面積、ピーク幅、ピーク対称性をモニターおよび評価しました(表 2)。保持時間の %RSD は、各カラム(n = 3)およびプールしたデータセット(n = 9)のすべてのプローブについて 1% 未満でした。ピーク面積の再現性は、各カラムおよびプールされたデータサンプルについて %RSD 5% 未満と良好でした。同様に、ピーク幅(半値幅)とピーク対称性についても、低い %RSD が得られました。
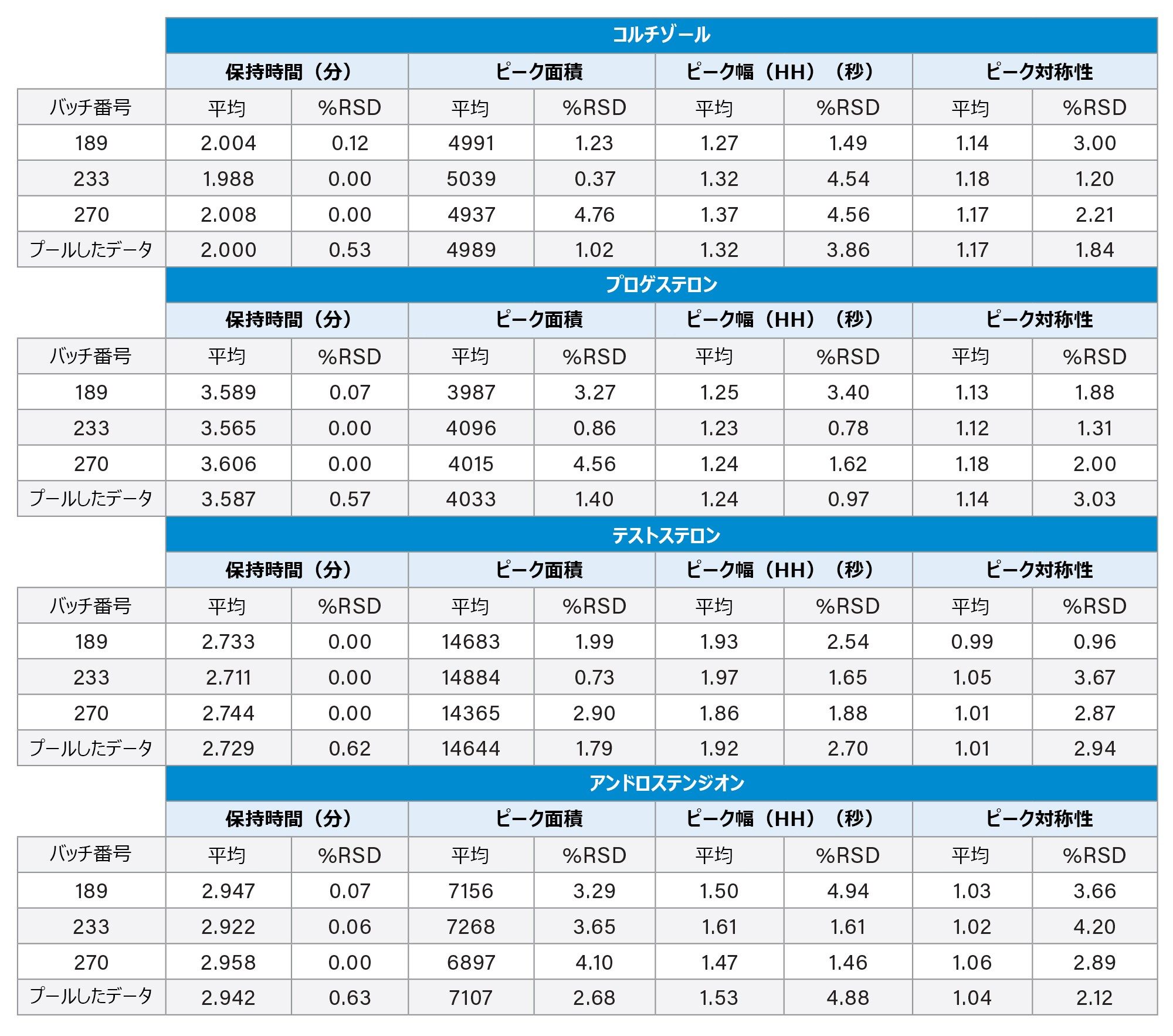
5 年にわたって製造された充塡剤でも、このアッセイのバッチ間再現性は良好です。このレベルの再現性を備えた充塡剤を使用することで、数年に及ぶこともあるアッセイの使用期間の間、同じ性能が得られることが保証されます。ウォーターズのカラムは、厳格な品質管理および製造プロセスを通じてこのレベルの再現性を提供しており、これらのカラムで得られるデータが最高品質であることが保証されます。
結論
ウォーターズの粒子およびカラムの製造プロセスの品質を実証するため、5 年間にわたって製造された 3 バッチの ACQUITY HSS T3 固定相を使用して、ヒト血清中の内因性ステロイドホルモンを分離しました。再現性試験のためのすべてのサンプル前処理に SPE を使用しました。
これら 3 つのバッチでは、再現性のあるクロマトグラフィー性能が示されました。保持時間の %RSD 値は、各カラムおよびプールしたデータセット(n = 9)について 1% 未満でした。また、ピーク面積、ピーク幅、ピーク対称性の %RSD は、検出した分析種について 5% 未満でした。これらの結果からは、充塡剤が 5 年離れて製造されていても、同じ品質のデータが得られることを示しています。同様のデータが何年にもわたって得られるというこのレベルの保証は、新しい分析法を開発する際に非常に重要です。選択した固定相がロット間でも経年でも同等であることが分かっていることで、追加の再作業を必要とせずに、アッセイの使用期間を延ばすことができます。
謝辞
Jonathan Danaceau、Chelsea Plummer、Jonathan Turner、Kim Haynes の各氏に、このアプリケーションノートをレビューして頂き、貴重なフィードバックを頂きました。
参考文献
- Heyden YV, Nijhuis A, Smeyers-Verbeke J, Vandeginste BGM, Massart DL.Guidance for Robustness/Ruggedness Tests in Method Validation.Journal of Pharmaceutical and Biomedical Analysis.2001.723–753.
- Vervoort RJ, Ruyter E, Debets A, Claessens HA, Cramers C, de Jong GJ.Influence of Batch-To-Batch Reproducibility of Luna c18 (2) Packing Material, Nature of Column Wall Material, and Column Diameter on the Liquid Chromatographic Analysis of Basic Analytes.Journal of Separation Science. 2001.167–172.
- Summers M, Fountain K. Validation of a Method for the Separation of Ziprasidone and Its Degradants using Empower 2 with Method Validation Manager (MVM).Waters Application Note, 720004077, 2011.Accessed 10-Jan-2022.
- New LS, Chan ECY.Evaluation of BEH C18, BEH HILIC and HSS T3 (C18) Column Chemistries for the UPLC-MS-MS Analysis of Glutathione, Glutathione Disulfide, and Ophthalmic Acid in Mouse Liver and Human Plasma.Journal of Chromatographic Science.2008.209–214.
- Mohamed, M. Stability Indicating New RP-UPLC Method for Simultaneous Determination of a Quaternary Mixture of Paracetamol, Pseudoephedrine, Chlorpheniramine, and Sodium Benzoate in (Cold-Flu) Syrup Dosage Form.Journal of AOAC International. 2022.
- Sottani C, Grignani E, Cottica D, et.al.Development and Validation of a Bioanalytical UHPLC-MS/MS Method Applied to Murine Liver Tissue for the Determination of Indocyanine Green Loaded in H-Ferritin Nanoparticles.Frontiers in Chemistry 2022.
- Elmongy H, Masquelier M, Ericsson M. Development and Validation of a Uhplc-Hrms Method for the Simultaneous Determination of the Endogenous Anabolic Androgenic Steroids in Human Serum.Journal of Chromatography A.2019.1613.
- Foley D, Carlton LJ.Confidence in Your Calibrators: Confidence in Your Calibrators: MassTrak Endocrine Steroid Calibrators and Quality Control Sets for the LC-MS/MS Analysis of Steroid Hormones.Waters Application Note, 720007401, 2021.Accessed 10-Jan-2021.
- Zhang X, Danaceau JP, Chambers EC.Quantitative Analysis of THC and its Metabolites in Plasma Using Oasis PRiME HLB for Toxicology and Forensic Laboratories.Waters Application Note, 720005820, 2019.Accessed 13-Jan-2022.
- Zhang X, Danaceau JP, Chambers EC.Simple, Fast, and Clean Extraction of Synthetic Cannabinoids from Whole Blood Using Oasis PRiME HLB. Waters Application Note, 720005417, 2015.Accessed 14-Jan-2022.
720007529JA、2022 年 2 月