利巴韦林相关化合物亲水作用液相色谱(HILIC)方法的缩放与迁移(至现代HPLC系统)
摘要
在不同粒径色谱柱之间缩放方法以及在LC系统之间迁移时,实现相同的色谱分离和等效的结果是成功的关键。在本研究中,我们将用于活性药物成分(API)利巴韦林和相关化合物分析的HILIC方法从1.7 µm (2.1 × 50 mm)色谱柱放大至2.5 µm (3.0 × 75 mm)和3.5 µm (4.6 × 100 mm)色谱柱(填料相同)。随后,将该方法从ACQUITY™ UPLC™ H-Class PLUS系统迁移至ACQUITY Arc™、Arc HPLC和Alliance™ iS HPLC System。通过评估不同系统上的色谱分离效果、系统适应性以及方法生成的分析结果,验证了迁移后的等效性能。
优势
- 方法可在Waters™ UHPLC和HPLC系统之间成功迁移
- 沃特世方法转换计算器通过计算运行条件来实现方法的缩放,从而获得相同的分离效果和性能
- Empower中的“智能梯度起点”功能可补偿系统延迟体积的差异,在迁移方法时无需手动调整梯度表
简介
分析方法通常使用亚2 µm颗粒的色谱柱开发,目的是加快方法开发过程并缩短分析运行时间。这些方法通常需要采用低扩散液相色谱(LC)系统以实现理想的色谱分离效果。然而,这些方法经常需要转换到未配备低扩散系统的质量控制(QC)实验室。在这种情况下,需要将方法缩放到专为高扩散HPLC设计的较大颗粒色谱柱上1。 接收实验室需要证明相同分析能够生成等效结果,以确保产品的一致性并符合法规指南要求2。
在不同的LC系统之间进行色谱方法缩放和迁移是一项艰巨的任务。不同的系统通常具有不同的延迟体积和柱外体积,这可能导致梯度方法的色谱分离效果不佳和峰畸变,进而导致缩放/迁移后的分析结果不一致。在进行方法缩放和迁移时,必须考虑系统特性的差异3。
本研究展示了一种针对利巴韦林及其相关化合物分析的HILIC方法的缩放,以及迁移至现代HPLC系统的过程4。 利巴韦林是一种用于治疗慢性丙型肝炎病毒(HCV)感染的抗病毒药物5。 该方法之前是在亚2 µm颗粒色谱柱上开发的。在本研究中,该方法从1.7 µm颗粒色谱柱缩放至2.5 µm和3.5 µm颗粒色谱柱。随后,该方法从ACQUITY UPLC H-Class PLUS系统(1.7 µm色谱柱)迁移至ACQUITY Arc (2.5 µm)、Arc HPLC和Alliance iS HPLC System (3.5 µm)。在每个系统上评估包括色谱分离效果、系统适应性以及分析结果在内的性能特征,以衡量方法缩放和迁移是否成功。
实验
样品描述
标准品溶液
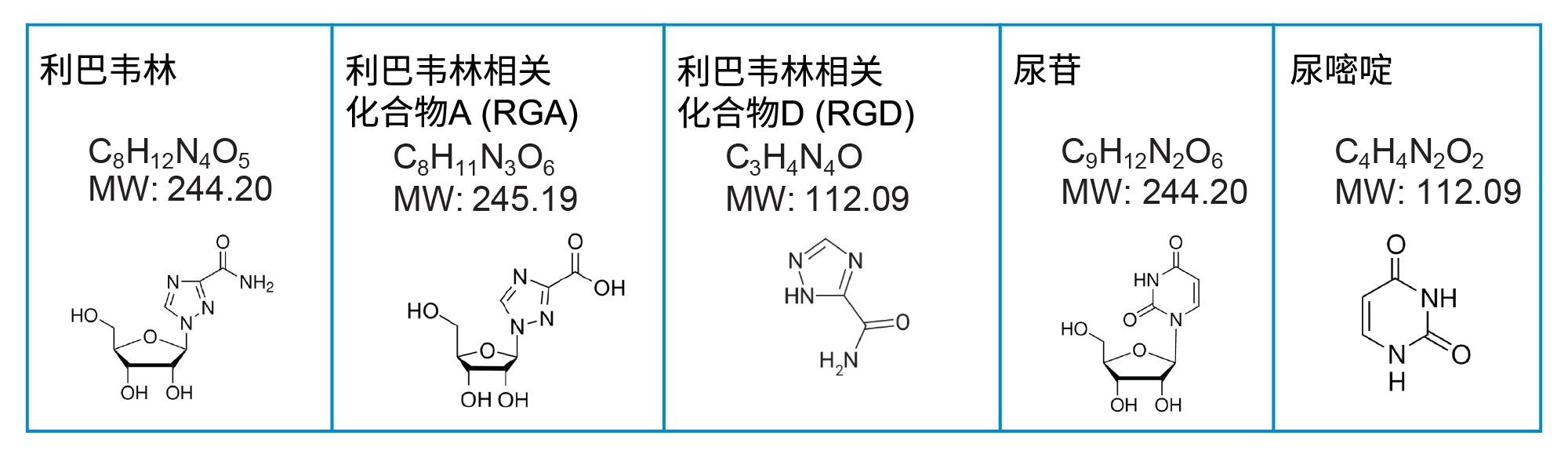
利巴韦林及其相关化合物的纯标准品(图1.)购自Sigma-Aldrich。使用50:50乙腈/水溶液配制浓度为1.0 mg/mL的单标储备液。用90:10乙腈/水稀释剂稀释储备液,制得含有0.1 mg/mL利巴韦林API和10 µg/mL相关化合物的混标溶液。
方法条件
|
流动相A: |
乙腈 |
|
流动相B: |
水 |
|
流动相C: |
含1%氢氧化铵的100 mM碳酸氢铵溶液(pH 10) |
|
柱温: |
30 °C |
|
检测: |
UV检测波长为220 nm |
|
样品瓶: |
LCMS最大回收样品瓶,容积2 mL,P/N:600000670CV |
|
样品温度: |
10 °C |
|
清洗溶剂: |
灌注/样品/针:90:10乙腈/水 密封清洗液:10:90乙腈/水 |
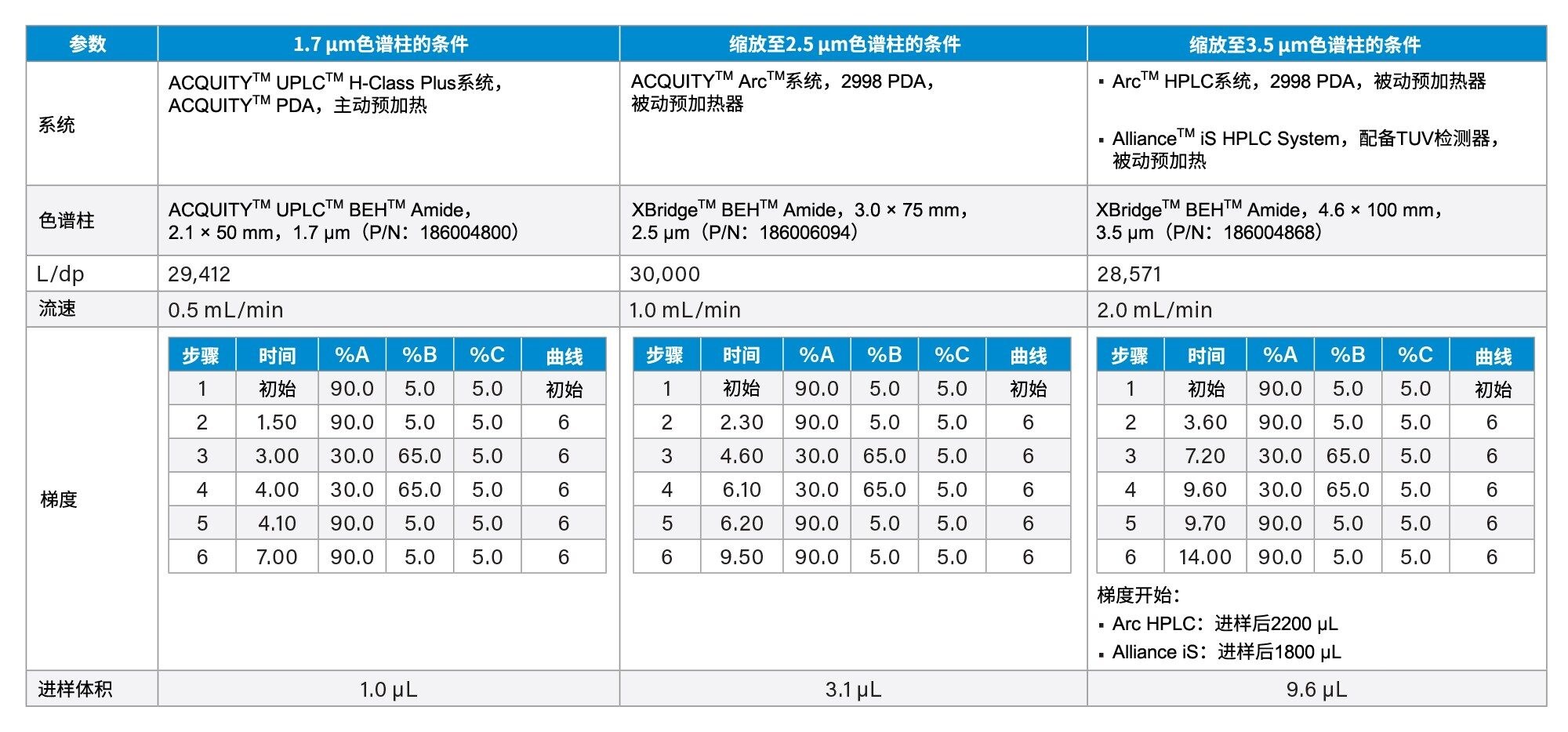
表1汇总了1.7 µm、2.5 µm和3.5 µm颗粒色谱柱的方法条件。使用沃特世方法转换计算器对流速、进样体积和梯度洗脱进行几何比例缩放6。
数据管理
|
色谱软件: |
Empower™ 3 Feature Release 5Service Release 5 (FR5 SR5) 搭载Alliance iS HPLC System的Empower 3.8.0 |
使用Empower软件采集和处理数据。使用Empower项目中内置的报告模板创建处理数据的汇总报告。
结果与讨论
注意事项:缩放和迁移方法
不同LC平台之间的方法缩放和迁移可能受到诸多因素的影响。当涉及不同粒径的缩放时,色谱柱柱长(L)与粒径(dp)的比率必须与原始方法相同,以保持色谱分离效果。包括流速、进样体积以及梯度时间在内的参数需要按几何比例进行调整,以实现等效的色谱分离和性能。
仪器特性(包括延迟和柱外体积)会影响色谱分离的质量,因此在不同系统之间迁移方法时应考虑这些特性3。与2.5~5 µm颗粒色谱柱的方法相比,使用亚2 µm颗粒色谱柱的方法运行的系统通常延迟体积小、扩散低。如果在延迟体积大、扩散高的系统上使用亚2 µm颗粒色谱柱,可能会导致梯度方法中色谱分离不良和峰畸变,从而对相同分析产生不同的结果。关于LC系统延迟体积的测量步骤,可在一篇白皮书中找到7。
案例研究:利巴韦林及相关化合物
本研究使用沃特世方法转换计算器将用于利巴韦林及其相关化合物分析的HILIC方法从1.7 µm放大至2.5 µm和3.5 µm颗粒色谱柱6。 原始方法使用长50 mm的1.7 µm颗粒色谱柱,得到的L/dp = 29,412。放大后的方法分别使用了2.5 µm和3.5 µm颗粒、75 mm和100 mm长的色谱柱,得到的L/dp分别为30,000和28,571。表1列出了使用1.7 µm、2.5 µm和3.5 µm颗粒色谱柱的方法的操作条件。
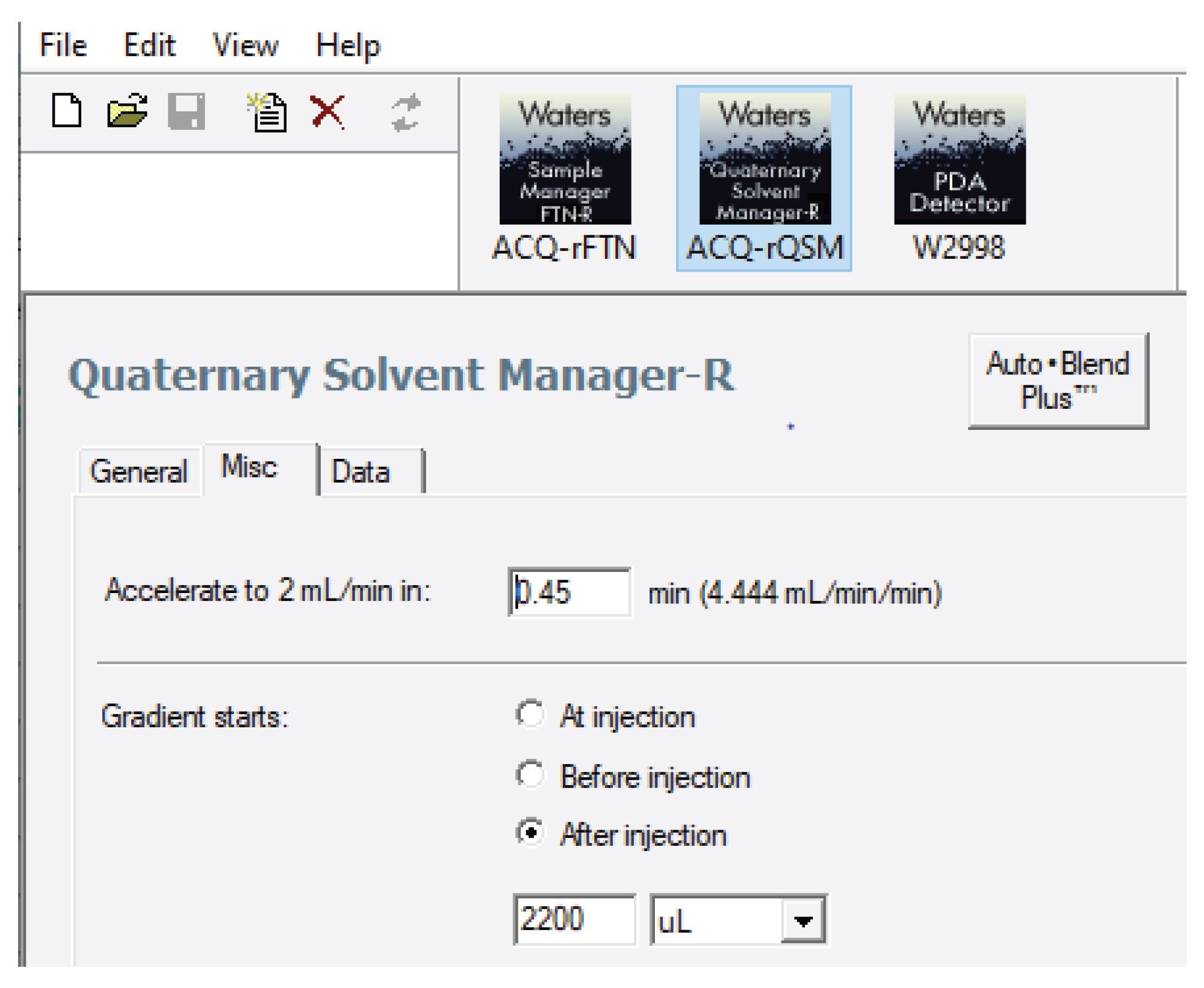
ACQUITY UPLC H-Class PLUS系统的延迟体积(0.375 mL)比ACQUITY Arc (1.19 mL)、Arc HPLC (1.35 mL)和Alliance iS HPLC System (1.5 mL)系统更小。因此,目标方法的梯度起点通过Empower中的“智能梯度起点”技术进行了调整。图2展示了Arc HPLC系统的梯度开始时间调整示例。梯度调整为在进样2200 µL后开始。“智能梯度起点”功能可补偿系统延迟体积的差异,无需手动调整梯度表。
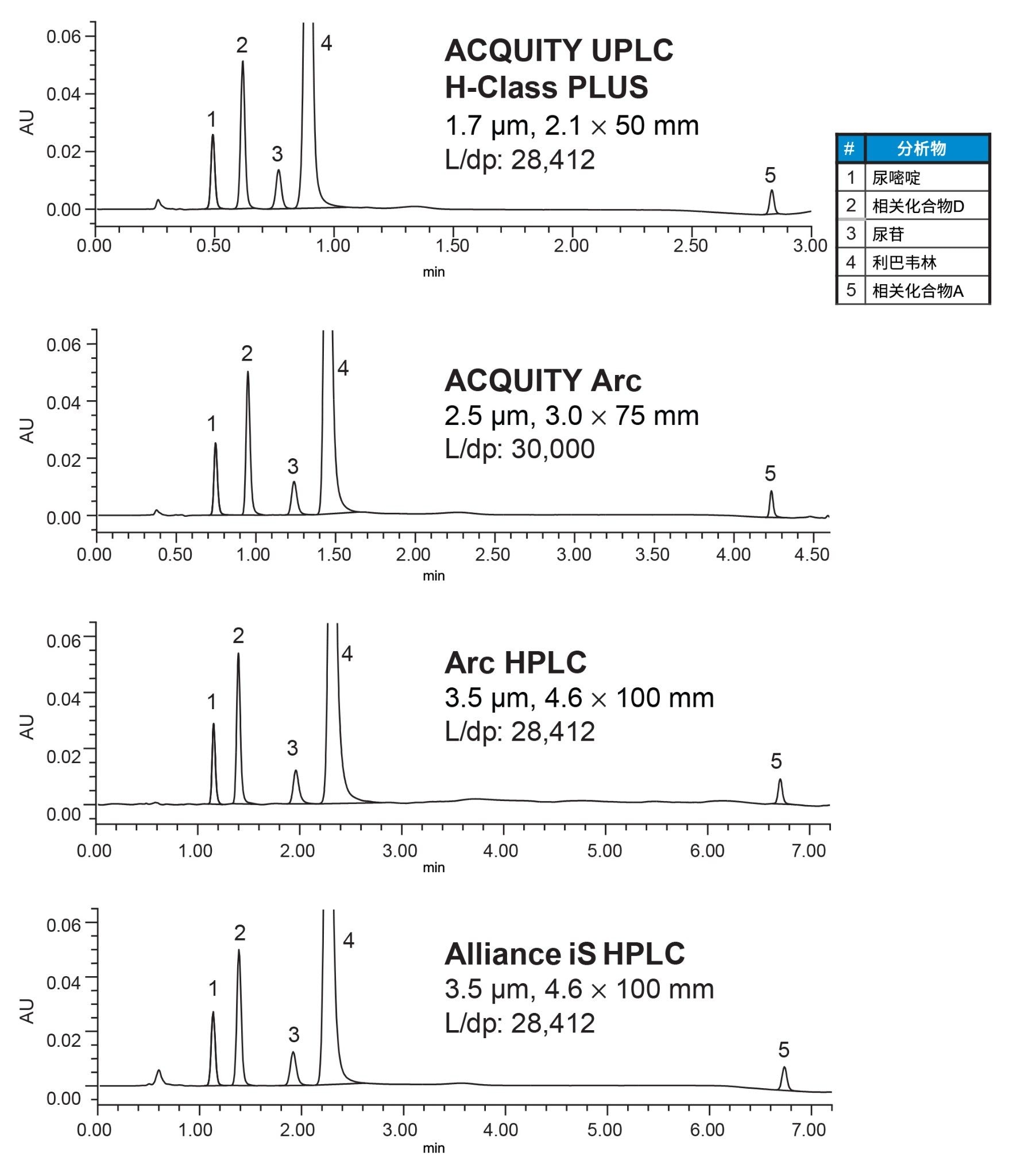
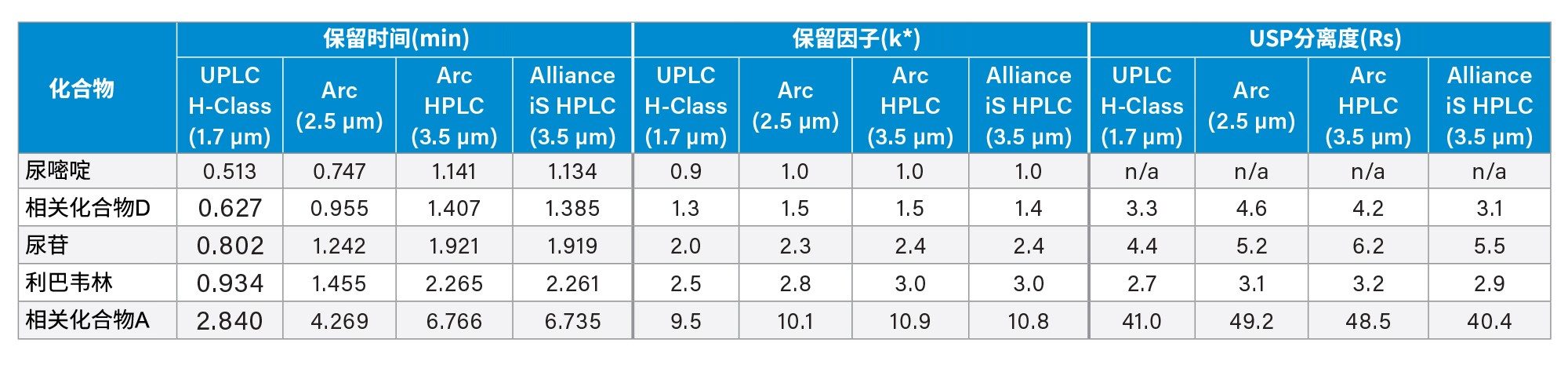
ACQUITY Arc、Arc HPLC和Alliance iS HPLC System 得到的色谱分离结果与ACQUITY UPLC H-Class PLUS系统得到的数据相当(图3)。前四个峰在等度条件下洗脱,最后一个峰(相关化合物A)在梯度过程中洗脱。四个系统获得的分离参数相当,包括保留时间、保留因子(k*)和峰间USP分离度(Rs)(表2)。
系统适应性
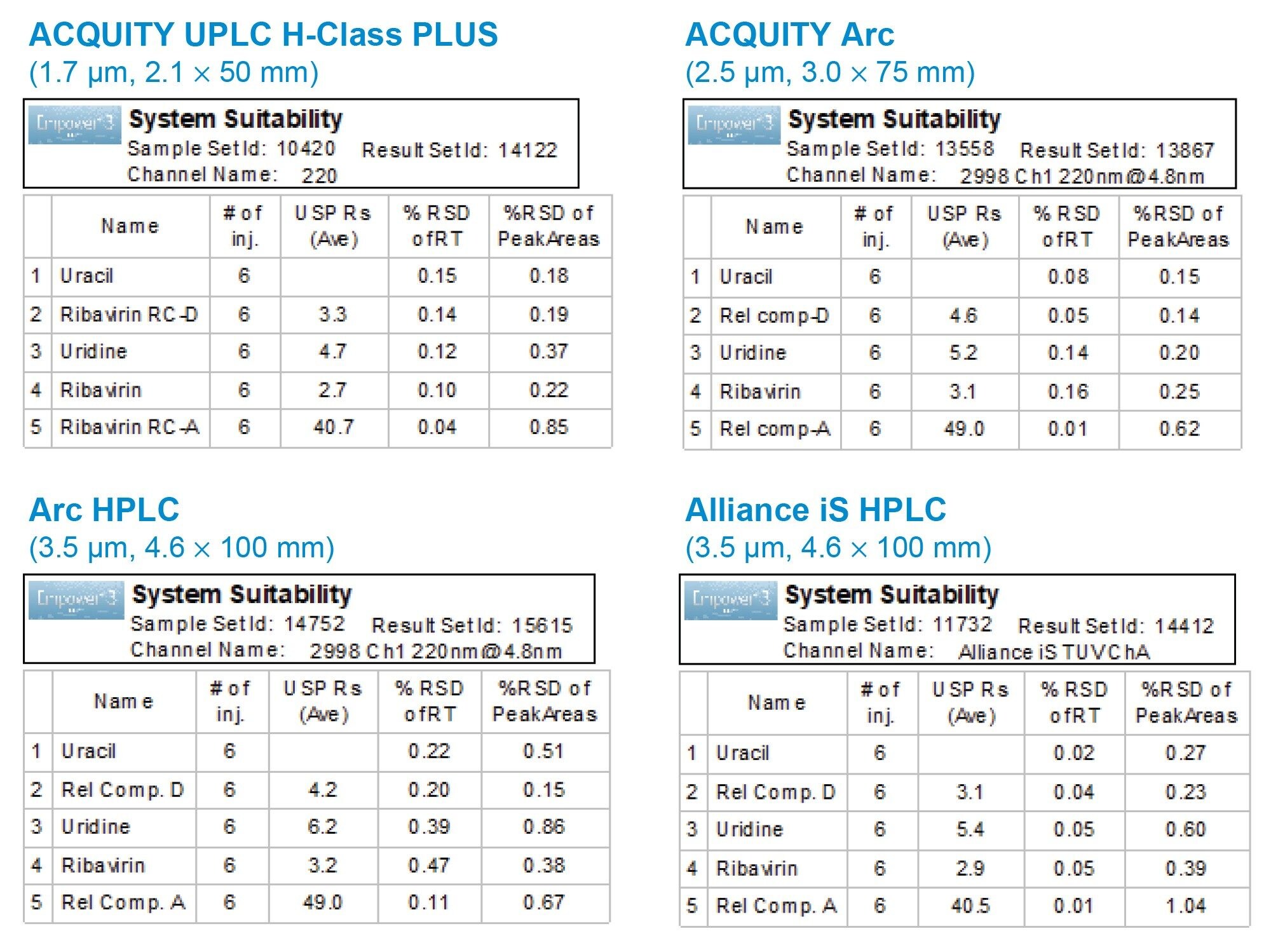
通过测量标准溶液(包含100 µg/mL的利巴韦林API和10 µg/mL相关化合物)六次重复进样的重复性评估了方法在各系统上的性能。ACQUITY Arc、Arc HPLC和Alliance iS HPLC System均获得了优异的峰面积和保留时间重复性,并且与ACQUITY UPLC H-Class PLUS系统获得的结果一致(图4)。
相关化合物的分析结果
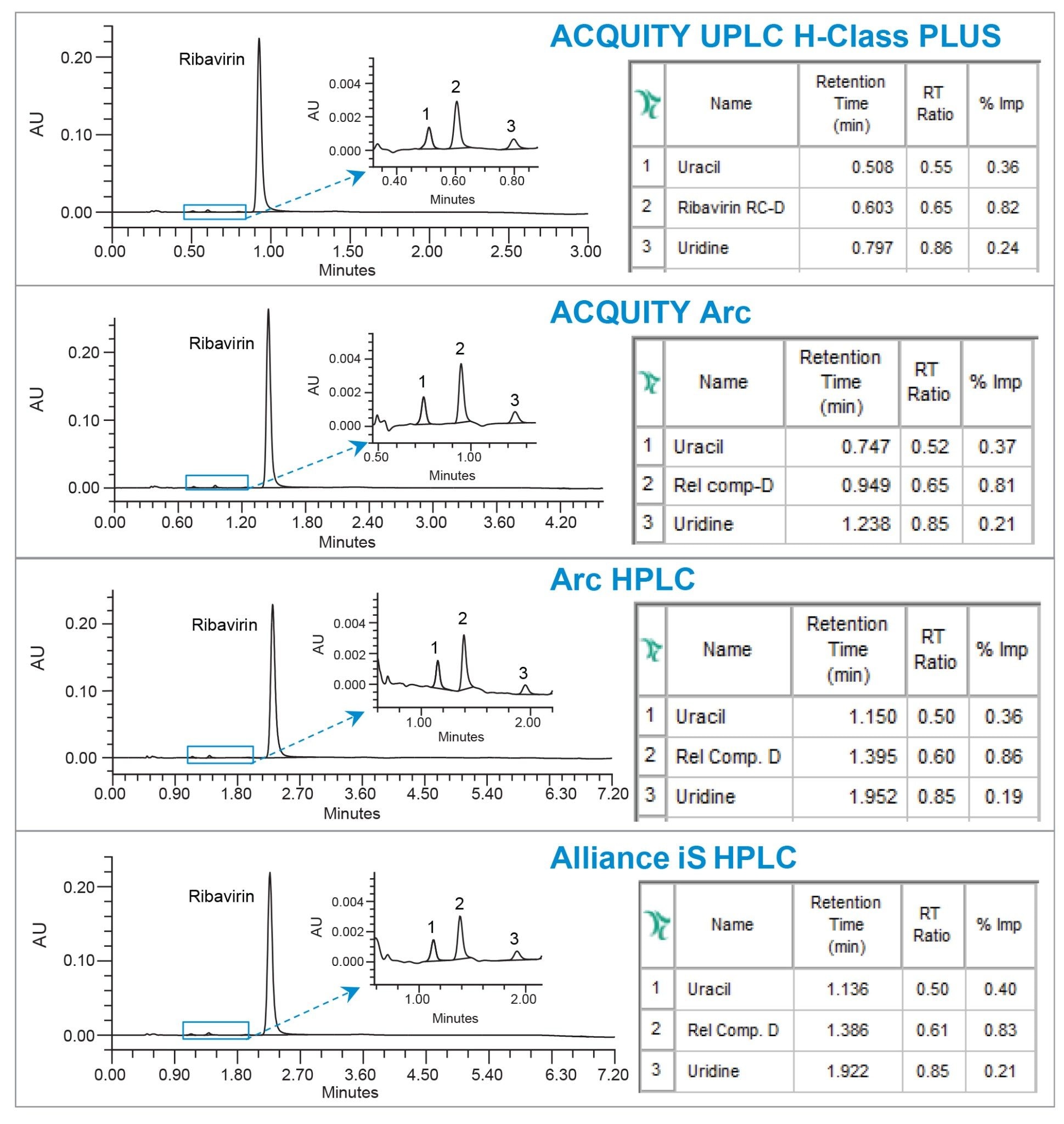
为了展示方法在相关化合物含量(杂质%)测定中的性能,向一份API样品溶液中加入相关化合物,并在配备适当色谱柱尺寸的不同系统上运行分析。使用Empower软件计算各相关化合物的峰面积与API峰面积的比值,得出检测结果。ACQUITY Arc、Arc HPLC和Alliance iS HPLC System得到的分析结果与ACQUITY UPLC H-Class PLUS系统的结果一致(图5)。使用Empower软件比较各相关化合物与利巴韦林API的保留时间,不同系统上计算得出的相对保留时间(RRT值)相当。
结论
在本研究中,一种分析利巴韦林及其相关化合物的HILIC方法成功实现了从1.7 µm至2.5 µm和3.5 µm颗粒色谱柱的方法放大,同时方法从ACQUITY UPLC H-Class PLUS系统迁移至扩散更高的LC系统(包括ACQUITY Arc、Arc HPLC和Alliance iS HPLC System)。目标系统在色谱分离、系统适应性和分析结果方面与ACQUITY UPLC H-Class PLUS系统产生的数据相当。
系统特性(包括延迟体积和柱外体积)会影响色谱性能质量,因此在不同LC平台之间进行方法缩放和迁移时,必须将这些因素纳入考虑,以提高方法转换的成功率。
参考资料
- Dong MW.Ultrahigh-Pressure Liquid Chromatography, Part III: Potential Issues: This Installment on Ultrahigh-Pressure Liquid Chromatography (UHPLC) Review the Potential Problems That May Be Encountered Using HPLC Systems and Methods, and Proposes Strategies for Their Migration.LC-GC North America, 35–11, 2017.
- USP General Chapter 〈1224〉, Transfer of Analytical Procedures.United States Pharmacopeia USP 43-NF 38, official prior 2013.
- Hong H, McConville PR.什么是延迟体积和柱外体积?它们如何影响方法转换?沃特世白皮书, 720005723ZH, 2018.
- Berthelette KD, Walter T, Naughton S, Turner JE, Zampa N. 剖析新型冠状病毒病(COVID-19):使用亲水作用色谱法快速分析利巴韦林与相关化合物.沃特世应用纪要, 720006957ZH, 2020年.
- 利巴韦林:https://medlineplus.gov/druginfo/meds/a605018.html
- 沃特世方法转换计算器. https://www.waters.com/waters/support.htm?lid=134891632&type=DWNL
- Waters Corporation, Protocol for Gradient Delay (Dwell Volume) Measurement. Waters Applications Notebook, 720004313EN, p. 67–69, 2013.
720008255ZH,2024年2月