使用MaxPeak™ Premier色谱柱和QDa™质谱检测器开发奥利司他强制降解样品的分析方法
摘要
新药开发需要进行各种测试来确保消费者安全。从生物利用度研究到稳定性研究,在药物放行前,我们需要了解有关药物及其作用机制的各种信息。在开发过程中,通常需要执行强制降解研究,以更好地了解化合物在降解条件下是如何分解的。这项研究不仅提供有关分子稳定性的重要信息,还揭示了降解物的信息,这些降解产物可以进一步研究以发现潜在的问题。在这些强制降解研究中,需要开发一种耐用的液相色谱(LC)方法来完全分离不同的降解物,使后续工作(例如降解物的分离)更轻松。
本应用纪要介绍奥利司他强制降解研究方法的开发过程,这是一种获FDA批准的减肥药,能抑制胰腺脂肪酶,结合节食和运动有望达到减肥效果。研究中使用了五种不同的固定相、两种不同的强溶剂(乙腈和甲醇)以及两种流动相pH,共测试11种条件。最终的方法条件使用ACQUITY™ Premier BEH™ C18、甲醇流动相和低pH,使大多数峰(包括未降解的奥利司他)都获得了良好的分离度。我们仅用不到两天的时间就完成了该样品的方法开发。
优势
- 使用系统性筛选策略快速开发方法
- 14种化合物均获得良好的峰形
- 检出的所有降解物和奥利司他主峰均实现基线分离
简介
开发新药时需要进行各种测试(包括降解研究),以确保形成的任何降解物对消费者都是安全的,同时还要测试分子的总体稳定性。强制降解研究通常与储存稳定性研究一起进行,两者都试图获取分子在不同条件下的信息。强制降解研究的目的是更好地了解分子在促进水解或过氧化物降解的条件下的化学稳定性。此外,考察的降解途径通常还包括光降解和热降解。储存稳定性测试的实施条件更加接近现实,即将最终产品置于典型的储存条件下,在几个月后进行测试,确保没有发现分子降解的现象。无论是哪种研究,都需要采用耐用的LC方法来鉴定所有降解物。无论是使用专用的MS设备(例如高分辨率质谱仪(HRMS))进行鉴定,还是通过标准加入法进行鉴定,让所有峰都实现基线分离对于确保生成准确可靠的数据都非常重要。
本应用纪要开发出一种用于奥利司他(一种获FDA批准的非处方和处方减肥药)强制降解研究的方法。奥利司他(如图1所示)是一种他汀类药物衍生物,可以抑制胰腺脂肪酶,阻止摄入脂肪的分解,使其排出体外,而不是被身体吸收1-2。
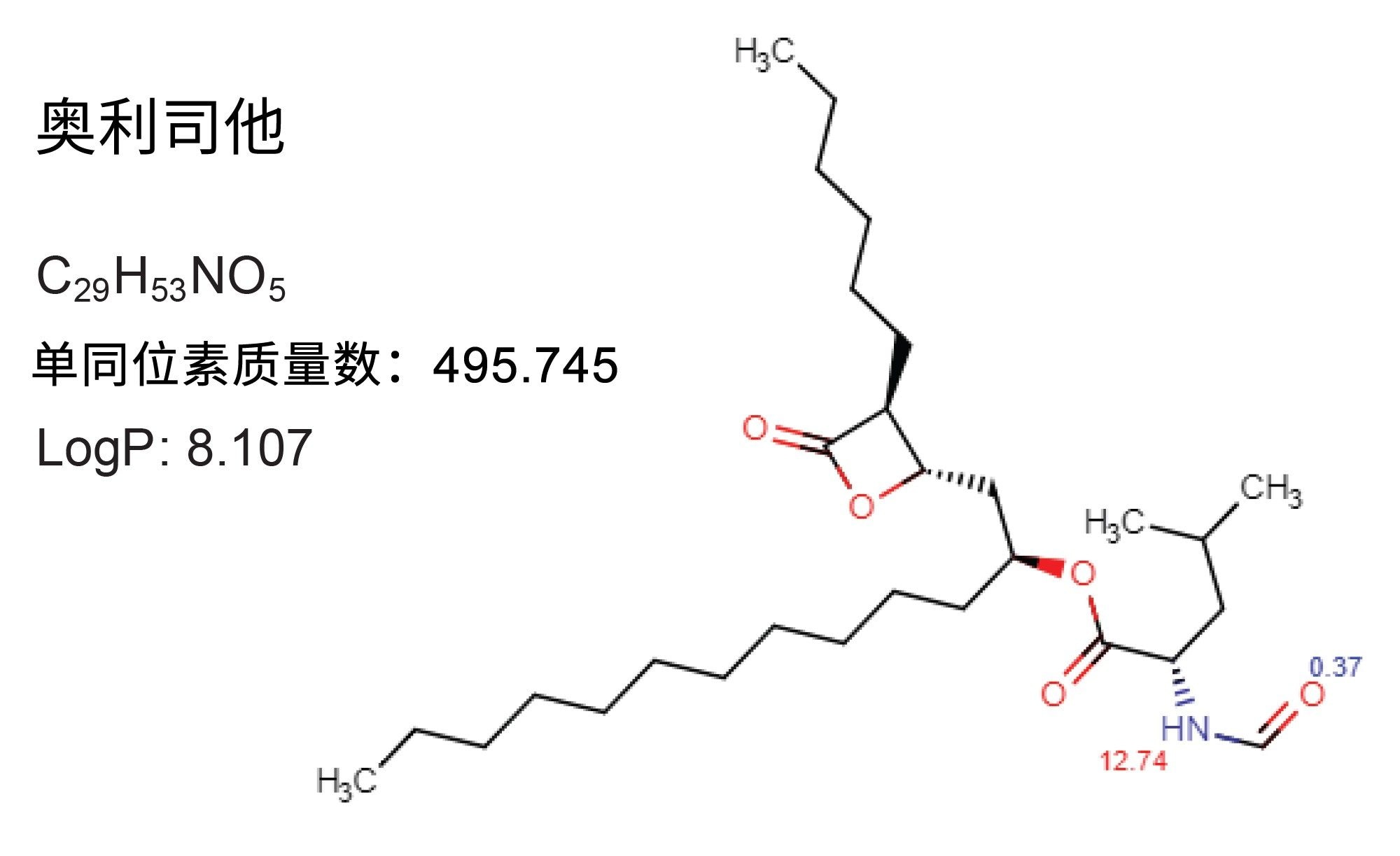
本研究的方法是通过系统性筛选策略开发的,这种策略过去已被证明能够高效、快速且可靠地开发新的LC方法3-6。 系统性筛选策略可引导用户完成方法开发过程中的特定步骤,消除方法开发过程中存在的不确定性。若将该方法开发过程与采用MaxPeak高性能表面(HPS)技术的MaxPeak Premier色谱柱相结合,可使结果更加可靠。MaxPeak Premier色谱柱采用专门设计的色谱柱硬件,可消除分析物与色谱柱金属表面之间的非特异性吸附7-9。 消除这些不良相互作用有助于生成更可靠的数据。该硬件的优势在生物分子(例如寡核苷酸和肽)以及一些小分子(例如核苷酸)上表现较为明显10-12。 不过,这些色谱柱在金属配位化合物以及制剂药中也有优势13-14。 这些色谱柱在过去的强制降解研究中就表现出优异性能,因此本研究也使用它们15-16。
实验
样品描述
使用乙腈:水(71:29)配制1 mg/mL的奥利司他储备液。分别在三个样品瓶中应用强制降解,向每个样品瓶中加入1 mL储备液。降解时,所有样品均加热至70 °C。对于酸水解和碱水解,分别加入100 μL 1 N HCl或1 N NaOH。对于热降解,则加入100 μL样品稀释剂。将样品在该温度下静置2小时后,合并所有三个样品瓶,这不仅是为了淬灭酸降解和碱降解反应,也是为了将所有降解物合并到一个样品中。然后分析样品,并使用ACQUITY QDa质谱检测器按质量数追踪降解物。
方法条件
液相色谱条件
|
LC系统: |
ACQUITY UPLC H-Class Plus系统,配备四元溶剂管理器(QSM)和可选的溶剂选择阀、流通针式样品管理器(SM-FTN)、色谱柱管理器、两台辅助色谱柱管理器和QDa质谱检测器 |
|
检测: |
MS全扫描(ESI+) 降解物和API使用的SIR,如所示 |
|
色谱柱: |
ACQUITY Premier BEH C18, 2.1 x 50 mm, 1.7 µm(P/N:186009452) ACQUITY Premier CSH™苯己基柱, 2.1 × 50 mm, 1.7 µm(P/N:186009474) ACQUITY Premier HSS™ PFP, 2.1 x 50 mm, 1.7 µm(P/N:186010036) ACQUITY Premier HSS T3, 2.1 x 50 mm, 1.7 µm(P/N:186009467) ACQUITY Premier BEH Shield RP18, 2.1 x 50 mm, 1.7 µm(P/N:186009497) |
|
柱温: |
30 °C |
|
样品温度: |
10 °C |
|
进样体积: |
1.0 µL |
|
流速: |
0.50 mL/min |
|
流动相A: |
Milli-Q水 |
|
流动相B: |
乙腈 |
|
流动相C: |
甲醇 |
|
流动相D1: |
2%甲酸的水溶液 |
|
流动相D6: |
200 mM氢氧化铵的水溶液 |
|
筛选梯度条件: |
流动相Dx在整个梯度中保持5%不变。流动相B/C在6.86 min内以线性梯度从5%增加到95%,保持1.14分钟,恢复到5%并保持2.3分钟。总运行时间:10.30分钟。 |
数据管理
|
色谱软件: |
Empower™ 3 Feature Release 4 |
结果与讨论
系统性筛选策略中的每一步都旨在解决一个特定问题。但是,在进行任何测试之前,都必须先设定方法目标。这些目标可以基于数据,即所有峰实现基线分离;也可以基于最终用户的需求,例如尽可能缩短运行时间。目标由分析人员设定,并且通常与实验室最佳实践保持一致。本研究的目标包括:1) 获得良好峰形(定义为USP拖尾因子值介于0.8~1.2之间);2) 所有峰均实现基线分离。实现这两个目标可确保所有定量工作都能轻松可靠地进行,并为其他活动(例如方法验证或转移到其他实验室)提供良好的开端。设定目标后,分析人员将了解何时可以停止方法开发过程,避免在已经可以接受的方法上进行额外的优化工作,并且可以开始实际测试。
系统性筛选策略的第一步是使用乙腈流动相和在高pH条件下保持稳定的C18固定相,在高pH和低pH条件下测试样品。本研究选择ACQUITY Premier BEH C18色谱柱,因为它在pH高达12的条件下保持稳定。这一步的目的是确定对样品具有最佳保留作用的pH条件。这一步只评估分析物的保留性,简化决策流程。图2展示了分别使用氢氧化铵和甲酸流动相在高pH和低pH条件下分离强制降解样品的结果。
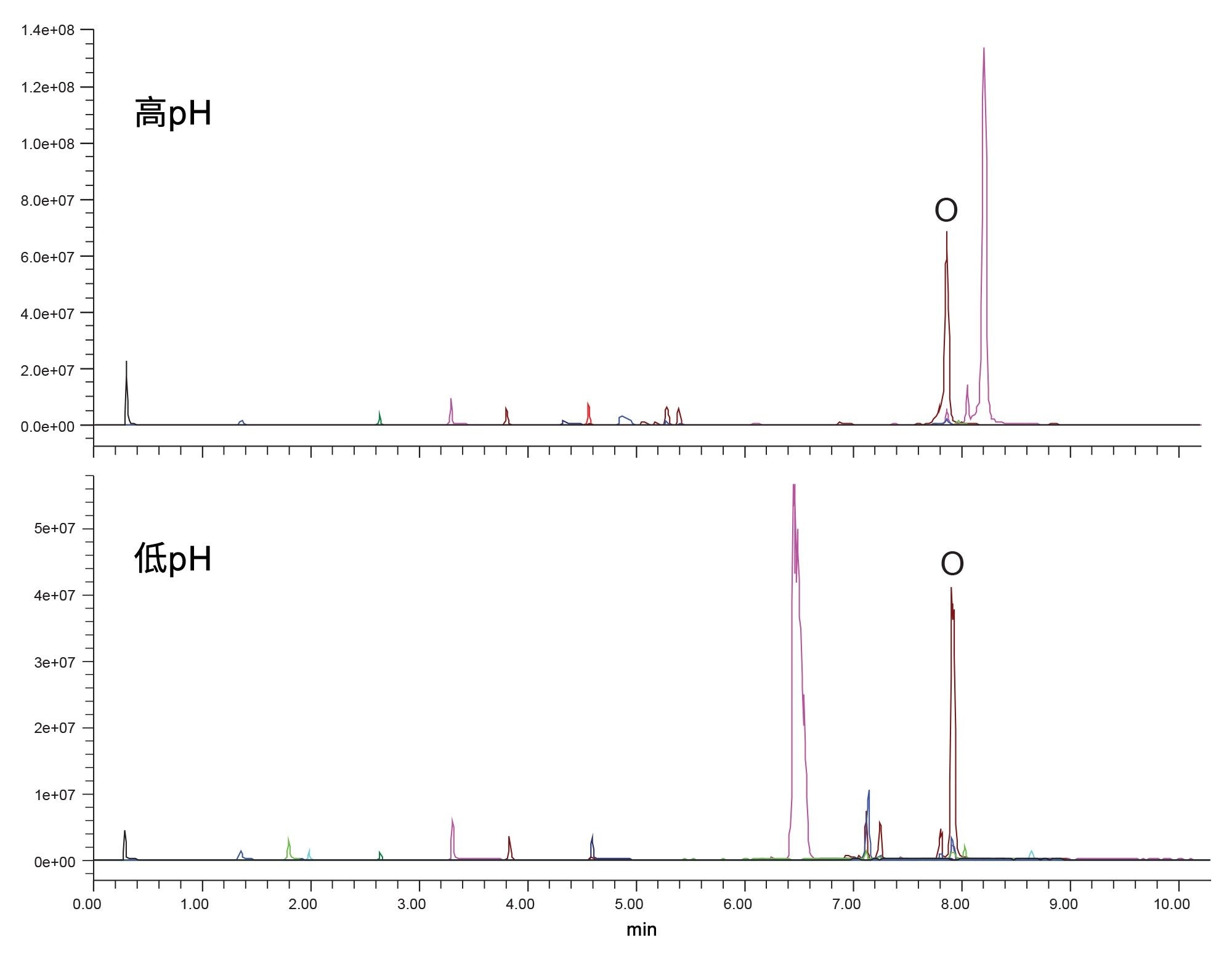
检查高pH和低pH条件下的结果表明,两种条件都不太好。有些峰在低pH条件下具有更高的保留性,而其他峰则在高pH条件下表现更好。主峰“奥利司他”(图中用O表示)在两种pH条件下的保留性没有变化。鉴于酰胺官能团的pKa高于测试的pH,这一结果符合预期。因此,在低pH和高pH条件下,奥利司他都会发生电离。如果没有明显更好的条件,最好采用默认的低pH条件进行进一步测试。有相当多的色谱柱在低pH条件下保持稳定,因此可以使用的固定相有很多。高pH条件限制了可用的潜在选择性,可能会妨碍下一步,即筛选色谱柱固定相和流动相强溶剂。基于上述原因,在后续步骤中选择低pH条件。
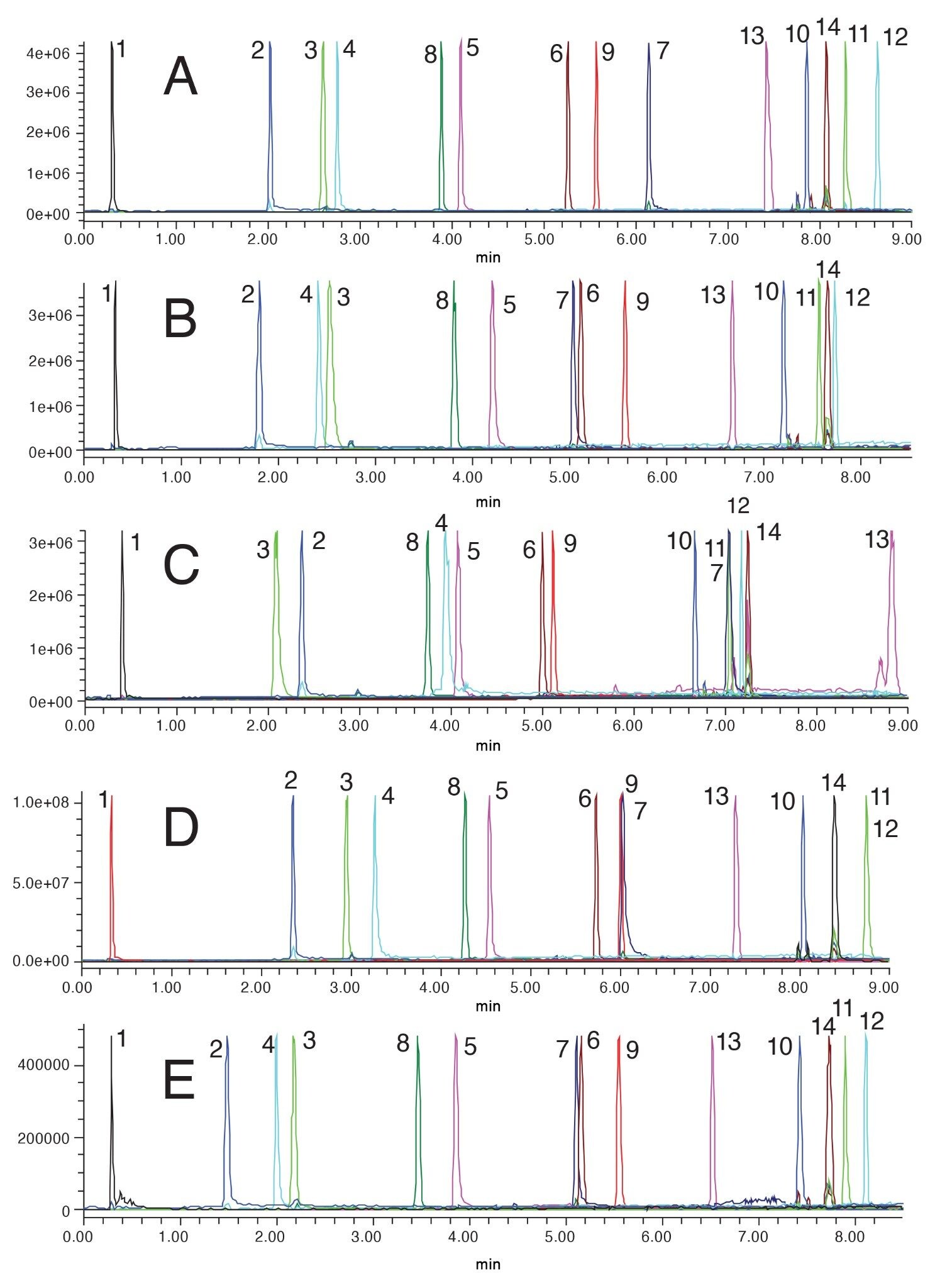
如前文所述,系统性筛选策略的下一步是筛选各种固定相和流动相强溶剂。为使这一步充分发挥作用,应选择多种固定相。这意味着要选择不同的键合相、基质颗粒,甚至可能要选择供应商。本研究选择了五种色谱柱,这些色谱柱均采用了MaxPeak Premier色谱柱硬件。选择ACQUITY Premier BEH C18色谱柱是因为上一步就使用了该色谱柱,并且它也是一款性能良好的通用色谱柱。接下来选择ACQUITY Premier CSH苯己基柱。苯己基键合相可提供各种独特的次级相互作用(包括π-π相互作用),尤其是在使用甲醇时。此外,由于该色谱柱采用表面带电杂化(CSH)颗粒技术,因此阴离子分析物与颗粒上的少量正电荷之间可能会发生弱离子交换相互作用17。 接下来选择ACQUITY Premier HSS PFP色谱柱,因为与之前选择的其他两种色谱柱相比,它提供了更大的选择性差异。五氟苯基(PFP)键合相不仅可以提供类似于苯己基的π-π相互作用,其氟化环还可以参与分析物的偶极-偶极相互作用。高强度硅胶(HSS)颗粒为纯硅胶,而之前选择的颗粒均为杂化颗粒。HSS颗粒可以为碱性探针提供独特的相互作用,但存在峰形不佳的潜在风险。选择的第四种色谱柱是ACQUITY Premier HSS T3色谱柱,这款色谱柱由于高保留性HSS颗粒上的C18键合相具有中等覆盖率,专门用于保留极性分析物。在初步筛选中,单个峰的保留性很差,此固定相可以为探针带来一些额外的保留性。最后选择的色谱柱是ACQUITY Premier BEH Shield RP18色谱柱。相较于BEH C18,这款固定相利用了BEH颗粒和键合相(内嵌氨基甲酸酯基团),使某些分析物的基本峰形得到改善,同时还提供了一些独特的选择性。图3和图4分别展示了使用乙腈和甲醇流动相得到的筛选结果。
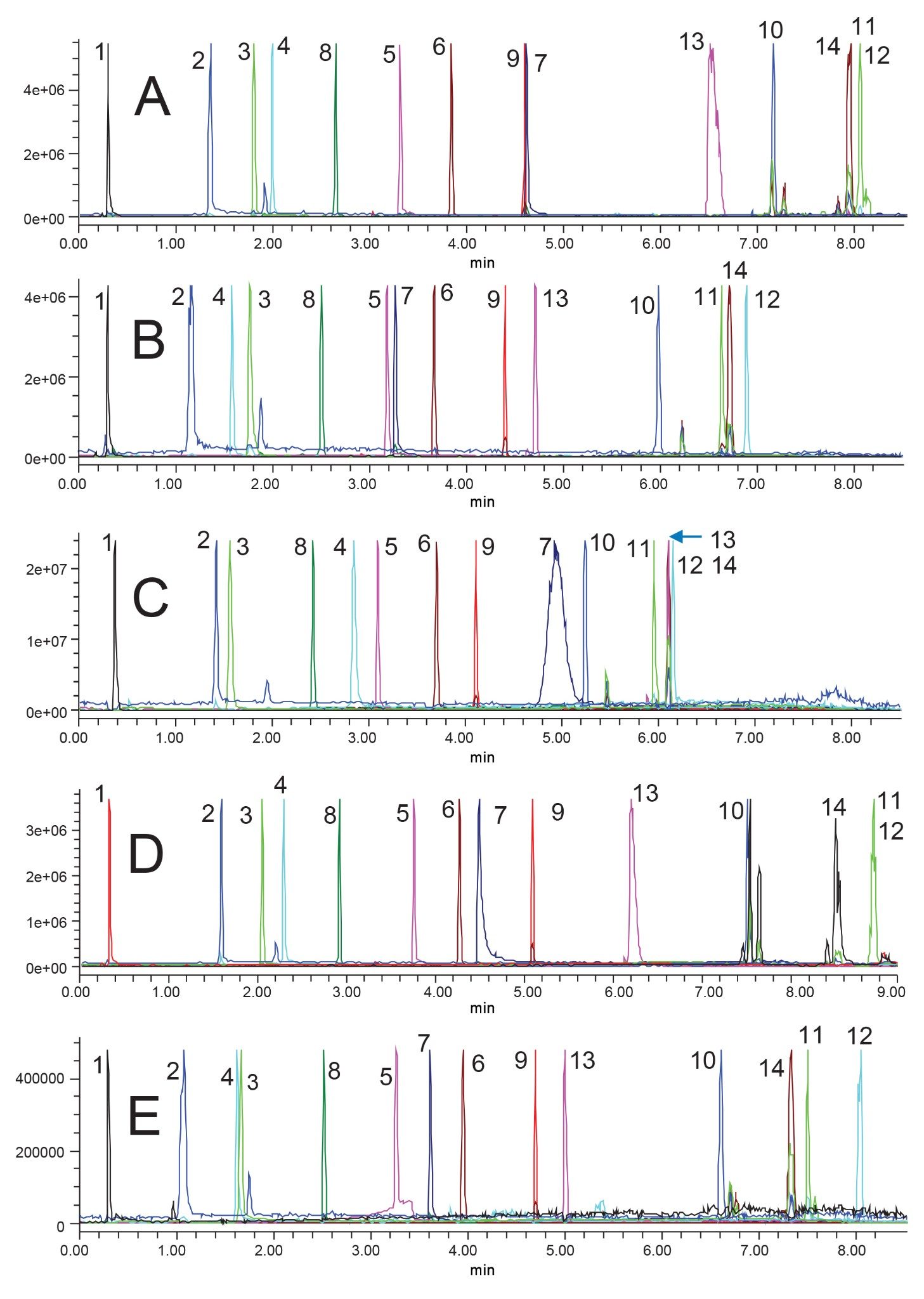
遗憾的是,使用乙腈不能为该样品提供可用的方法。测试的所有色谱柱上都存在至少一组共洗脱峰。此外,对于HSS PFP (3C)、HSS T3 (3D)和BEH Shield RP18 (3E),至少有一个峰的峰形不佳。在HSS PFP色谱柱上,组分7的峰虽然对称性良好,但非常宽。在HSS T3色谱柱上,组分10的峰分裂,组分7的峰明显拖尾。在BEH Shield RP18色谱柱上,组分5的峰形较差,并且有一个与组分2的质量数相同的次级峰在组分3之后洗脱。由于这些条件都不符合我们的目标,因此只有在使用甲醇流动相未能得到合适的色谱图时,才会考虑这些条件。只有在检查了乙腈和甲醇的结果之后,才能选择最佳分离条件进行优化。
不过,即使未得到合适的色谱图,不同色谱柱之间仍然存在一些选择性差异。检查组分3和组分4的洗脱顺序,并在不同的色谱柱上追踪这些峰,可帮助我们深入了解这些组分的化学特性。例如,组分4在HSS颗粒色谱柱(无论是使用PFP固定相还是T3固定相)上的保留性最强,表明该组分具有弱碱性官能团,因为与BEH和CSH杂化颗粒相比,该探针与HSS颗粒上的游离硅醇可以更好地相互作用。在CSH苯己基柱和BEH Shield RP18色谱柱上,组分4在组分3之前洗脱,这一保留性能是认为组分4具有碱性官能团的有力证明。上述示例很好地说明了选择多种固定相对方法开发至关重要的原因。即使色谱柱结果不理想或未达到分析目标,通过考察分析物与不同固定相的相互作用,仍然可以对分析物的化学特性提供深入了解。
使用甲醇流动相的分析结果单一,能够满足方法的目标要求,这是使用ACQUITY Premier BEH C18色谱柱实现的。如图4A所示,所有峰都实现良好分离。组分3和4虽然洗脱时间接近,但也实现了基线分离,组分10、14和11的峰簇也是如此。这些探针的峰形也较为良好。使用甲醇时,其他被测色谱柱的结果都更差,出现了共洗脱现象。有趣的是,在HSS PFP色谱柱上使用乙腈(3C)时,组分7观察到宽峰,而使用甲醇流动相时(4C)未观察到。这可能是因为甲醇允许固定相与分析物之间发生一些次级相互作用。使用乙腈流动相时观察到的其他峰形问题,使用甲醇时未观察到,这可能是由于两种流动相的选择性略有不同所致。
与乙腈一样,不同固定相配合甲醇使用时所获得的选择性各不相同。此外,由于本研究同时使用了乙腈和甲醇,因此可以使用给定的固定相比较这两种流动相的效果。例如,如果将CSH苯己基柱配合乙腈使用时得到的分析结果(3B)与相同色谱柱配合甲醇使用时得到的分析结果(4B)相比较,可以看出选择性差异。虽然分析物的洗脱顺序不变,但使用这两种溶剂时,组分5、7、6、9和13的选择性均发生了变化。使用乙腈时,组分5和组分7共流出,而使用甲醇时这两种组分可以分离,但迫使组分7与组分6共流出。与甲醇相比,使用乙腈时,组分13的洗脱时间与组分9非常接近,这只能部分解释为流动相的洗脱强度所致。这些比较突出强调了在方法开发过程中同时筛选乙腈和甲醇的重要性。虽然这会增加检测过程所花费的时间,但从结果中收集信息至关重要。
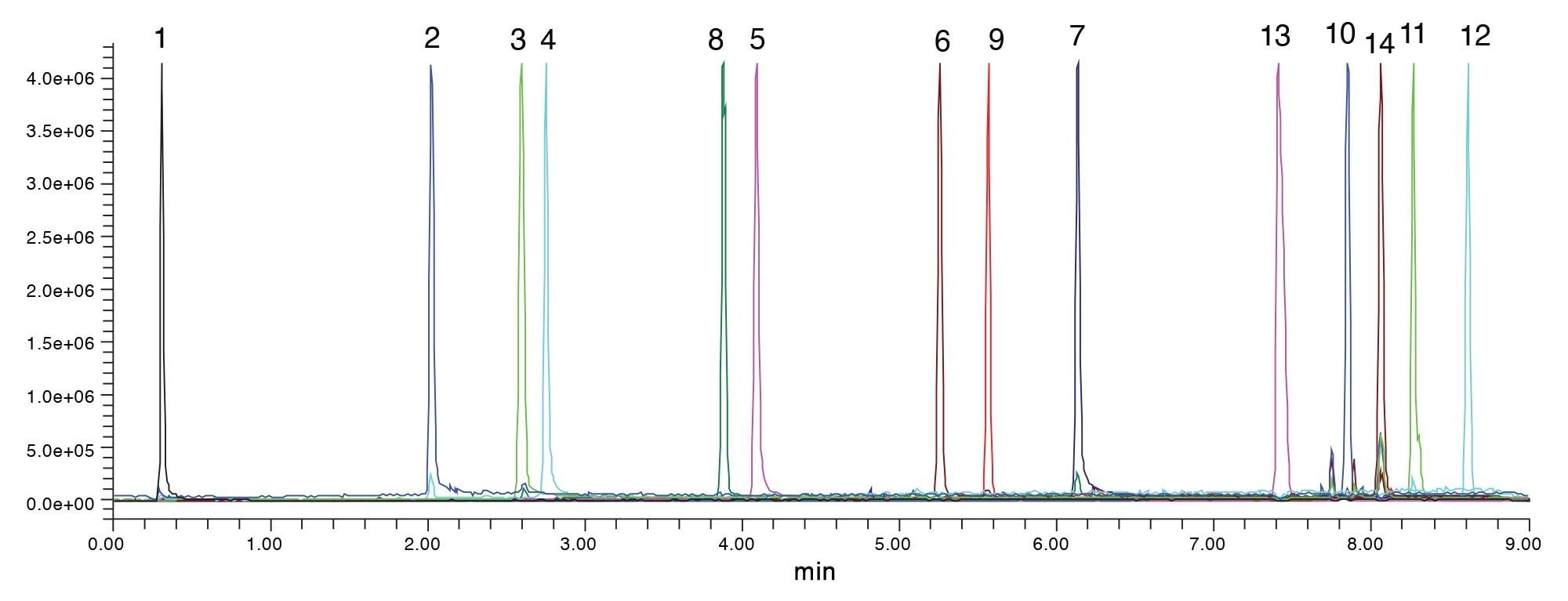
本研究所用样品的最终测试条件为:使用ACQUITY Premier BEH C18色谱柱,在甲醇流动相中添加甲酸,如图5所示。此方法现在可用于其他检测,包括降解物的定量甚至鉴定。此外,由于在批次检测中可能也需要监测降解物,因此可以将该方法转移到QC团队的产品放行检测中。
结论
强制降解研究在药物开发过程中很常见,因为不仅可以研究分子的稳定性,还可以对潜在的降解物评估其潜在毒性或其他影响。这些研究也可以作为在制剂药的批次放行检测中开发稳定性指示方法的第一步。本应用纪要展示了减肥药奥利司他的强制降解研究以及开发合适的稳定性指示方法的方法开发过程。我们将系统性筛选策略与MaxPeak Premier色谱柱结合使用,简化了方法开发过程。系统性筛选策略为分析人员在开发新方法时应遵循的步骤提供了严格的框架,有助于减少方法开发过程中的错误和疑虑。方法开发分三步进行:首先使用高pH和低pH流动相测试样品,评估保留性。接下来,锁定pH,使用多种固定相以及乙腈和甲醇流动相筛选色谱柱。最后,如果需要,可以在色谱柱筛选步骤优化最佳分离条件,以满足分析人员设定的所有分析标准。
使用MaxPeak Premier色谱柱可消除分析物与色谱柱硬件之间可能发生的任何非特异性吸附,进一步改进方法开发过程。首次进样即可获得可靠的数据,从而消除对结果的任何疑虑。确定结果之后,我们就能在方法开发过程中更快地制定决策。以奥利司他强制降解为例,我们在不到两天的时间内就开发出一种适用于所有14种分析物的方法。
参考资料
- Al-Suwailem A.K., Al-Tamimi A.S., Al-Oumar M.A., Al-Suhibani M.S. Safety and Mechanism of Action of Orlistat (Tetrahydrolipstatin) as the First Local Antiobesity Drug.Journal of Applied Sciences Research.(2006).205–208.
- Hadvary P, Lengsfeld H, Wolfer HJ.Inhibition of Pancreatic Lipase In Vitro by the Covalent Inhibitor Tetrahydrolipstatin.Biochemical Journal.(1989) 357–361.
- Maziarz M, McCarthy S, Wrona M. 使用系统性筛选策略提高方法开发效率.沃特世应用纪要.720005026ZH.
- Berthelette KD, Nguyen JM, Turner, J. 在配备UV和QDa检测器的ACQUITY Arc上使用系统性筛选策略对10种抗生素化合物进行方法开发.沃特世应用纪要.720007352ZH.
- Berthelette KD, Turner JE, Walter TH, Haynes K. 使用系统性筛选策略和MaxPeak HPS技术开发去铁胺及其强制降解产物的UHPLC分析方法.沃特世应用纪要.720007834ZH.
- Hong P, McConville P. 在液相色谱方法开发中实施系统性筛选策略的全面解决方案,沃特世白皮书.720005268ZH。
- Delano M, Walter TH, Lauber M, Gilar M, Jung MC, Nguyen JM, Boissel C, Patel A, Bates-Harrison A, Wyndham K. Using Hybrid Organic-Inorganic Surface Technology to Mitigate Analyte Interactions with Metal Surfaces in UHPLC.Anal.Chem. 93 (2021) 5773-5781.
- Walter TH, Alden BA, Belanger J, Berthelette K, Boissel C, DeLano M, Kizekai L, Nguyen JM, Shiner S. Modifying the Metal Surfaces in HPLC Systems and Columns to Prevent Analyte Adsorption and Other Deleterious Effects.LCGC Supplements (2022) 28–34.
- Smith K, Rainville P. 利用MaxPeak高性能表面和Atlantis Premier BEH C18 AX色谱柱提高LC-MS分析的灵敏度.沃特世应用纪要. 720006745ZH.
- Reed C, Hong P, Wong N, Birdsall R. 在ACQUITY™ Premier系统上使用MaxPeak™ Premier色谱柱技术改善含磷酸肽的肽图分析分离结果.沃特世应用纪要. 720008136ZH.
- Addepalli B, Araya M, Lauber MA.使用MaxPeak Premier BEH C18 300 Å寡核苷酸分析专用柱改善长链寡核苷酸分析物的分离度.沃特世应用纪要. 720007926ZH.
- Jung MC, Lauber MA.MaxPeak高性能表面(HPS)技术在改善灵敏度和动态范围方面的表现:关于核苷酸检测的案例研究.沃特世应用纪要. 720007053ZH.
- Zabala G, Berthelette K, Gu W, Haynes K. 使用改为2.5 µm颗粒的MaxPeak Premier色谱柱提高USP专论方法分析对乙酰氨基酚的重现性,沃特世应用纪要. 720007938ZH.
- Boissel C, Walter TH, Shiner S. ACQUITY Premier解决方案改善去铁胺(一种铁螯合药物)的UPLC-MS分析.沃特世应用纪要.720007239ZH.
- Berthelette K, Deloffi M, Kalwood J, Haynes K. 使用MaxPeak Premier HPLC色谱柱在Alliance HPLC系统上进行Janus激酶抑制剂巴瑞替尼的强制降解研究.沃特世应用纪要. 720008113ZH.
- Berthelette K, Turner J, Walter TH, Haynes K. 使用系统性筛选策略和MaxPeak HPS技术开发去铁胺及其强制降解产物的UHPLC分析方法.沃特世应用纪要. 720007834ZH.
- Alden B, Smith K, Rainville P, Walter TH, Gilar M. Retention of Anions on Charged Surface Hybrid Columns.Waters Poster. https://www.waters.com/webassets/cms/library/docs/2018hplc_alden_csh_anions.pdf
720008225ZH,2024年3月