核酸聚合酶是催化遗传信息复制和转录的酶,因此它们也是非常重要的药用靶点,这不足为奇。病毒聚合酶与人类聚合酶之间的结构差异为有效的抗病毒治疗带来了希望,可以用底物模拟抑制剂靶向病毒DNA或RNA聚合酶。SARS-CoV-2的RNA聚合酶负责基因组复制。针对新型冠状病毒的多种抗病毒治疗目前正在开展临床试验,以考察其体外疗效。其中一种药物甚至已被FDA批准用于COVID-19治疗,即瑞德西韦(GS-5734),这是一种氨基磷酸酯前药,可在细胞内转化为具有活性的三磷酸盐形式。这些抗病毒药及其他类似药物的前景使新药发现项目和临床研究激增。
在某些情况下,通过液相色谱与光学检测或质谱联用来监测生物转化活动具有重要意义。迄今为止,核苷酸类似物大都使用离子配试剂(如三丁胺)进行分离1。 这些离子对试剂有助于改善亲水性酸性分析物的保留性能,对金属吸附所致的样品损失问题有抑制作用。同时,强离子对试剂(如三丁胺)可能抑制电离,导致难以切换回其他LC-MS技术。
本应用纪要利用杂化硅胶表面以及混合模式色谱法,采用醋酸铵流动相,为体外细胞分析或药代动力学分析和剂量研究可能适用的方法提供了一个良好开端。
有关本应用的更多信息,或者如需了解沃特世如何帮助您抗击COVID-19疫情,请联系COVID19Response@waters.com
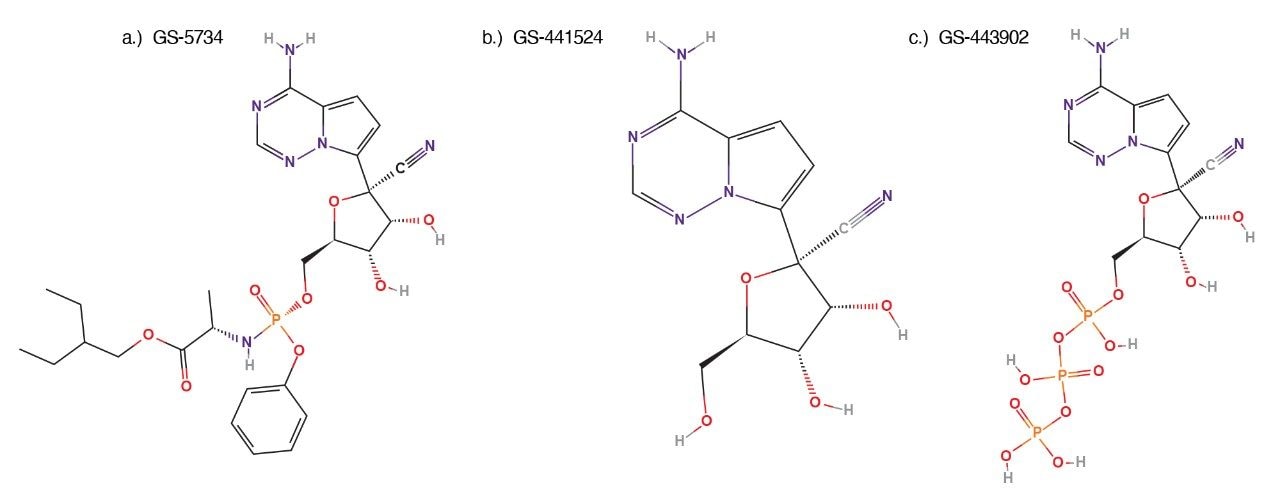
瑞德西韦(GS-5734,图1a)是一种试验性小分子抗病毒药,已证明对包括冠状病毒在内的多个病毒家族的RNA病毒具有活性。瑞德西韦是核苷GS-441524(图1b)的前药,两者都在细胞内代谢为具有活性的三磷酸核苷(GS-443902,图1c)5。 瑞德西韦最初开发用于治疗埃博拉病毒感染2,业界目前开展了大量研究,旨在改变现有抗病毒药物的用途,使其能够单独或与其他疗法联合用于治疗SARS-CoV-2感染4。
在这些分子的分离中,三磷酸核苷的保留和峰形是一项无法避免的挑战。尽管使用离子对试剂和HILIC模式色谱可以分离该化合物,但我们选择将混合模式色谱与醋酸铵缓冲液结合使用,考察其与光学检测器或质谱检测器配合使用时能否实现简单、快速的分析。
混合模式色谱(MMC)利用固定相与分析物之间的多种相互作用来实现分析物的分离。流动相pH、离子强度和有机物含量均可能影响分析物的保留和选择性。Atlantis BEH C18 AX固定相是基于亚乙基桥杂化颗粒的混合模式反相/阴离子交换固定相3。 利用亚乙基桥杂化颗粒,流动相pH值的适用范围更宽,C18基团与阴离子交换基团的存在也提供了基于疏水性或离子特性分离分析物的能力。此外,Atlantis BEH C18 AX固定相是一款使用MaxPeak高性能表面色谱柱硬件进行填充的色谱材料,旨在减少酸性分析物与不锈钢的相互作用6。
使用Atlantis Premier BEH C18 AX色谱柱,在以下实验条件下分析瑞德西韦(GS-5734)、其母体核苷(GS-441524)和三磷酸核苷(GS-443902)。
|
液相色谱系统: |
ACQUITY Premier四元系统 |
|
检测器1: |
ACQUITY Premier PDA检测器 |
|
检测器2: |
ACQUITY QDa质谱检测器 |
|
色谱柱: |
Atlantis Premier BEH C18 AX 1.7 μm色谱柱(2.1 × 50 mm) |
|
柱温: |
50 °C |
|
样品温度: |
12 °C |
|
进样体积: |
1 μL |
|
流速: |
0.5 mL/min |
|
流动相A: |
100%乙腈 |
|
流动相B: |
IonHance CX-MS浓缩液A,pH 5(按1:5稀释),部件号:186009280 |
|
流动相C: |
100% 18MΩ水 |
|
流动相D: |
IonHance醋酸铵浓缩液,pH 6.8(按1:5稀释),部件号:186009705 |
标准品从多家供应商购得。瑞德西韦(GS-5734,图1a)购自Ambeed(美国伊利诺伊州阿灵顿海茨,邮编60004),瑞德西韦核苷(GS-441524,图1b)购自Biosynth-Carbosynth(美国伊利诺伊州艾塔斯卡,邮编60143),三磷酸瑞德西韦核苷(GS-443902,图1c)购自AOBIOUS, Inc(美国马萨诸塞州格洛斯特,邮编01930)。
将瑞德西韦和三磷酸瑞德西韦核苷按500: 50 μg/mL和50: 500 μg/mL的浓度比配制同时包含这两种标准品的溶液。这些浓度比旨在模拟从给药到开始代谢转化的两个不同的时间点。将瑞德西韦核苷的单组分标准品制成浓度为10 μg/mL和100 μg/mL的溶液。
利用四元泵和IonHance浓缩缓冲液(包含20% (v/v)乙腈)在线制备色谱流动相。将制得的浓缩缓冲液用4%乙腈按1:5的比例稀释,使IonHance CX-MS浓缩液A (pH 5)的最终浓度为100 mM,IonHance醋酸铵浓缩液(pH 6.8)的最终浓度200 mM。将1:5稀释液与18 MΩ水和乙腈混合以创建梯度。最终梯度为:使用线性梯度(曲线6),在4 min内从0%乙腈:5 mM醋酸铵(pH 6.8)增加至60%乙腈:20 mM醋酸铵(pH 6.8);然后在0.5 min内恢复至初始条件。在较长时间的8 min梯度运行中,也得到了良好的结果(图2)。
瑞德西韦的logP值(2.01)中等,因此预测需要相对较高百分比的乙腈以洗脱前药。同时预测pH对于三磷酸核苷的保留具有重要影响。
使用等度洗脱条件以及用10 mM醋酸铵制得的流动相(乙腈含量范围40%~60%),计算一系列进样得到的瑞德西韦的保留因子。此外,本研究还评估了pH值4.8和6.8的影响。
为获得大于1但小于10的保留因子,无论水性流动相的pH值如何,都需要对瑞德西韦使用至少40%~60%的乙腈。优选较高的有机相终点,以便将该方法潜在地应用于其他疏水性更高的分析物。与筛选瑞德西韦的分析条件一样,三磷酸瑞德西韦核苷的分析也使用了两个pH值。但大多数分析均使用优选的pH 6.8。尽管二磷酸盐与三磷酸盐形式之间的分离度稍低,但是在较高的pH下得到的峰仍比采用pH 4.8的流动相所得到的峰更尖锐。必要时可以调节流动相pH以微调分离结果。
两种标准溶液的比较如图2所示。上方色谱图(图2a)由瑞德西韦:三磷酸瑞德西韦核苷10:1的样品获得,下方色谱图(图2b)则由相反比率(瑞德西韦:三磷酸瑞德西韦核苷1:10)的样品获得。图2a和图2b中瑞德西韦的柱上载样量分别为约0.8 nmol和0.08 nmol,与Gilead Sciences之前在生物分析研究中所用的实验条件相当1。

使用ACQUITY QDa质谱检测器确认峰鉴定结果,并提取各种分析物的m/z值(图3)。还利用最终梯度分析了瑞德昔韦核苷(GS-441524)(图4)。虽然该分析物在梯度中较早洗脱,不干扰三磷酸核苷,但它可能为进一步优化梯度提供新的开端。


混合模式固定相Atlantis BEH C18 AX提供了独特的选择性,在包含多官能团分析物的样品分析中,它被视为一种良好的方法设计开端。
本应用纪要利用pH稳定的杂化硅胶颗粒表面,并在pH 6.8下操作混合模式色谱柱,如果与传统的硅胶基质反相/混合模式固定相配合使用,该pH可能导致分析物降解。Atlantis BEH C18 AX混合模式固定相同时具有C18和阴离子交换基团,均可促进色谱分离。在pH 6.8下,在梯度内调整阴离子交换位点以洗脱三磷酸瑞德西韦,而C18基团在瑞德西韦的保留方面发挥更重要的作用。在这些条件下,三磷酸瑞德西韦可以实现良好保留并与瑞德昔韦充分分离,这也是本研究的主要目的。 可对方法进行其他优化,以提高三磷酸瑞德西韦的峰对称性,例如减少柱上进样量。
在分离中使用不含离子对试剂的醋酸铵流动相,从而可以选择使用光学检测以及质谱检测。通过使用现成的MS认证浓缩缓冲液,可快速、轻松地制备流动相。
随着新药发现项目的启动,分析人员可能希望将该方法应用于体外细胞研究。同样,通过进一步优化,该技术可能在分析由生物体液制备的聚合酶抑制剂及其代谢物方面受到青睐。
720007146ZH,2021年2月