本文介绍了一种利用单四极杆质谱检测器ACQUITY QDa同时分析血清中维生素A和E的临床研究方法。萃取方法为之前所用LC-MS/MS方法的改进版,使用HLB Prime进行样品制备。色谱分析采用ACQUITY UPLC HSS PFP色谱柱进行,结合SIR模式下的ACQUITY QDa检测,提供了一种准确、灵敏的方法来分析血清中的维生素A和E。进样周期仅5 min,对血清中维生素A和E的灵敏度分别达到100 ppb和1 ppm。
过去,大多数维生素A和E分析都是采用配备UV检测器的HPLC系统。即使采用LC-MS/MS方法分析维生素A和E,液-液萃取(LLE)等萃取方法仍需要很长的萃取时间,且溶剂消耗量大,分析时间长。之前,我们已经展示了一种基于LC-MS/MS的临床研究方法,该方法仅需要100 μL的样品体积,并缩短了分析时间1。 利用Oasis HLB PRiME (SPE)去除磷脂是性能提升的关键因素。本技术简报将展示LC-MS如何对血清中的维生素A和E实现准确、灵敏地分析。
将同位素标记的内标加入100 μL血清中,然后添加乙醇进行蛋白沉淀。离心后,将上清液用乙醇/水(5:3)稀释,使乙醇/水的最终比例为2:3。将650 μL所得溶液加载到Oasis HLB洗脱板上进行样品净化。用20%乙腈水溶液洗涤样品,然后用100%乙腈洗脱。将洗脱液用水进一步稀释至200 μL(图1)。利用HLB PRiME可免去活化和蒸发步骤。将20 μL所得提取物进样至LC-MS进行分析。
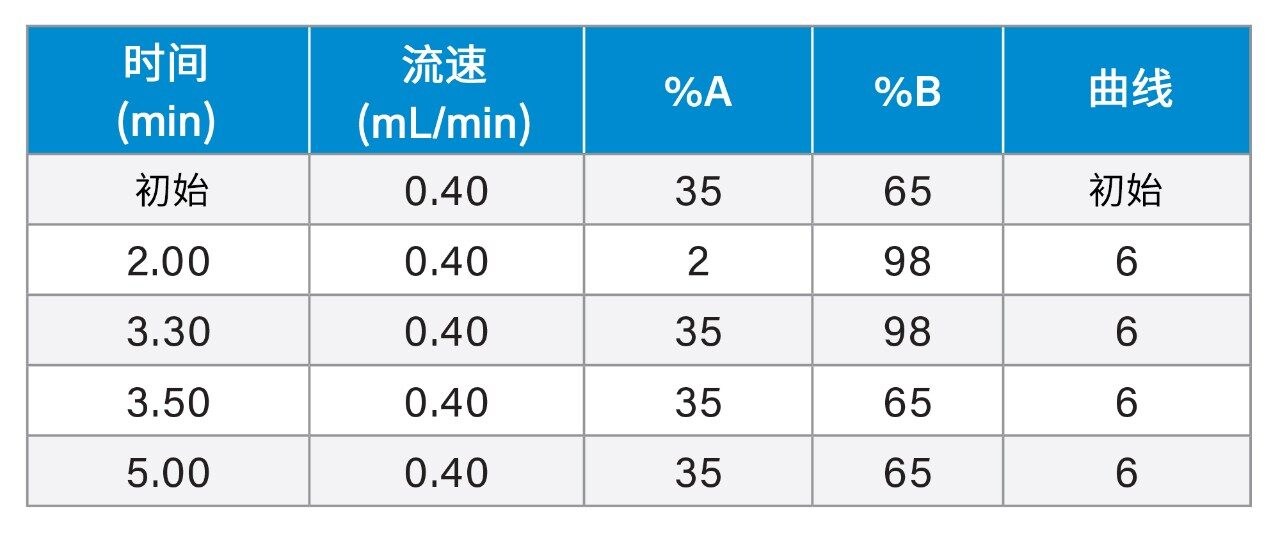
使用装配ACQUITY HSS PFP色谱柱(1.8 μm, 2.1 x 50 mm,部件号:186005965)的ACQUITY UPLC H-Class PLUS系统,用65%流动相A (MP A)增加至100% MP A的梯度进行洗脱,以达到分离目的。利用ACQUITY QDa在ESI正离子和SIR模式下检测相应的质子化加合物。进样周期为5 min。
|
液相色谱系统: |
ACQUITY UPLC H-Class参数 |
|
样品瓶: |
包含1 mL内衬管的96孔收集板(部件号:186000855) |
|
色谱柱 |
ACQUITY UPLC HSS PFP色谱柱, 2.1 × 50 mm, 1.8 µm(部件号:186005965) |
|
柱温: |
40 °C |
|
样品温度: |
10 °C |
|
进样体积: |
20 µL |
|
流速: |
0.40 mL/min |
|
流动相A: |
水 + 2 mM醋酸铵 + 0.1%甲酸 |
|
流动相B: |
甲醇 + 2 mM醋酸铵 + 0.1%甲酸 |
|
质谱系统: |
ACQUITY QDa |
|
电离模式: |
ESI+ |
|
采集模式 |
SIR |
|
毛细管电压: |
0.8 kV |
|
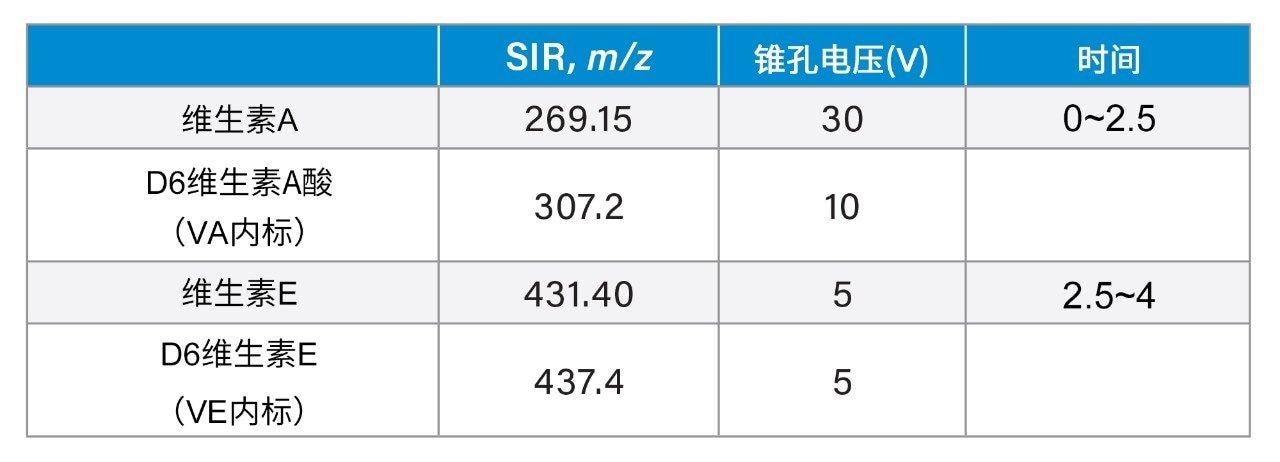
锥孔电压: |
参见通道详情 |
|
LC-MS软件: |
MassLynx 4.2版 |
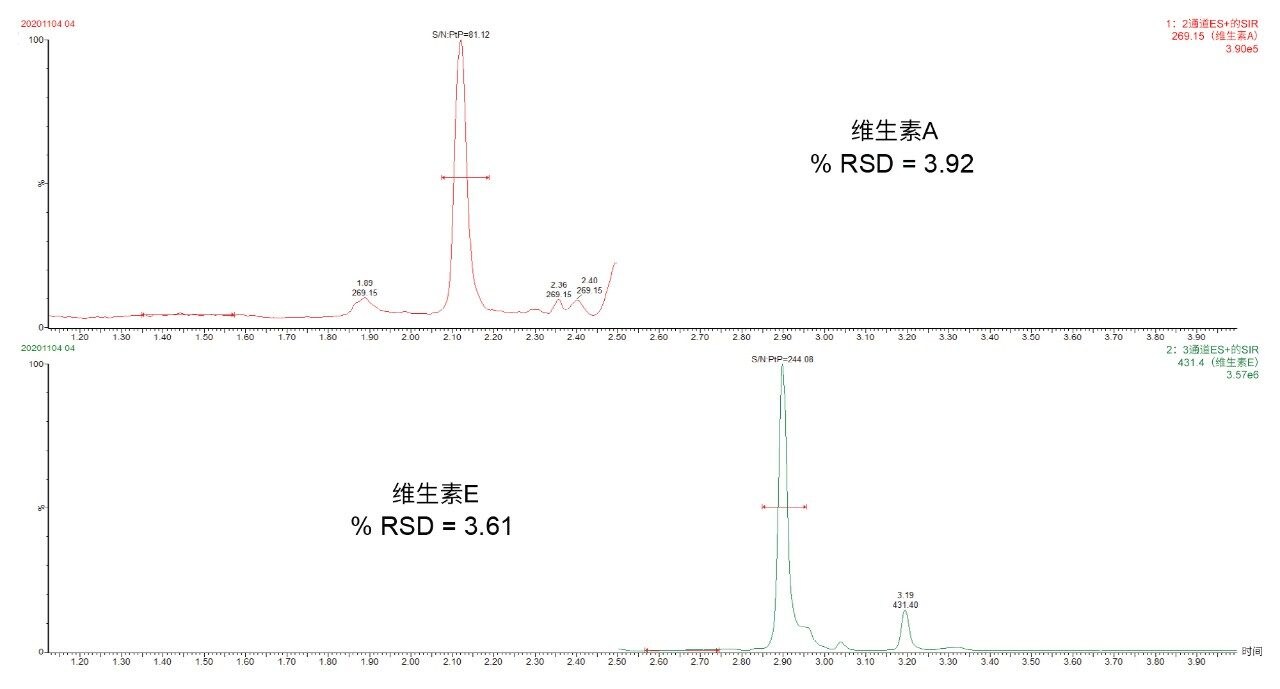
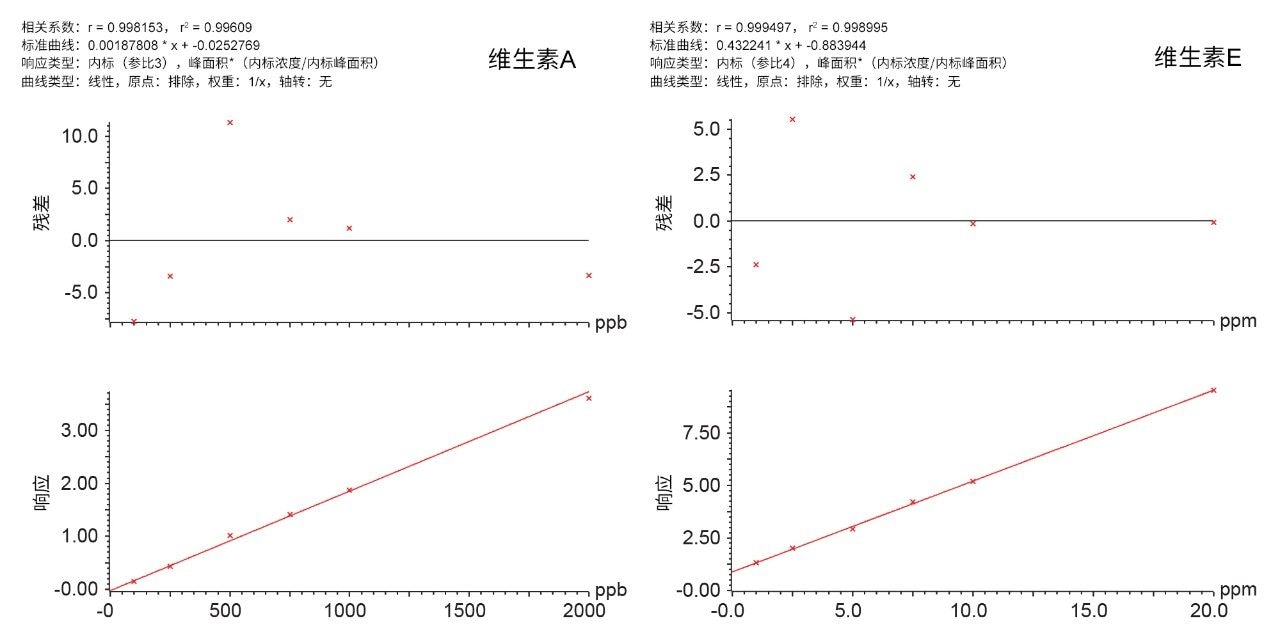
图2显示了经处理的血清(MSG2000)中100 ppb维生素A和1 ppm维生素E的色谱图。分析灵敏度研究表明,100 ppb维生素A和1 ppm维生素E均可实现定量分析(%RSD <20,偏差<15%,S/N >10)。对于维生素A,该方法在100 ppb至2000 pp的范围内呈线性;对于维生素E,则在1 ppm至20 ppm的范围内呈线性。两种化合物在10次独立试验中得到的相关系数(r2) >0.993。图2列举了一些标准曲线。
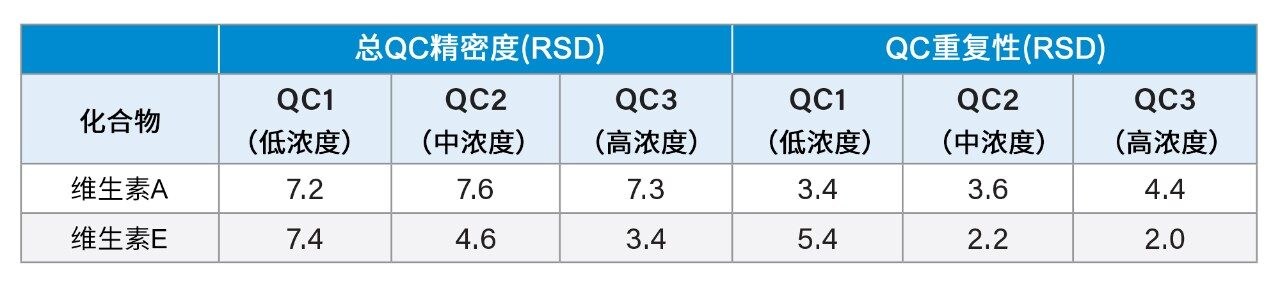
通过在5天内提取并分析经处理的血清中低浓度到高浓度的5个重复样品(n = 25),评估方法精密度。维生素A和E在所有检测浓度下的重复性和总精密度均≤8% CV,结果汇总于表1中。测试样品与对照样品相比,检测的典型内源性干扰物质的所有%回收率计算值均在±15%以内。
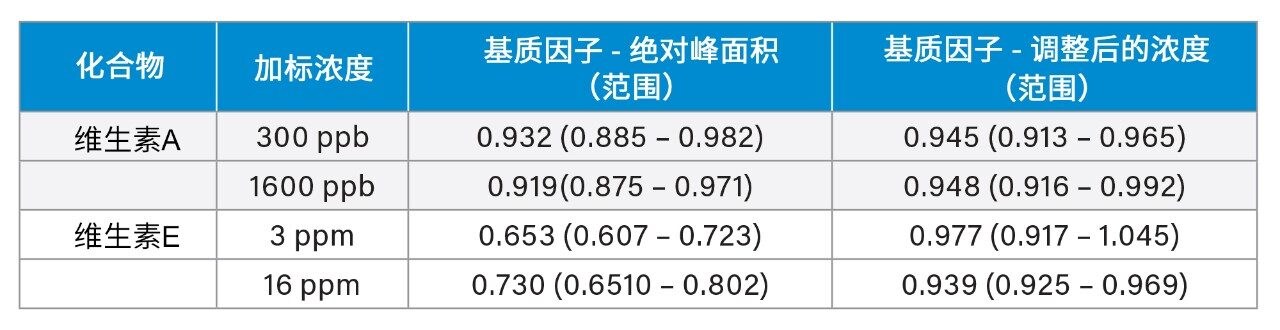
使用内标进行补偿后,来自六个供体的测试样品与对照样品之间的基质因子结果在±15%范围内(表2)。在维生素E中观察到基质抑制作用(平均值=0.653和0.730),但得到内标补偿(平均值=0.977和0.939)。
本文探讨了UPLC单四极杆质谱系统ACQUITY UPLC-ACQUITY QDa在脂溶性维生素临床研究分析中的应用。结果表明,即使在复杂基质中,该方法也具有良好的准确度和分析灵敏度。与LLE相比,样品制备相对简单,运行时间相比传统的HPLC-UV方法大大缩短。
720007164ZH,2021年2月