Las terapias genéticas basadas en vectores virales son formulaciones de productos farmacéuticos de gran tamaño compuestas por proteínas y ácidos nucleicos que contienen más de 200 000 átomos. La cromatografía líquida (LC) de Waters combinada con la detección óptica (UV, MALS) y la espectrometría de masas (MS) proporcionan los medios analíticos para caracterizar y cuantificar con exactitud estas estructuras heterogéneas y sus atributos, tanto a niveles intactos como de componentes, lo que da soporte a soluciones de vectores virales robustas. Las mediciones de rutina incluyen el título viral, el análisis de agregados/impurezas, los ratios de proteínas virales, el análisis de modificación y mapeo de péptidos, la eficacia de la encapsidación y la integridad del genoma en los flujos de trabajo de las soluciones de vectores virales.
Seminario online: Unión de la innovación y la industria mediante la espectrometría de masas con detección de carga
Acelere el proceso desde el análisis de muestra hasta la toma de decisiones con waters_connect para el análisis de soluciones de vectores virales y biofarmacéutico, con aplicaciones para el análisis de masa intacta, la confirmación de secuencias, la monitorización de procesos y mucho más.
Equipe el laboratorio con el CDS Empower y obtenga gestión avanzada de los datos del laboratorio para los análisis de vectores virales, lo que incluye la adquisición, el tratamiento y la generación de reportes.
El software ASTRA proporciona control del instrumento, adquisición de datos, análisis y generación de reportes con el módulo de análisis de vectores virales. Proporcionamos un método SEC-MALS de plataforma, creado específicamente para la cuantificación de AAV, que se puede personalizar fácilmente para cada producto y cada serotipo.
Permita la medición de varios atributos, incluido el análisis de variantes por tamaño y agregación, con las columnas GTxResolve Premier SEC de alta eficacia de Waters, que aceleran el análisis y reducen el consumo de muestra.
Mejore la recuperación con la cromatografía AEX de Waters, que utiliza una fase estacionaria no porosa de alta eficacia (p. ej.: Protein-Pak Hi Res Q) combinada con gradientes salinos optimizados para una técnica compatible con el control de calidad (QC) para mediciones de vacío/lleno.
Identifique y mida la abundancia relativa de proteínas virales utilizando las columnas MaxPeak Premier BEH C4 con par iónico DFA para un rendimiento óptimo de LC y MS.
Fase estacionaria de amida diseñada para una alta reproducibilidad entre lotes de vectores virales, proteínas de cápside y ácidos nucleicos. Las variantes oxidadas y fosforiladas se pueden separar fácilmente de sus equivalentes no modificadas con una separación HILIC aplicada de forma óptima.
Confirme la secuencia, la modificación postranslacional (PTM) o la degradación de las proteínas virales mediante el mapeo de péptidos y las columnas CSH™ de Waters que proporcionan alta resolución para esta aplicación.
Optimice la productividad y el éxito de su laboratorio con Waters Global Services para mantener el máximo rendimiento del sistema, minimizar el tiempo de inactividad, abordar los desafíos de las aplicaciones y cumplir con los estrictos requisitos de cumplimiento normativo.
Maximice los recursos y minimice el riesgo con las opciones de pago de Waters Capital, que incluyen la actualización de equipos obsoletos, la obtención de soporte personalizado y la combinación de servicios en un único pago mensual.
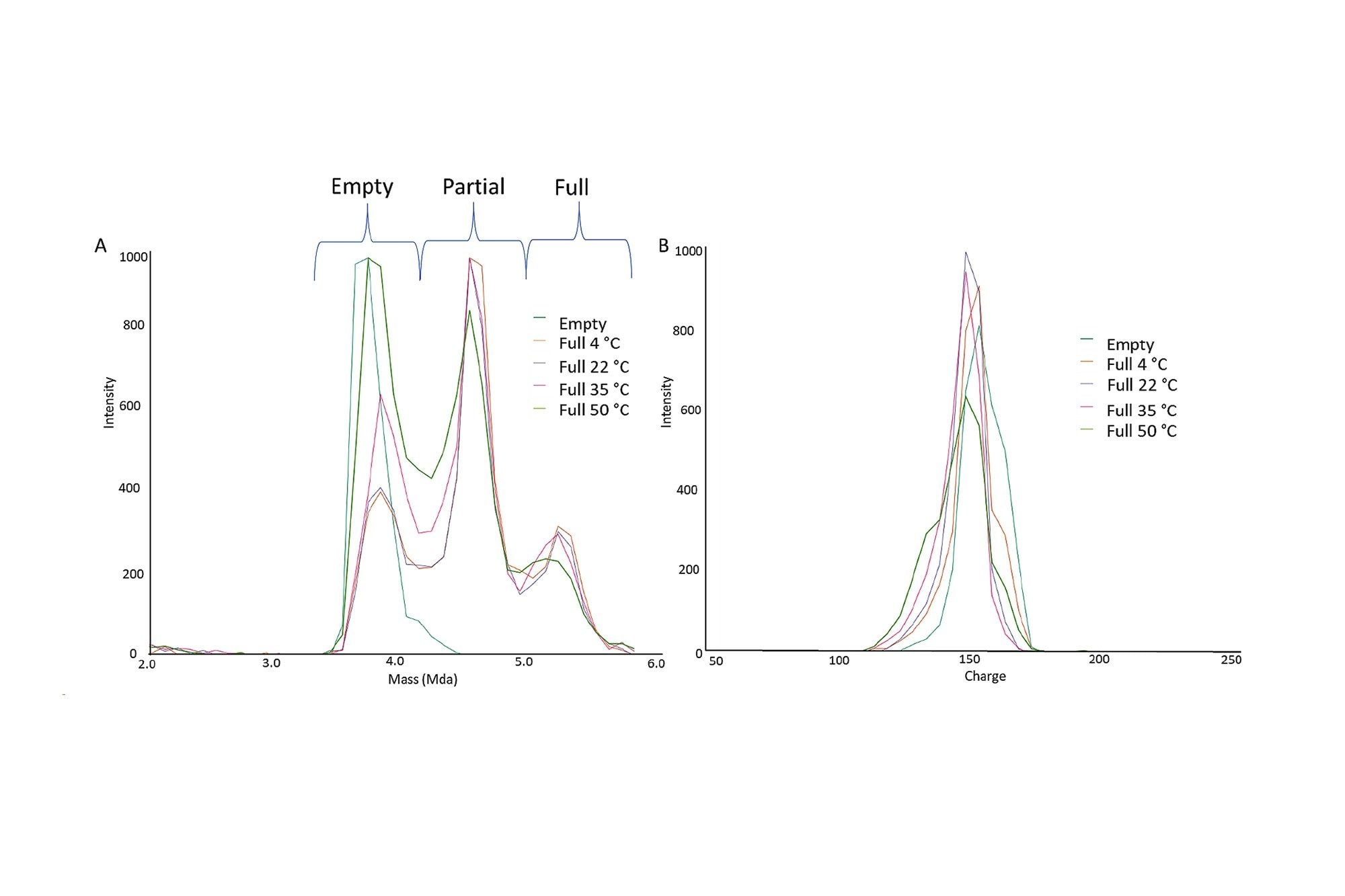
a) Espectro de masas superpuesto de AAV8 ampliado al intervalo de masas de 2,5-6 MDa con el 100 % de la cápside vacía y llena, tratada con incubaciones de 30 minutos a 4, 22, 35 y 50 °C. b) Espectro de carga de AAV8 ampliado al intervalo de masas de 2,5-6 MDa con el 100 % de la cápside vacía y llena, tratada con incubaciones de 30 minutos a 4, 22, 35 y 50 °C.
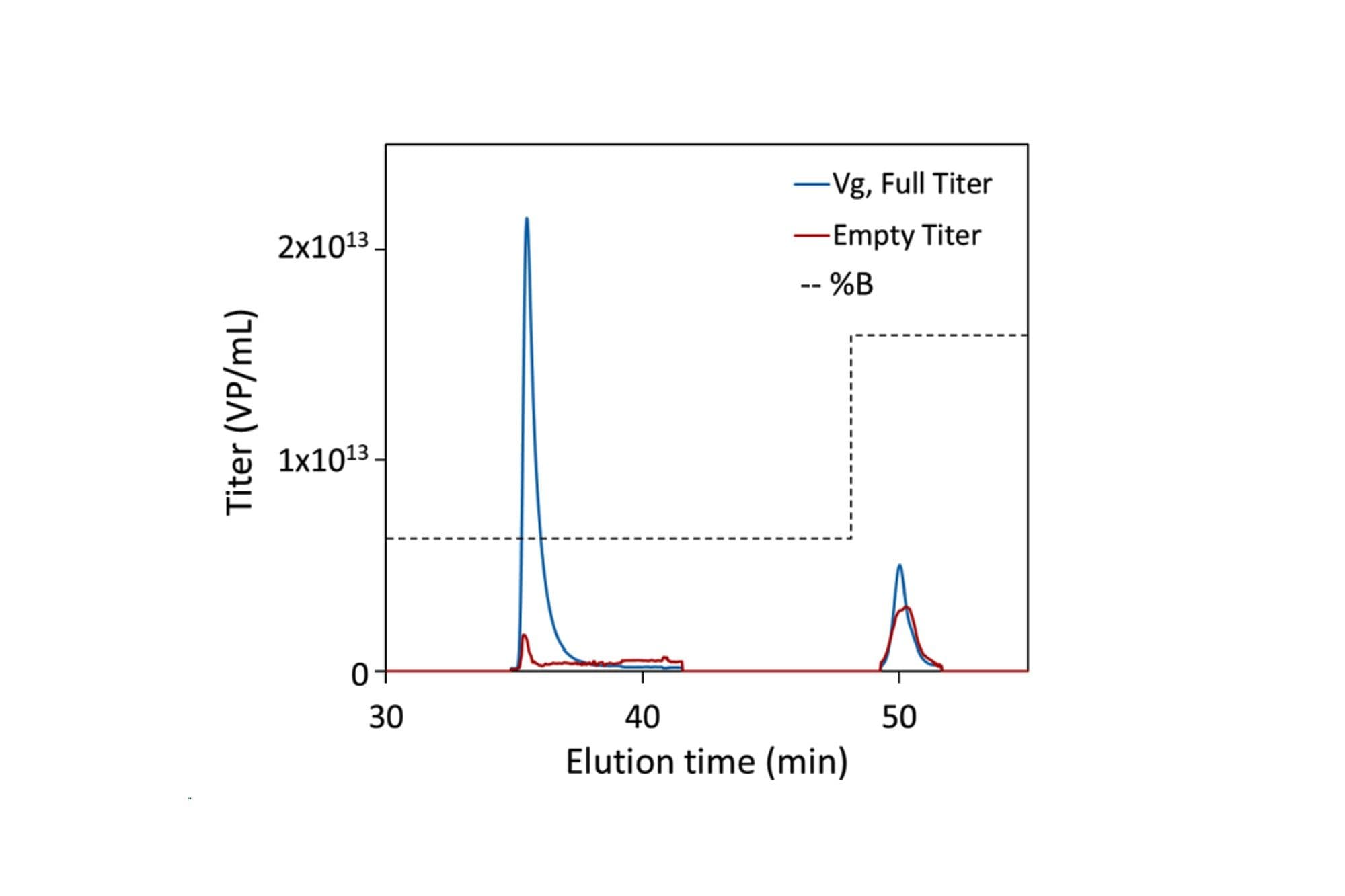
Títulos lleno (azul) y vacío (rojo) determinados por RT-MALS durante la elución (34-48 minutos) y la extracción (>48 minutos) en el gradiente lineal final. La fuerza iónica de la solución tampón se representa mediante la línea negra discontinua.
Vistas ampliadas de un cromatograma AAV2 obtenido con material de acero inoxidable (partícula de 4,6 x 150 mm, 5 µm, trazado rojo) frente a material MaxPeak HPS (columna XBridge Premier GTx BEH SEC de 450 Å y 2,5 µm, 4,6 x 150 mm, trazado negro). Las separaciones se realizaron con una fase móvil que contenía una solución tampón de fuerza iónica estándar (fosfato de 10 mM, pH de 7,4 + KCl de 200 mM).
La cuantificación relativa de las proteínas VP se midió mediante detección óptica, que incluía (A) UV y (B) fluorescencia (FLR). La anotación de picos muestra la asignación y la abundancia relativa calculada de los componentes detectados. Con la detección FLR, la relación S/N de VP3 es casi cinco veces mayor que la relación S/N del uso de detección UV con una carga de masa 10 veces mayor, lo que sugiere una mejora de aproximadamente 50 veces en la sensibilidad.
