多重反射 TOF MS テクノロジーを使用した、モノクローナル抗体の高度なペプチドマッピング
要約
ペプチドマッピングは、バイオ医薬品の特性解析およびモニタリング、特にモノクローナル抗体(mAb)などのバイオ医薬品の開発における主要なアプローチです。これにより、ペプチドレベルの詳細な分析を行って、タンパク質のアイデンティティーと配列の確認や、機能に影響を及ぼす可能性のある予測される修飾の位置特定や製品関連不純物の特定が行えます。さらに、十分に特性解析されたバイオ医薬品のペプチドマッピングは、プロセスモニタリングや後期開発、製品発売に役立ちます。
このアプリケーションブリーフでは、Waters™ mAb トリプシン消化標準試料の分析に、新規の多重反射飛行時間型(MRT)質量分析計と組み合わせた ACQUITY™ Premier UPLC システムを使用するメリットについて説明します。特性解析は、waters_connect UNIFI™ アプリのペプチドマッピングワークフローを用いて行いました。その結果により、Xevo MRT MS プラットフォームの高感度、高質量分解能、一貫した ppm 以下の質量精度、および waters_connect での統合されたデータ取り込み・解析機能が浮き彫りになっています。これにより、非常に信頼性の高い特性解析機能が得られ、製品開発およびプロセス開発においてより迅速かつ適切な意思決定が可能になります。
アプリケーションのメリット
- 高レベルの感度により、mAb の詳細な特性解析や低レベルの PTM およびペプチド特性の検出が可能に
- 5 桁のダイナミックレンジにより、低レベルのプロダクトバリアントや分解物を含む複雑なサンプルの分析が可能に
- 1 ppm 以下の一貫した質量誤差により、プロダクトおよび不純物の同定が確実に
はじめに
モノクローナル抗体(mAb)のペプチド消化物レベルの分析は、mAb 医薬品の品質と一貫性を確保するために、そのライフサイクル全体にわたって使用される主要な分析法です。バイオ医薬品のパイプラインが拡大されるにつれ、製品開発およびプロセス開発における効率的な意思決定のために、低レベルの mAb の修飾を正確かつ一貫して特性解析できる信頼性の高い自動分析法を展開することがますます重要になっています。これには、組織全体のラボに容易に展開できる、頑健で使いやすい分析プラットフォームが必要になります1。
Xevo MRT MS システムは、このようなプラットフォームの典型例です。このシステムでは、新規の四重極多重反射型飛行時間設計を使用してイオンの飛行経路を拡張することで、スキャンレート 50 Hz で最大 100K の質量分解能が得られ、デュアルゲイン ADC 検出器を使用して、より優れた感度、ダイナミックレンジ、ppm 以下の質量精度が可能になって、信頼性の高いペプチドマッピングが行えます。UNIFI アプリを搭載したコンプライアンス対応の waters_connect ソフトウェアにより、自動のデータ取り込み、解析、レポート作成が行え、統合および自動化されたワークフローにより、初期および拡張した製品特性解析に焦点を当てる MS コアラボの枠を超えて分子が移動する際における LC-MS 分析の利便性が向上します。
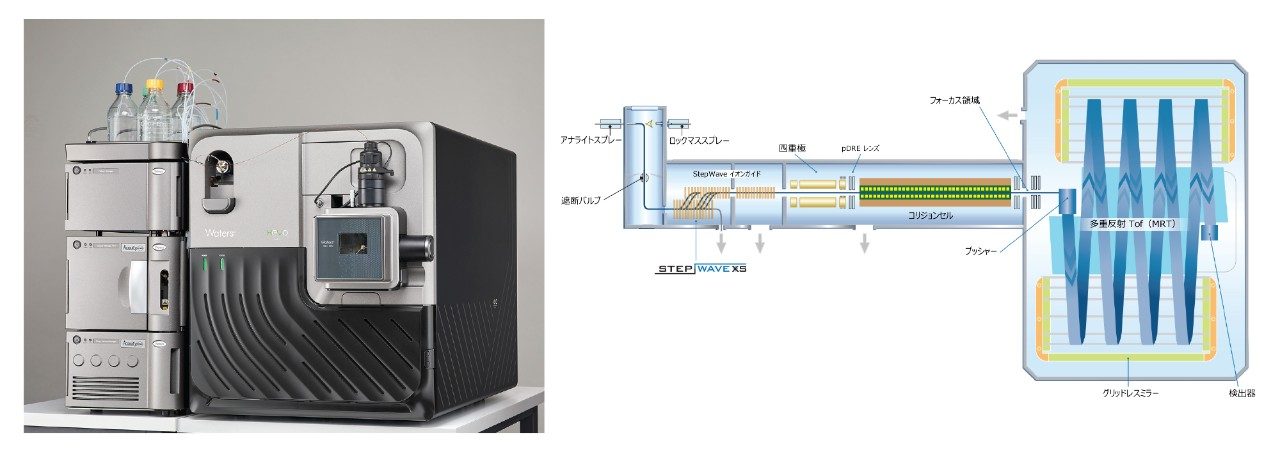
実験方法
サンプル
Waters mAb トリプシン消化標準試料(製品番号:186009126)を使用して LC-MS の性能を評価し、ペプチドレベルのタンパク質分析を行う際のシステム適合性を確保しました。この凍結乾燥標準試料は、マウス細胞株で発現したヒト化 IgG1κ である NIST レファレンス物質 8671(NIST mAb)を還元およびアルキル化したものです。
この mAb サンプルを調製するため、200 μL の超高純度 Milli-Q 水を 40 μg の消化物のバイアルに加え、濃度を 200 ng/μL にしました。次に、このサンプルをさらに希釈して、カラムロードを評価できる濃度範囲 2000 ng ~ 0.002 ng にしました。
LC 条件
|
LC システム: |
ACQUITY Premier UPLC システム(バイナリー) |
|
検出: |
UV 280 nm |
|
バイアル: |
TruView™ LCMS 品質保証 12 × 32 mm スクリューネックバイアル、トータルリカバリー、キャップおよびスリット入り PTFE/シリコンセプタム付き(製品番号:186005663CV) |
|
カラム: |
ACQUITY Premier BEH™ C18、1.7 µm 2.1 mm × 100 mm(製品番号:186009453) |
|
カラム温度: |
40.0 ℃ |
|
サンプル温度: |
6.0 ℃ |
|
注入量: |
0.2 ~ 10 µL |
|
流量: |
0.250 mL/分 |
|
移動相 A: |
0.1% ギ酸水溶液 |
|
移動相 B: |
0.1% ギ酸含有アセトニトリル |
グラジエントテーブル
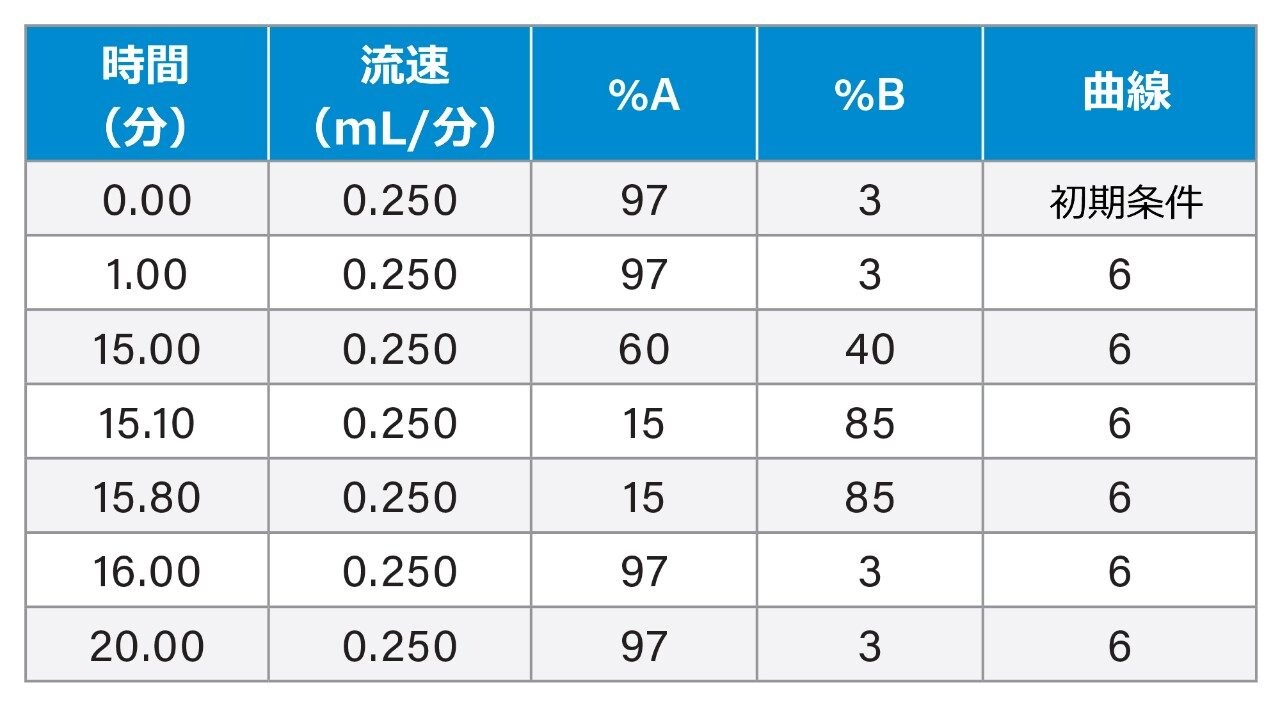
MS 条件
|
MS システム: |
Xevo MRT MS |
|
モード: |
フラグメンテーションによる MSE フルスキャン |
|
質量範囲: |
m/z 50 ~ 2000 |
|
極性: |
+ve |
|
スキャンレート: |
2 Hz |
|
コーン電圧: |
25 V |
|
フラグメンテーションコリジョンエネルギーランプ: |
25 ~ 50 V |
|
イオン源温度: |
120 ℃ |
|
脱溶媒温度: |
400 ℃ |
|
脱溶媒ガス: |
800 L/時間 |
|
キャピラリー電圧: |
3.00 kV |
結果および考察
NIST mAb 消化標準試料のペプチドマッピングデータを UPLC-Xevo MRT MS システムで取り込んで、ワークフロー全体のパフォーマンスを評価し、質量精度、質量分解能、感度に関する特定の装置機能をレポートしています。データ非依存的フラグメンテーションを使用して MSE モードでデータを取り込み、ペプチドの割り当て、割り当てられた修飾部位の位置特定を行いました。
waters_connect UNIFI アプリのペプチドマッピングワークフロー内の自動データ解析により、軽鎖と重鎖の両方について、質量許容範囲 1 ppm 未満で高いシーケンスカバー率(96% LC、98% HC)が得られました。図 2、3、4 に、ペプチドマッピング実験からの出力結果が含まれています。
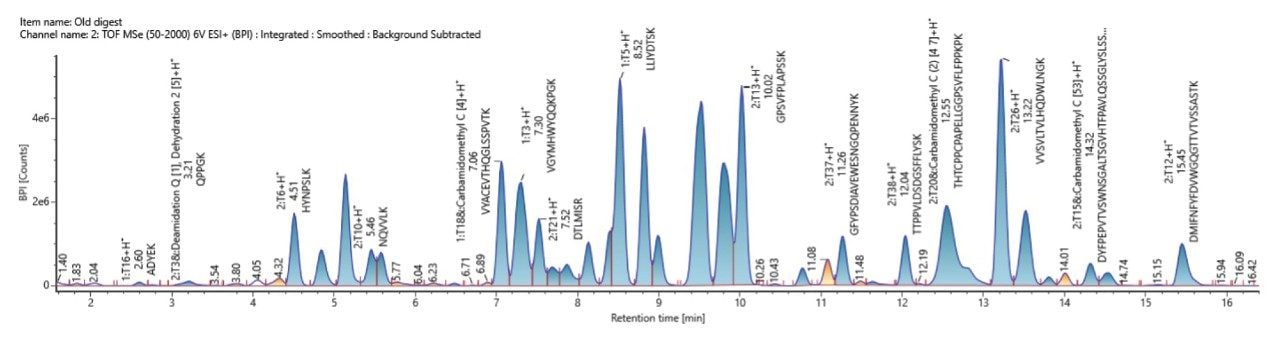

図 4 に示すように、割り当てられたペプチドのリストを NIST mAb の in-silico 消化物との比較により作成したところ、分析法で定義された修飾も説明されました。このリストは、強度、質量許容範囲、一致したフラグメントの数によってフィルタリングしてランク付けすることができます。高いランクで割り当てられたペプチドはすべて質量誤差が 1 ppm 未満であり、データ非依存的 MSE フラグメンテーションで得られた多数の一致する b/y フラグメントによってさらに確認されました2,3,4。
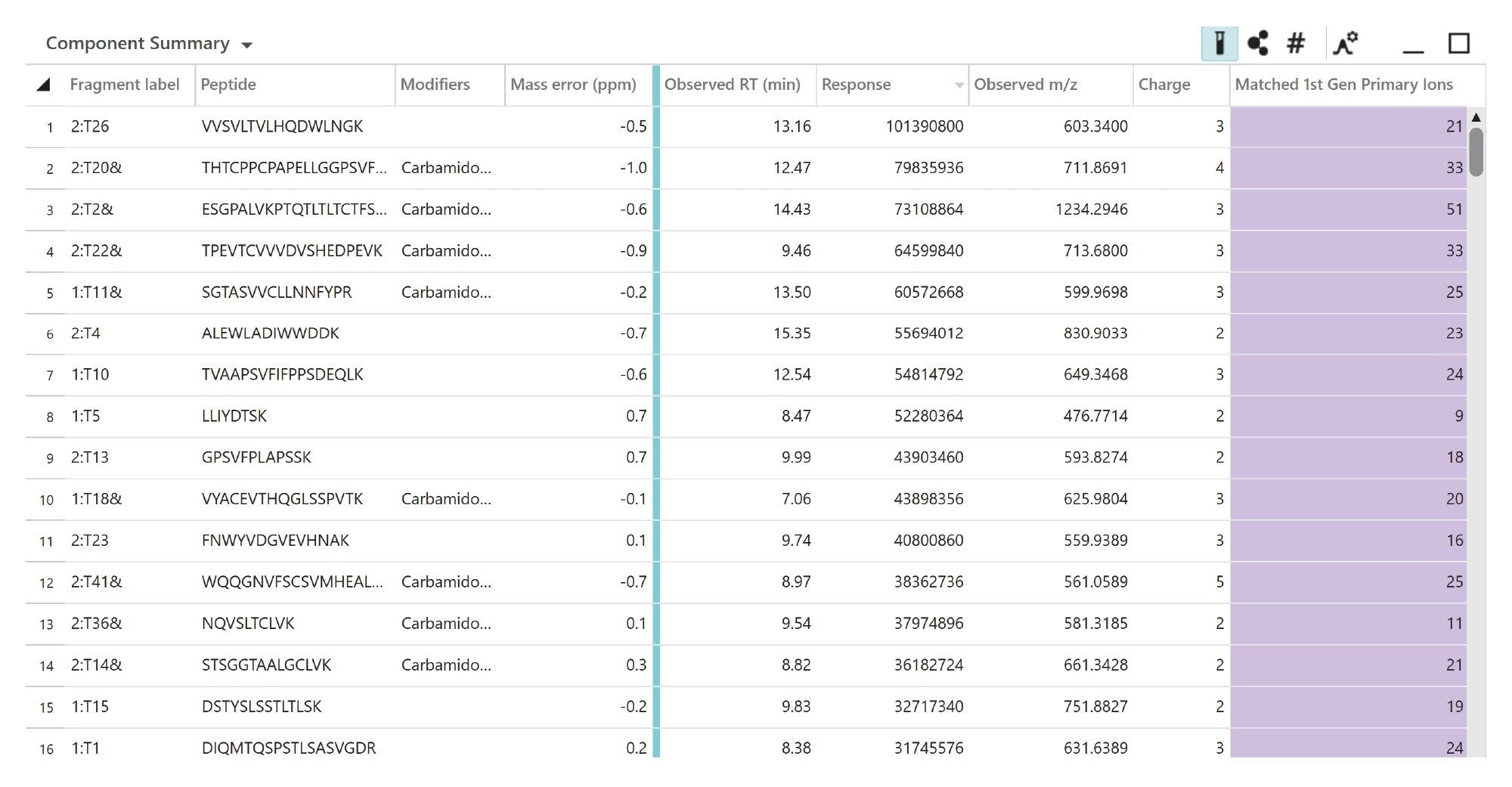
MSE を分析に利用することで、タンパク質のペプチドマッピングに基づく特性解析用の包括的なデータセットが得られます。従来のデータ依存的取り込みメソッドとは異なり、MSE はデータ非依存的取り込みを採用しており、1 回の分析ですべての MS1 ペプチドイオンの MS2 フラグメントイオンを捕獲することができます。このアプローチにより、精密質量フラグメンテーションデータに基づいた高いシーケンスカバー率と、MS1 ピークの定量による正確な定量の両方が、1 回の注入で得られます。MSE は、プリカーサーデータやフラグメントデータをルーチンに再現性よく生成できるため、ペプチドイオンの割り当て、タンパク質製剤やタンパク質原薬の製品関連バリアントや不純物の相対的定量に適しています。バイアスがないという MSE の性質により、低存在量のペプチドでも特徴的なフラグメントを確認でき、mAb の特性解析の詳細さおよび再現性が向上します。
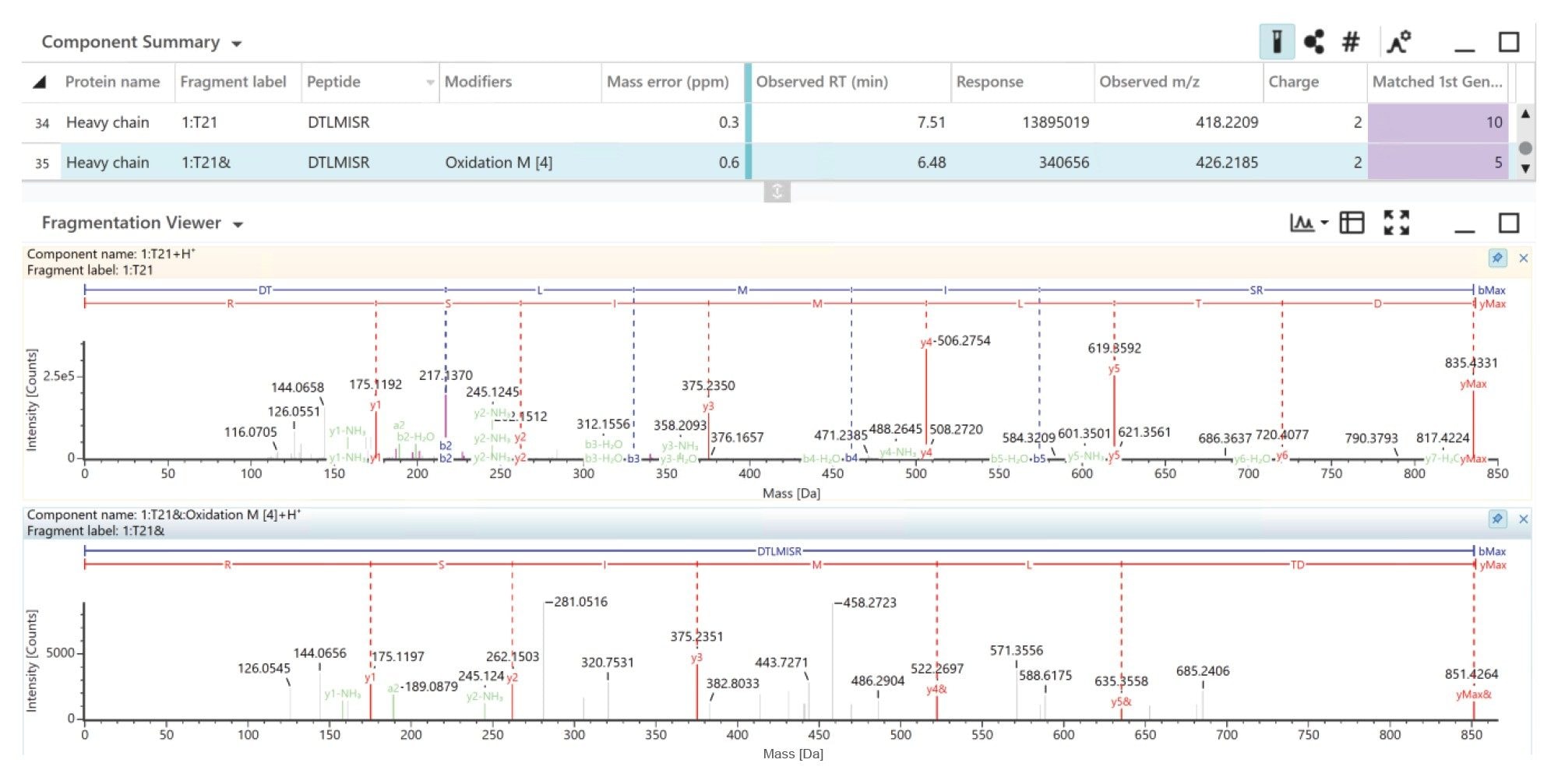
図 5 に DTLMISR ペプチドを示しており、ネイティブバリアントと酸化バリアントの両方が ppm 以下の質量精度で実測されています。DTLMISR ペプチドの酸化バリアント(RT 6.48 分)は、非修飾ペプチド(RT 7.52 分)より早く溶出しています。質の高い MSE フラグメンテーションスペクトルにおいて、y4、y5 およびプリカーサーで +15.9949 Da の質量シフトが確認され、メチオニン残基で酸化が起きていることがわかります。
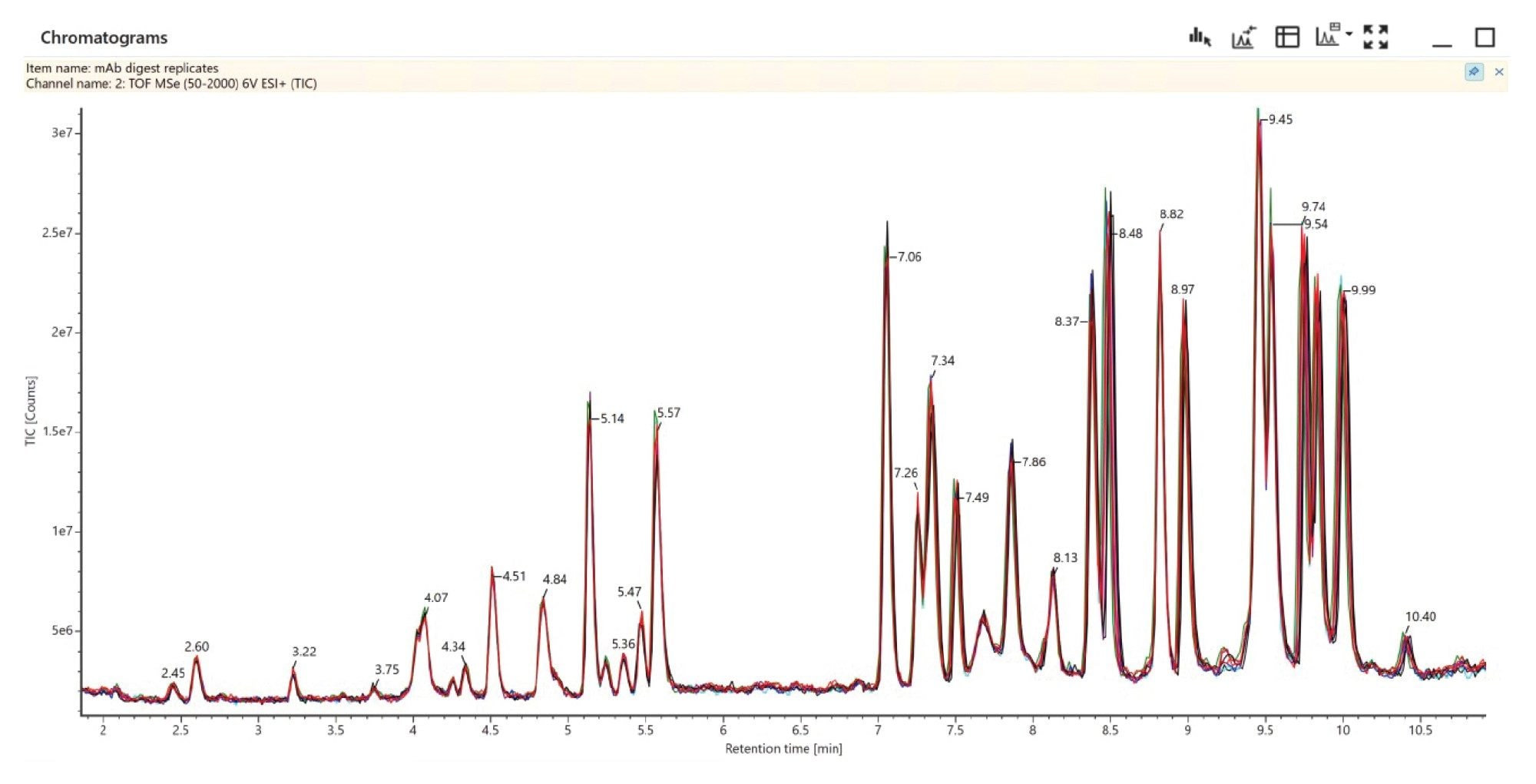
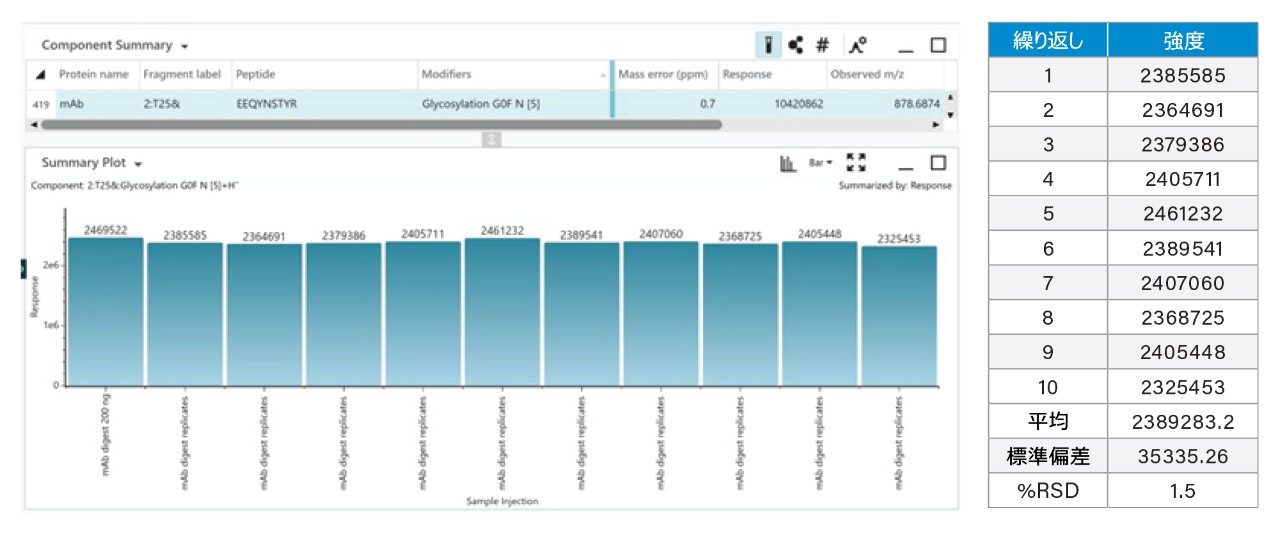
10 回繰り返し注入での T25 糖ペプチド(G0F)のレスポンス(図 6)では、ほぼ完全にオーバーラップした重ね描きクロマトグラムが見られたことから、データ非依存的 LC-MSE ペプチドマッピングアプローチは本質的に再現性が良好であることが実証されました。これらのクロマトグラムでは、10 回の注入にわたって、一貫した UPLC クロマトグラフィーおよび一貫した LC-MS 検出レスポンスが見られます。図 7 では、このことをさらに拡張して、繰り返し注入にわたる HC T25 糖ペプチド G0F の合計 MS1 レスポンスを示しており、強度の RSD が 1.5% であることがわかります。
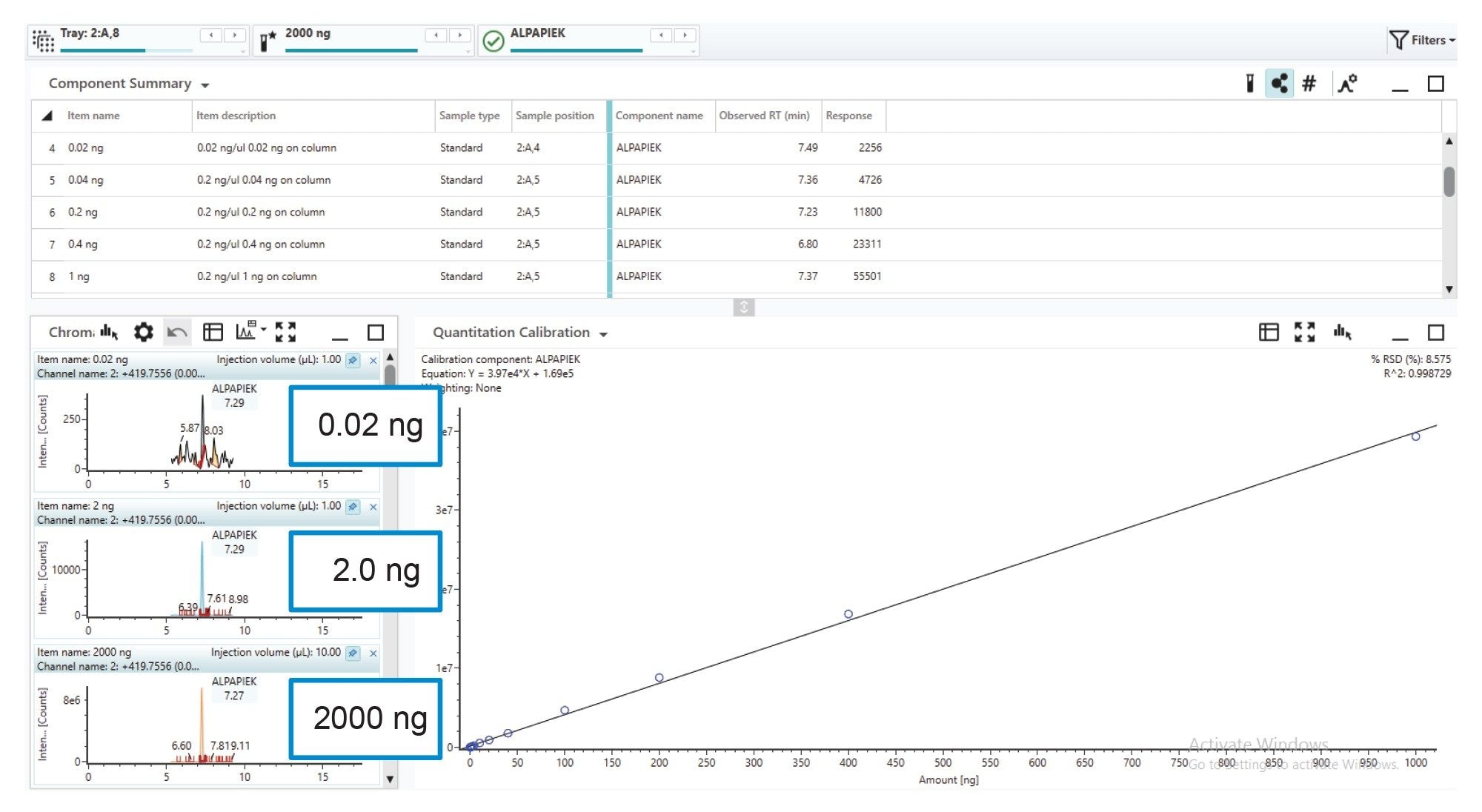
包括的なタンパク質の不純物分析において、トリプシンペプチドのさまざまなイオン化電位が得られ、広い相対濃度にわたって修飾ペプチドが検出および定量できるためには、少なくとも 4 桁のダイナミックレンジが必要です。図 8 の希釈系列では、消化物のカラムロードが 2000 ng、2 ng、0.02 ng(5 桁)の mAb 消化標準試料である特定のペプチドの抽出イオンクロマトグラムを示しており、MS1 レスポンスが 1000 ng ~ 0.02 ng の範囲で直線的であることがわかります。
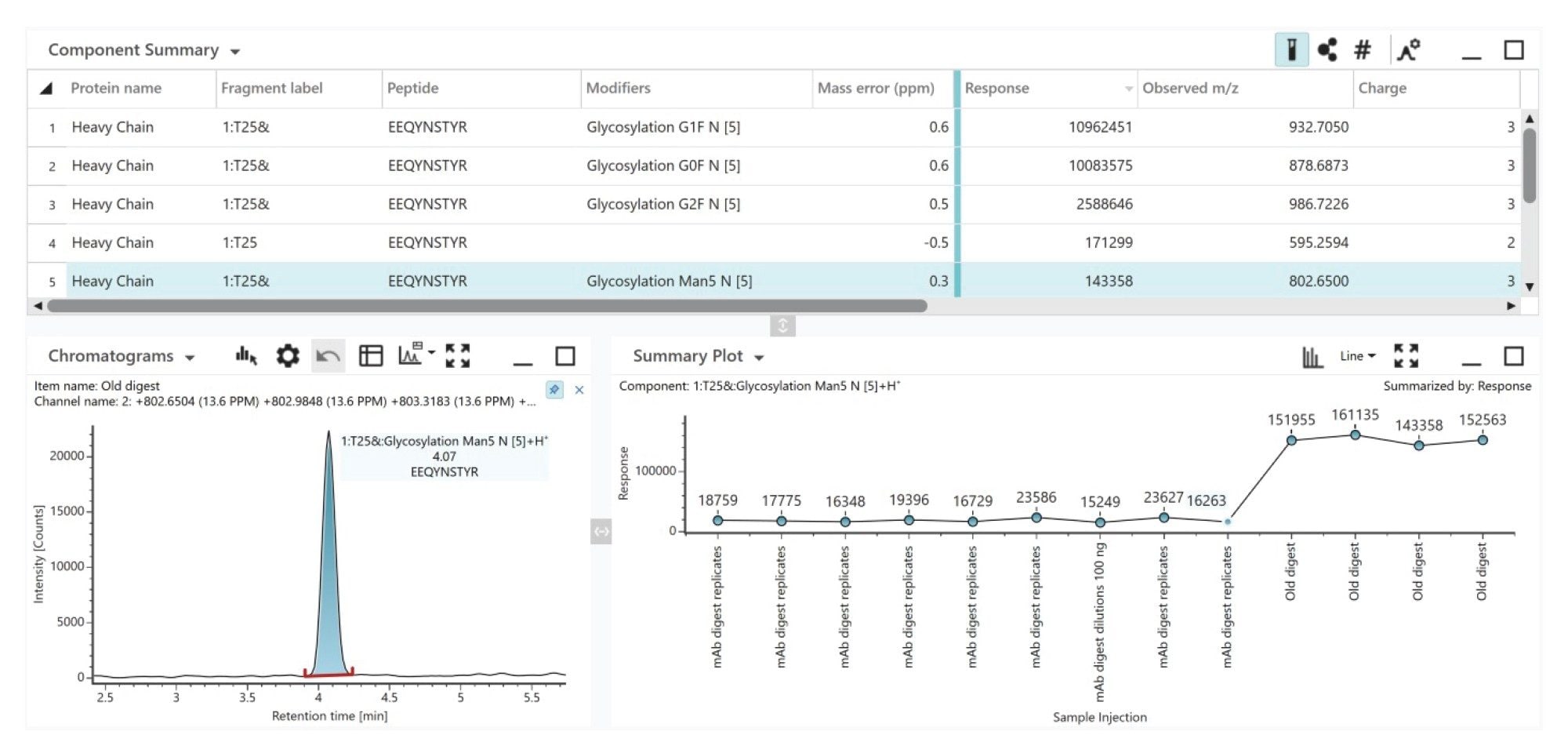
グリコシル化部位の特定とプロファイリングは、モノクローナル抗体(mAb)の生物学的活性、安全性プロファイル、治療における有効性を理解するために不可欠です。本稿では、質量誤差 1 ppm 未満で割り当てられた糖ペプチドについて、図 9 に示すように、Xevo MRT MS システムを使用するペプチドマッピングワークフローにより、NIST mAb 標準試料についていかに一貫した糖ペプチド MS レスポンスが得られるかを説明します。この一貫性により、強調表示した T25 Man5 糖ペプチドについて、2 つの mAb バッチ間での mAb レベルの望ましくない Man5 レベルの傾向の変化も観察できます。
結論
Xevo MRT 質量分析計によってペプチドベースのバイオ医薬品の特性解析に多くのメリットがもたらされ、信頼性の高い配列確認とプロダクトバリアントや不純物の割り当てが行えます。高性能多重反射飛行時間(MRT)テクノロジーにより、ppm 以下の質量精度が実現して、プリカーサーデータとフラグメンテーションデータの両方に基づく確実なペプチド割り当てが可能になり、ペプチドイオンについて、スキャン速度および m/z に依存せずにほぼ 100,000 FWHM の有効質量分解能が得られて、マップ全体にわたって正確な分析種の同定が確保されます。
この卓越した MS 検出性能が、waters_connect インフォマティクスプラットフォーム上の UNIFI アプリ内で、合理化されたコンプライアンス対応の自動ワークフローにより補完され、これらによって個々のサンプル、および分析したサンプルのより大きなデータセットにわたって、ペプチドマッピングデータの取り込み、解析、レビュー、レポート作成が統合されます。
全体として、Xevo MRT 質量分析計は、信頼性の高い実験結果を得るための頑健で効率的なプラットフォームを提供し、これによってバイオ医薬品の分析者が、バイオ医薬品の開発と販売に関して確実な意思決定ができるようになることが実証されました。
詳細については、Xevo MRT 質量分析計をご覧ください。
参考文献
- European Medicines Agency (EMA). (2016). Guideline on development, production, characterisation and specification for monoclonal antibodies and related products. EMA/CHMP/BWP/532517/2008.EMA website.
- Nilini Ranbaduge, Henry Shion, Ying Qing Yu.Routine Peptide Mapping Analysis using the BioAccord System.Waters Application Note 720006466.2019.
- Kellen DeLaney, Samantha Ippoliti, Lisa Reid, Owen Cornwell, Ying Qing Yu, Emma Harry, Mark Towers.Applying Peptide Mapping and Multi-Attribute Method (MAM) Workflow for Biosimilar mAb Drug Products Comparison on the Xevo™ G3 QTof Platform Waters Application Note 720007632.2022.
- Vera B. Ivleva, Ying Qing Yu, Scott J. Berger, Weibin Chen.Generating Automated and Efficient LC-MS Peptide Mapping Results with the Biopharmaceutical Platform Solution with UNIFI Waters Application Note 720004620.2013.
ソリューション提供製品
720008737JA、2025 年 3 月