リバビリン類縁化合物の親水性相互作用液体クロマトグラフィー(HILIC)分析法の最新の HPLC システムへのスケーリングおよび移行
要約
同一のクロマトグラフィー分離および同等の結果を得ることは、分析法を、異なる粒子径のカラムにわたって正常にスケーリングし、LC システム間で移行するために非常に重要です。この研究では、医薬品有効成分(API)であるリバビリンおよび類縁化合物の HILIC 分析法を、1.7 µm(2.1 × 50 mm)のカラムから同等のケミストリーの 2.5 µm(3.0 × 75 mm)および 3.5 µm(4.6 x 100 mm)のカラムにスケーリングしました。次にこの分析法を ACQUITY™ UPLC™ H-Class PLUS システムから ACQUITY Arc™ システム、Arc HPLC システム、Alliance™ iS HPLC System に移行しました。この分析法を用いて異なるシステムで得られたクロマトグラフィー分離、システム適合性、アッセイ結果を評価したところ、性能が等価であることが示されました。
アプリケーションのメリット
- Waters™ の UHPLC とHPLC システムの間で分析法を正常に移行
- Waters カラムカリキュレーターは、同一の分離および性能が得られる動作条件を計算することで、分析法のスケーリングを支援
- Empower の Gradient SmartStart 機能により、システムデュエルボリュームの差が補正され、分析法の移行時におけるグラジエントテーブルの手動での調整が不要
はじめに
分析法の開発は多くの場合、分析法開発プロセスの速度を速め、分析時間を短縮するために、粒子径 2 µm 以下のカラムで行われます。これらの分析法は一般に、最適なクロマトグラフィー分離を得るために、低拡散液体クロマトグラフィー(LC)システムを必要とします。分析法は多くの場合、低拡散システムが備わっていない品質管理(QC)ラボに移管されます。この場合、高拡散 HPLC で使用するように設計されたより大きな粒子に分析法をスケーリングする必要があります1。 分析法を受け取る側のラボは、品質の一貫性および規制遵守を確保するために、同一の分析においては同等の結果が得られることを実証する必要があります2。
異なる LC システム間でのクロマトグラフィー分析法のスケーリングおよび移行は、困難な作業になる場合があります。多くの場合、システムはデュエルボリュームとカラム外容量が異なるため、グラジエントメソッドにおいてクロマトグラフィー分離の低下とピークの歪みを来たし、スケーリング/移行した後のアッセイで一貫性のない結果になることがあります。分析法をスケーリングおよび移行する際は、システム特性の違いを考慮する必要があります3。
この研究では、リバビリンおよび類縁化合物の分析用の HILIC 分析法の最新の HPLC システムへのスケーリングおよび移行について実証します4。 リバビリンは、慢性 C 型肝炎ウイルス(HCV)感染の治療に使用される抗ウイルス薬です5。 この分析法は以前、粒子径 2 µm 以下のカラムで開発されました。この試験では、分析法を粒子径 1.7 µm のカラムから粒子径 2.5 µm および 3.5 µm のカラムにスケーリングしています。次に、分析法を ACQUITY UPLC H-Class PLUS システム(1.7 µm のカラム)から ACQUITY Arc システム(2.5 µm)、Arc HPLC システムおよび Alliance iS HPLC Systems(3.5 µm)に移行しています。クロマトグラフィー分離、システム適合性、アッセイの結果などの性能特性を各システムで検討して、分析法のスケーリングおよび移行が成功したかどうかを評価します。
実験方法
サンプルの説明
標準溶液
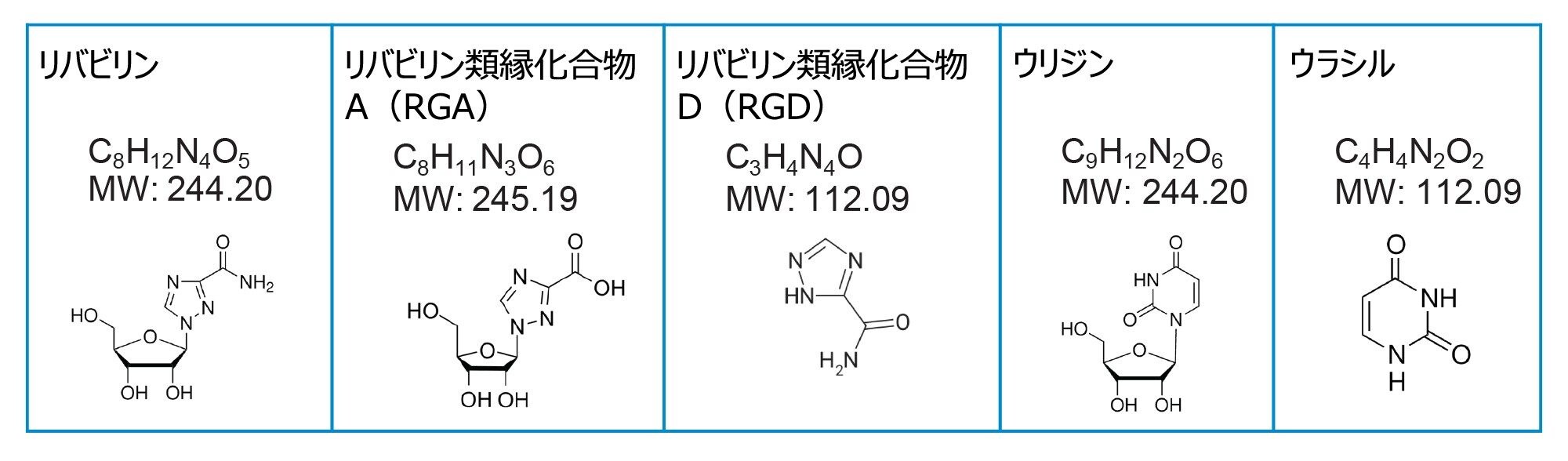
リバビリンおよび類縁化合物の純標準試料(図 1)は Sigma-Aldrich から購入しました。個別のストック溶液は 50:50 アセトニトリル/水中に 1.0 mg/mL になるように調製しました。ストック溶液を 90:10 アセトニトリル/水希釈溶媒で希釈して、リバビリン API が 0.1 mg/mL、類縁化合物が 10 µg/mL の濃度で含まれる混合標準溶液を調製しました。
分析条件
|
移動相 A: |
アセトニトリル |
|
移動相 B: |
水 |
|
移動相 C: |
1% 水酸化アンモニウム含有 100 mM 重炭酸アンモニウム溶液(pH 10) |
|
カラム温度: |
30 ℃ |
|
検出: |
UV @ 220 nm |
|
バイアル: |
LCMS マキシマムリカバリー、容量 2 mL(製品番号:600000670CV) |
|
サンプル温度: |
10 ℃ |
|
洗浄溶媒: |
パージ/サンプル/ニードル:90:10 アセトニトリル/水 シール洗浄:10:90 アセトニトリル/水 |
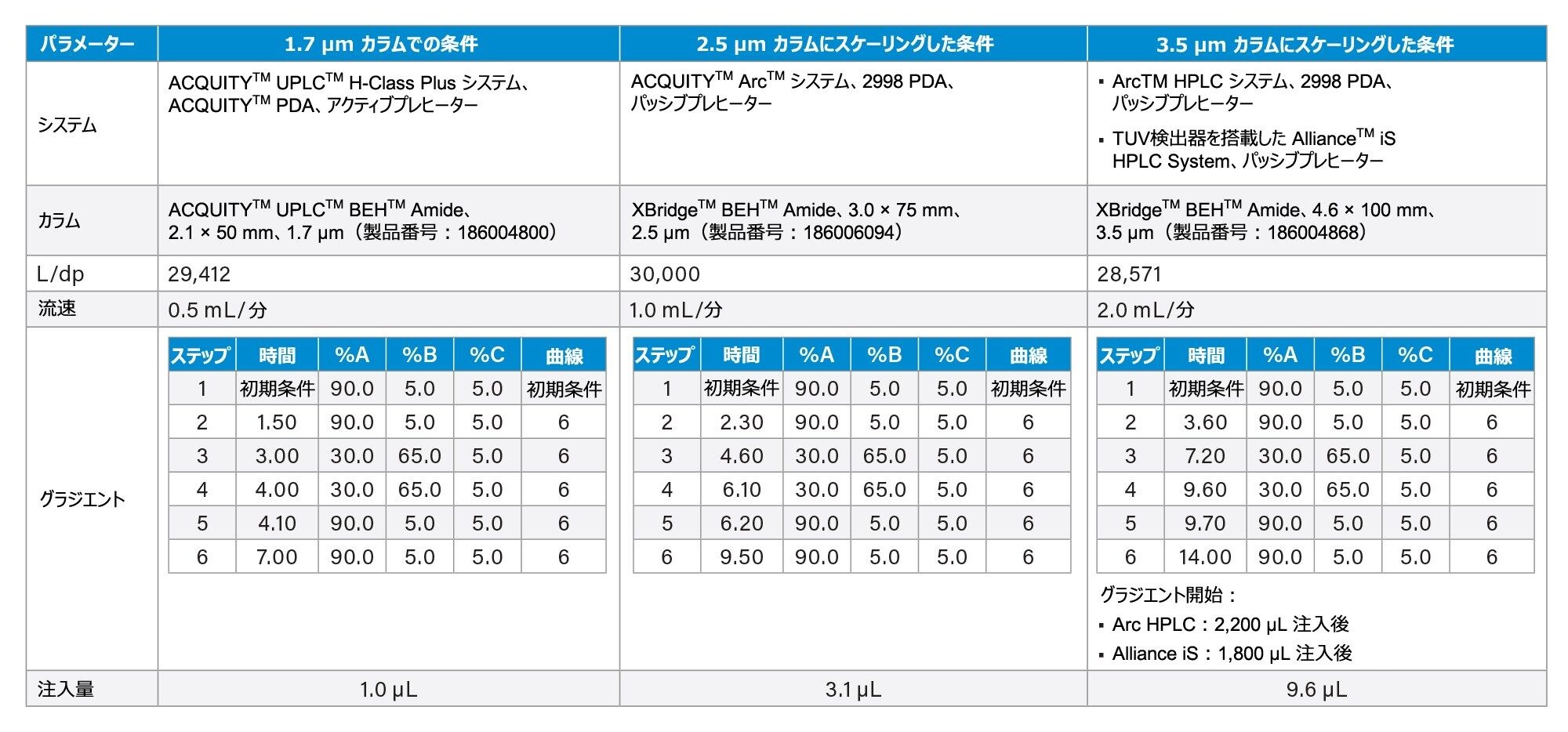
粒子径 1.7 µm、2.5 µm、3.5 µm のカラムに使用した分析法条件を表 1 にまとめます。Waters カラムカリキュレーターを使用して、流速、注入量、グラジエント溶出を幾何学的にスケーリングしました6。
データ管理
|
クロマトグラフィーソフトウェア: |
Empower™ 3 Feature Release 5Service Release 5(FR5 SR5) Empower 3.8.0 および Alliance iS HPLC System |
Empower ソフトウェアを使用してデータ取り込みおよび解析を行いました。Empower プロジェクトに組み込まれているレポートテンプレートを使用して、解析済みデータのサマリーレポートを作成しました。
結果および考察
注意事項:分析法のスケーリングおよび移行
異なる LC プラットフォーム間での分析法のスケーリングおよび移行は、多くの要因の影響を受ける可能性があります。異なる粒子径の間でスケーリングする場合、分析法のクロマトグラフィー分離を維持するために、カラム長(L)と粒子径(dp)の比率を元の分析法と同じにしなければなりません。同等のクロマトグラフィー分離および性能を得るために、流速、注入量、グラジエント時間などのパラメーターを幾何学的にスケーリングします。
デュエルボリュームやカラム外容量などの装置特性がクロマトグラフィー分離の質に影響する可能性があるため、異なるシステム間で分析法を移行させる際は、このことを考慮する必要があります3。粒子径 2 µm 以下のカラムで操作していた分析法は一般に、粒子径 2.5 ~ 5 µm のカラムを使用する分析法と比較して、デュエルボリュームが小さい低拡散のシステムで実行します。デュエルボリュームが大きい高拡散システムで粒子径 2 µm 以下のカラムを使用すると、グラジエントメソッドにおけるクロマトグラフィー分離が不良になり、ピークの歪みが生じることがあります。そのため、同じアッセイでも異なる結果になることがあります。LC システムのデュエルボリュームを測定するための手順が、ホワイトペーパーに記載されています7。
ケーススタディ:リバビリンおよび類縁化合物
この試験では、Waters カラムカリキュレーターを使用して、リバビリンおよび類縁化合物の HILIC 分析法を粒子径 1.7 µm のカラムから粒子径 2.5 µm および 3.5 µm のカラムにスケーリングしました6。 元の分析法では、長さ 50 mm、粒子径 1.7 µm のカラムを使用していたため、L/dp = 29,412 になりました。この分析法を、粒子径 2.5 µm と 3.5 µm、長さ 75 mm と 100 mm のカラムにスケーリングし、L/dp がそれぞれ 30,000 と 28,571 になりました。粒子径 1.7 µm、2.5 µm、3.5 µm のカラムを使用して実行する分析法の操作条件を表 1 に記載しています。
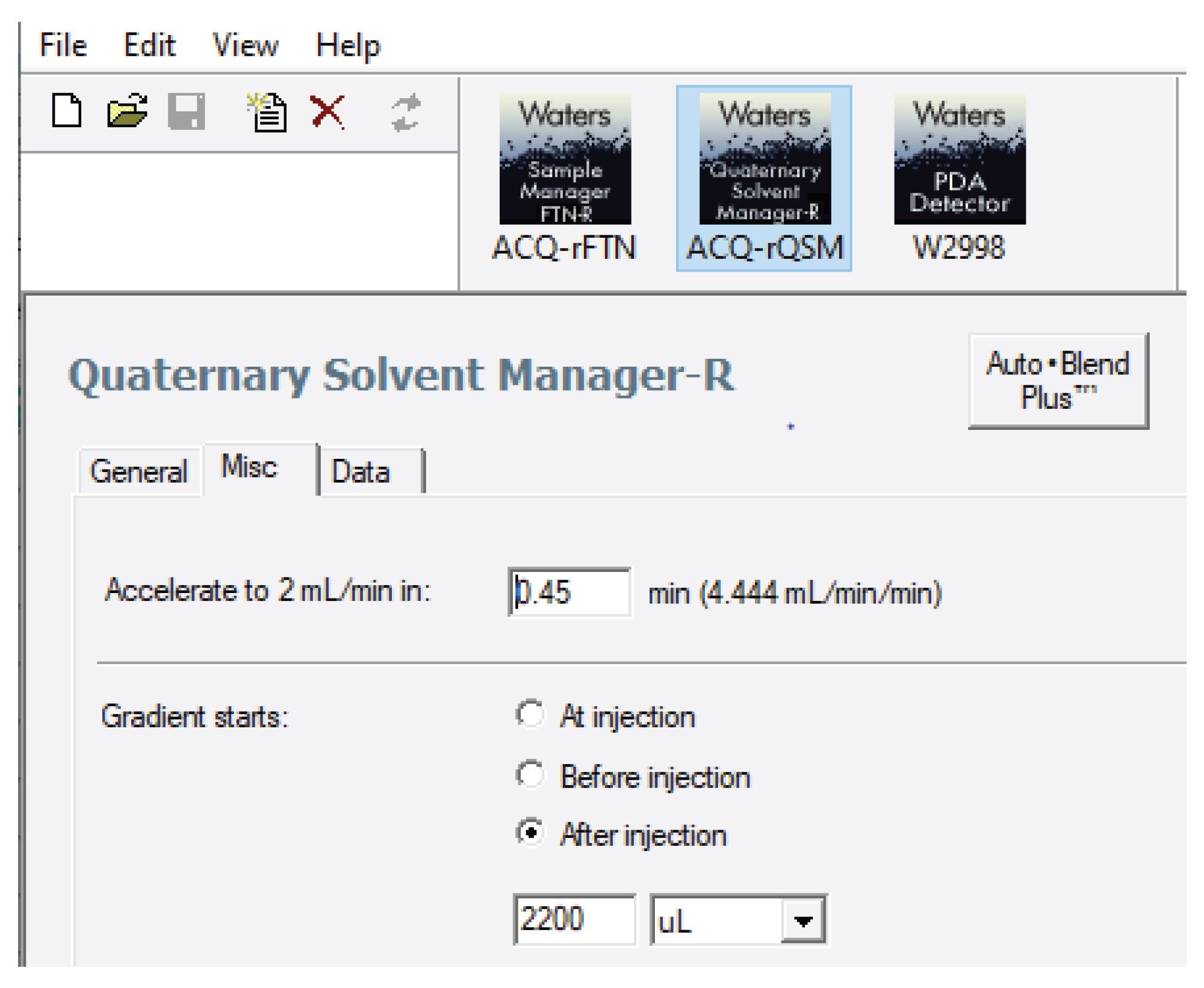
ACQUITY UPLC H-Class PLUS システムは、ACQUITY Arc システム(1.19 mL)、Arc HPLC システム(1.35 mL)、Alliance iS HPLC System(1.5 mL)と比較して、デュエルボリューム(0.375 mL)が小さくなっています。このため、Empower 内の Gradient StartSmart テクノロジーを使用して、ターゲット分析法のグラジエント開始時間を調整しました。Arc HPLC システムのグラジエント開始時間の調整の例を図 2 に示します。注入後 2200 µL で開始するようにグラジエントを調整しました。Gradient SmartStart 機能により、システムのデュエルボリュームの差が補正され、グラジエントテーブルを手動で調整する必要がなくなりました。
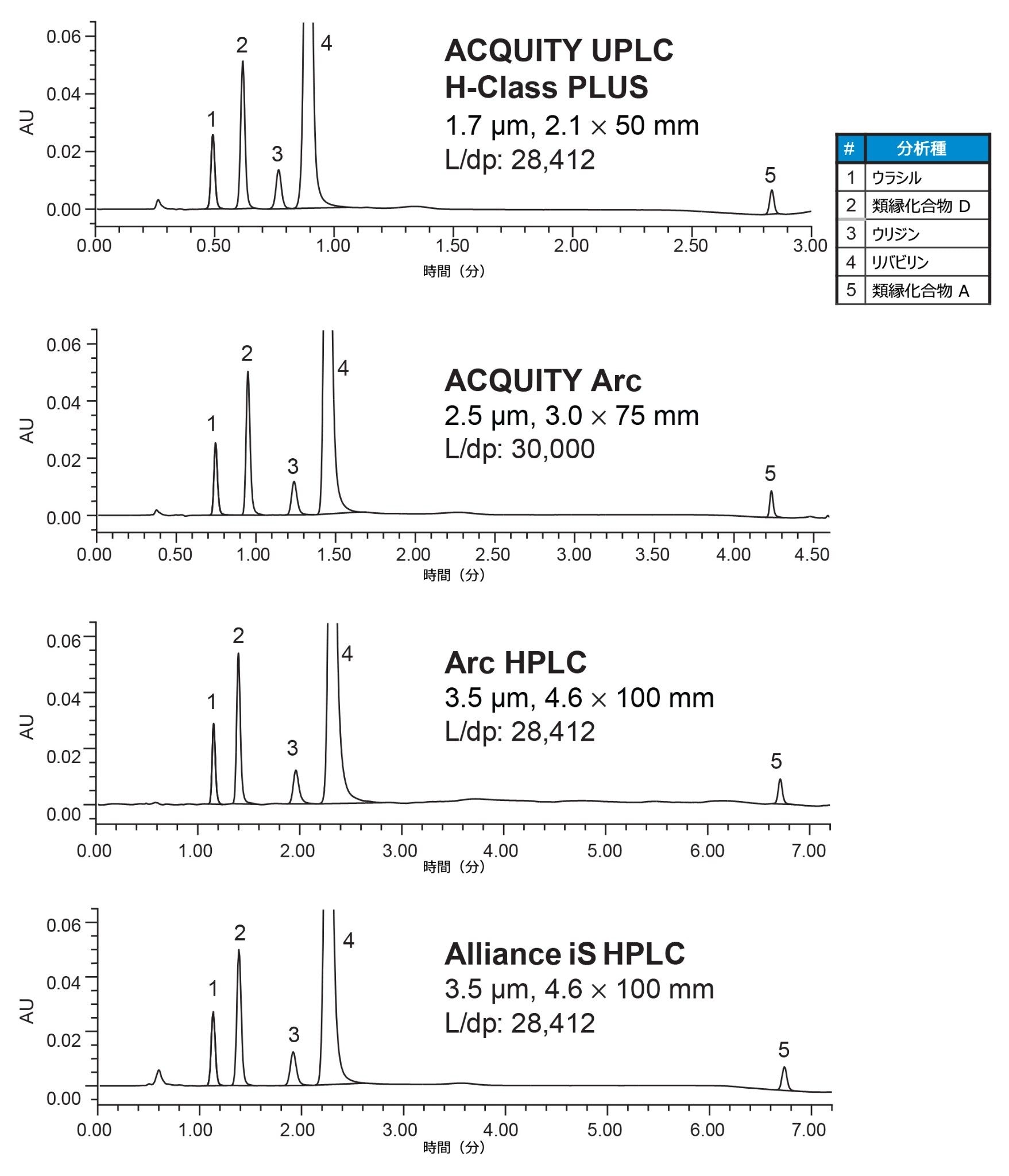
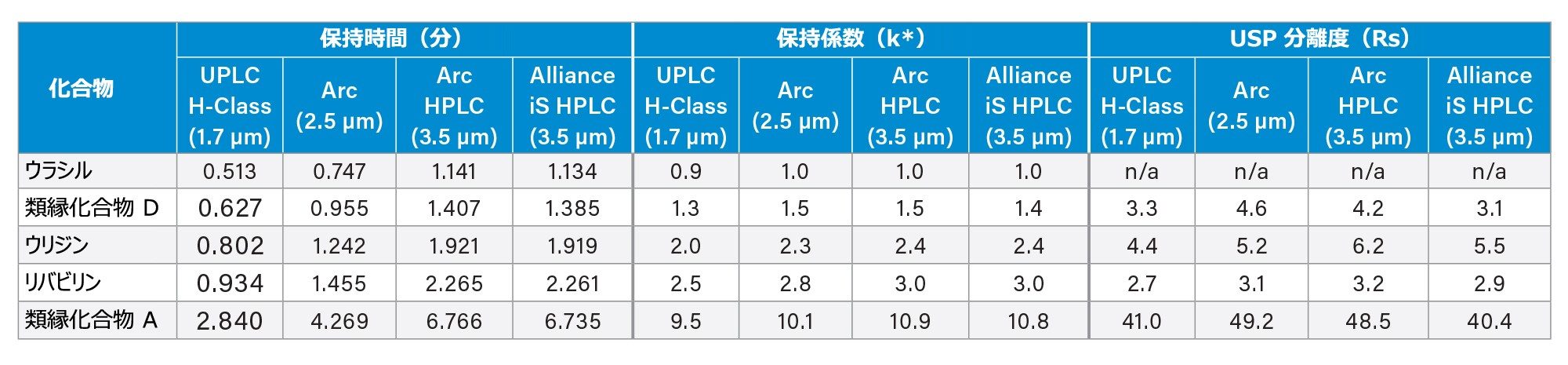
ACQUITY Arc システム、Arc HPLC システム、Alliance iS HPLC Systems でのクロマトグラフィー分離は、ACQUITY UPLC H-Class PLUS システムでのデータと同等でした(図 3)。最初の 4 本のピークはアイソクラティック条件で溶出し、最後のピーク(類縁化合物 A)はグラジエント中に溶出しています。保持時間、保持係数(k*)、ピーク間の USP 分離度(R)などの分離パラメーターは、4 つのシステムすべてで同等でした(表 2)。
システム適合性
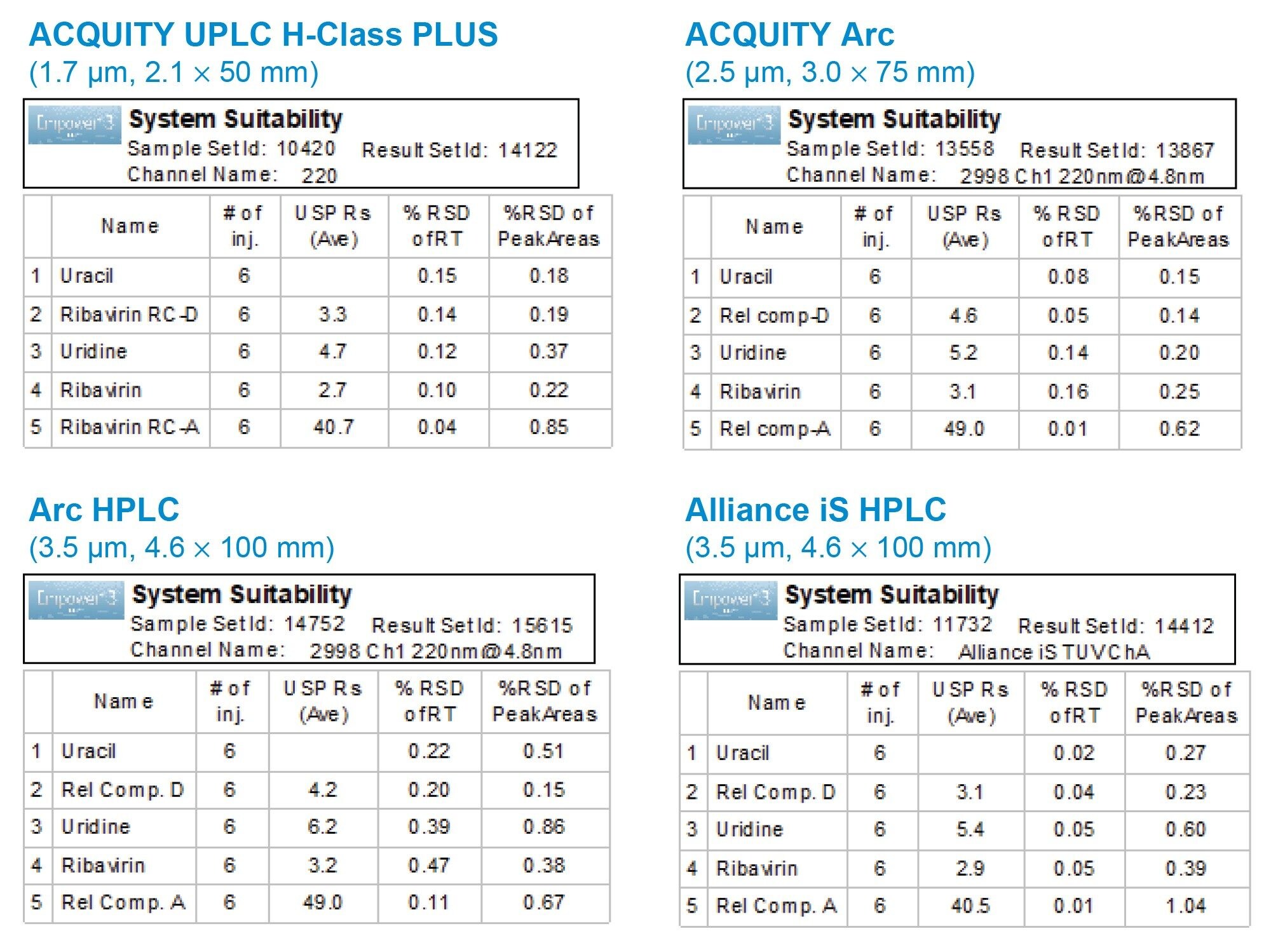
各システムでの分析法の性能を、100 µg/mL のリバビリン API および 10 µg/mL の類縁化合物を含む標準溶液の 6 回繰り返し注入における併行精度を測定することで評価しました。ACQUITY Arc システム、Arc HPLC システム、Alliance iS HPLC Systems で得られたピーク面積と保持時間の併行精度は優れており、ACQUITY UPLC H-Class PLUS システムで得られた結果と一致していました(図 4)。
類縁化合物のアッセイ結果
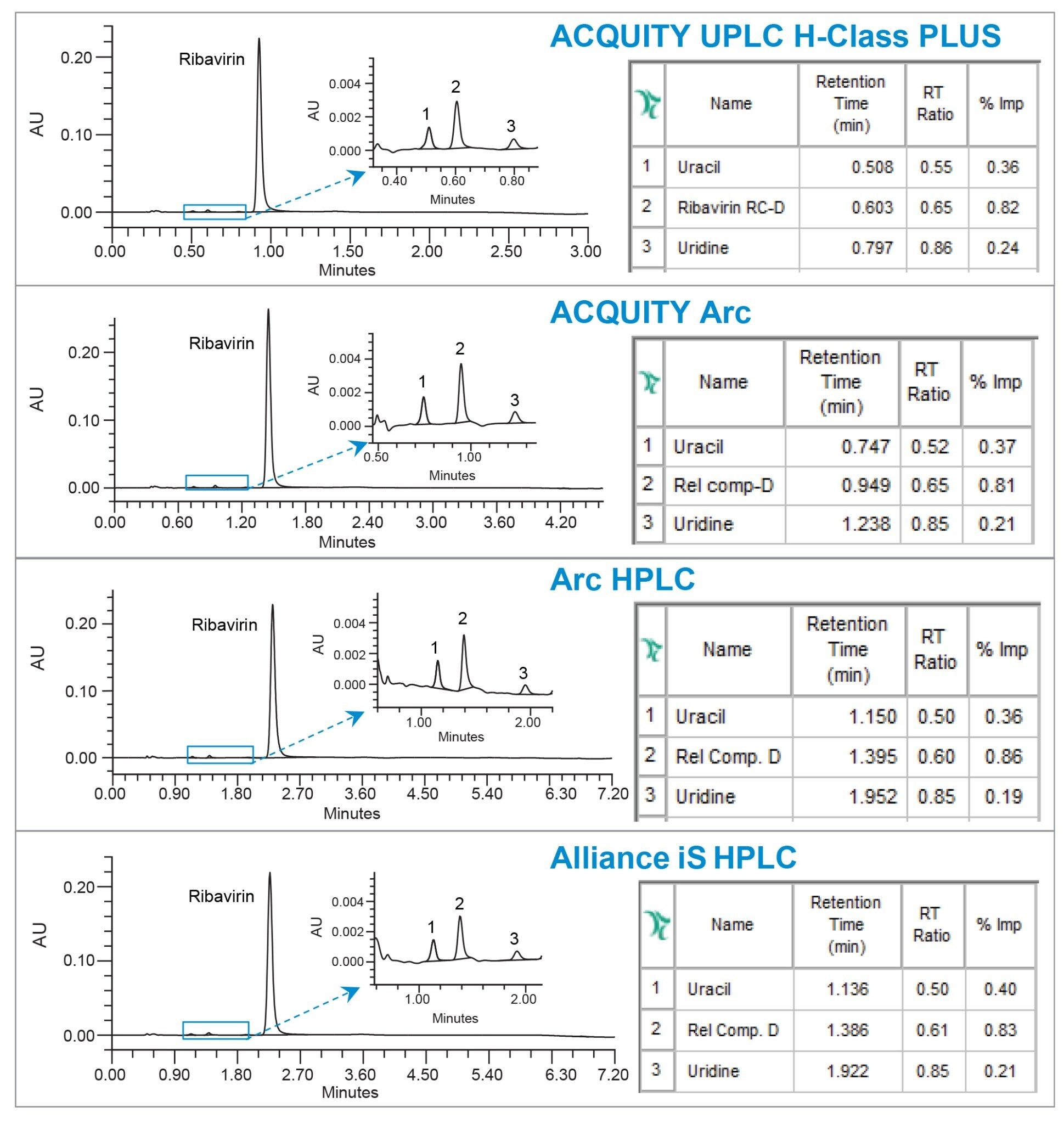
類縁化合物の含量(不純物の割合)のアッセイにおける分析法の性能を実証するために、API サンプル溶液に類縁化合物をスパイクし、適切なカラムサイズのさまざまなシステムで実行しました。アッセイ結果は、Empower ソフトウェアを使用して、得られた各類縁化合物のピーク面積を API のピーク面積と比較することによって計算しました。ACQUITY Arc システム、Arc HPLC システム、Alliance iS HPLC Systems で得られたアッセイ結果は、ACQUITY UPLC H-Class PLUS システムで得られた結果と一致していました(図 5)。Empower ソフトウェアを使用して計算した各類縁化合物の保持時間を、リバビリン API と比較することにより計算した相対保持時間(RRT 値)は、システム間で同等でした。
結論
リバビリンおよび類縁化合物の分析用の HILIC 分析法を、粒子径 1.7 µm のカラムから粒子径 2.5 µm および 3.5 µm のカラムに正常にスケーリングし、ACQUITY UPLC H-Class PLUS システムから ACQUITY Arc、Arc HPLC、Alliance iS HPLC などの高拡散 LC システムに移行しました。ターゲットのシステムにおいて、ACQUITY UPLC H-Class PLUS システムで生成されたデータと同等のクロマトグラフィー分離、システム適合性、アッセイ結果が得られました。
デュエルボリュームやカラム外容量などのシステム特性は、クロマトグラフィー性能の質に影響する可能性があり、異なる LC プラットフォーム間での分析法のスケーリングおよび移行の成功率を高めるには、これらを考慮する必要があります。
参考文献
- Dong MW.Ultrahigh-Pressure Liquid Chromatography, Part III: Potential Issues: This Installment on Ultrahigh-Pressure Liquid Chromatography (UHPLC) Review the Potential Problems That May Be Encountered Using HPLC Systems and Methods, and Proposes Strategies for Their Migration.LC-GC North America, 35–11, 2017.
- USP General Chapter 〈1224〉, Transfer of Analytical Procedures.United States Pharmacopeia USP 43-NF 38, official prior 2013.
- Hong H, McConville PR.Dwell Volume and Extra-Column Volume: What Are They and How Do They Impact Method Transfer?. Waters White Paper, 720005723EN, 2018.
- Berthelette KD, Walter T, Naughton S, Turner JE, Zampa N. Comprehending COVID-19: Fast Analysis of Ribavirin and Related Compounds Using Hydrophilic Interaction Chromatography.Waters Application Note, 720006957, 2020.
- Ribavirin: https://medlineplus.gov/druginfo/meds/a605018.html
- Waters Columns Calculator.https://www.waters.com/waters/support.htm?lid=134891632&type=DWNL
- Waters Corporation, Protocol for Gradient Delay (Dwell Volume) Measurement. Waters Applications Notebook, 720004313EN, p. 67–69, 2013.
720008255JA、2024 年 2 月