HRMS システムで OligoWorks™ SPE マイクロプレートキットを用いた、ラット血漿から抽出した脂質結合アンチセンスオリゴヌクレオチド(ASO)の定量
要約
探索バイオアナリシスラボは、創薬のプロセスで重要な役割を果たします。このようなラボは、各プロジェクトの多数の候補をサポートする任務を担っており、厳しいスケジュールに縛られているため、スクリーニングプロセスを慎重かつ効率的に行って、迅速な意志決定を行えるようにする必要があります。そのため、これらのラボでは、標準化された分析ワークフローを使用して、頑健なサンプル前処理と定量 LC-MS ワークフローを円滑に進めることにより、分析法開発にかかる時間を最小限に抑えています。本研究では、OligoWorks SPE マイクロプレートキットを使用したラット血漿からの脂質結合 ASO の抽出と高い回収率に焦点を当てるとともに、データの質を損なうことなく生産性を最大化する汎用 HRMS データ取り込みメソッドも紹介します。
アプリケーションのメリット
- OligoWorks SPE マイクロプレートキットにより、最小限の分析法開発で、バイオマトリックスから医薬品用オリゴヌクレオチドを抽出および LC-MS 定量するための、界面活性剤を使用しない標準化されたキットベースのソリューションを提供
- Xevo™ G3 QToF HRMS 装置を利用することにより、オリゴヌクレオチド医薬品の高感度で頑健、かつ正確な低レベルでの検出および定量が可能になり、探索ラボや初期開発ラボにおける効率的なスクリーニングが容易に実現
- 探索バイオアナリシスラボ全体にわたって採用および導入できる、簡素化および合理化されたワークフロー
はじめに
オリゴヌクレオチド医薬品(ONT)は、遺伝子の転写および翻訳のレベルで疾患生物学に対処する強力な能力と、ターゲットに対する高い特異性および低毒性から、今日の多くの医薬品開発者が注目している重要な分野です。このクラスの核酸医薬品のパイプラインが継続して拡大するにつれて、開発の各段階を通してその探索と進展をサポートするための、高感度で正確、かつ頑健なバイオアナリシスアッセイのニーズも増大しています。探索バイオアナリシスラボでは、多数の候補をスクリーニングする必要があるため、分析試験のほとんどの側面を合理化して効率を高める努力を払っています。さまざまなオリゴヌクレオチドにわたって機能する標準化されたサンプル前処理アプローチは、この点で極めて有用であり、このようなラボにおける分析法開発にかかる時間とコストを大幅に削減することができます。さらに、高分解能質量分析(HRMS)は多くの場合、ノンターゲットの方法でデータを収集するのに使用され、単一の汎用的な分析法をさまざまな分析種にわたって展開することができます。HRMS システムで得られる情報が豊富なデータのもう 1 つの重要な利点は、後の段階で再調査が可能なことです。これによって、分析種の ADME プロファイルの理解が深まり、対象代謝物のスクリーニングが可能になるため、薬物候補の開発を加速することができます。
この論文では、OligoWorks SPE マイクロプレートキット(OligoWorks キット)を使用してラット血漿から脂質結合アンチセンスオリゴヌクレオチド(ASO)を抽出し、続いて LC-HRMS システムで定量を行う分析ワークフローについて説明します。OligoWorks キットは、バイオマトリックスから多様な一連のオリゴヌクレオチド医薬品を、高い回収率と少ないマトリックス効果で抽出できる、シンプルで幅広く適用可能なサンプル前処理ソリューションです。サンプルを抽出した後、Xevo G3 四重極飛行時間型(QToF)HRMS 装置と組み合わせた ACQUITY™ H-Class UPLC™ で、高感度で頑健、かつ効率的な定量分析を容易に行える汎用的なデータ取り込みメソッドを用いて LC-MS 分析を実施しました。これにより、医薬品用オリゴヌクレオチドの分析を行う探索バイオアナリシスラボの生産性を向上できる標準化された分析ワークフローを実証しました。
実験方法
LC-MS クロマトグラフィー分離および実験条件
液体クロマトグラフィー
|
LC システム: |
FTN を搭載した ACQUITY UPLC H-Class PLUS システム |
|
カラム: |
ACQUITY Premier Oligonucleotide C18 カラム、130 Å、1.7 μm、2.1 × 50 mm |
|
カラム温度(℃): |
55 ℃ |
|
サンプル温度(℃): |
10 ℃ |
|
移動相 A: |
1% HFIP(ヘキサフルオロ-2-プロパノール)、0.1% DIPEA(N,N-ジイソプロピルエチルアミン)含有水溶液 |
|
移動相 B: |
0.75% HFIP(ヘキサフルオロ-2-プロパノール)、0.0375% DIPEA(N,N-ジイソプロピルエチルアミン)含有 65% アセトニトリル:35% 水 |
|
パージ溶媒: |
25:25:25:25 メタノール:アセトニトリル:イソプロパノール:水 |
|
注入量(µL): |
10 µL |
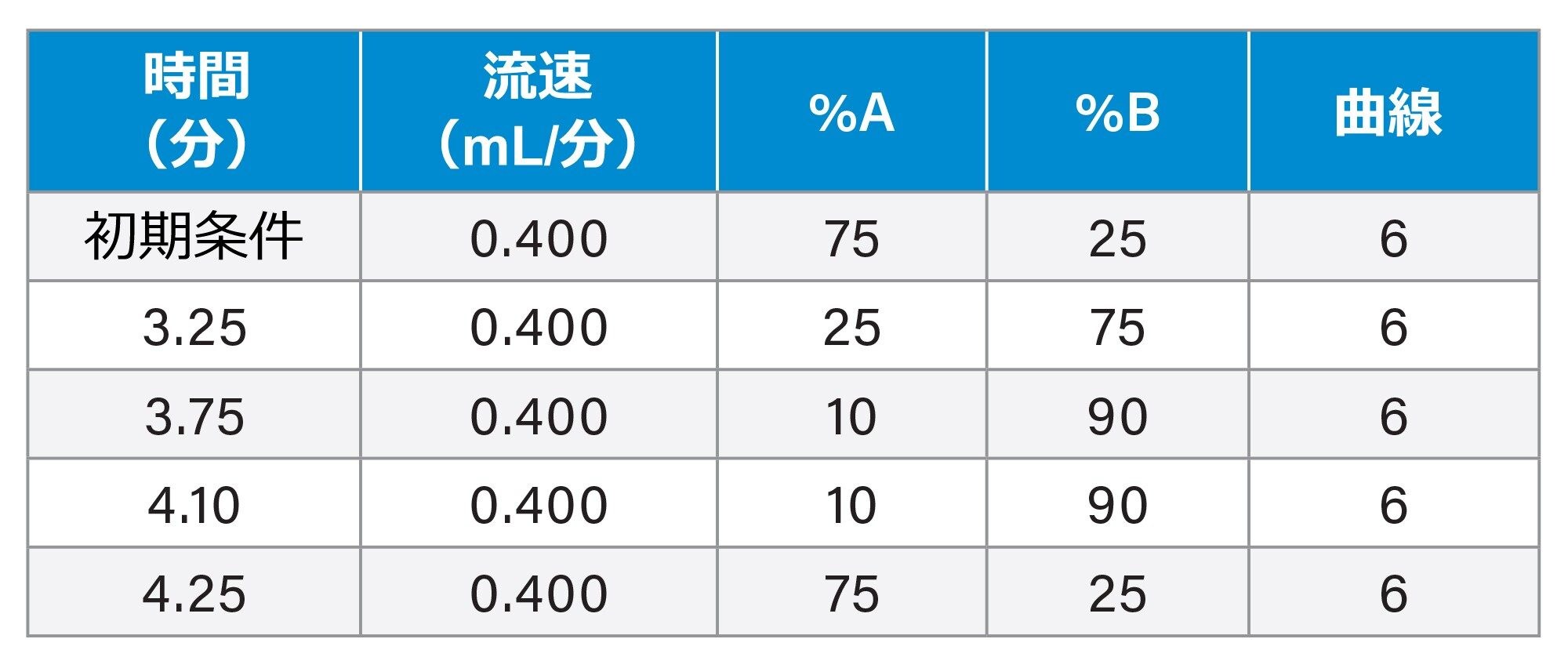
LC グラジエントテーブル
MS システム条件
|
MS システム: |
Xevo G3 QToF |
|
イオン化モード: |
ESI- |
|
取り込みモード: |
MS フルスキャン |
|
キャピラリー電圧(kV): |
2 |
|
脱溶媒温度(℃): |
600 |
|
脱溶媒ガス流量(L/時間): |
1000 |
|
コーンガス流量(L/時間): |
150 |
|
コリジョンガス流量(L/時間): |
0.2 |
|
ネブライザー(bar): |
7 |
データ管理
|
装置コントロールソフトウェア: |
waters_connect™ |
|
定量ソフトウェア: |
UNIFI™ |
ケミカル、試薬、材料、溶媒
脂質結合 ASO LC-MS の標準試料(モノアイソトピックニュートラル質量 6046.08484 Da)は、Waters™ Corporation(米国、マサチューセッツ州ミルフォード)から入手しました(製品番号:186010747)。内部標準(IS)は、BioSearch Tech(デンマーク、リストルプ)によって合成された、対象分析種と数ベースペア異なるカスタム合成脂質結合オリゴヌクレオチド(モノアイソトピックニュートラル質量 5716.9361 Da)を用いました。
MS グレードのアセトン、メタノール、水、アセトニトリル、イソプロパノール、ヘキサフルオロ-2-プロパノール(HFIP)、N,N-ジイソプロピルエチルアミン(DIPEA)、酢酸アンモニウムは Sigma Aldrich(米国、ミズーリ州セントルイス)から購入しました。K2 EDTA ラット血漿は BioIVT(米国、ニューヨーク州ウェストベリー)から入手しました。DNase/RNase フリー蒸留水は、ThermoFisher Scientific から購入し(製品番号: 10977015)、オリゴヌクレオチド標準試料の調製および SPE サンプル溶出液の希釈に使用しました。OligoWorks キット(製品番号:186010614)はウォーターズコーポレーション(米国、マサチューセッツ州ミルフォード)から入手しました。
OligoWorks SPE 洗浄試薬の調製
OligoWorks SPE 洗浄溶媒 1:50 mM 酢酸アンモニウムバッファー(pH 5.5)は、3.84 g の酢酸アンモニウムを秤量し、容量を 1 リットルにして、pH を 5.5 に調整することにより調製しました。
OligoWorks SPE 洗浄溶媒 2:2 種類の洗浄溶媒を、洗浄溶媒 2 の候補として評価しました。
- 10% メタノール/90% 水溶液は、100 mL のメタノールを 900 mL の水に加えて調製しました。
- 30パーセント メタノール/70パーセント 水溶液は、300 mL のメタノールを 700 mL の水に加えて調製しました。
ストック溶液、検量線、QC サンプル前処理
脂質結合 ASO および IS を、50 µL の 20% アセトン:80% DNA/RNAse フリー水に再溶解し、それぞれのストック濃度を 100 nmol/mL にしました。脂質結合 ASO をラット血漿にスパイクして、検量線(1~1,000 pmol/mL)および QC ポイント(LQC-5 pmol/mL、MQC-50 pmol/mL および HQC-750 pmol/ mL)を作成しました。IS はさらに 20% アセトン溶液で 100 倍希釈して、濃度 1 nmol/mL にしました。次に、この IS ストックを、最終濃度 50 pmol/mL になるように検量線および QC ポイントにスパイクしました。
Oligoworks SPE マイクロプレートキットを使用したサンプル前処理および抽出
調整した検量線および QC サンプルを、OligoWorks SPE キットおよびコンポーネントの取扱説明書(720008066EN)に記載されているプロトコルに従って、ラット血漿から 3 回繰り返し抽出しました。簡単に説明すると、100 µL の検量線サンプルおよび QC サンプルを Eppendorf 1 mL ディープウェルプレートに添加し、RapiZyme Proteinase K 消化モジュールに付属の試薬とプロトコルを使用して消化してから、OligoWorks SPE マイクロプレートおよび溶離液を使用して抽出しました。
結果および考察
脂質結合 ASO LC-MS 標準試料(製品番号:186010747)は、完全にホスホチオエート化した骨格、5' パルミチン酸修飾、メトキシエチル修飾末端を含む 16 残基のギャップマーアンチセンスオリゴヌクレオチド(ASO)です。以下がその配列です。哺乳類の遺伝子とまったくホモロジーがないネガティブコントロール配列も含まれています。5' 修飾は、5'-パルミチン酸-C6 CE ホスホロアミダイトを使用して導入されています。この修飾の化学構造を以下に示します。アスタリスク(*)は PS 結合、MOE はメトキシエチル 2' 修飾、MeC は 5 メチルシチジン残基をそれぞれ表します。
5’ d 5-Pal-*-MOE-MeC-*-MOE-G-*-MOE-MeC-*C*G*A*T*A*A*G*G*T*A*- MOE-MeC-*-MOE-A-*-MOE-MeC 3’
内部標準も、分析種と同様の修飾を含む脂質修飾アンチセンスオリゴヌクレオチドで、以下に示すように、対象分析種と数残基異なるだけです。
5' d 5-Pal-MOE-MeC-*-MOE-G-*-MOE-MeC-*C*G*A*T*A*A*G*G*T*-MOE-A-*-MOE-MeC-*-MOE-A 3'
OligoWorks SPE プロトコルの最適化
脂質結合 ASO の最初の血漿からの回収およびマトリックス効果の実験は、OligoWorks SPE Care and Use Manual(『OligoWorks SPE 取扱説明書』)に記載されている、出発点としてのサンプル前処理および抽出プロトコルを使用して行いました。これらの実験の LC-MS 分析は ACQUITY PREMIER LC システムと Xevo TQ-Absolute タンデム四重極(TQ)装置を使用して行い、MRM 分析は [M-9H+]- のプリカーサーイオン m/z 671.1 と m/z 95.1 のフラグメントイオン、および分析法セクションに記載されているものと同じクロマトグラフィー条件およびカラムを使用して行いました。出発プロトコルを使用した場合、得られた脂質結合 ASO および IS の回収率はそれぞれ約 80% および 60% でした。 マトリックス効果は 15% 未満でした(データは示していません)。これらの回収率は許容範囲内に収まっていますが、回収率を高め、感度を最大化するために、SPE プロトコルをさらに最適化することを試みました。
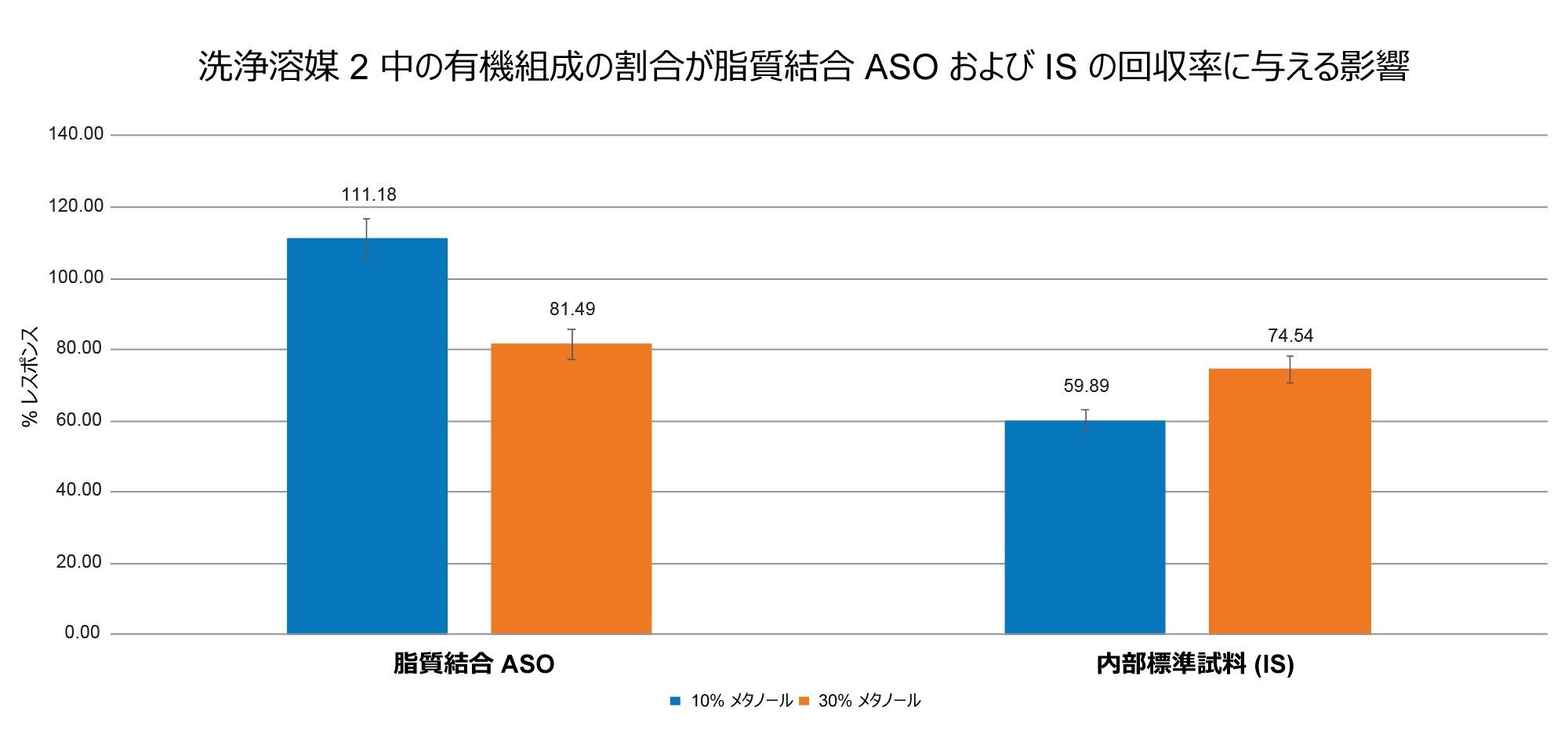
OligoWorks SPE WAX 吸着剤は、ポリマー性の逆相弱陰イオン交換ミックスモード吸着剤です。このバイモーダル機能は、ロード、洗浄、溶出の各ステップにおけるプロトコルの最適化に活用することができます。まず、洗浄 2 のステップの最適化から始めました。これは、このステップが、対象分析種の保持に影響する可能性があるとともに、望ましくないマトリックス成分の除去にも影響するためです。洗浄溶媒 2 の有機組成を 30% メタノール(取扱説明書で推奨されている洗浄溶媒 2 組成)から 10% メタノールに下げると、ターゲット脂質結合 ASO の回収率が大幅に向上しましたが、IS の回収率は低下しました。 この特定の例では、メタノール組成が大きいために、ターゲット脂質結合 ASO が洗浄 2 ステップで部分的に溶出していました。 一方、洗浄 2 のメタノール組成を下げると、IS の回収率低下が見られました。この性能を図 1 に示しています。このデータから明らかなように、配列において密接に関連する分析種について、SPE の洗浄 2 のステップの有機溶媒の割合によって異なる回収率になることがあります。
LC-MS 分析法開発
LC グラジエントの最適化
OligoWorks SPE の取扱説明書に記載されている LC グラジエントを、脂質結合 ASO および IS の分析の出発点として使用しました。このグラジエントを使用すると、分析種と IS はクロマトグラフィーの最後の方に溶出しました(データは示していません)。これは、複合脂質によって分析種に加わった疎水性が原因である可能性があります。そのため、LC グラジエントを最適化して、開始条件の有機溶媒の割合を大きくし、グラジエントがより急勾配(3.25 分で 25% から 75% B まで)になるようにしました。この LC 条件を使用することで、分析種および IS のピークがグラジエントの中央で溶出しました(データは示していません)。さらに、最適な性能が保証されるようにオリゴヌクレオチドで QC テスト済みの ACQUITY™ Premier Oligonucleotide BEH™ C18 カラムを使用することにより、オリゴヌクレオチドとカラムハードウェア間の非特異的陰イオン性相互作用(ベースでのピーク幅約 5 秒)が最小限に抑えられ、感度と再現性の向上に役立ちました。
HRMS データ取り込みおよび解析
Xevo G3 QToF MS により、詳細な特性解析から正確な定量まで、対象分析種のサンプル情報が最大化します。waters_connect 内の UNIFI アプリケーションを使用して、ノンターゲットでデータを収集するために、フル MS スキャン実験(m/z 50 ~ 2000、スキャン時間 0.2秒)をセットアップしました。このアプローチにより、追加の分析法開発の必要なく、多様なセットの分析種に使用できる単一の取り込みメソッドが可能になります。図 2 に、ラット血漿から抽出した脂質結合 ASO 標準試料(100 pmol/mL)の、m/z 671.2297 のプリカーサー [M-9H+]-(図 2A)および m/z 863.2976 のプリカーサー [M-7H+](図 2B)の MS スペクトルを示します。
![脂質結合 ASO LC-MS 標準試料のプリカーサー(A)[M-9H+]-(m/z 671.2297)および(B)[M-7H+]- (m/z 863.2976)の代表的な質量スペクトル](/content/dam/waters/ja/app-notes/2024/720008256/720008256en-f2.jpg.82.resize/img.jpg)
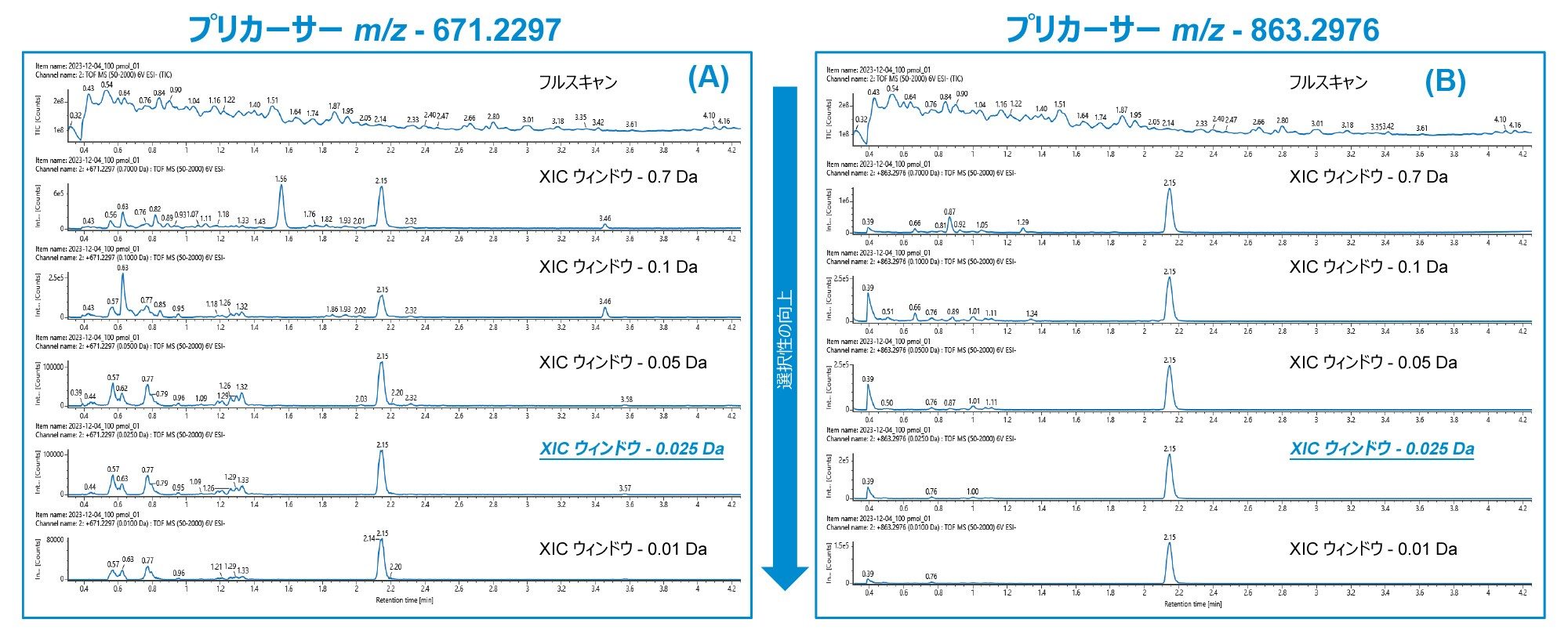
データ取り込みの容易さに加えて、Xevo G3 QToF の高い分解能により、データをより深く調べることができ、狭い質量抽出(XIC)ウィンドウを使用してシグナル対ノイズ比(S/N)を最大化することができます。TQ 装置は、ルーチンに単位分解能 +/- 0.7 Da で動作します。HRMS システムの高い分解能により、m/z 0.001 Da の差で分離した質量を一貫して区別することができます。HRMS データの解析においては、さまざまな XIC ウィンドウを評価して望ましくないマトリックス成分由来の MS シグナルを除去できると同時に、対象分析種の m/z に注目して、十分なシグナルを得ることができます。これにより、分析種のシグナルを維持しつつ、バックグラウンドノイズを最小限に抑え、S/N 比を向上させることができます。ただし、ある点を超えて XIC ウィンドウを狭くし過ぎると、分析種のピーク面積のカウントに悪影響が出始める上に、クロマトグラム中のバックグラウンドピークに大きな影響を与えることがなくなります。したがって、分析種のピーク面積のカウントを損なうことなく、望ましくないバックグラウンド成分由来のシグナルを最小化することの間のバランスを取れるよう、理想的な XIC ウィンドウを見つける必要があります。
脂質結合 ASO について、XIC ウィンドウ 0.7 ~ 0.01 Da を評価しました。図 3 から明らかなように、XIC ウィンドウが狭くなるにつれて、マトリックス成分由来の非特異的なバックグラウンドピークが小さくなり続けて、よりきれいなクロマトグラフィーバックグラウンドが得られ、アッセイの選択性が向上します。最終的な定量では、きれいなバックグラウンドと十分な分析種のピーク面積カウントの間の最適なバランスが得られる XIC ウィンドウ 0.025 Da を選択しました。
感度、正確性、精度
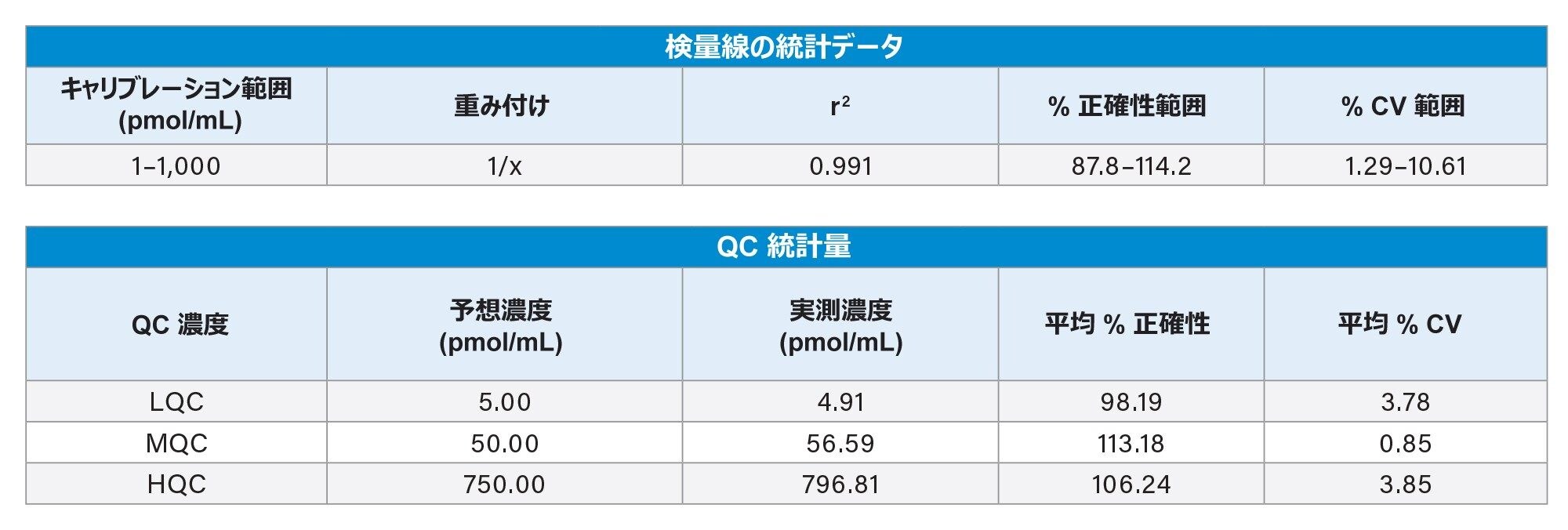
ラット血漿にスパイクし、OligoWorks キットを使用して抽出し、Xevo G3 QToF MS システムで分析した脂質結合 ASO は、1 ~ 1,000 pmol/mL の範囲で直線性を示し、1/x 重み付けを使用すると線形回帰(r2)0.991 が得られました。検量線のすべてのポイントにおける %正確性の範囲は 87.8 ~ 114.2 であり、曲線上のすべてのポイントにおける %CV の範囲は 1.29 ~ 10.61 でした(表 1)。
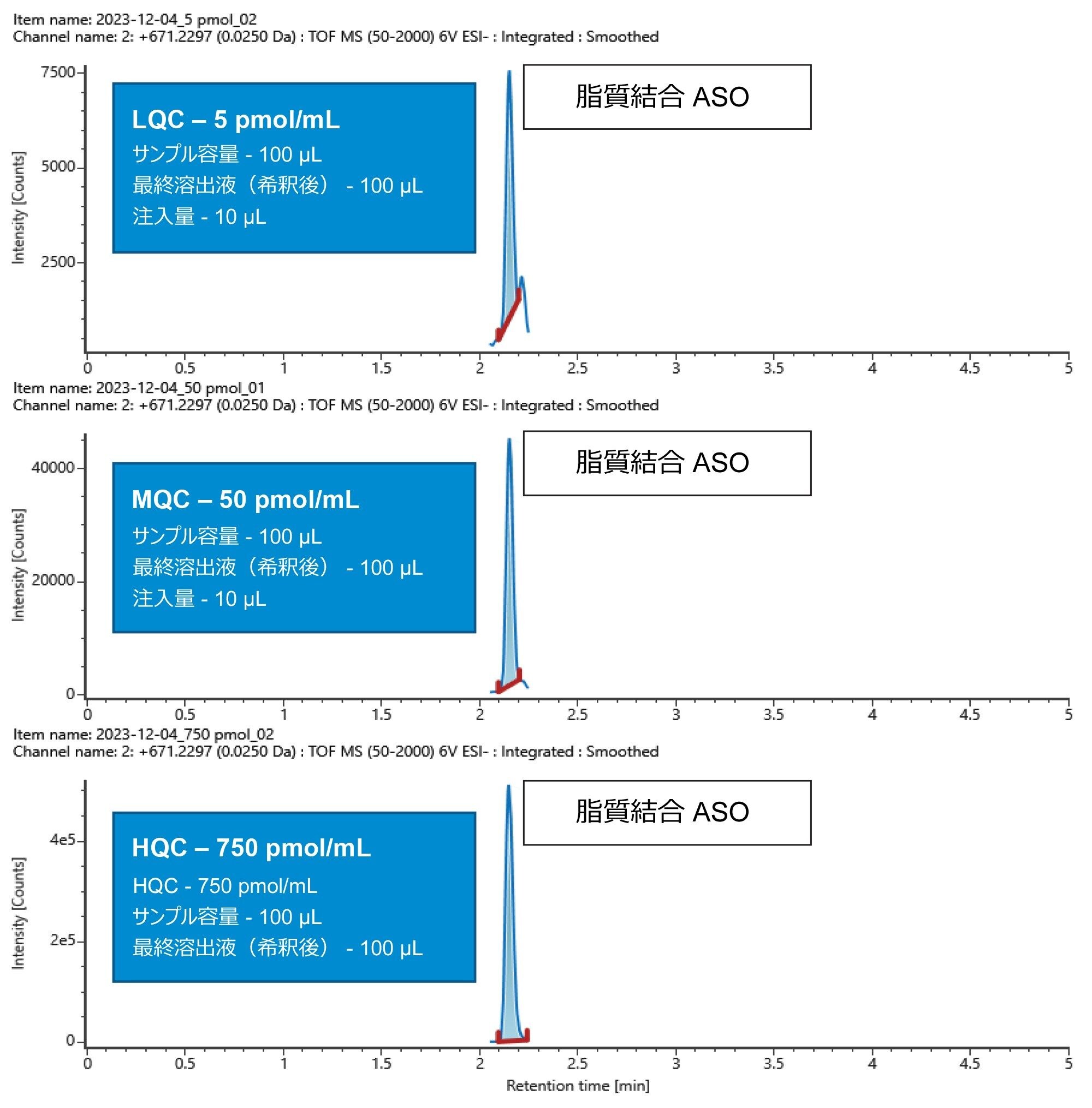
LQC(5 pmol/mL)、MQC(50 pmol/mL)、HQC(750 pmol/mL)の平均 %正確性および平均 %CV はそれぞれ 98.19% と 3.78%、113.18% と 0.85%、106.24% と 3.85% でした(表 1)。図 4 の代表的な QC クロマトグラムからわかるように、検量線と QC ポイントの面積カウントは、濃度の増加とともに直線的に増加しました。
結論
探索バイオアナリシスラボは多くの場合、サポートする必要がある多数のプロジェクトと分析種に対応するために、標準化および合理化されたワークフローを求めています。この点に関する効率と生産性を向上させるため、OligoWorks SPE マイクロプレートキットを使用して対象分析種を生体マトリックスから抽出し、続いて Xevo G3 QToF HRMS 装置でノンターゲット定量を行うシンプルで導入しやすいワークフローを実証しました。
脂質結合 ASO LC-MS 標準試料について、1 ~ 1000 pmol/mL の範囲で直線性の検量線が得られ、すべての検量線と QC ポイントが FDA のバイオアナリシス分析法バリデーションガイドラインに適合していました。
参考文献
720008256JA、2024 年 2 月