QC 環境でのバイオ医薬品の分析用の最新の HPLC としての Alliance™ iS Bio HPLC システムの導入
要約
MaxPeak™ High Performance Surfaces(HPS)テクノロジーを採用した Alliance iS Bio HPLC システムは、バイオ医薬品の製造環境における表面と分析種の相互作用を低減するように設計されたバイオイナートな LC システムです。最新の HPLC 装置である Alliance iS Bio HPLC システムは、ウォーターズの革新的な MaxPeak HPS テクノロジー、直感的なタッチスクリーン操作、エラーを最小限に抑える自動分析前チェック、Intelligent Method Translator App(iMTA)などの機能を搭載して設計されています。これらの機能を合わせることにより、製造環境で用いられる分析法を最新化し、リソースを節約し、バイオ医薬品のスループットを高めることができます。この試験では、バイオ医薬品のルーチン QC テスト環境で Alliance iS Bio HPLC システムを評価します。オリゴヌクレオチドをテストケースとして選択した理由は、新規の治療法としての重要性が高いことに加えて、分析種と表面の相互作用の影響を受けやすいことから、Alliance iS Bio HPLC システムに採用されている MaxPeak HPS テクノロジーのメリットを享受できると考えられたためです。この試験では、オリゴヌクレオチドの分離において、古いシステムと比較して、ピーク高さが最大 30%、ピーク面積が最大 15% 増加していました。さらに、最新のカラムケミストリーにスケーリングした場合、分析時間、溶媒、サンプル消費量が最大 1/3 に低減しました。これらの結果は、Alliance iS Bio HPLC システムがバイオ医薬品の分析およびルーチン検査のための次世代の HPLC プラットフォームとして、QC 環境に最適であることを実証しています。
アプリケーションのメリット
- Alliance iS Bio HPLC システムは、QC 環境で一貫した性能を発揮します。
- MaxPeak High Performance Surfaces により、金属に吸着しやすい分析種の回収率が高まります。
- Intelligent Method Translator App により、分析法移管におけるエラーが低減し、時間を節約できます。
- Alliance iS Bio HPLC システムにより、スケーリングしたメソッドにおける運用コストと廃液を削減できます。
はじめに
バイオ医薬品は、過去 10 年にわたり、ガンや稀少疾患の治療薬として用途が着実に増加してきました。それらの成功の一因として、疾患に合わせて調整できると同時に有害な副作用を最小限に抑えられることから、特異性と安全性において従来の治療法より優れていることが挙げられます。オリゴヌクレオチドベースの治療法は、筋ジストロフィーや脊髄性筋萎縮症などの疾患の治療におけるバイオ医薬品の最新の進歩の 1 つであり、さらに最近では新型コロナウイルス感染症(COVID-19)の蔓延をコントロールするためのワクチンとして使用されています1。 この種の細胞・遺伝子治療は、核酸の相互作用に基づいており、この相互作用は、ヌクレオシド塩基の結合によって細胞中の特異的発現を誘発するように設計された配列を形成することによって生じます。合成手順は十分に理解され、制御されていますが、合成プロセス中に生じる不純物をモニターして管理することが重要です。
医薬品の安全性を保証するため、製造環境の支援ラボでは、リリースの前に、医薬品に関連する既知の不純物や重要品質特性(CQA)をモニターする必要があります。イオン対逆相クロマトグラフィー(IP-RPLC)は、オリゴヌクレオチドの分離に広く使用されている手法です2。 IP-RPLC 手法では、オリゴヌクレオチドのリン酸骨格と、固定相に吸着するイオン対試薬由来の正に荷電したアミンの間のイオン対に基づいて、オリゴヌクレオチドがサイズ別に効果的に分離されます。ただし、リン酸はキレート剤であることが知られており、金属との複合体を形成する可能性があります。骨格の負に荷電したリン酸基は、金属表面と強く相互作用する傾向があるため、オリゴヌクレオチドではこの点が問題になる場合があります。このような相互作用は、回収率の低下、ばらつきの増加、ピークテーリングなどのクロマトグラフィーのアーティファクトを引き起こす可能性があります。QC ラボでは、一貫した結果を適時に得られる頑健な分析法が求められており、このようなことは許容できません。バイオ医薬品の分析用に設計された LC プラットフォームを使用して、これらの相互作用を最小限に抑え、頑健な性能を発揮させられることが製造環境には理想的です。
Alliance iS Bio HPLC システムは Alliance iS HPLC システムの革新的な設計に基づいており、これらの困難なモダリティに対するウォーターズの回答となります。Alliance iS Bio HPLC システムは、バイオ医薬品の製造環境向けに特別に設計された、バイオイナートな HPLC システムです。この革新的な HPLC プラットフォームは、システム全体にわたって MaxPeak HPS テクノロジーによる生体適合性コンポーネントを使用したバイオイナートな流路を採用しており、バイオ医薬品アプリケーションに取り組む品質管理ラボに最適です。MaxPeak Premier カラムをサポートするこのシステムにより、バイオ医薬品サンプルの分析およびルーチン検査において、分離能と感度の向上およびピークテーリングの低減が可能になります3。 これらの機能を組み合わせることで、効率的な分析法開発が可能になり、一貫した信頼できる結果が得られます。
この試験の目的は、オリゴヌクレオチド標準試料(OST)と完全にチオ化されたホスホロチオエート(PS)オリゴヌクレオチドサンプル(GEM91)という 2 つのサンプルを分析することにより、Alliance iS Bio HPLC システムの潜在的なメリットを評価することです4。 従来のプラットフォームと、最新の HPLC プラットフォームである新規 Alliance iS Bio HPLC システムの間で比較分析を行いました。
実験方法
Alliance iS Bio HPLC システムの性能を古いシステムと比較しました。MassPREP™ オリゴヌクレオチド標準試料(OST)には、1 nmol の 15、20、25、30、35 mer のオリゴデオキシチミジン(製品番号:186004135)が含まれています。バイアルの内容物を 250 μL の脱イオン水に溶解して、最終濃度を 4 pmol/μL とし、このサンプルの 10 μL(40 pmol)をカラムに注入しました。GEM91:25 mer の完全にチオ化されたホスホロチオエート(PS)オリゴヌクレオチド CTC TCG CAC CCA TCT CTC TCC TTC T(分子量 7776 Da)。GEM91 は 0.5 mg/mL の濃度で注入しました。
古いシステムの条件
|
LC システム: |
古いシステム |
|
検出: |
UV/Vis 2489、λ = 260 nm |
|
カラム: |
XBridge™ BEH™ C18、5 µm、130Å、4.6 mm × 100 mm(製品番号:186003115)、 XBridge BEH C18、2.5 µm、130Å、4.6 × 100 mm(製品番号:186006039) |
|
カラム温度: |
60 ℃ |
|
サンプル温度: |
5 ℃ |
|
注入量: |
10 µL |
|
流量: |
OST は 0.65 mL/分、GEM91 は 0.50 mL/分 |
|
移動相: |
A:25 mM HAA 水溶液、pH = 7.0 B:25 mM HAA 含有水/ACN = 40/60、pH= 7.0 C:水 D:アセトニトリル |
|
クロマトグラフィーソフトウェア: |
Empower™ 3、FR4 |
Alliance iS Bio HPLC システムの条件
|
LC システム: |
Alliance iS Bio HPLC システム |
|
検出: |
TUV、λ = 260 nm |
|
カラム: |
XBridge Premier Oligonucleotide BEH C18、2.5 µm、130Å、4.6 × 50 mm(製品番号:186009901、+eConnect 製品番号:186009901RF)、2.5 µm、130Å、4.6 × 100 mm(製品番号:186009902、+eConnect 製品番号:186009902RF)、2.5 µm、130Å、4.6 × 150 mm(製品番号:186009903、+eConnect 製品番号:186009903RF) 注:カラムトラッキングのメリットは Empower 3.8.0 で最大限に活用できます。 |
|
カラム温度: |
60 ℃ |
|
サンプル温度: |
5 ℃ |
|
注入量: |
OST は 10 µL、GEM91 は、50 mm カラムの場合 10 µL、100 mm カラムの場合 20 µL、150 mm カラムの場合 30 µL。 |
|
流量: |
OST では 0.65 mL/分。GEM91 では、5 µm カラムの場合 0.50 mL/分、2.5 µm カラムの場合 1.00 mL/分 |
|
移動相: |
A:25 mM HAA 水溶液、pH = 7.0 B:25 mM HAA 含有水/ACN = 40/60、pH= 7.0 C:水 D:アセトニトリル |
|
クロマトグラフィーソフトウェア: |
Empower 3.8.0 |
Waters MassPrep OST 分析のグラジエントテーブル
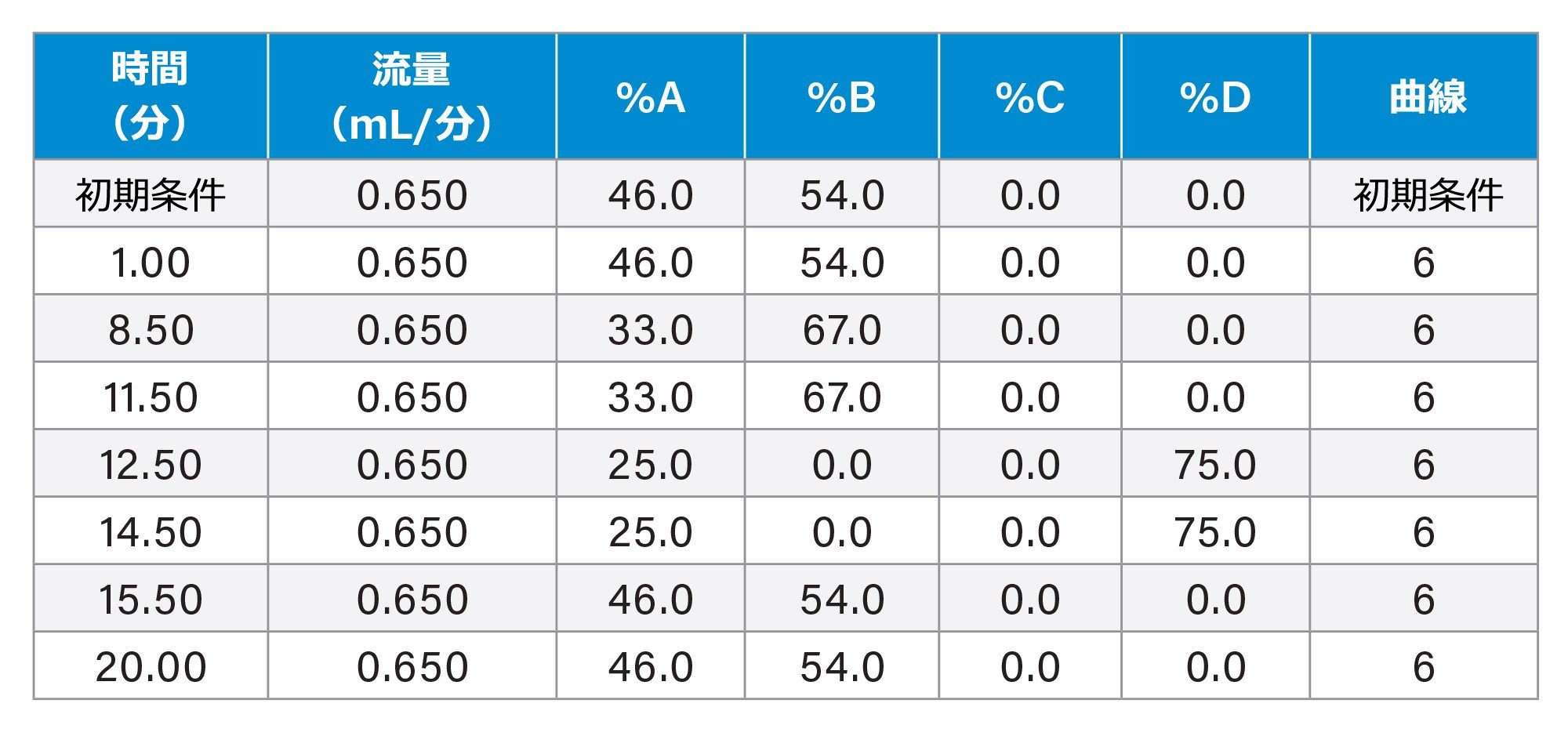
GEM91 分析のグラジエントテーブル
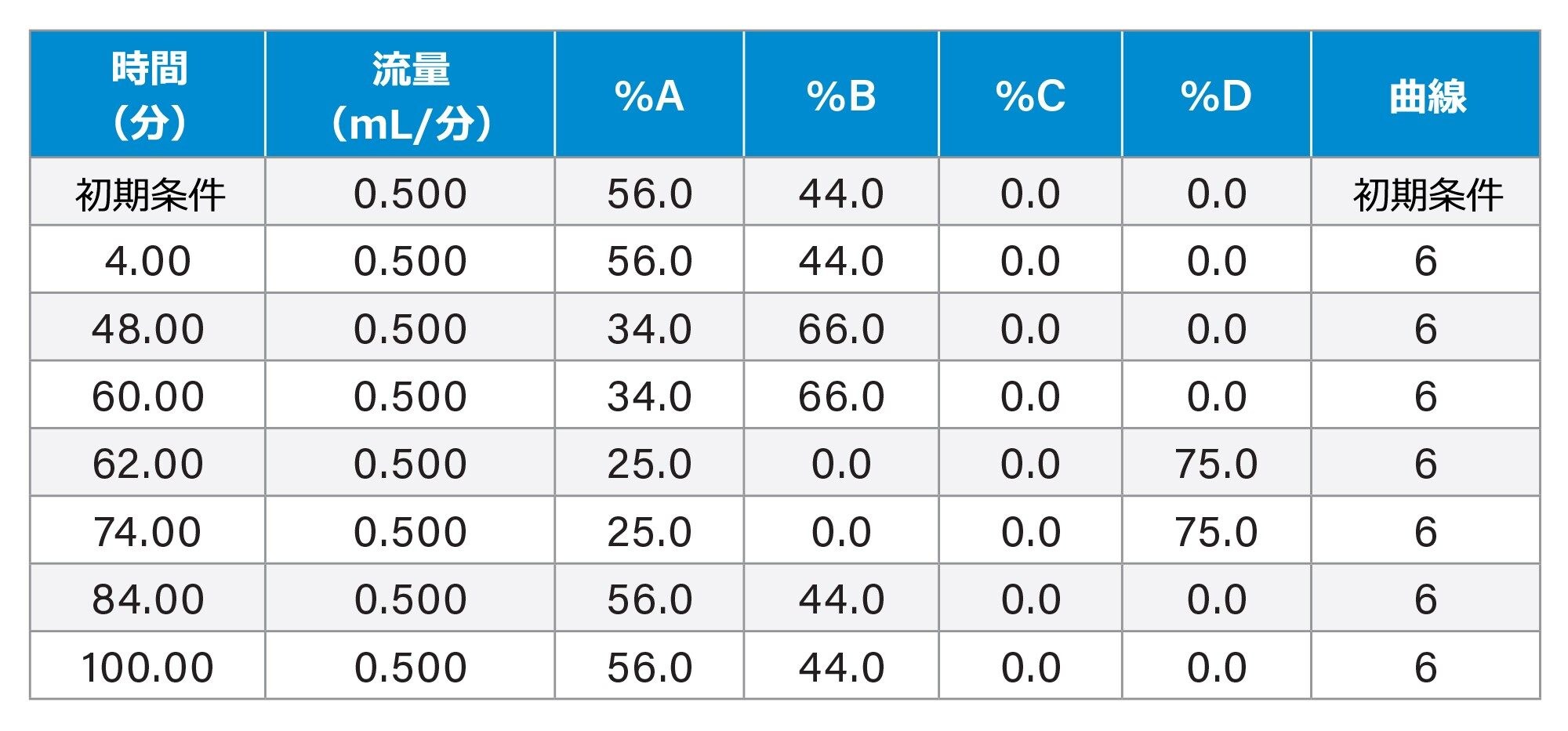
結果および考察
オリゴヌクレオチド MaxPeak HPS テクノロジーのメリット
オリゴヌクレオチドは、リン酸骨格がキレートするという性質により、LC 分離の回収率が低いことで知られています。その結果、分析における分析種の回収率を高めるため、表面の不動態化手順に長時間かかる場合があります。Alliance iS Bio HPLC システムは、バイオイナート設計の一環として MaxPeak HPS テクノロジーを用いています。これにより、分析種と表面の相互作用(オリゴヌクレオチドの分析の場合に該当)が低減するように設計されています。この点に関して Alliance iS Bio HPLC システムを評価するため、オリゴヌクレオチド標準試料の回収率を、2.5 µm、130Å、4.6 × 100 mm、XBridge BEH C18 カラムを搭載した古いシステムと、2.5 µm、130Å、4.6 × 100 mm、XBridge Premier Oligonucleotide BEH C18 カラムを搭載した Alliance iS Bio HPLC システム(最新の HPLC)という 2 つのシステムで比較しました。各システムに MassPrep OST 標準試料を 20 回注入しました。イオン対試薬として酢酸ヘキシルアンモニウム(HAA)を使用しました。移動相は、pH 7 の 25 mM HAA 水溶液(MP A)および水とアセトニトリルの混合液(MP B)を使用して調製しました。図 1 に示すように、MaxPeak Premier Oligonucleotide カラムを搭載した Alliance iS Bio HPLC システムでは、オリゴヌクレオチド分析に大きな改善が見られました。具体的には、20 nt のピークを代表的な完全に分離されたピークとすると、平均してピーク高さは最大 30%(図1A)、ピーク面積は 14% 増加(図1B)しており、感度および回収率が向上していることがわかります。さらに、Alliance iS Bio HPLC システムではより短時間で最大の回収率が得られるため、時間のかかる不動態化手順が不要になります。この効率は、Alliance iS Bio HPLC システムおよびカラムのバイオイナートという側面に起因するものであり、MaxPeak HPS テクノロジーにより、オリゴヌクレオチドのリン酸骨格と、システムおよびカラムのハードウェアの金属表面との間の非吸着性のキレート化が効果的に低減して、分析種の回収率が向上します。
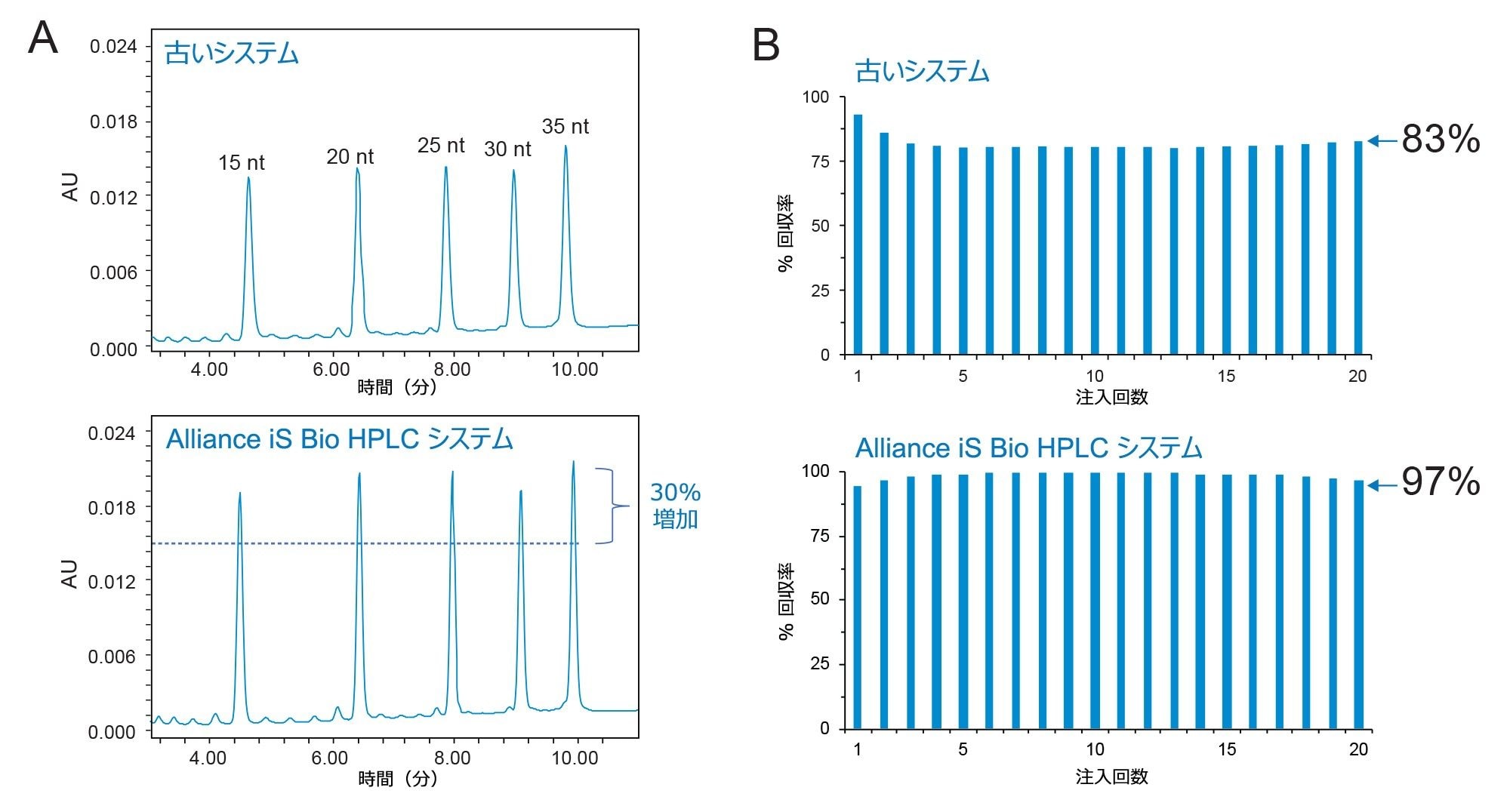
古いシステムから Alliance iS Bio HPLC システムへの分析法の移管。
バイオイナート表面のメリットが確認されたので、Alliance iS Bio HPLC システムの性能をさらに調査するために、業界をより代表するサンプルを使用して、完全にチオ化されたオリゴヌクレオチド医薬品候補 GEM91 を分析しました。GEM91 は原薬として精製されているにもかかわらず、モニタリングが必要な微量の不純物が含まれています。装置間の同等性を確保するために、両方のシステムで同じ分析法とカラムを使用しました。分析法の移管を支援するため、Alliance iS Bio HPLC システムでは、移管プロセスを迅速にし、転記ミスを減らす手段として、Intelligent Method Translator App(iMTA)へのアクセスをユーザーに提供しています。この試験では、iMTA(図 2A、2B)を使用して古いシステムから分析法条件をエクスポートし、Alliance iS Bio HPLC システム内でその分析法を再生しました。データからわかるように、古い HPLC 分析法に代表的なケミストリーフォーマット(5 µm、130Å、4.6 × 100 mm)を使用して、Alliance iS Bio HPLC システム(図 2D)で古い分析法のクロマトグラム(図 2C)が問題なく再現しました。不純物プロファイル(ピーク 1 ~ 3 として同定)を詳しく調べると、Alliance iS Bio HPLC システムに組み込まれた MaxPeak HPS によって、微量不純物のシグナル対ノイズ比が最大 40% 増大しました。この改善は、オリゴヌクレオチドなどの高度な治療法に重要な分子種を分析する際における、回収率と正確度の向上につながります。
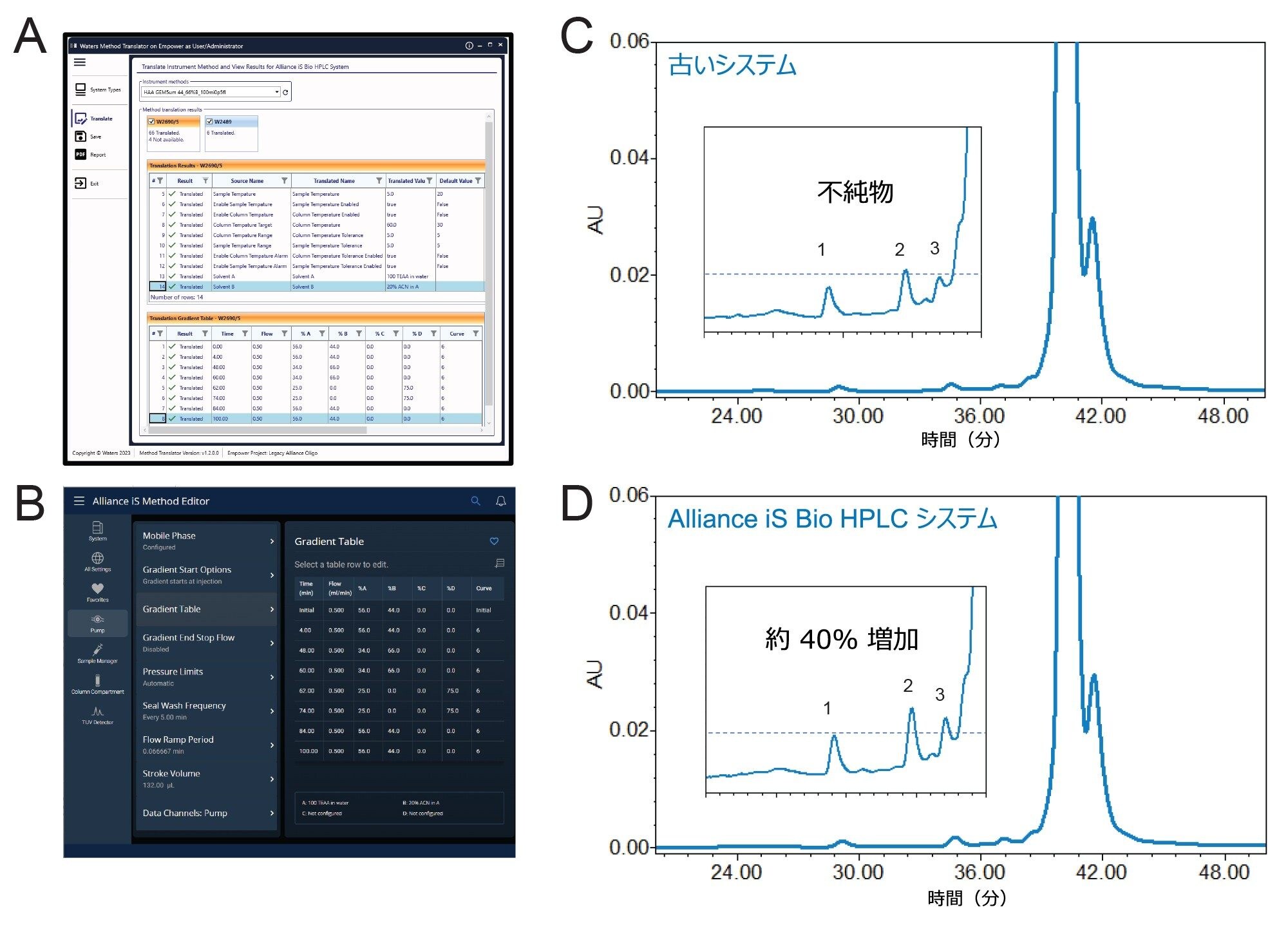
分析法の最新化
最新の HPLC 装置である Alliance iS Bio HPLC システムにより、最大 10,000 psi の圧力をサポートすることができ、最新のカラムテクノロジーのメリットを活用して、リソースを節約してスループットを高めることができます。このテクノロジーの特徴として、分離効率が高まるように設計された小さい粒子径とカラム直径が挙げられます。この点を実証するするため、Waters カラムカリキュレーターを使用して、従来の内径 4.6 mm(粒子径 5 µm)のカラム型式からより新しい 2.5 µm 粒子固定相に、分析法をスケーリングしました。スケーリングの分析法を評価するため、カラム長 50 mm、100 mm、150 mm について試験しました。図 3 に示すように、GEM91 および関連する不純物についてのピークの選択性は、粒子が小さいカラム全体にわたって保持されていました。このことは、4 つの不純物ピークの相対保持時間のリストに基づいて判定しました。分析法の最新化により、バリデーション済み分析法を支える選択性が維持されるだけでなく、新たなメリットも得られます。カラム長を 150 mm から 50 mm に短縮することで、時間、サンプル、溶媒の消費量が 3 分の 1 に低減されました。このことから Alliance iS Bio HPLC システムの費用対効果の高さが実証されました。
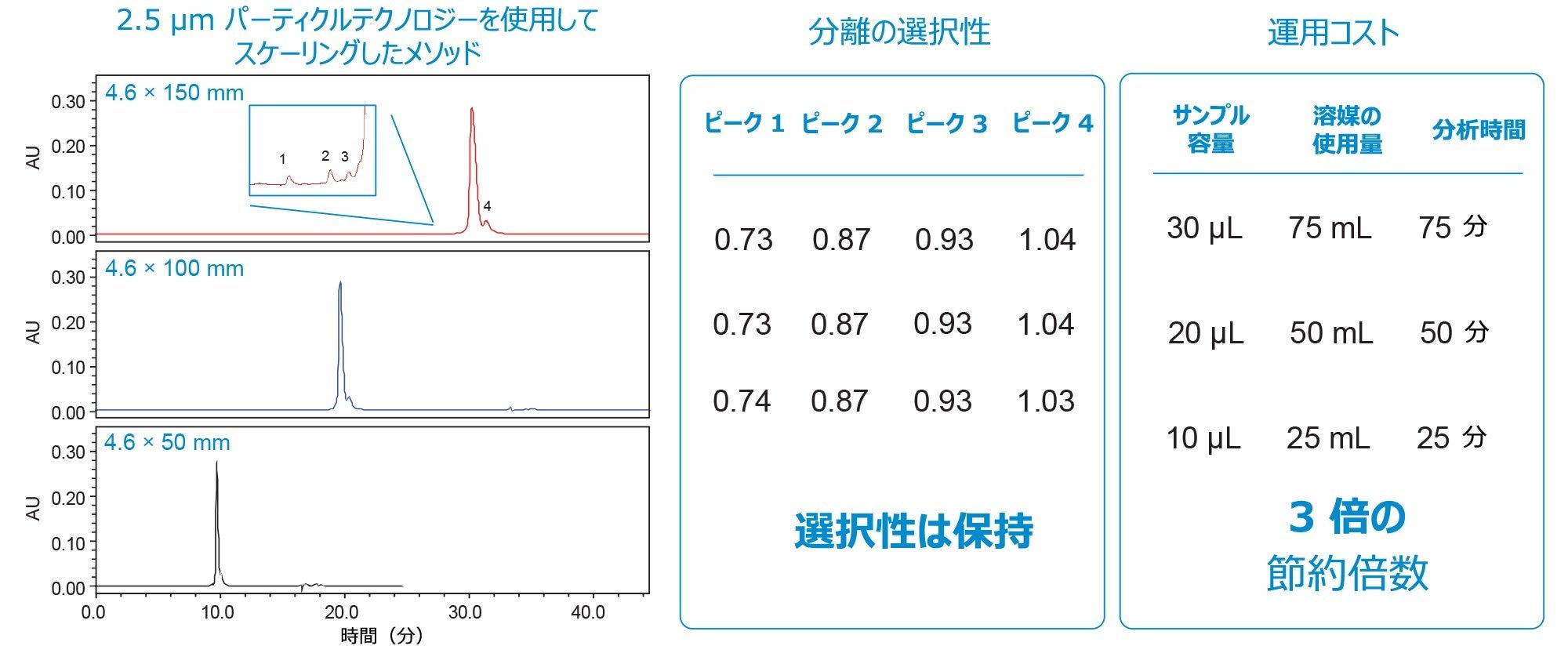
分析法の最新化
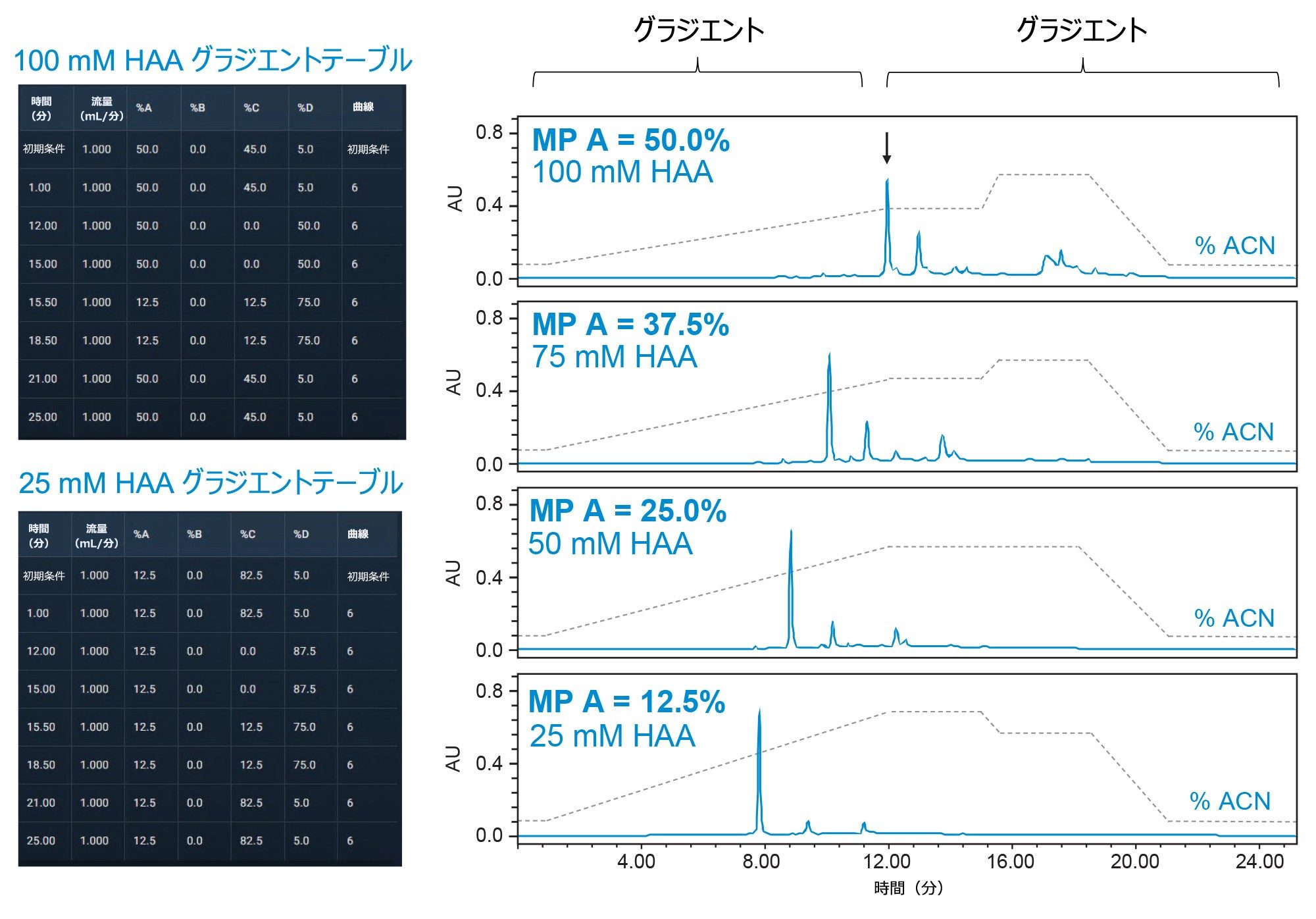
Alliance iS Bio HPLC システムの価値は、最新のカラムケミストリーに対応する機能に留まりません。Alliance iS Bio HPLC システムの設計の一環としてクオータナリーソルベントマネージャが使用されていることにより、QC ラボにおいて分析法をより効率的に最適化することができます。分析法の適格性評価とバリデーションでは、多くの場合、ある程度の開発と最適化が行われます。このプロセスには、サンプルおよび移動相の複数の調製物が含まれる場合があり、その過程で条件を段階的に試験します。これは繰り返しプロセスであるため、運用コストの増大、時間のロス、溶媒の消費につながる可能性があります。4 つの移動相リザーバーを備えた Alliance iS Bio HPLC システムにより、クオータナリー溶媒混合が可能になり、分析法の最適化における柔軟性と効率が高まります。このことを実証するするため、200 mM の高濃度 HAA ストック溶液を移動相 A として調製しました。移動相 C および D では、水とアセトニトリルを用いて HAA 濃度を制御し、グラジエントを送液しました。移動相 A を 50% ~ 12.5% に調整することで、単一の移動相調製物を使用して、25 mM ~ 100 mM の範囲の HAA 濃度を効果的に評価することができます。この例を図 4 に示します。ここでは、グラジエント内で GEM91 オリゴヌクレオチド(矢印で示す)を溶出するのに最適な HAA 濃度をスカウティングするために、すべての分析でアセトニトリルを 5%(MP D)から増加させました。この例では、100 mM HAA は高濃度すぎることが観察され、グラジエントの最後にオリゴヌクレオチドが溶出しています。さらに、この最終アセトニトリル濃度は、オリゴヌクレオチドに続いて一部の移動相不純物を溶出させるのに不十分と判断されました。この場合、イオン対濃度を減らすことで、試薬の使用量を節約でき、グラジエント開発スペースにおけるコントロールが容易になりました。その結果、イオン対濃度として 25 mM HAA が、グラジエントスペース内でオリゴヌクレオチドを溶出させるのに十分であると判断され、さらなる分析法の最適化が可能になりました。
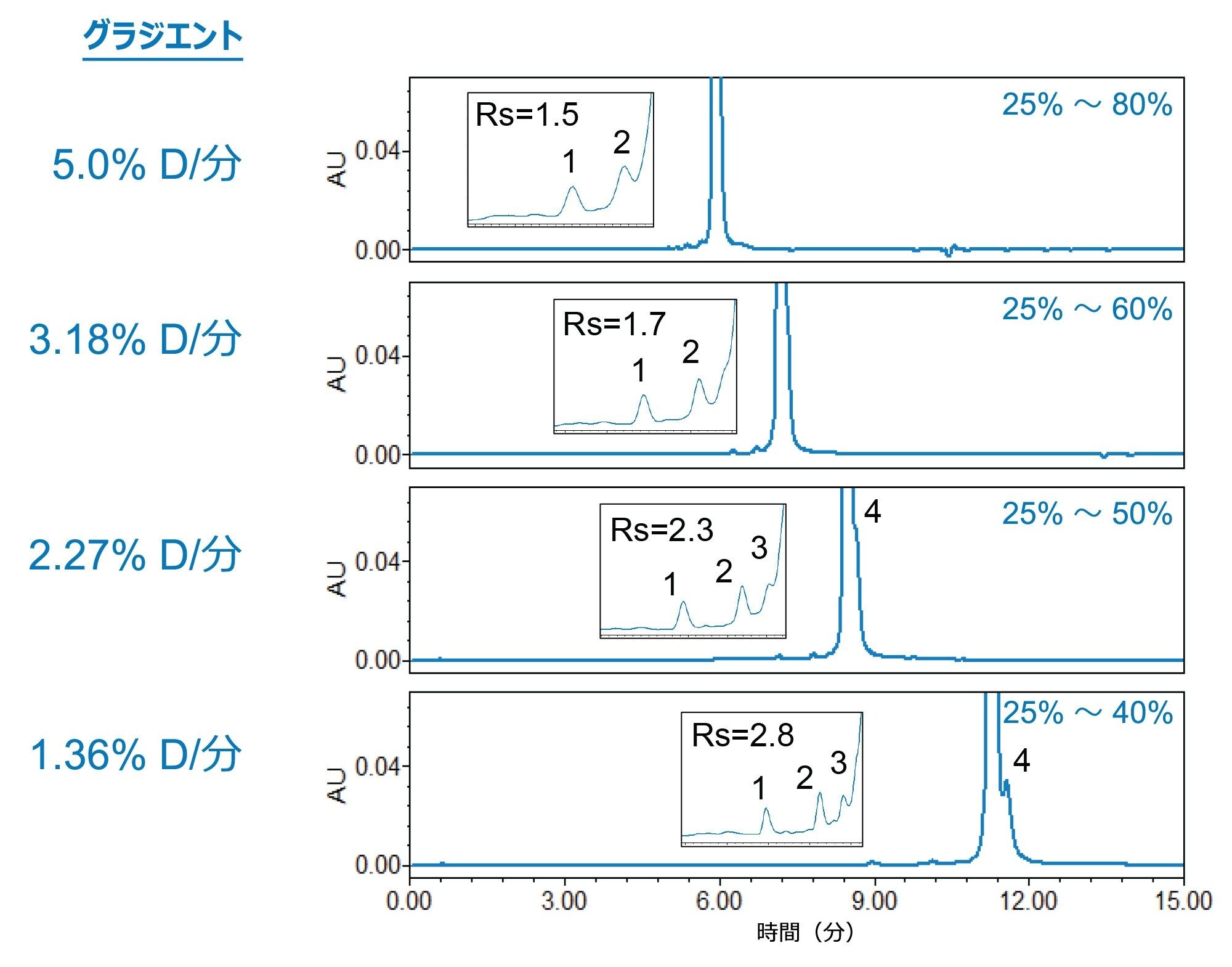
25 mM という条件(MP A = 12.5%)を用い、同じ移動相調製物を使用して、ピークの選択性をさらに最適化しました。このアプローチにより、実験に費やす時間を節約できるだけでなく、溶媒使用量と廃液の生成を減らすことで、実験による環境負荷を低減することもできます。移動相 D を使用してグラジエントの傾きを最適化することで、不純物とメインピークの間の分離が向上しました。図 5D に示すように、11 分間のグラジエントを 5% D/分から 1.36% D/分に最適化することで、不純物(ピーク 1 ~ 4)間の分離が向上するとともに、総分析時間を 25 分と比較的短く保つことができました。
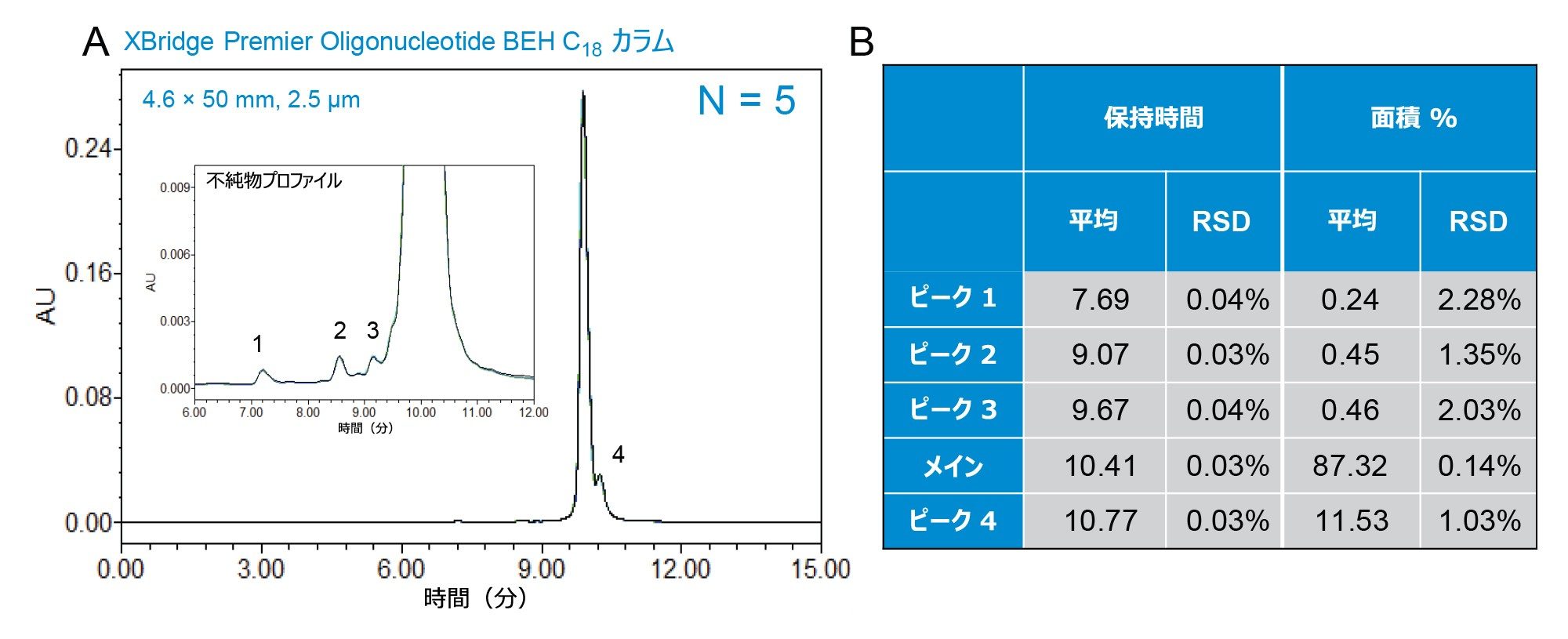
2.5 µm、130Å、4.6 × 50 mm、XBridge Premier Oligonucleotide BEH C18 カラムを使用し、最適化した条件を用いて、GEM91 の 5 回繰り返し注入について、分析法の再現性を評価しました。図 6A の 5 回繰り返し注入の重ね描きでわかるように、Alliance iS Bio HPLC システムにより、一貫した結果が迅速に得られます。図 6B に示すように、不純物のピーク(1 ~ 4)は、保持時間で 0.05% RSD 未満、ピーク面積割合で 3% RSD 未満を示しています。全体として、このアプローチにより、全体の運用コストを削減し、バイオ医薬品向けの環境にやさしい分析法を開発することができます。これによって、より少量の溶媒および試薬を使用して、一貫性のある頑健な結果が得られます。
結論
この試験で得られた観察結果から、Alliance iS Bio HPLC システムが、オリゴヌクレオチドなどのバイオ医薬品の分析に適しており、製造環境における支援ラボの現在および将来のニーズに対処するのに格好の位置を占めていることが示唆されました。Alliance iS Bio HPLC システムと XBridge Premier Oligonucleotide カラムを使用することで、オリゴヌクレオチドである polyT 標準試料のピーク回収率が 15% 向上し、代表的なオリゴヌクレオチドサンプル(GEM91)中の不純物のシグナル対ノイズ比が 40% 増加しました。このシステムの性能は、GEM91 サンプルの 5 回繰り返し注入にわたる不純物の面積割合における相対標準偏差(RSD)が 3% 未満であることによって実証されました。Alliance iS Bio HPLC システムのクオータナリーソルベントマネージャにより、分析法条件を迅速かつ効率的にスカウティングでき、バイオ医薬品の分析におけるコストと時間の節約において Alliance iS Bio HPLC システムによって得られる価値が実証されました。
参考文献
- Ziyi Chen, Zhiliang Liu, Yali Feng, Aochen Shi, Liqing Wu, Yi Sang, Chenxi Li, Global research on RNA vaccines for COVID-19 from 2019 to 2023: a bibliometric analysis.Sec.Vaccines and Molecular Therapeutics, Volume 15–2024.
- Koshel BM, Birdsall RE, Yu YQ.Improving Recovery and Quantitation of Oligonucleotide Impurities Using ACQUITY Premier with MaxPeak HPS Technology.Waters Application Note 720007238.April 2021.
- Martin Gilar, Zhimin Li, Jason MacLean.Improved Chromatographic Analysis of Oligonucleotides with ACQUITY Premier Oligonucleotide BEH C18 Columns.Waters Application Note 720007012.August 2023.
- Kathryn Brennan, Mary Trudeau, Michael Donegan, Paul D. Rainville.Improved Oligonucleotide SPE-LC-MS Analysis Using MaxPeak High Performance Technology.720007019, September 2020.
720008288JA、2024 年 4 月