臨床研究用 Xevo TQ Absolute を使用した血清中の遊離テストステロンの分析
研究目的のみに使用してください。診断用には使用できません。
要約
本稿では、平衡透析と Xevo™ TQ Absolute 質量分析計を使用して優れた分析感度が得られる、血清中の遊離テストステロン分析用の臨床研究法について説明します。
この臨床研究法では、少量の血清と平衡透析後の液-液抽出手順を使用しました。ACQUITY™ UPLC™ I-Class PLUS FL システムを使用して、ACQUITY BEH™ C18 カラムでテストステロンを分離し、Xevo TQ Absolute 質量分析計でマルチプルリアクションモニタリング(MRM)を用いて検出を行いました。開発したメソッドは、200 µL の血清を使用して 1 ~ 500 pg/mL の範囲で良好な分析感度と選択性を示し、この範囲全体での精度は 8.4% CV 以下でした。
アプリケーションのメリット
- わずか 200 µL の血清からの遊離テストステロン(0.5 pg/mL)の分析感度に優れた分析
- 平衡透析にかかる時間が短い(2 時間)
- 前処理済みサンプルの容量が小さいため、必要に応じて再分析が可能
はじめに
臨床研究における遊離テストステロンの分析は、主に遊離テストステロンが総テストステロンの 3% に満たないために分析感度が課題になり、また平衡透析が複雑で時間がかかるプロセスであるため、困難な作業でした。
しかし、Xevo TQ Absolute を使用し、Thermo Scientific™ の迅速平衡透析(Rapid Equilibrium Dialysis、RED)用インサートおよびプレートを使用して、迅速かつ制御されたインキュベーションを行うことで、この課題は解決しました。遊離テストステロン分析用の、分析感度が高く、精密で正確な研究法が開発されました。
平衡透析法により、血清中の結合テストステロンから遊離テストステロンを分離し、液液抽出を使用して遊離テストステロンを別の溶媒に濃縮・洗浄しました。最終的な抽出液を ACQUITY UPLC I-Class PLUS FL システムに注入し、ここで遊離テストステロンは、ACQUITY BEH C18 カラムで分離され、Xevo TQ Absolute 質量分析計で検出されました(図 1)。
実験方法
サンプルの説明
1.0 mg/mL のテストステロン認証レファレンス物質(CRM)(Merck、英国)溶液を使用して、1 M ストック(Merck、英国)から希釈して pH 7.4 に調整した 52.75 mM HEPES バッファー中に 1 ~ 500 pg/mL の範囲の一連のキャリブレーション試薬を調製しました。
社内品質管理サンプル(QC)は、処理済み MSG4000 血清(Golden West Biologicals、米国)、未処理血清、および個々のオスの血清サンプル(BioIVT、英国)を使用して、約 2.79、8.80、134 pg/mL の濃度になるように調製しました。
100 µg/mL のテストステロン-13C3 認証レファレンス物質(CRM)(Merck、英国)溶液を使用して、作業用内部標準試料を調製しました。
平衡透析
RED デバイスインサート(Thermo Scientific、英国)を RED デバイスの再使用可能ベースプレート(Thermo Scientific、英国)に追加しました。200 µL の血清をマトリックスチャンバーに添加し、pH 7.40 ± 0.03 に調整した 52.75 mM HEPES バッファー 400 µL をバッファーチャンバーに入れました。プレートをシーリングテープ(Thermo Scientific、英国)で密封し、37 ℃ に温度校正済みのオービタルシェーカーに入れて、800 rpm で 2 時間攪拌しました。
液-液抽出
RED デバイスインサートを取り外し、遊離ホルモンを含むジアシル酸を RED デバイスの再使用可能ベースプレートのウェル内に残しました。300 µL のジアシル酸を 2 mL の微量遠心チューブに移し、1000 pg/mL のテストステロン-13C3 を含むメタノールを 30 µL 添加しました。30 秒間の混合ステップ(マルチチューブボルテックスミキサーで 2500 rpm)の後、1.5 mL のメチル tert-ブチルエーテルを添加し、チューブに蓋をして振とうした後(2500 rpm で 5 分間)、16100 g で 2 分間遠心しました。1.3 mL の上清をきれいな Waters 2 mL 96 ウェルサンプルコレクションプレート(製品番号:186002482)に移し、窒素を用いて温度 40 ℃ で乾固させました。最後に、70 µL の 50/50 v/v 移動相 A:移動相 B を添加し、プレートを Waters 角型ウェルキャップマット(製品番号:186002484)で密封して、2500 rpm で 30 秒間振とうした後、分析しました。
LC 条件
|
カラム: |
ACQUITY UPLC BEH C18 カラム、130 Å、2.1 × 100 mm、1.7 µm(製品番号:186002352) |
|
カラム温度: |
50 ℃ |
|
サンプル温度: |
10 ℃ |
|
注入量: |
25 μL |
|
注入モード: |
パーシャルループ |
|
ニードルサイズ: |
20 µL |
|
サンプルシリンジ: |
250 µL |
|
サンプルループ: |
50 µL |
|
流量: |
グラジエントテーブルを参照 |
|
移動相 A: |
0.2 mM フッ化アンモニウム水溶液 |
|
移動相 B: |
0.2 mM フッ化アンモニウムメタノール溶液 |
|
弱洗浄溶媒: |
5%(v/v)メタノール水溶液 |
|
強洗浄溶媒: |
25/25/25/25(v/v/v/v)アセトニトリル/メタノール/IPA/水 |
|
分析時間: |
4.5 分 |
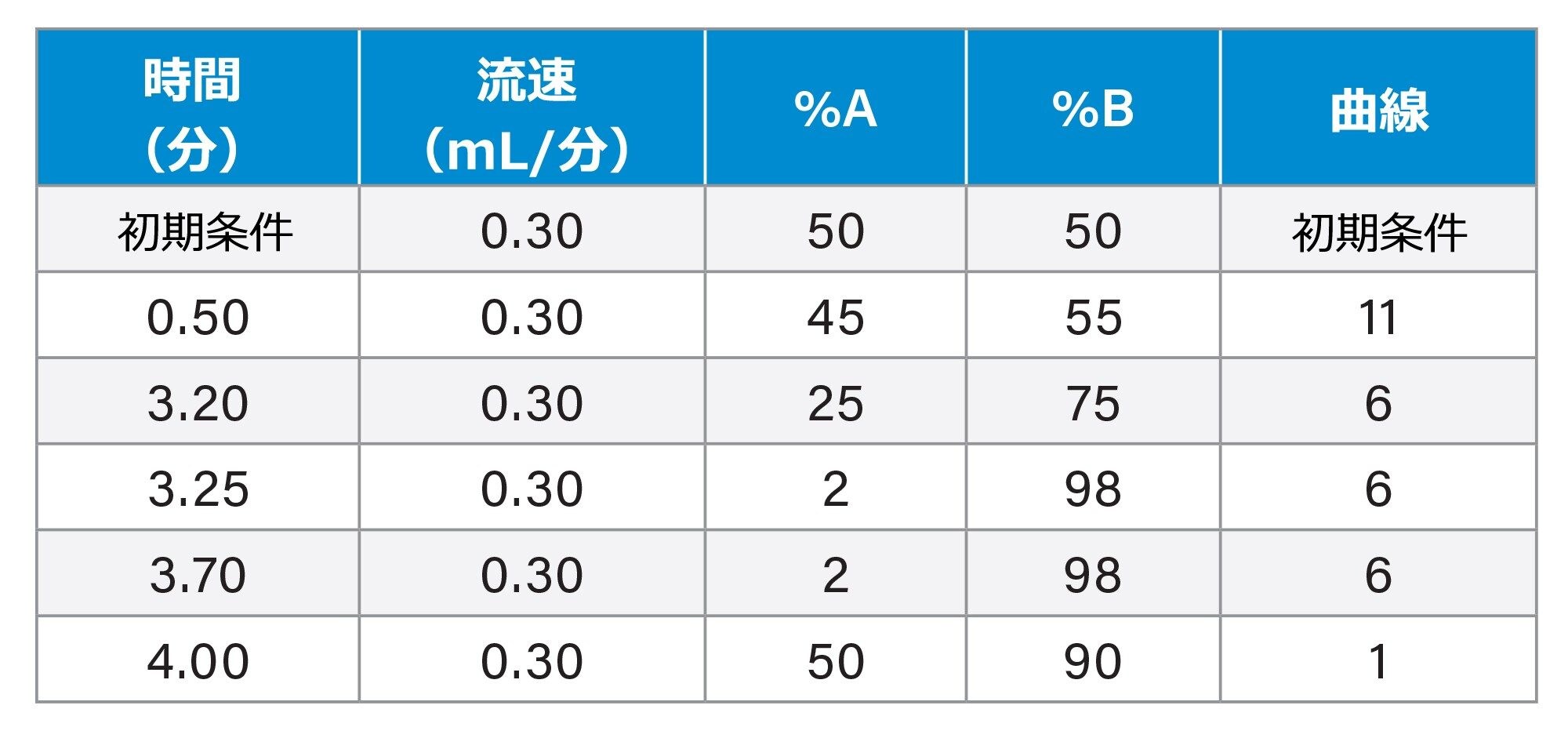
グラジエントテーブル
MS 条件
|
MS システム: |
Xevo TQ Absolute 質量分析計 |
|
イオン化モード: |
ESI+ |
|
キャピラリー電圧: |
1.2kV |
|
脱溶媒温度: |
650 ℃ |
|
イオン源温度: |
150 ℃ |
|
脱溶媒ガス: |
1000 L/時間 |
|
コーンガス: |
150 L/時間 |
|
MS1 分解能: |
ユニット(0.7 Da) |
|
MS2 分解能: |
ユニット(0.7 Da) |
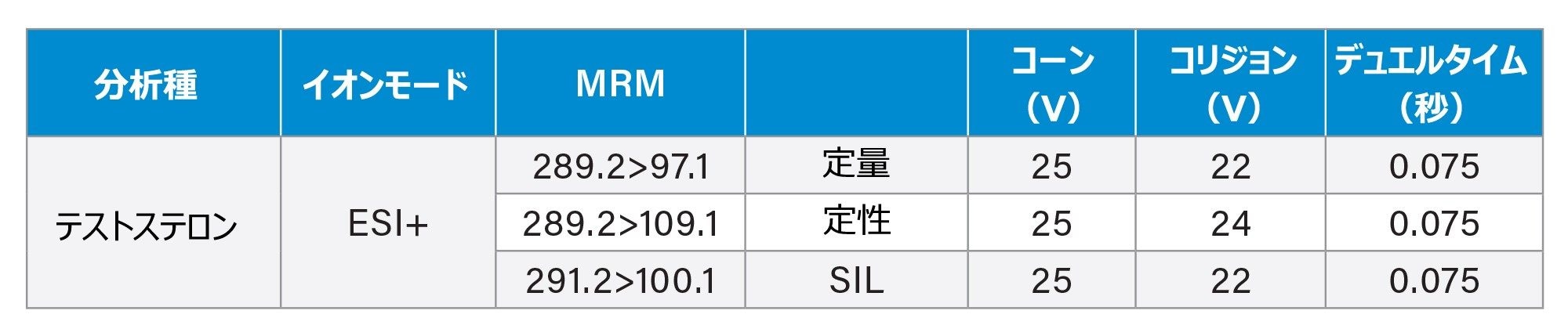
MRM パラメーター
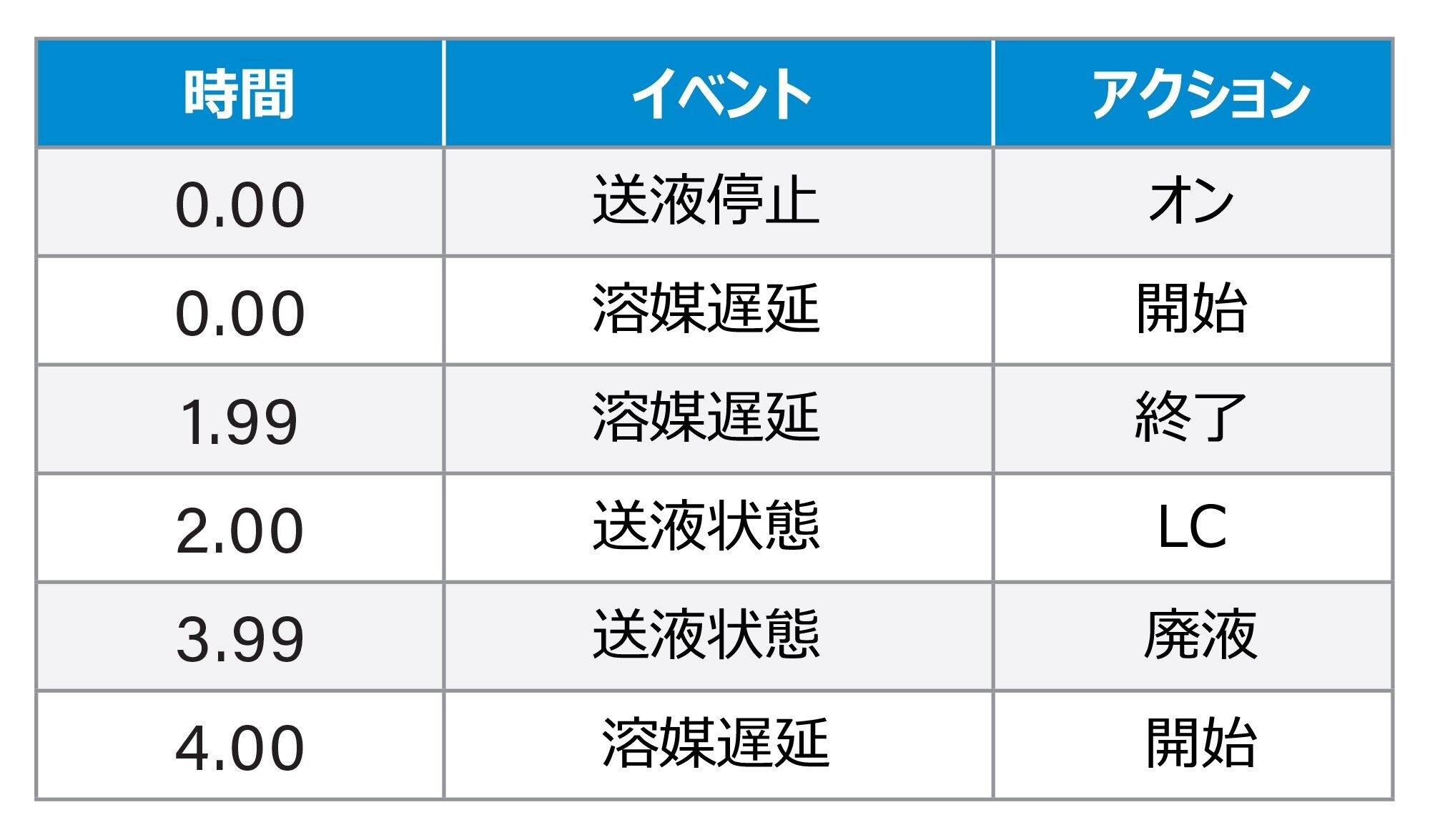
メソッドイベント
データ管理
|
MS ソフトウェア: |
MassLynx™ v4.2 ソフトウェア(SCN 1042) |
|
インフォマティクス: |
TargetLynx™ XS v4.2アプリケーションマネージャー |
結果および考察
ACQUITY UPLC BEH C18 カラム、130Å、2.1 mm × 100 mm、1.7 µm を使用して、遊離テストステロンおよびその内部標準試料をバックグラウンドノイズが比較的低い領域にクロマトグラフィー保持しました。注入間のサイクル時間は 5.3 分で、1 時間で 11 サンプル分析できました。システム適合性試験では、50/50 v/v 移動相 A/移動相 B 中 25 pg/mL テストステロン溶液を使用してシステムの分析感度のベンチマークを行い、分析の前のクロマトグラフィーベースラインノイズが低いことを確認しました。
この臨床研究法では、0.5 ~ 650 ng/mL の範囲で直線性が見られ、すべての分析実行にわたって r2 が 0.995 以上でした。500 pg/mL のサンプルからブランクサンプルへの顕著なキャリーオーバーは見られませんでした。最終抽出物は、サンプルマネージャー内 10 ℃ で 24 時間安定であることがわかりました。
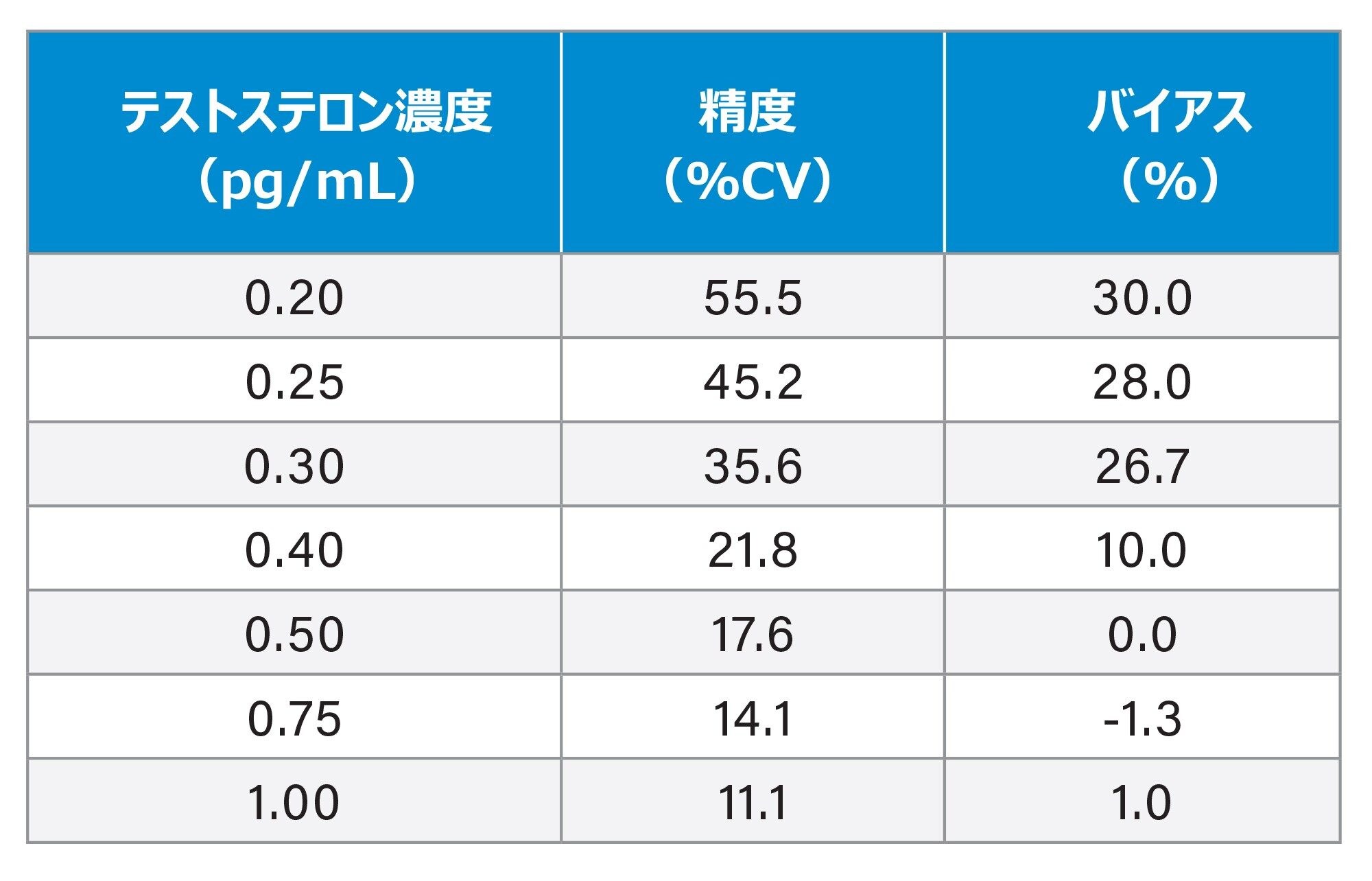
分析感度の調査を、pH 7.4 に調整した 52.75 mM HEPES バッファー中 0.20、0.25、0.30、0.40、0.50、0.75、1.00 pg/mL の低濃度テストステロンについて、10 回繰り返しの分析を 5 回実行して行いました(n = 50)。この調査により、測定間隔の下限(LLMI)、つまり精度が 20% 以下でバイアスが 15% 以下である濃度 0.5 pg/mL が達成できることが示されました。結果は表 1 に示しています。
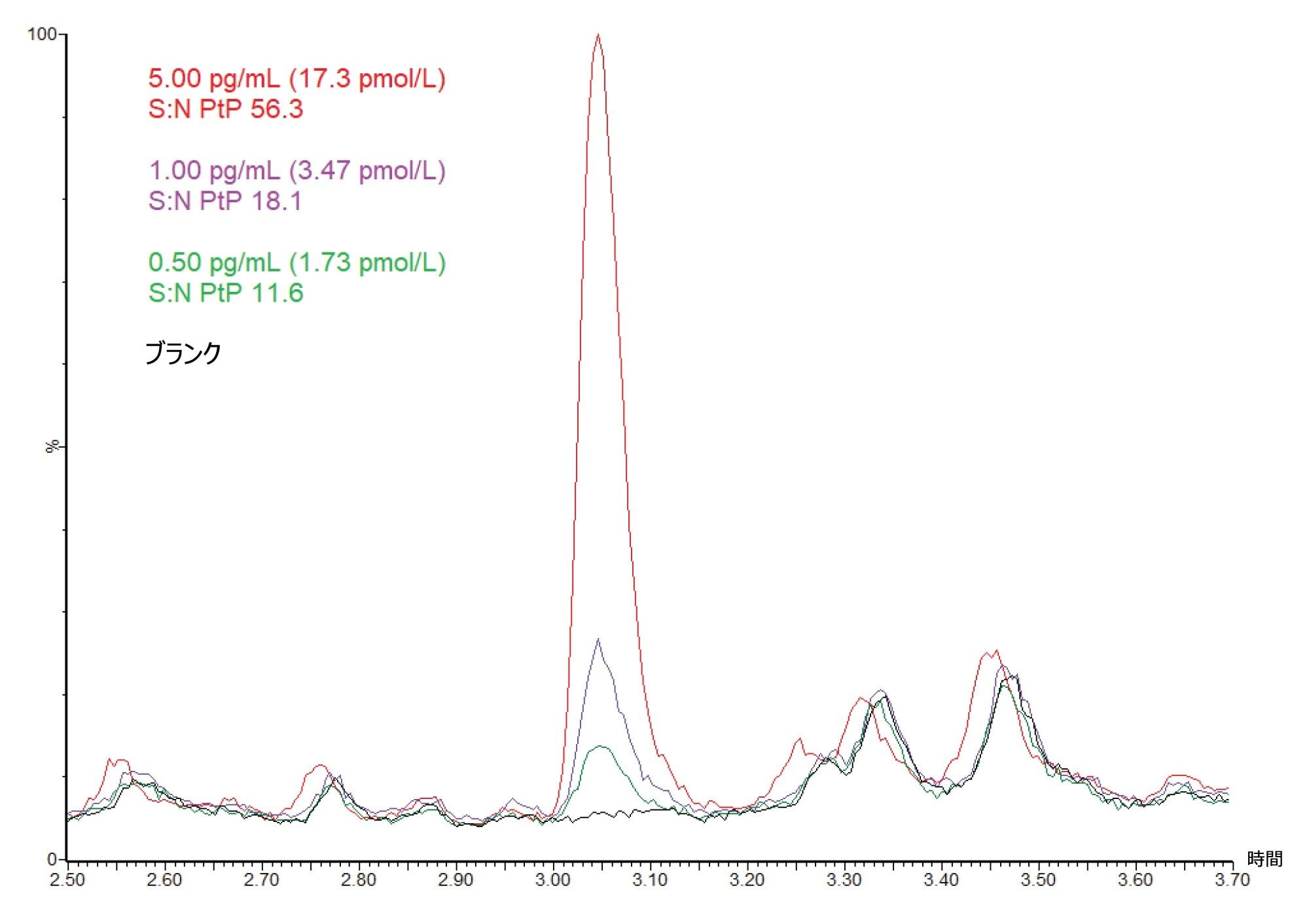
ブランクの 52.75 mM HEPES バッファー抽出物、0.50 pg/mL の抽出物(LLMI に対応)、1.00 pg/mL の抽出物(キャリブレーション試薬 1 の濃度)、5.00 pg/mL の抽出物の代表的なクロマトグラムを図 2 に示しており、これによりこの臨床研究法を使用して得られる分析感度がわかります。
3 回繰り返しの MSG4000 処理血清および低濃度・高濃度のテストステロン添加後のサンプルを抽出することにより、マトリックス効果を定量的に評価しました。コントロールサンプルは、pH 7.4 に調整した 52.75 mM HEPES バッファーを使用して同じように調製しました。ピーク面積に基づくマトリックス効果は 96% ~ 102% の範囲、RSD は 2.4% 以下であり、イオン増強もイオン抑制も認められませんでした。
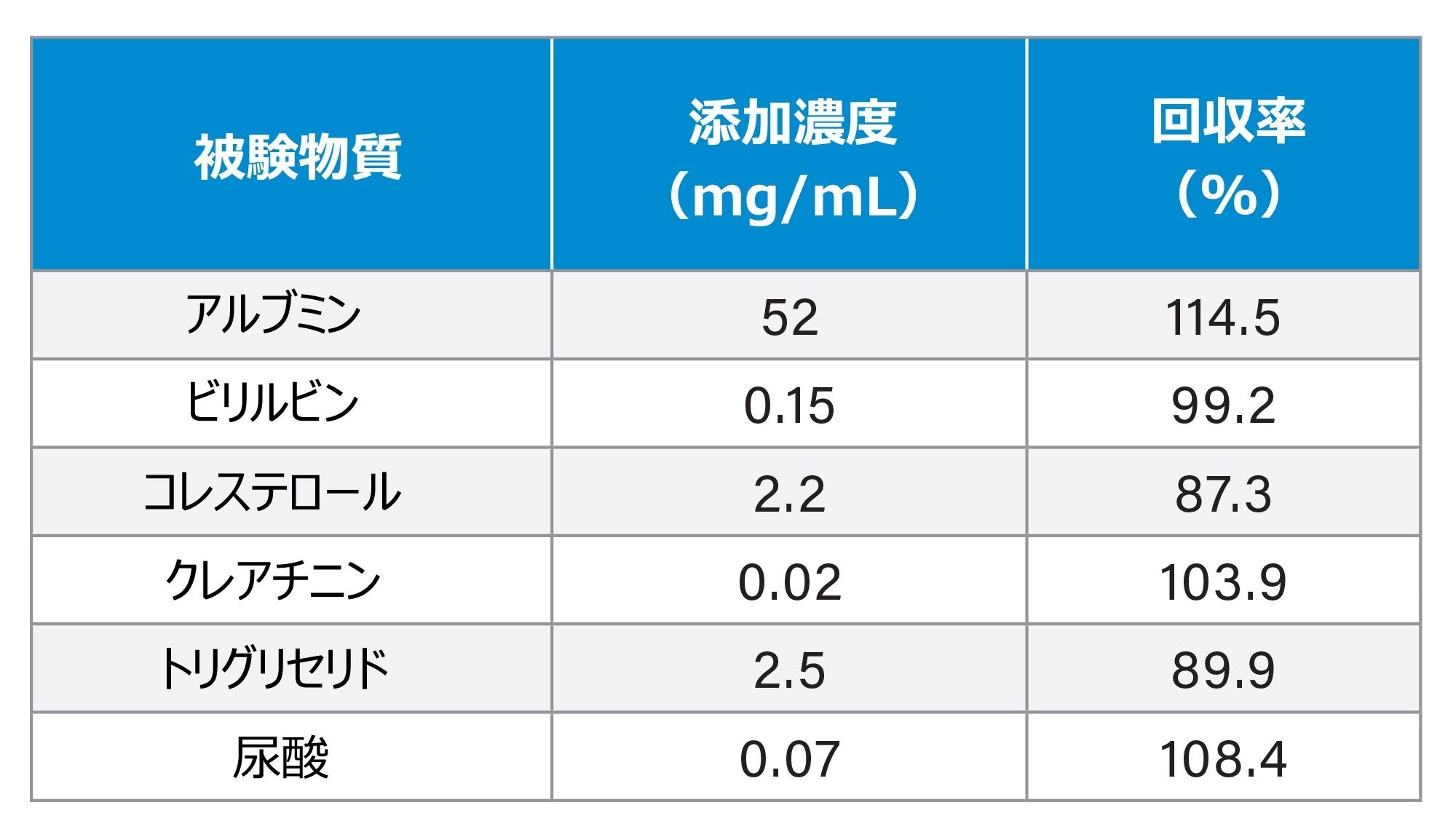
高濃度の幅広い内因性化合物(アルブミン、ビリルビン、コレステロール、クレアチニン、トリグリセリド、尿酸)を使用して、干渉試験を実施しました。濃度約 25 pg/mL の遊離テストステロンを含むプールした血清サンプルにおいて、テストサンプルおよびコントロールサンプルを 3 回繰り返しで分析しました。有意の干渉は認められず、回収率は 87.3 ~ 114.5 の範囲でした。表 2 にサマリーを示します。
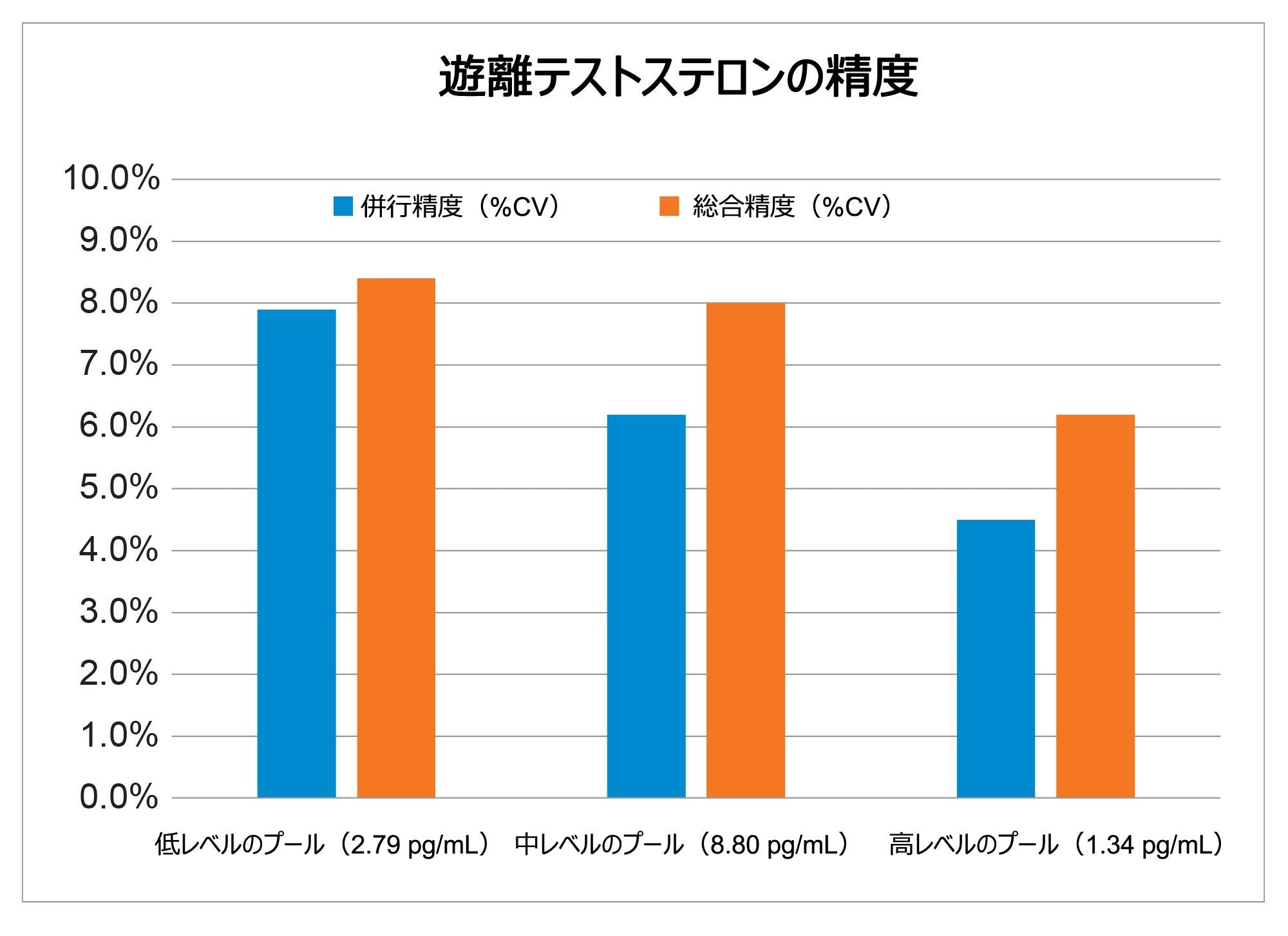
低、中、高(2.79、8.80、134 pg/mL)の血清中遊離テストステロンの QC 濃度で、各濃度 5 回繰り返しで 5 回の分析を実行し、このメソッドの総合精度と併行精度を評価しました(n = 25)。総合的な再現性および併行精度は 8.4% RSD 以下でした。図 3 に、これらの精度実験の結果を示します。
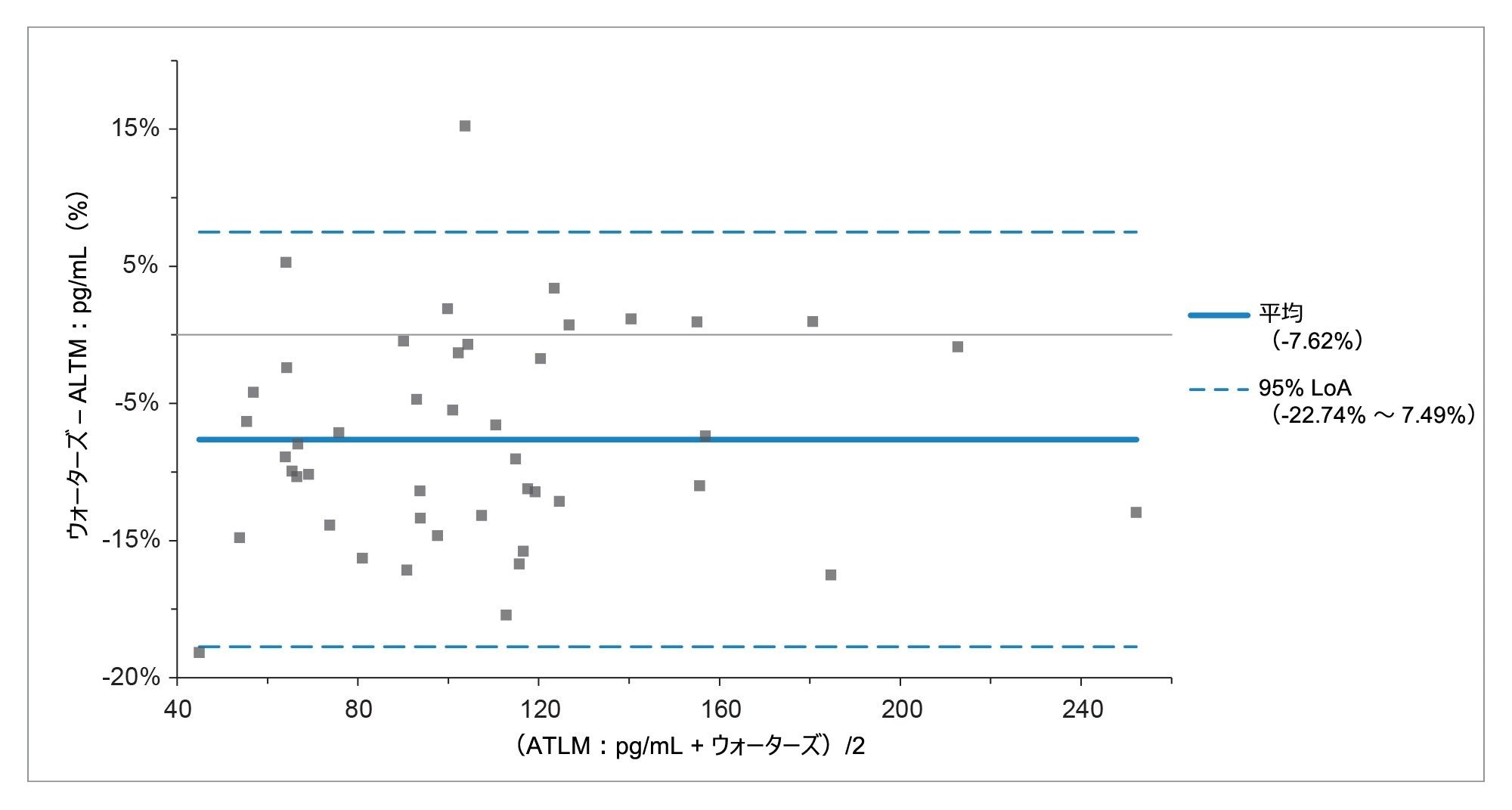
メソッドの性能を評価するために、英国 NEQAS から入手した濃度範囲 50.1 ~ 268.6 pg/mL の 45 例のオスの血清サンプルを分析し、結果をこのメソッドの全ラボトリム平均(ALTM)と比較しました。Passing-Bablok 回帰および Bland-Altman 一致性分析の両方をこのデータセットに適用し、ALTM 値と比較して、観測された性能を評価しました。Passing-Bablok 回帰では、式 y=-2.869 + 0.947x が得られ、Bland-Altman 一致性分析(図 4)では、-7.6% という小さい負の平均バイアスが見られましたが、全体として強く一致していることが示されました。
結論
平衡透析、ACQUITY UPLC I-Class PLUS FL システム、Xevo TQ Absolute 質量分析計を使用して、血清中の遊離テストステロンを測定する LC-MS/MS による臨床研究法を開発しました。このメソッドにより、200 µL の血清から最低 0.5 pg/mL の遊離テストステロンが検出され、サンプルは必要に応じて再分析できます。
- このメソッドは、顕著なキャリーオーバー、干渉、マトリックス効果がなく、良好な直線性を示す
- このメソッドの総合的な再現性および併行精度は 8.4% RSD 以下であった
- このメソッドは、英国 NEQAS の外部品質保証スキームと強く一致している
最後に、平衡透析ステップがわずか 2 時間で完了し、48 サンプルで構成される完全なプレートが 5 時間以内に調製できることから、このメソッドは迅速かつ効率的と言えます。
720008237JA、2024 年 2 月