臨床研究用の Capitainer® B デバイス搭載 Xevo™ TQ Absolute を使用した全血中の免疫抑制剤の LC-MS/MS 分析
研究目的のみに使用してください。診断用には使用できません。
要約
今回、ピペッティングした少量のヒト全血から採取した乾燥血液スポットに液-液抽出を使用する臨床研究分析法について説明します。
アプリケーションのメリット
- Xevo TQ Absolute を使用した少量のサンプルの分析感度
- クロマトグラフィーおよび質量検出器の分析における選択性により、短い分析時間で 4 種類の分析種を同時に分析可能に
- Capitainer B デバイスにより、少量サンプルで良好な精度と正確性を実現
はじめに
以前、Deprez らにより、シクロスポリン、エベロリムス、シロリムス、タクロリムスの分析用の、少量の全血から Capitainer B デバイスのインレットへのピペッティングによる既知量の乾燥血液スポットの作成を用いた、正確で再現性の高い LC-MS/MS 分析法が実証されています1。
今回、ピペッティングした少量のヒト全血から採取した乾燥血液スポットに液-液抽出を使用する臨床研究分析法について説明します。Waters™ ACQUITY™ UPLC™ I-Class PLUS で Waters ACQUITY UPLC HSS C18 SB カラムを使用したクロマトグラフィー溶出は、1.5 分以内で完了しました。4 種類の分析種すべての同時分析、およびそれに続く Xevo TQ-S micro 質量分析計での検出(図 1)が、注入間の間隔 2.2 分で行えました。

実験方法
サンプル前処理
全血 MassTrak 免疫抑制剤キャリブレーション試薬およびシクロスポリン、エベロリムス、シロリムス、タクロリムスが含まれる品質管理セットを使用しました。2H12-シクロスポリン、13C22H4-エベロリムス、2H3-シロリムス、アスコマイシンをそれぞれ内部標準として使用しました。
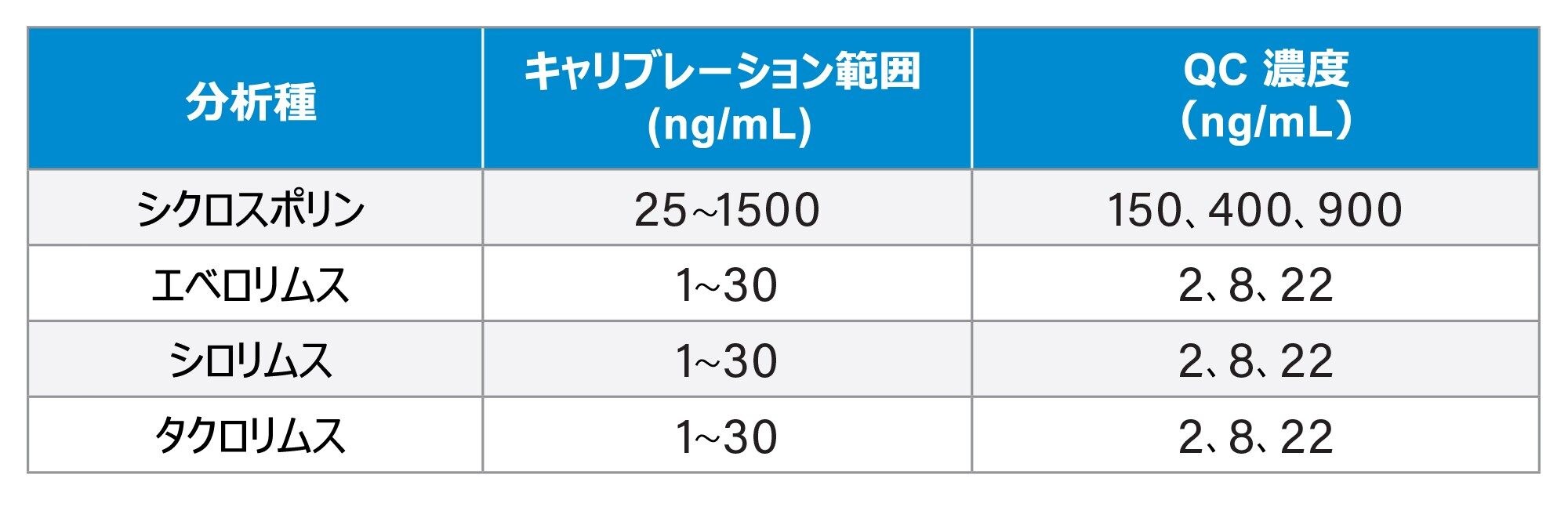
キャリブレーション試薬および QC の濃度(低、中、高濃度)については、表 1 に詳細に示されています。
サンプル抽出
30 µL のサンプルをデバイスのインレットにピペッティングし、10 µL の有効な乾燥血液スポットが形成されたのを確認してから一晩乾燥させます。乾燥血液スポットを微量遠心分離機チューブに移し、200 µL の作業用内部標準を添加してから、マルチチューブボルテックスミキサーで混合し(2500 rpm で 30 分間)、超音波処理し(20 分間)、最終的なボルテックス混合(2500 rpm で 10 分間)を行います。0.05M 塩酸 10 µLおよび tert-メチルブチルエーテル 1 mL を添加します。マルチチューブボルテックスミキサーで混合し(2500 rpm で 3 分間)、25155 g で 2 分間遠心分離します。上層から 850 µL をトータルリカバリーバイアル(製品番号:186005669CV)に移し、窒素流下 40 ℃ で蒸発乾固します。200 µL の移動相 A:移動相 B 50:50(v:v)に再溶解します。
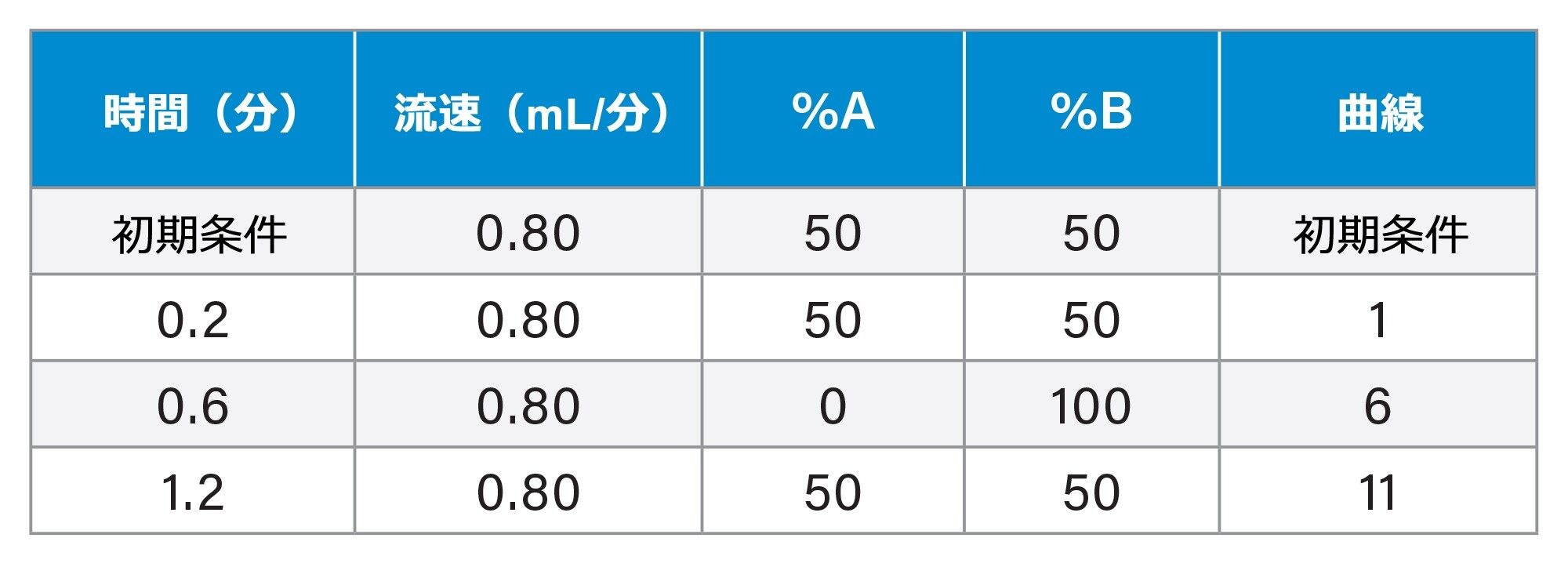
UPLC 条件
|
システム: |
ACQUITY UPLC I-Class PLUSFL 付き |
|
ニードル: |
20 µL |
|
ループ: |
50 µL |
|
カラム: |
ACQUITY UPLC HSS C18 SB カラム、1.8 µm、2.1 mm × 30 mm (製品番号:186004117) |
|
カラム温度: |
55 ℃ |
|
サンプル温度: |
10 ℃ |
|
注入量: |
20 µL |
|
注入モード: |
先行ロードを無効にしたパーシャルループ |
|
移動相 A: |
0.05 mM フッ化アンモニウム水溶液 |
|
移動相 B: |
0.05 mM フッ化アンモニウムメタノール溶液 |
|
弱洗浄溶媒: |
水:メタノール 95:5(v/v)、600 µL |
|
強洗浄溶媒: |
水:メタノール:アセトニトリル:イソプロパノール 25:25:25:25(v/v/v/v)、200 µL |
|
シール洗浄溶媒: |
水:メタノール 80:20(v/v) |
|
分析時間: |
1.5 分(2.2 分) |
MS 条件
|
システム: |
Xevo TQ Absolute |
|
分離: |
MS1(0.7 FWHM)、MS2(0.7 FWHM) |
|
取り込みモード: |
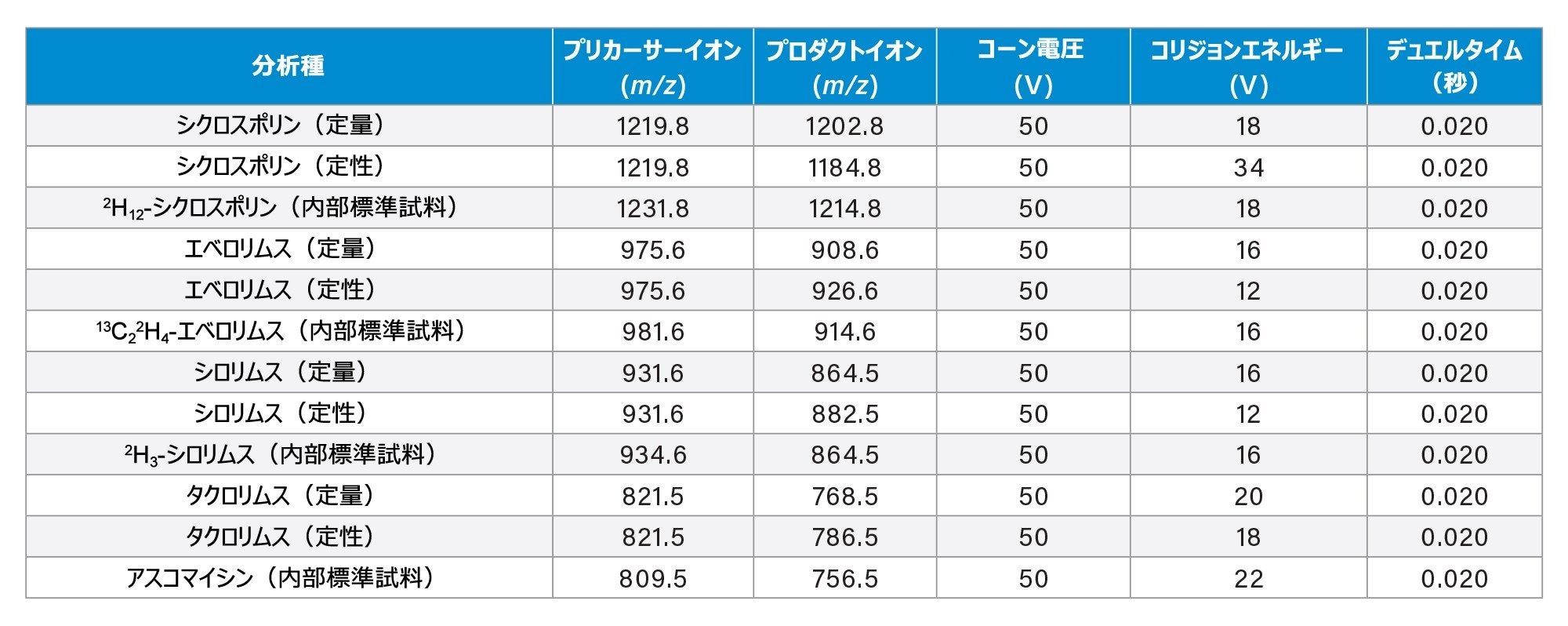
マルチプルリアクションモニタリング(MRM)(詳細は表 3 を参照) |
|
極性: |
ESI+イオン化(ESI+) |
|
キャピラリー: |
1.0 kV |
|
イオン源温度: |
120 ℃ |
|
脱溶媒温度: |
400 ℃ |
|
スキャン間遅延: |
0.003 秒 |
|
チャンネル間遅延: |
0.02 秒 |
データ管理
MassLynxTM v4.2(TargetLynx™ アプリケーションマネージャー搭載)
結果および考察
この分析法を使用して、分析を 5 回行いました。
図 2 に、キャリブレーション試薬 1(25 ng/mL シクロスポリンおよび 1 ng/mL エベロリムス、シロリムス、タクロリムス)のクロマトグラムの例を示します。
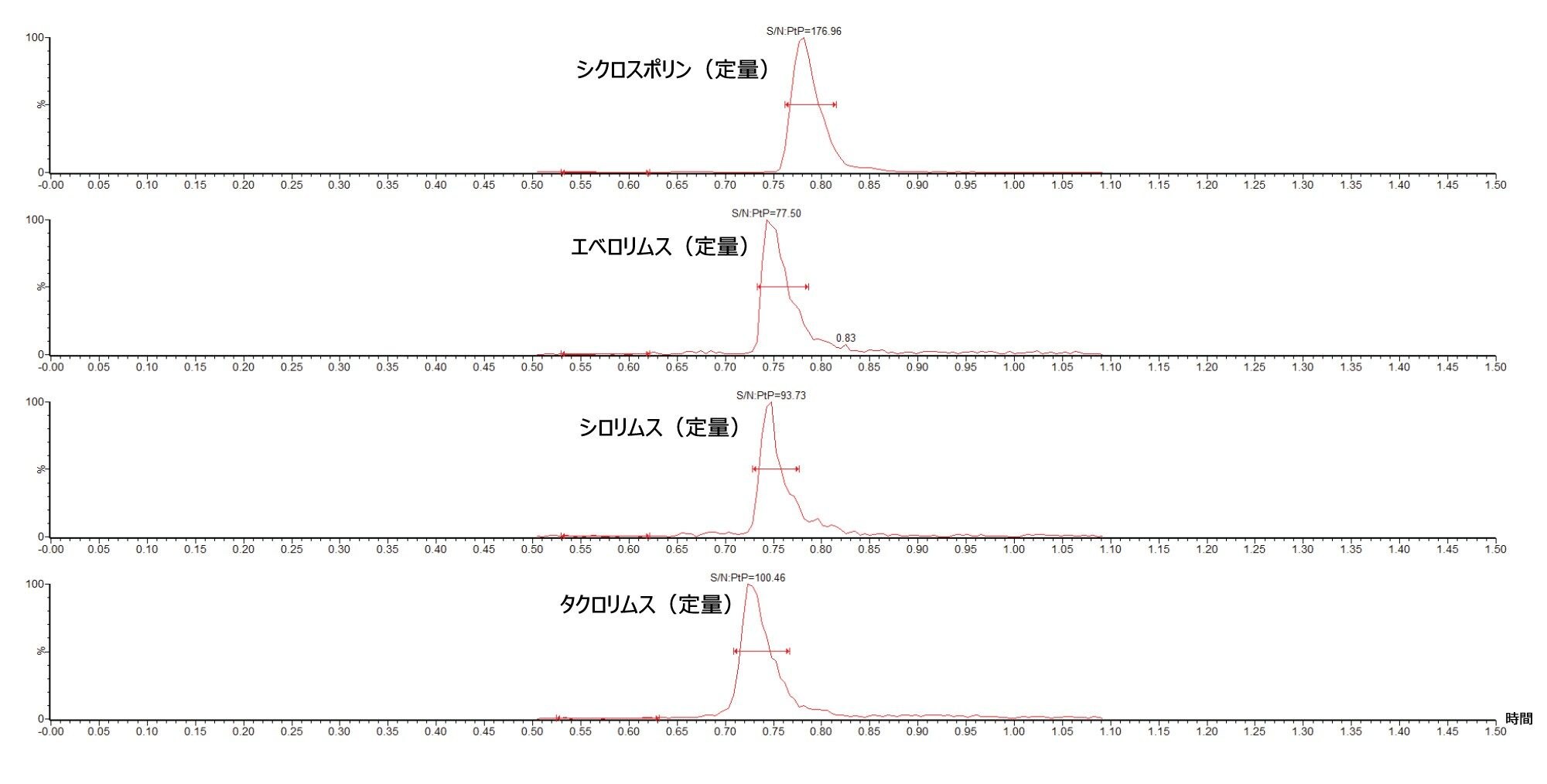
最低量のキャリブレーション試薬での分析感度は、5 回の分析にわたって S/N 比(PtP)が 10:1 を超えることが実証されました(表 4)。
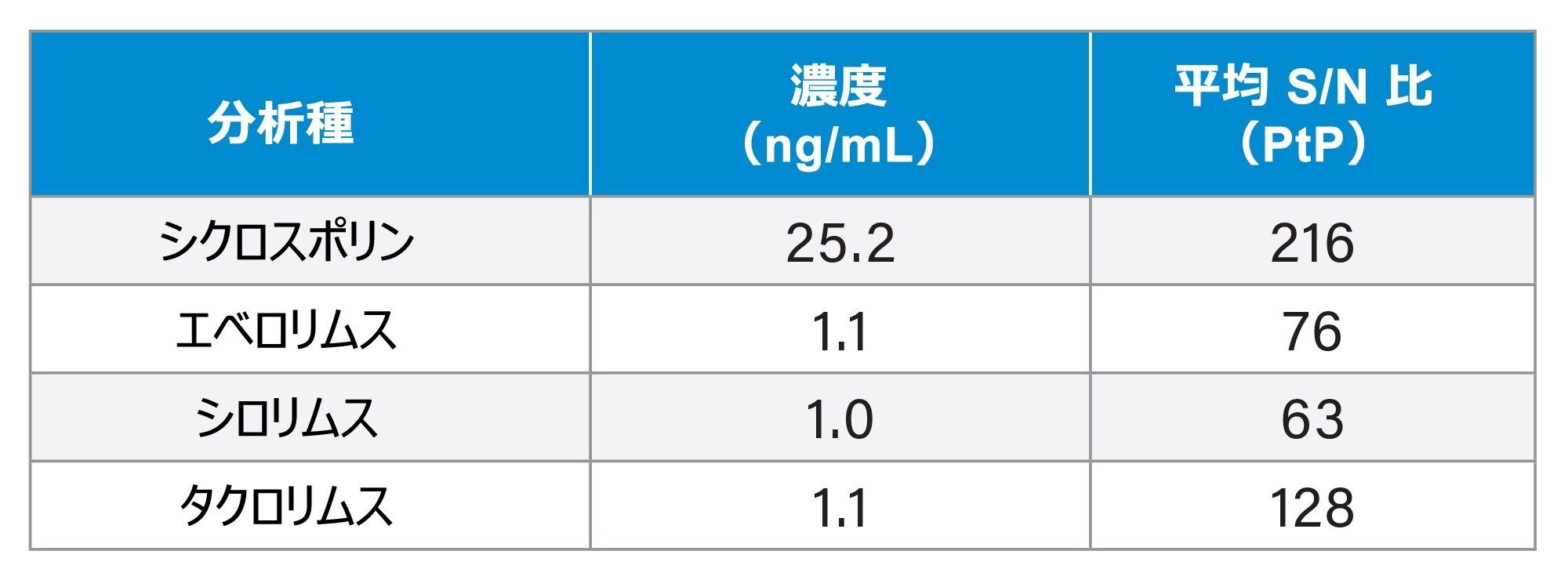
シクロスポリン、エベロリムス、シロリムス、タクロリムスのブランクサンプルと共にキャリブレーション試薬 6 サンプルを分析した後の各分析で、システムキャリーオーバーは見られませんでした。
各免疫抑制剤について、5 回の分析にわたって検量線は直線性を示し、それぞれのキャリブレーション範囲にわたって r2≥0.99 でした(表 1)。
合計精度は、連続しない 5 日間にわたって 3 濃度の全血プールを 5 回繰り返しで抽出・定量することによって測定しました(n = 25)。例外的に、シクロスポリンの試験は 4 日間で行いました(n=20)。各レベルで QC 試料を 5 回繰り返し分析することによって併行精度を評価しました。図 3 にこれらの実験の結果を示します。評価した 3 濃度での合計精度と併行精度は ≤7.6% RSD でした。
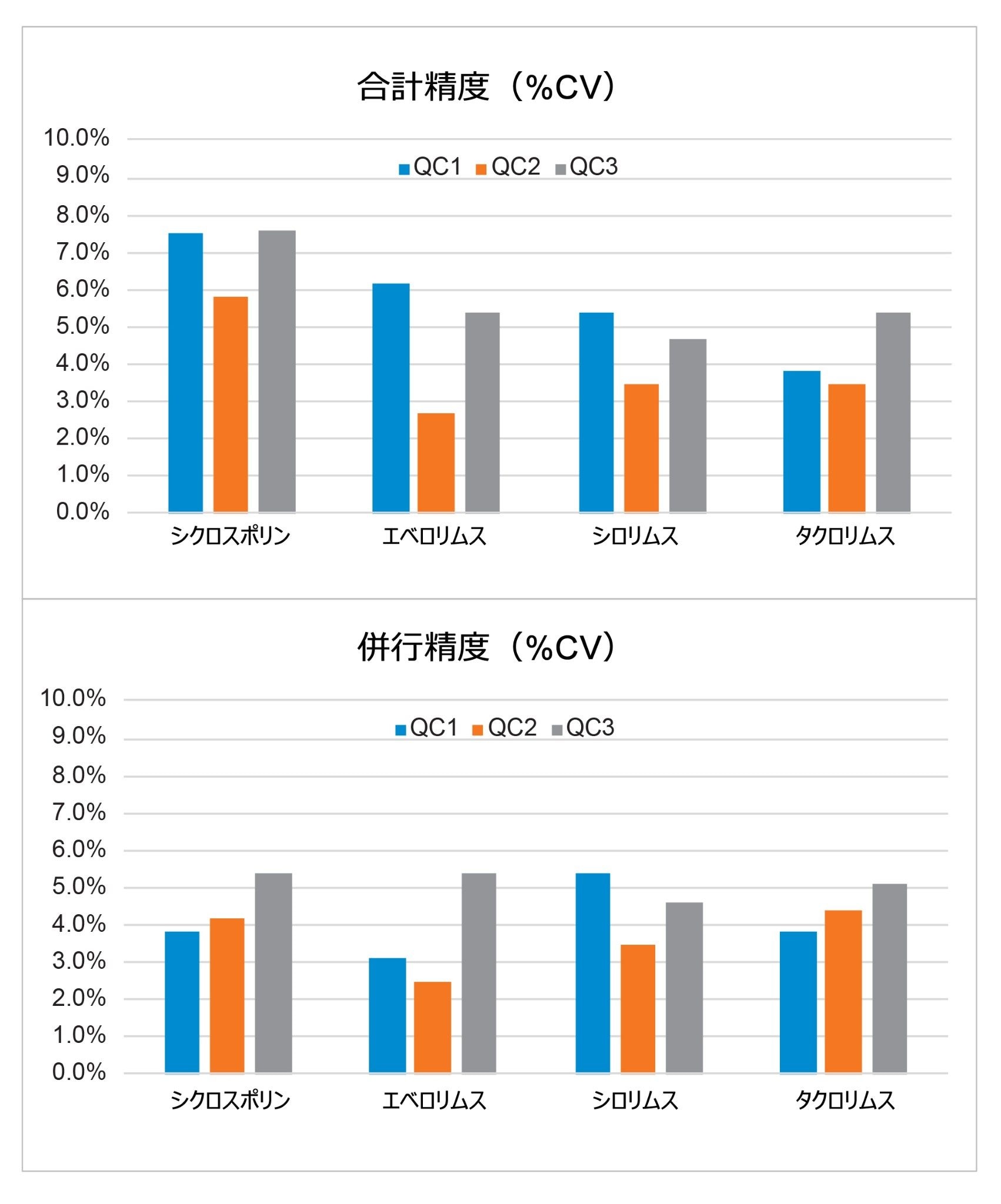
分析法の正確性を評価するため、LGC(英国、ベリー)全血外部品質保証サンプルを調達して分析しました。サマリーは表 5 に示されています。
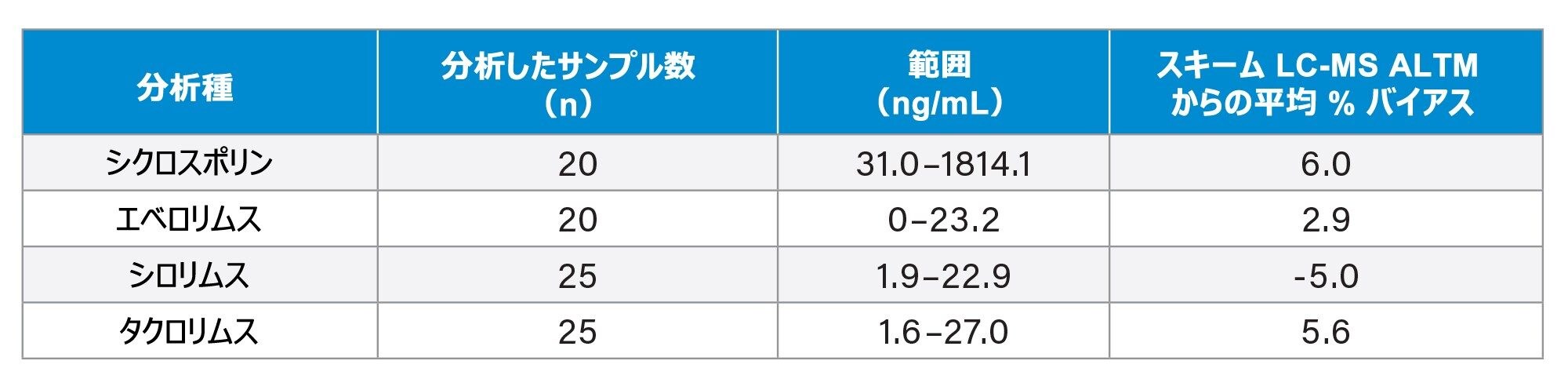
結論
非常に少量の全血と乾燥血液スポットを生成するための Capitainer B デバイスを使用して、免疫抑制薬であるシクロスポリン、エベロリムス、シロリムス、タクロリムスの同時分析が、注入間の間隔が 2 分あまりの 1 回の分析で行えました。
この分析法の性能特性は、試験したすべての分析種および濃度にわたって、良好な分析感度、合計精度、併行精度(≤7.6% RSD)を示しています。
最後に、外部品質保証サンプルの分析で良好な一致が得られ、この分析法の正確性について高い信頼性が示されました。
謝辞
本試験のために、Capitainer B デバイスを提供していただいた Capitainer 社に感謝いたします。1Deprez S, Van Uytfanghe K and Stove CP.Liquid chromatography-tandem mass spectrometry for therapeutic drug monitoring of immunosuppressants and creatinine from a single dried blood spot using the Capitainer qDBS device.Analytica Chimica Acta. 1242 (2023) 340797.
720007893JA、2023 年 3 月