カラムの再現性の検討:製造時期が互いに離れている 3 つのバッチの 1.8 µm HSS T3 固定相を用いたヒト尿中の内因性カフェインおよび代謝物の分析
要約
液体クロマトグラフィー質量分析(LC-MS)システムおよびタンデム質量分析計(LC-MS/MS)を搭載した液体クロマトグラフィー装置を使用する尿検査は、臨床およびメタボロミクス市場において一般的な試験です1-3。 分析種の所定のグループに対して開発された単一のアッセイを何千ものサンプルに実行して、患者の健康、薬物の開発、創薬に関連する結果を得ることができます。そのためには、分析条件およびクロマトグラフィーカラムの信頼性が最も重要になります。分析法開発中にカラムの再現性を試験することにより、開発された分析法が必要な期間適用できることが確実になります。尿中のカフェイン代謝物の LC-MS/MS 分析を実施し、5 年間の期間にわたる 3 つのバッチで同等な結果が得られたことから、HSS T3 固定相は信頼性が高いことが示されました。
アプリケーションのメリット
- 製造時期が互いに離れている 3 つのバッチの HSS T3 充塡剤において、バッチ間性能が同等
- 固相抽出を使用し、直接希釈注入法と比較した場合のシグナルおよび検出の改善
はじめに
特に高品質の LC 固定相とカラムを使用することで、アッセイで生成されたデータが、時間が経過しても正確で再現性があることが保証されます。LC 固定相の品質は、特定のアッセイについてのバッチ間再現性試験によって測定できます。これにより、製造された各ロットの充塡剤が同等に機能することが保証されます。ほとんどのバッチ間試験は、分析法バリデーションキット内の充塡剤など、特定の時期に製造された 3 バッチの充塡剤を使用して行われます。これらのキットは正しく機能しますが、それらを使用して得られるのは、製品の全体的な品質のスナップショットのみである可能性があります。全体像を把握するには、製造時期が互いに離れているバッチをテストする必要があり、これによって製品全体の品質の範囲が改善します。
ACQUITY™ HSS T3 固定相は、全多孔性シリカ粒子を使用した一般的に使用される C18 結合相です。この相は、リガンドの密度を下げた固定相によって、疎水性化合物の分離に悪影響を及ぼすことなく、従来の C18 よりも極性分析種が保持されるように設計されています。リガンドの密度が低いことにより、ベースパーティクルとの相互作用が増加する一方、100% 水系移動相に適合します。この相は、多くのアプリケーションや論文で、剤形中の低分子医薬品からバイオ分析アプリケーションに至るまで、様々な分離に使用されています4–6。HSS T3 充塡剤の品質を実証するために、3 本のカラムに異なるバッチの充塡剤を使用しました。これらの充塡剤は、2016 年から 2021 年までの 5 年間に製造されたものです。次に、固相抽出(SPE)および直接希釈注入サンプル前処理をしてから、3 本のカラムすべてを使用して、ヒト尿中の内因性カフェインおよび代謝物を分離しました。
実験方法
サンプルの説明
直接希釈注入実験において、ヒト尿を注入前に水で 1:1 に希釈しました。SPE の場合、サンプルを Oasis™ HLB 1 cc 30 mg カートリッジ(製品番号:WAT094225)にロードし、1 mL の水で 2 回洗浄してから、0.5 mL の 100% アセトニトリルで 2 回溶出しました。この溶出物を 60 ℃ の窒素下で蒸発乾固し、100 µL の Milli-Q 水で再溶解して分析に用いました。
分析条件
|
LC 条件 |
|
|
LC システム: |
ACQUITY UPLC™ I-Class Plus(バイナリーソルベントマネージャー(BSM)、サンプルマネージャーフロースルーニードル(SM-FTN)、PDA 検出器を搭載) |
|
検出: |
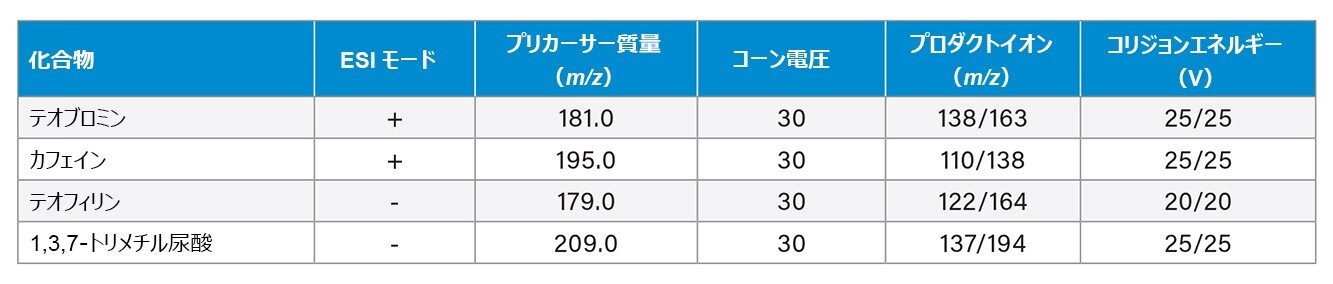
カフェイン代謝物の MRM(表 1 に概説) |
|
カラム: |
ACQUITY UPLC HSS T3、1.8 µm、2.1 × 50 mm(製品番号 186009467) 3 バッチの充塡剤: 188 – 2016 年 10 月に製造 233 – 2019 年 11 月に製造 270 – 2021 年 11 月に製造 |
|
カラム温度: |
30 ℃ |
|
サンプル温度: |
10 ℃ |
|
注入量: |
5.0 µL |
|
流速: |
0.6 mL/分 |
|
移動相 A: |
0.1% ギ酸含有 Milli-Q 水 |
|
移動相 B: |
0.1% ギ酸アセトニトリル溶液 |
|
グラジエントプロファイル: |
2% ~ 25% B を 2.5 分で、25% B を 0.5 分間ホールド |
MS 条件
|
MS システム: |
Xevo™ TQ-S micro |
|
イオン化モード: |
ESI+、ESI- |
|
取り込み範囲: |
MRM の概要を表 1 に示します |
|
キャピラリー電圧: |
3.0 kV |
|
コーン電圧: |
分析種によって異なる(表 1) |
|
脱溶媒温度: |
500 ℃ |
|
脱溶媒流量: |
500 L/時間 |
|
コーンガス流量: |
10 L/時間 |
データ管理
|
クロマトグラフィーソフトウェア: |
MassLynx™ V4.1 |
結果および考察
カラム間再現性試験の前に、2 つの異なるサンプル前処理手法を評価しました。通常の直接希釈注入法は、尿の分析で一般的に使用されています。その理由は、リン脂質などの内因性化合物が存在する可能性が低いからです。尿には、分析種の保持に影響する高濃度の塩が含まれている可能性があるため、サンプルのさらなる希釈が必要になります。これを、より多くの場合リン脂質を取り除くために血漿および血清のマトリックスに使用される SPE と比較しました。SPE では、サンプル中の分析種が濃縮される場合があります。尿中の一部の分析種は極端に低い濃度で検出されることがあるため、この濃縮効果は、尿の分析に有効な場合があります。図 1 には、SPE および直接希釈注入サンプル前処理を使用して、MS/MS によって検出した分析種の重ね描きが示されています。
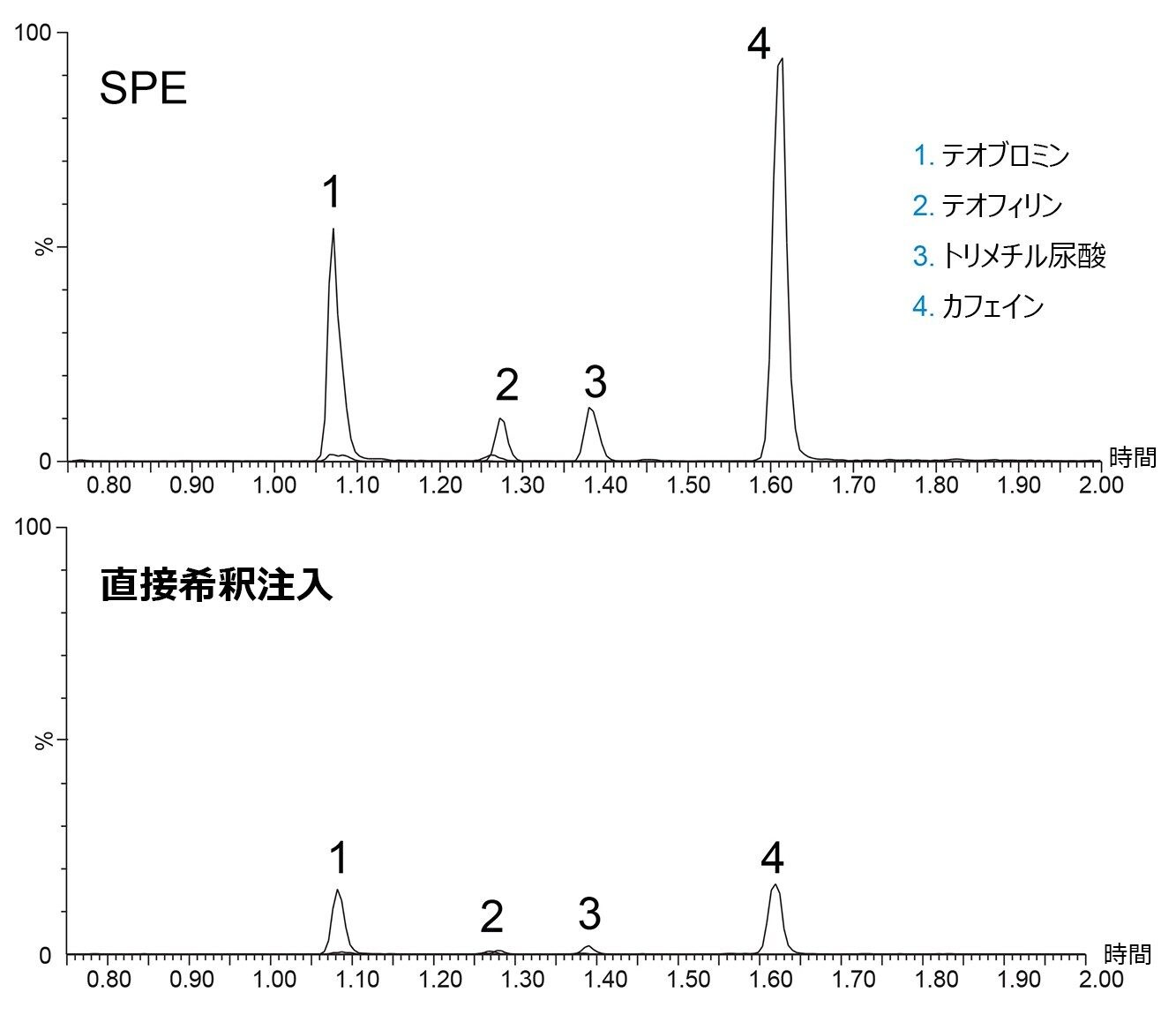
4 種類の分析種の強度は、希釈と比較して SPE で大幅に高くなっています。強度の改善は、SPE の濃縮効果、あるいはより清浄なサンプルによるイオン化効率の改善によると考えられます。より高いシグナルの達成により、検出および定量のより低い下限値が達成でき、分析法がより広いダイナミックレンジで適用できるようになります。このため、バッチ間評価に SPE を使用しました。
3 つの異なるバッチの ACQUITY UPLC HSS T3 吸着剤をステンレススチール製ハードウェアに充塡し、ヒト尿からのカフェインおよびその主要代謝物の分析に使用しました。カラムに充塡するために使用した材料のバッチは 5 年の期間にわたって製造されており、ウォーターズのすべての製品に適用される厳格な品質管理プロトコルにすべて適合しています。図 2 には、3 本の HSS T3 カラムすべてで得られた、カフェインおよびその主要な 3 種類の代謝物であるテオブロミン、テオフィリン、1, 3, 7-トリメチル尿酸のクロマトグラムが示されています。
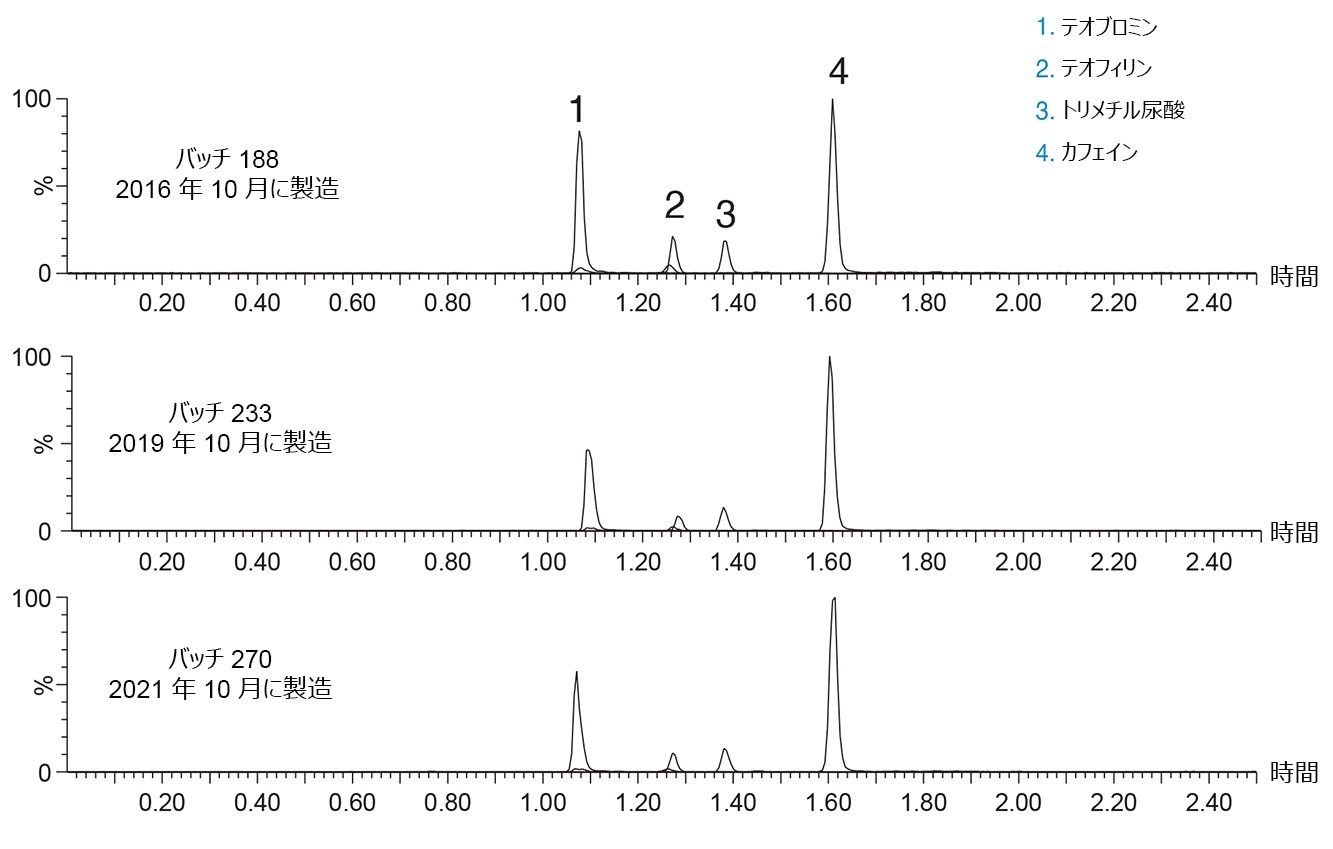
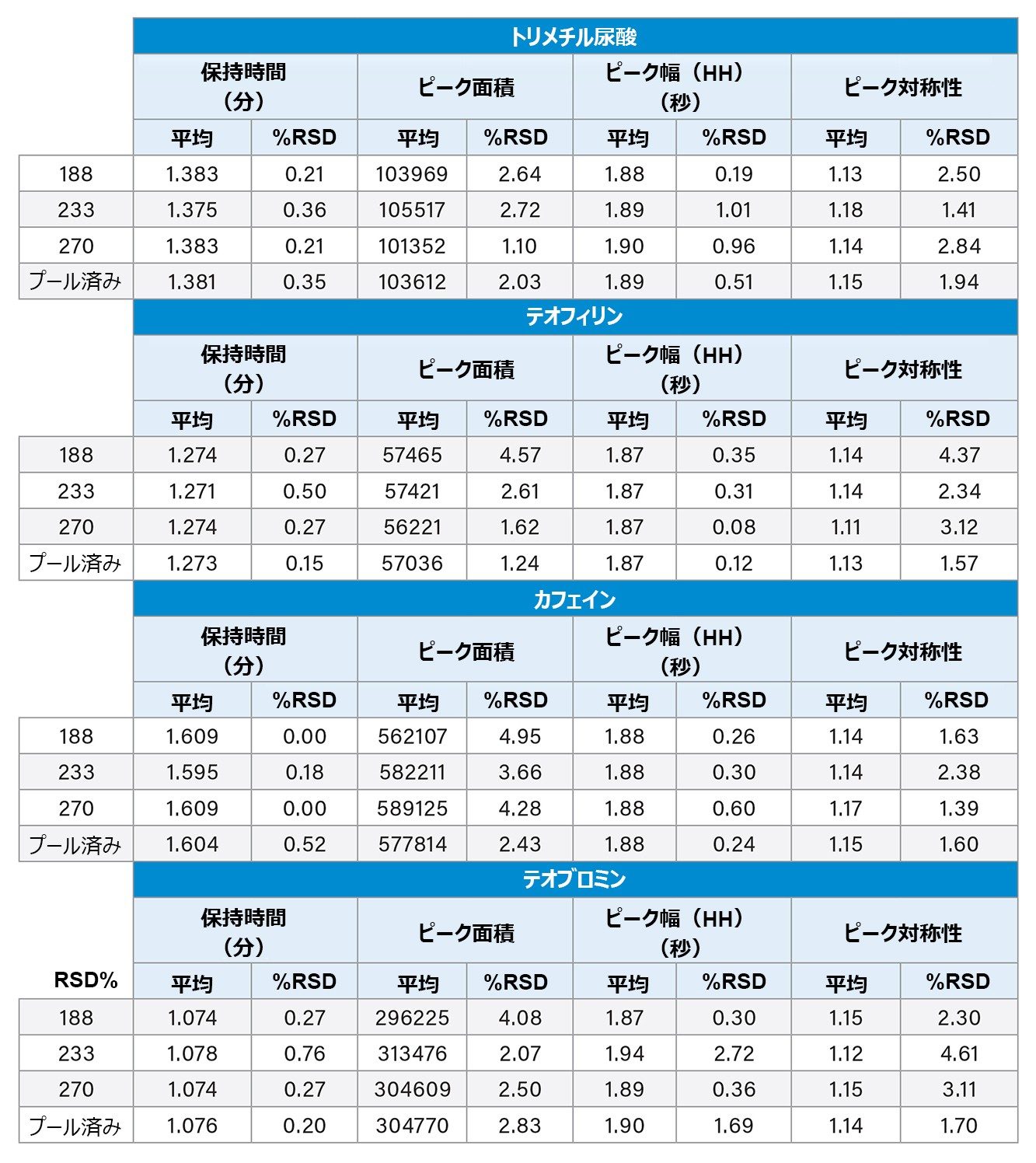
3 本のカラムは 4 種類の分析種すべてに対して、同等の保持力と選択性を示しています。ピーク面積、ピーク対称性、ピーク幅などのパラメーターにより、3 本のカラムすべてにわたって再現性のある結果が示されています。表 2 に示されているように、ピーク保持時間、ピーク面積、ピークの半値幅、ピークの対称性は、所定のカラムおよびプールされているデータセットに対してすべて 5% 未満です。
結論
ウォーターズの粒子およびカラム製造プロセスでの品質を実証するため、5 年間にわたって製造された 3 バッチの ACQUITY HSS T3 固定相を使用して、ヒト尿中の内因性カフェインおよび代謝物を分離しました。希釈によって十分な結果が得られなかったため、再現性試験用のサンプル前処理すべてに SPE を使用しました。
これら 3 つのバッチでは、再現性のあるクロマトグラフィー性能が示されました。保持時間の %RSD 値は、各カラムおよびプールしたデータセット(n = 9)について 1% 未満でした。また、ピーク面積、ピーク幅、ピーク対称性の %RSD は、検出した分析種について 5% 未満でした。これらの結果からは、充塡剤が 5 年離れて製造されていても、同じ品質のデータが得られることを示しています。同様のデータが何年にもわたって得られるというこのレベルの保証は、新しい分析法を開発する際に非常に重要です。選択した固定相がロット間でも経年でも同等であることが分かっていることで、追加の再バリデーションの必要なくアッセイの使用期間を延ばすことができます。
参考文献
- Wong GF、Lee WM、Li CK.Qualitative Screening of Amphetamine- and Ketamine-type Abuse Drugs in Urine Employing Dual Mode Extraction Column by Liquid Chromatography-Tandem Mass Spectrometry (LC-MS/MS).Journal of Analytical Toxicology.(2022).
- Peng KW、Klotz A、Guven A, Gray K、Friss T、et.al. Multiplexed LC-MS/MS Analysis of Methylsuccinic Acid, Ethylmalonic Acid, and Glutaric Acid in Plasma and Urine. Analytical Biochemistry. (2022).
- Jacyna J、Kordalewska M、Artymowicz M、Markuszewski M、Matuszewski M、Markuszewski M、Pre- and Post-Resection Urine Metabolic Profiles of Bladder Cancer Patients: Results of Preliminary Studies on Time Series Metabolomics Analysis.Cancers.(2022) 1210.
- Evaluation of BEH C18, BEH HILIC and HSS T3 (C18) Column Chemistries for the UPLC-MS/MS Analysis of Glutathione, Glutathione Disulfide, and Ophthalmic Acid in Mouse Liver and Human Plasma.Journal of Chromatographic Science.(2008).209–214.
- Mohamed, M. Stability Indicating New RP-UPLC Method for Simultaneous Determination of a Quaternary Mixture of Paracetamol, Pseudoephedrine, Chlorpheniramine, and Sodium Benzoate in (Cold-Flu) Syrup Dosage Form.Journal of AOAC International.(2022).
- Sottani C, Grignani E, Cottica D, et.al. Development and Validation of a Bioanalytical UHPLC-MS/MS Method Applied to Murine Liver Tissue for the Determination of Indocyanine Green Loaded in H-Ferritin Nanoparticles. Frontiers in Chemistry 2022.
- Thorn C、Aklillu E、McDonagh E、Klein T、Altman R、PharmGKB summary: Caffeine Pathway.Pharmacogenet Genomics.(2012) 389–395.
- Caffeine and Caffeine Metabolites – Urine Lab Procedure.Method UHPLC-ESI-MS/MS.Method number 4063.08. https://wwwn.cdc.gov/nchs/data/nhanes/2011-2012/labmethods/CAFE_G_MET.pdf Access 14-March-2022.
720007605JA、2022 年 4 月