
反応モニタリングは、新薬候補の合成における極めて重要なステップです。さまざまな溶媒や触媒など、多様な異なる条件下での化学反応の進行を評価するには、複数の分析が必要な場合があります。
反応モニタリングのためのサンプル分析の処理時間を短くすることより、迅速な意思決定とラボの効率向上が可能になります。
創薬化学の目標は、医薬品開発プロセスを正常に進め、最終的に医薬品となるリード分子を設計・合成することです。SAR 最適化プロセスでは、数百もの化合物が合成されるため、多数の反応が行われます。化学者にとって、情報に基づいてタイムリーに意思決定を行えるようにするためには、これらの反応について把握できていることが非常に重要です。起きていることをリアルタイムで知ることで、化学者がプロセス容器内の反応を設計および制御するのに役立ちます。つまり、製品の収率と純度を高め、副反応や副生成物を減らすことで、予期しないプロセスに伴うコストとリスクを削減することができます1。
Waters は最近、サンプル前処理がほぼ不要で、固体および液体サンプルを直接分析するための専用のノミナル質量検出器である RADIAN ASAP(Rapid Direct Analysis Atmospheric Pressure Solid Analysis Probe、高速直接分析大気圧固体分析プローブ)を発表しました。
RADIAN ASAP では、サンプルは反応容器から直接採取され、サンプル前処理をほとんど必要とせずに質量検出器に導入できるため、ほぼ瞬時に結果が得られて、反応の進行に対する判断を迅速に行うことができます。
実績のある頑健なシングル四重極型検出器と、定評のある ASAP ダイレクトサンプル分析2 を組み合わせることで、創薬化学者の分析の専門知識の有無を問わず、薬物合成反応時にノミナル質量データに迅速にアクセスできるようになります。
本研究では、β 遮断薬アテノロールの合成の反応モニタリングワークフローにおける直接分析のための迅速なスクリーニングワークフローについて説明します。
中間体 4- ヒドロキシフェニルアセタミド(4-HPA)からアテノロールへの変換をシミュレーションするために、サンプル前処理を行いました。
RADIAN ASAP では両方の分析種が正常に検出され、アテノロール(m/z 267 Da)のレスポンスの増加に伴い、4-HPA(m/z 152 Da)が減少することが示されました(図 1)。
アテノロールと(4-HPA)のサンプルを前処理し、5 タイムポイントにわたってアテノロール合成の進行をシミュレーションしました。
結果の再現性を実証するために、各「タイムポイント」で 5 サンプルを分析し、各分析種の個々のレスポンスの %RSD(相対標準偏差)と、反応の進行を反映するアテノロール:4-HPA 比を評価しました。
すべての標準品は、Sigma Aldrich chemicals(Poole、Dorset、英国)から調達しました。
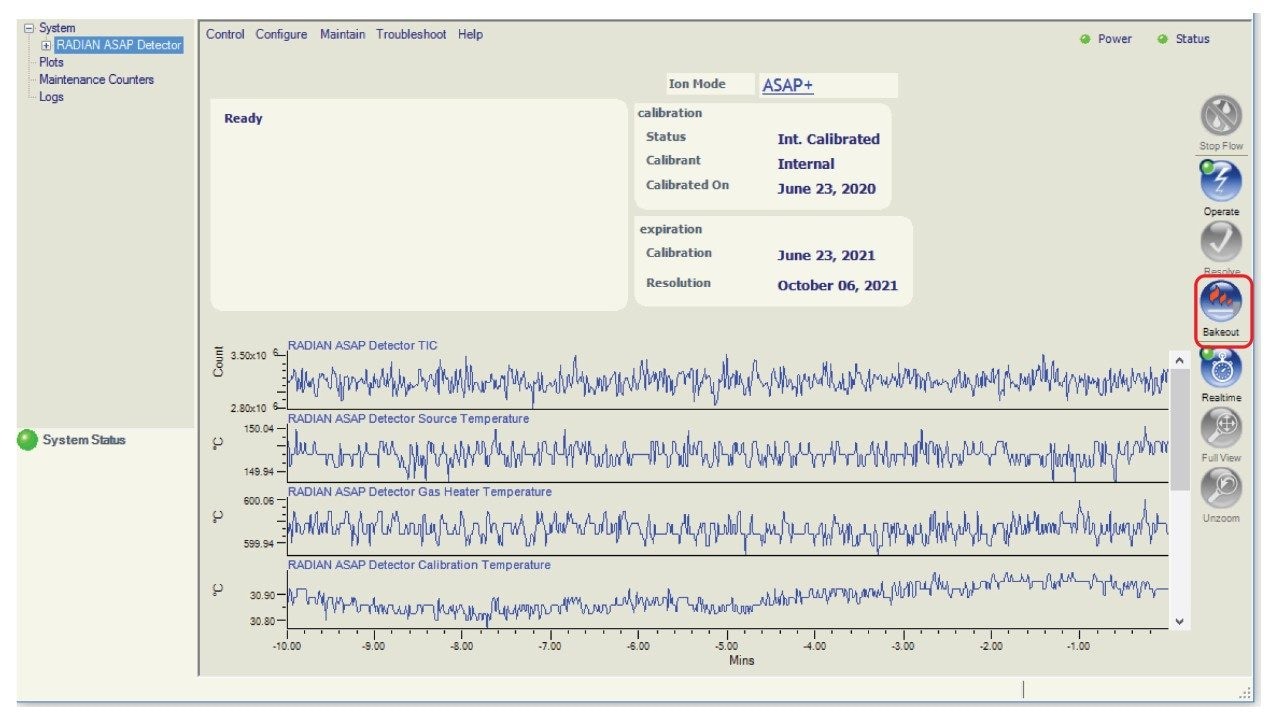
各回の繰り返しについて、ガラスキャピラリーを取り、サンプリングの前に RADIAN ASAP に挿入し、MassLynx の「ベークアウト」機能を用いてクリーニングしました(図 2)。このオプションを選択すると、フローガス温度が自動的に 600 °C に上昇して 1 分間保持され、サンプル結果に干渉する可能性のある汚染物質が除去されます。このプロセスが完了すると、サンプル分析の準備ができたことをシステムがユーザーに通知します。
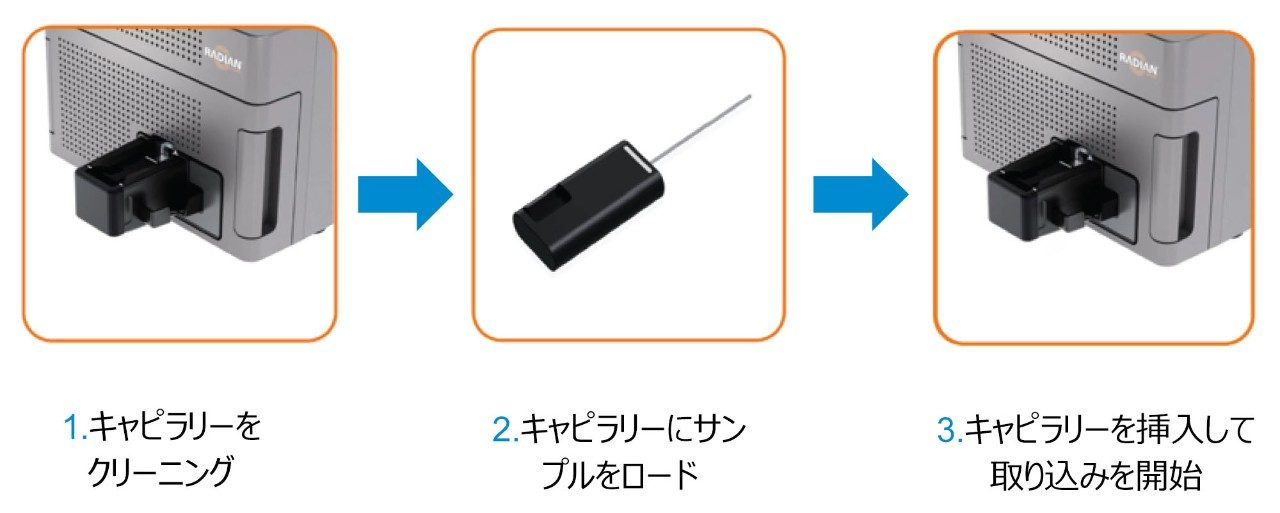
ベークアウト手順が完了したら、ガラスロッドを取り外し、約 10 秒間冷ましてから、最初のサンプルに浸し、RADIAN ASAP(図 3)に導入した後、取り外します。上記のベークアウト手順に従って、各サンプルに異なるガラスキャピラリーを使用して、この手順をサンプルごとに各 5 回行いました。
|
イオン化モード: |
ASAP+ |
|
コロナピン: |
3 µA |
|
脱溶媒ガス(N2)温度: |
500 ℃ |
|
脱溶媒ガス(N2)流量: |
3 mL/分 |
|
サンプルコーン電圧: |
10V |
|
測定モード: |
フルスキャン(連続) |
|
質量範囲: |
100 ~ 600 Da |
|
スキャン速度: |
2 Hz |
|
サンプリング方法: |
キャピラリー浸漬 |
|
MS ソフトウェア: |
MassLynx4.1 |
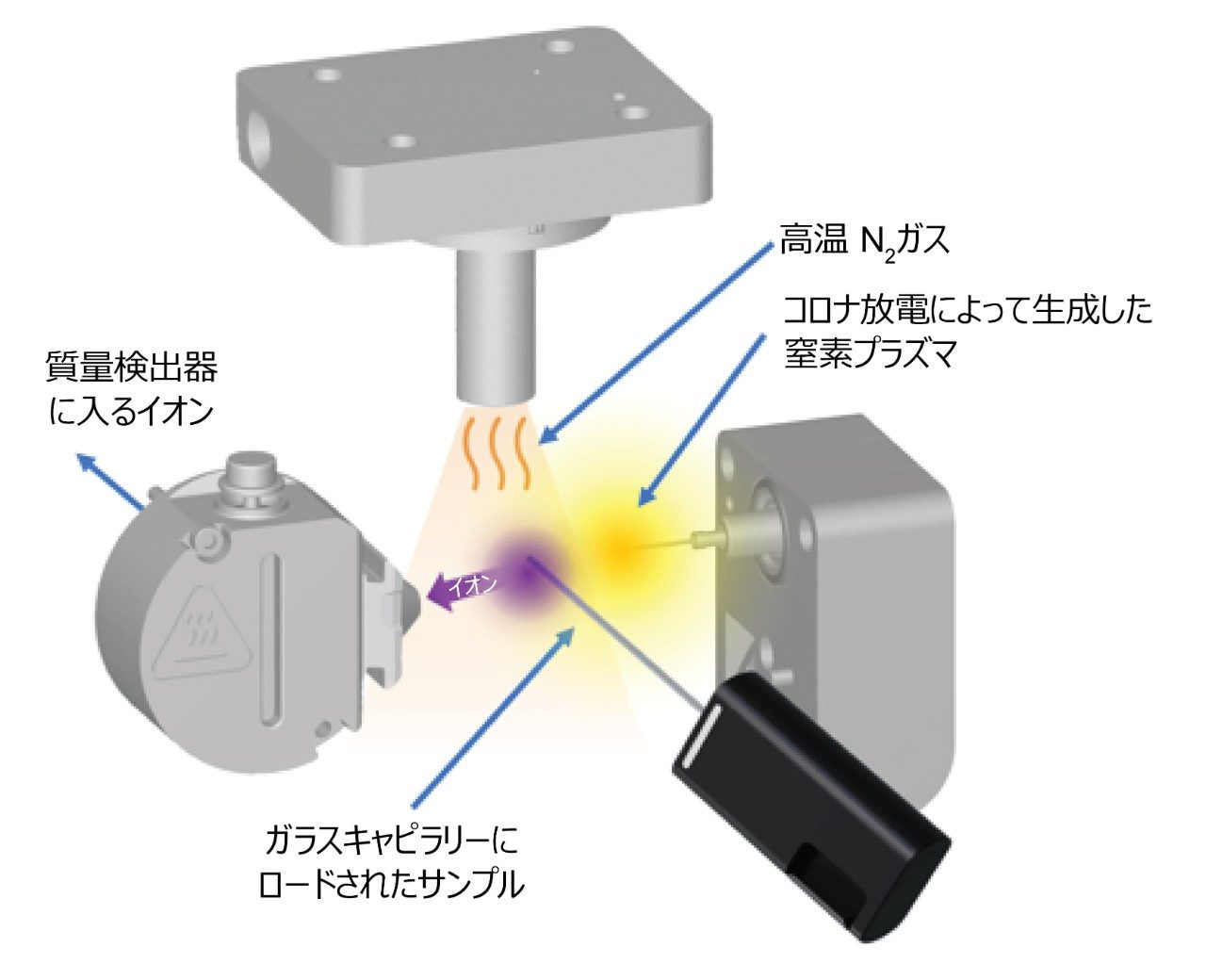
RADIAN ASAP(図 4)を用いてサンプルをイオン化するには、ガラスロッドのコロナ放電領域にサンプルを導入します。加熱窒素流を用いてサンプルを揮発させます。気化した分析種を N2 プラズマによってイオン化します。気化した分析種イオンを装置内に誘導し、シングル四重極質量検出器で分析します。
1973 年の Horning ら3 の論文に記載されているように、APCI のイオン化には 2 つの主要なメカニズムがあります。
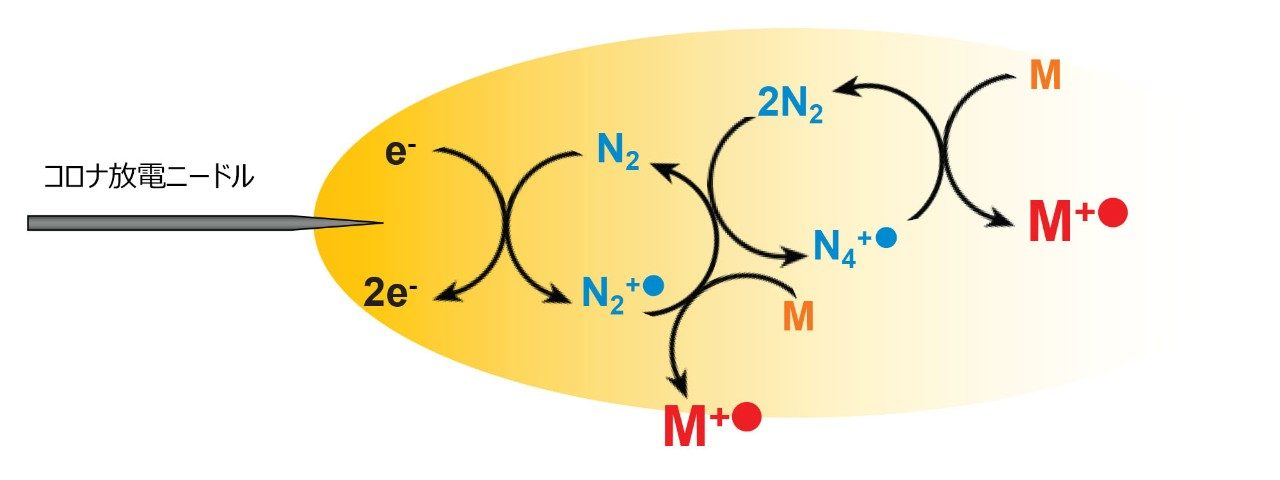
1 つ目は、イオンソース内の窒素のコロナ放電イオン化によって開始される電荷トランスファーメカニズムです(図 5)。これにより、窒素のラジカルカチオンが生成され、分析種分子との間で電荷移動が起こって分析種分子のラジカルカチオンが生成されます。
この形のイオン化は、非極性化合物の分析に特に有用で、プロトン性溶媒が存在しないイオン源条件でより広く使用されます。
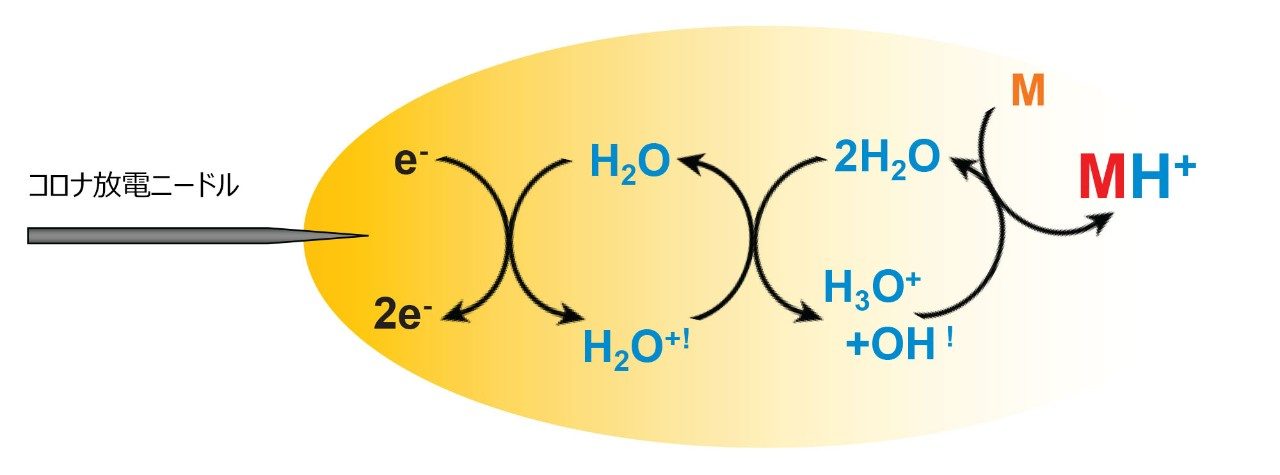
イオン化の 2 つ目のメカニズムは、プロトン移動です(図 6)。
これには、図に示すように、プロトンのソースとして働いてイオン化溶媒クラスターを形成する水やその他の溶媒(メタノールなど)の存在が必要です。
次に、プロトン移動によって分析種のイオン化が起こり、これが LC-MS の APCI に関わる主なイオン化経路になります。
この実験では、すべてのサンプルがメタノールに溶解しているため、後者のメカニズムが該当します。
装置は、「装置条件」の記載に従って設定しました。サンプルは、「実験方法」の記載に従って RADIAN ASAP に導入し、イオン強度および比は、MassLynx ソフトウェアから直接評価しました。
本番では、高速反応モニタリングのサンプルを単回採取して、反応の進行状況を迅速に評価しますが、ここでは結果の再現性を示すために、各サンプルを n=5 で採取しました。
サンプルを導入し、TIC(トータルイオンカウント)を取り込みました。TIC の例を図 7 に示します。
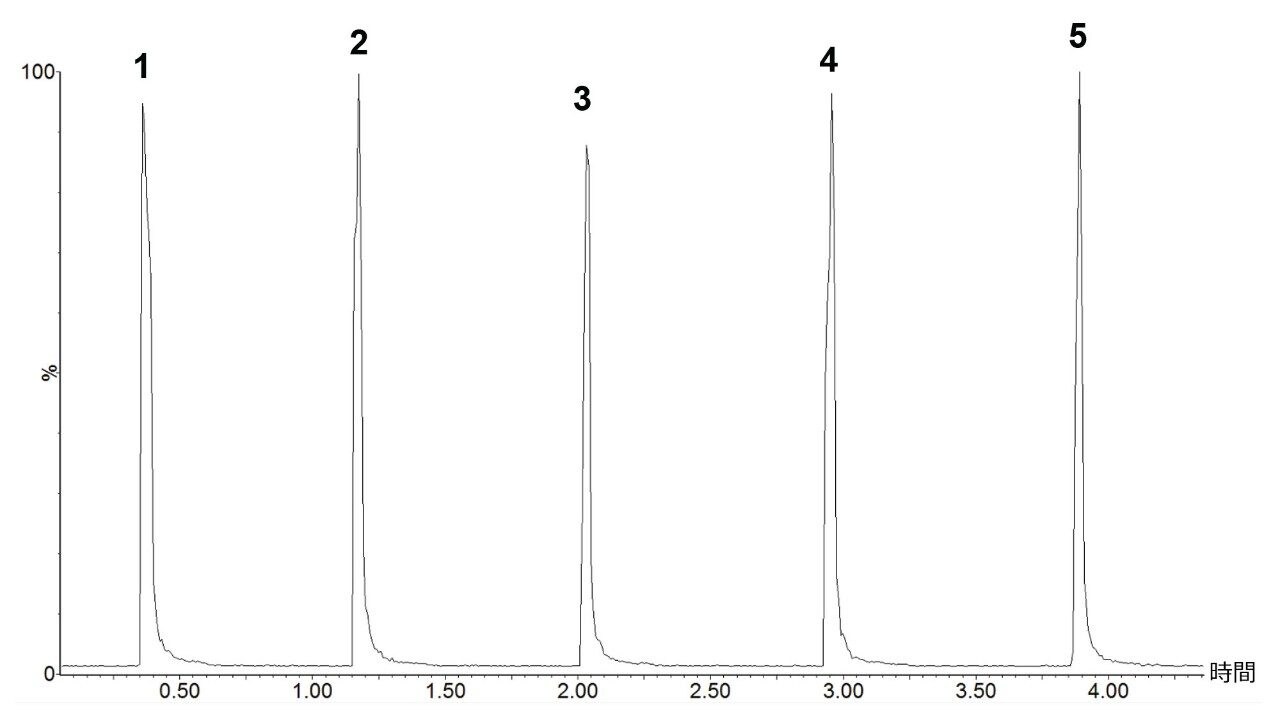
シミュレーションした各タイムポイントについて TIC から抽出したスペクトルは、サンプル内の各化合物の相対濃度を反映して、4-HPA(m/z 152Da)の減少とアテノロール(m/z 267Da)の増加を明確に示しています(図 8)。4-HPA のフラグメント候補(m/z 107Da)とダイマー(m/z 303Da)が観察されました。前者はソース内フラグメンテーションの結果であり、後者は高濃度の 4-HPA に関連するソース内反応の結果です。
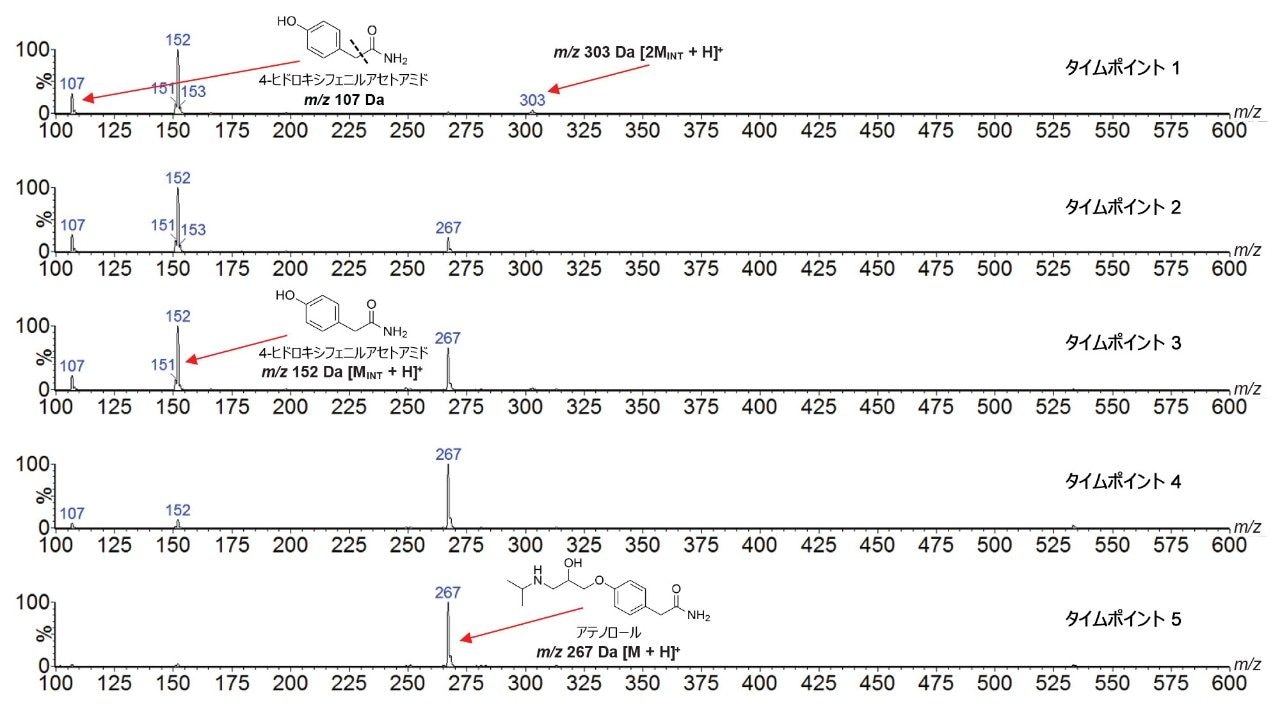
ASAP を用いる半定量分析は、以前は内部標準を用いて行われていました4,5。 反応モニタリングは反応物質と生成物の相関関係によって定義されるため、時間とともに変化する対象化合物間の比率を測定することで、半定量的モニタリングを行うことができます。
平均レスポンスを、表示されている両分析種の平均レスポンス比とともにプロットしました(図 9)。これにより、各分析種の強度変化が視覚化され、赤の線で示すアテノロールの相対強度が明確な上昇傾向を示しています。
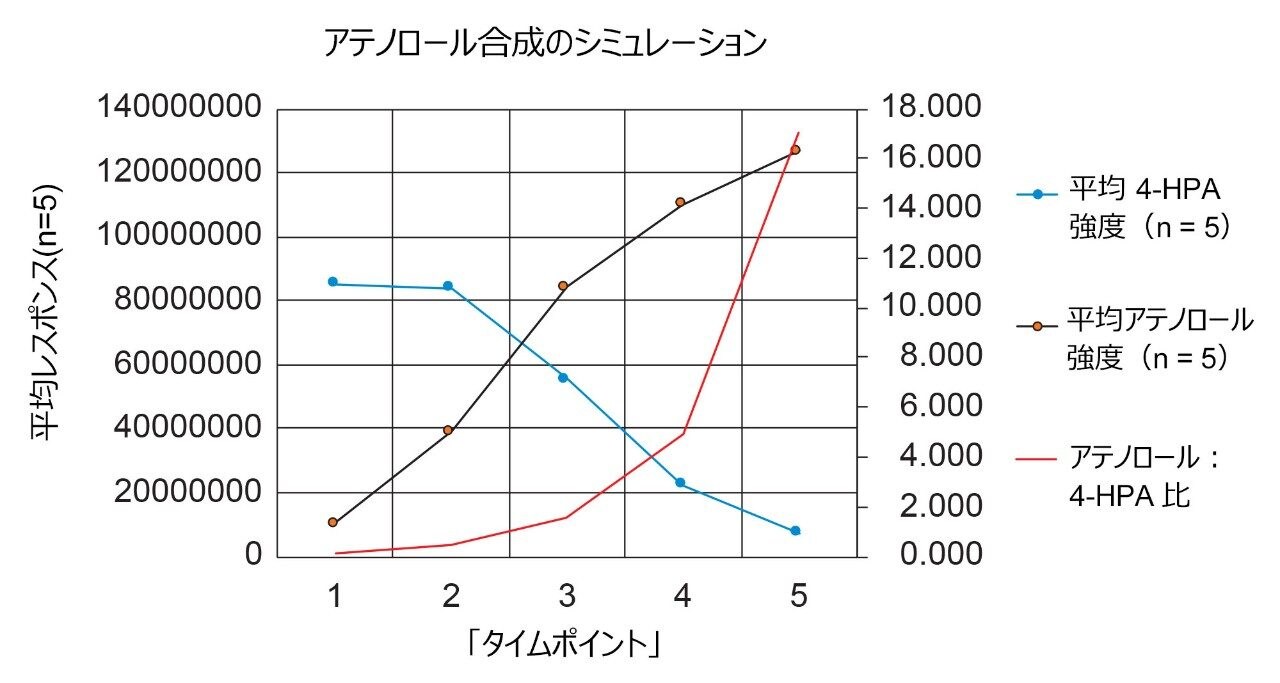
前述のように、サンプルは 5 回の繰り返しで測定することで、メソッドの再現性を保証しています。
ルーチンで実施する反応モニタリング法はすべて、結果の再現性を確保するために、バリデーションの要素の対象となります。
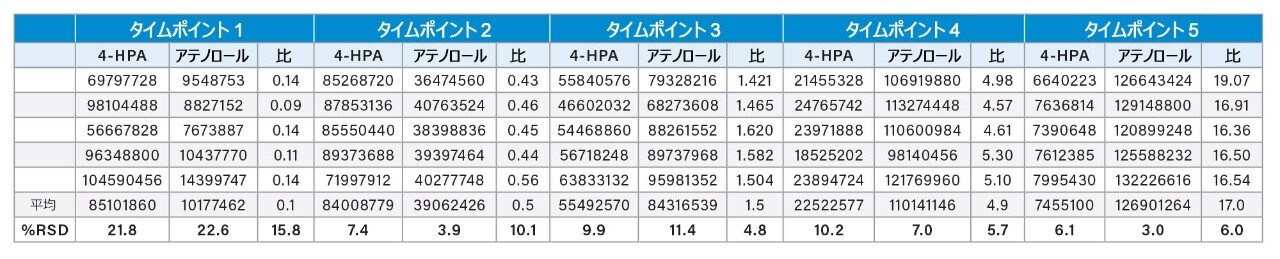
表 1 に、前処理したすべてのサンプル 5 回の繰り返しについての両方の分析種の個別の強度を示します。各サンプルの平均比の RSD は、4.8 ~ 15.8 です。
サンプルは手動で装置に導入され、クロマトグラフィー分離が不要であることを考えると、この数値は変動に関して非常に良好であることを示しています。
最低濃度のアテノロールで、%RSD 15.8% が認められました。これらの実験では、アテノロールは 4-HPA よりも高いイオン化強度を示しました。これが、低濃度でのより高い実験的ばらつきにつながった可能性があります。
RADIAN ASAP が、反応モニタリングのための貴重なツールとなる可能性があることが示されました。アテノロール合成の進行のシミュレーションを、クロマトグラフィー分離を必要とせずに迅速に行うことができるとともに、ほぼ瞬時に質量を確認できるノミナル質量データが得られました。
RADIAN ASAP は設置面積が小さく使いやすいため、ユーザーが熟練者でも初心者でも、さまざまな分析設定で導入することができます。
720007111JA、2021 年 1 月