
法中毒学目的のみに使用してください。
本研究は、法中毒学の臨床研究を支援するために、尿サンプルからの乱用薬物および疼痛管理薬物の正確かつ再現性のある定量を実現する、実用的で汎用性の高い SPE 戦略を提供することを目的としています。事前にバリデーション済みのメソッドを Hamilton Microlab STAR に移管し、これにより SPE の全手順に加えてすべてのサンプル前処理が実行されました。このような自動化戦略により、サンプル前処理のワークフローが簡素化および効率化され、生産性が最大限に高められ、人的ミスのリスクを低減するとともに、ピークの分析性能が保証されます。
液体クロマトグラフィーと質量分析計の組み合わせ(LC-MS/MS)は、1 回の取り込みで複数の化合物を迅速に分析するための一般的な手法です。ただし、装置分析は進歩しているにもかかわらず、サンプル前処理は、バイオ分析ワークフロー全体においてかなりの時間を要するステップであり、ミスの原因となる場合があります1。 LC-MS/MS バイオ分析の分析感度、選択性、頑健性の要件に基づくサンプル前処理手順には通常、単純な希釈、除タンパク(PPT)、液-液抽出(LLE)、保持型液-液抽出(SLE)、固相抽出(SPE)などがあります。これらのメソッドの開発、最適化、および導入は、特に大規模な分析種パネルでは時間がかかり、科学者間やラボ間の移管が困難になる場合があります。Hamilton Microlab STAR などの完全に自動化されたデバイスを採用し、サンプル前処理プロセスを効率化することで、分析者は他の作業に集中することができます。最も重要な点として、スパイクのミス、内部標準添加に関わるミス、試験者の非一貫性、サンプル移動時のミスなどの人的ミスを低減できる可能性が挙げられます2-5。 その結果、分析法の再現性と一貫性を向上できます。
本研究は、法中毒学の臨床研究を支援するために、尿サンプルからの乱用薬物および疼痛管理薬物の正確かつ再現性のある定量を実現する、実用的で汎用性の高い SPE 戦略を提供することを目的としています。事前にバリデーション済みのメソッドを Hamilton Microlab STAR に移管し、これにより SPE の全手順に加えてすべてのサンプル前処理が実行されました。6。 このような自動化戦略により、サンプル前処理のワークフローが簡素化および効率化され、生産性が最大限に高められ、人的ミスのリスクを低減するとともに、ピークの分析性能が保証されます。
すべての標準試料は、Cerilliant(Round Rock、TX)および Cayman Chemical (Ann Arbor、MI)から入手しました。混合原液は、分析種に応じて、2、10、25 μg/mL の濃度でメタノールで調製しました。安定同位体で標識した標準試料を、内部標準(IS)として使用しました。IS 原液は、1 μg/mL の濃度でメタノールで調製しました6。 原液をプールしたブランク尿中に希釈することで、サンプルを調製しました。
すべてのキャリブレーション標準試料および品質管理用サンプルは、プールしたブランク尿中にマニュアルで調製し、固相抽出を行いました。図 1 には、Hamilton Microlab STAR デッキのレイアウトと、この抽出プロセスに使用するアクセサリーを示しています。また、4 つの QC レベルの正確度と精度を比較するために、抽出プロセスもマニュアルで実行しました。前処理では、STAR リキッドハンドリング装置により加水分解バッファーに 100 μL の IS が添加された後、100 μL の尿が Oasis MCX μElution プレートの個々のウェルに添加され、吸引してサンプルが混合されます。インキュベーション後、STAR により 200 μL の 4% H3PO4 が添加され、吸引して混合されます。真空下で STAR のデッキの吸着床にサンプルをロードし、続いて 200 μL の 20% MeOH 水溶液で洗浄します。吸着剤は高真空下で乾燥します。サンプルは、2 x 25 μL の 5% 強アンモニア溶液 (28 ~ 30%) 含有 50:50 ACN:MeOH で溶出しました。すべてのサンプルを 150 μL の 97:2:1 H2O:ACN:ギ酸で希釈し、3 分間加熱シェーカーで混合してから LC-MS/MS に移して分析しました。ワークフロープロセスの詳細を図 2 に示しています。上記で詳しく説明した自動 SPE プロセス全体が、設定不要なスクリプトとして提供されており、Hamilton Microlab STAR または STARlet の構成に簡単に実装することができます。
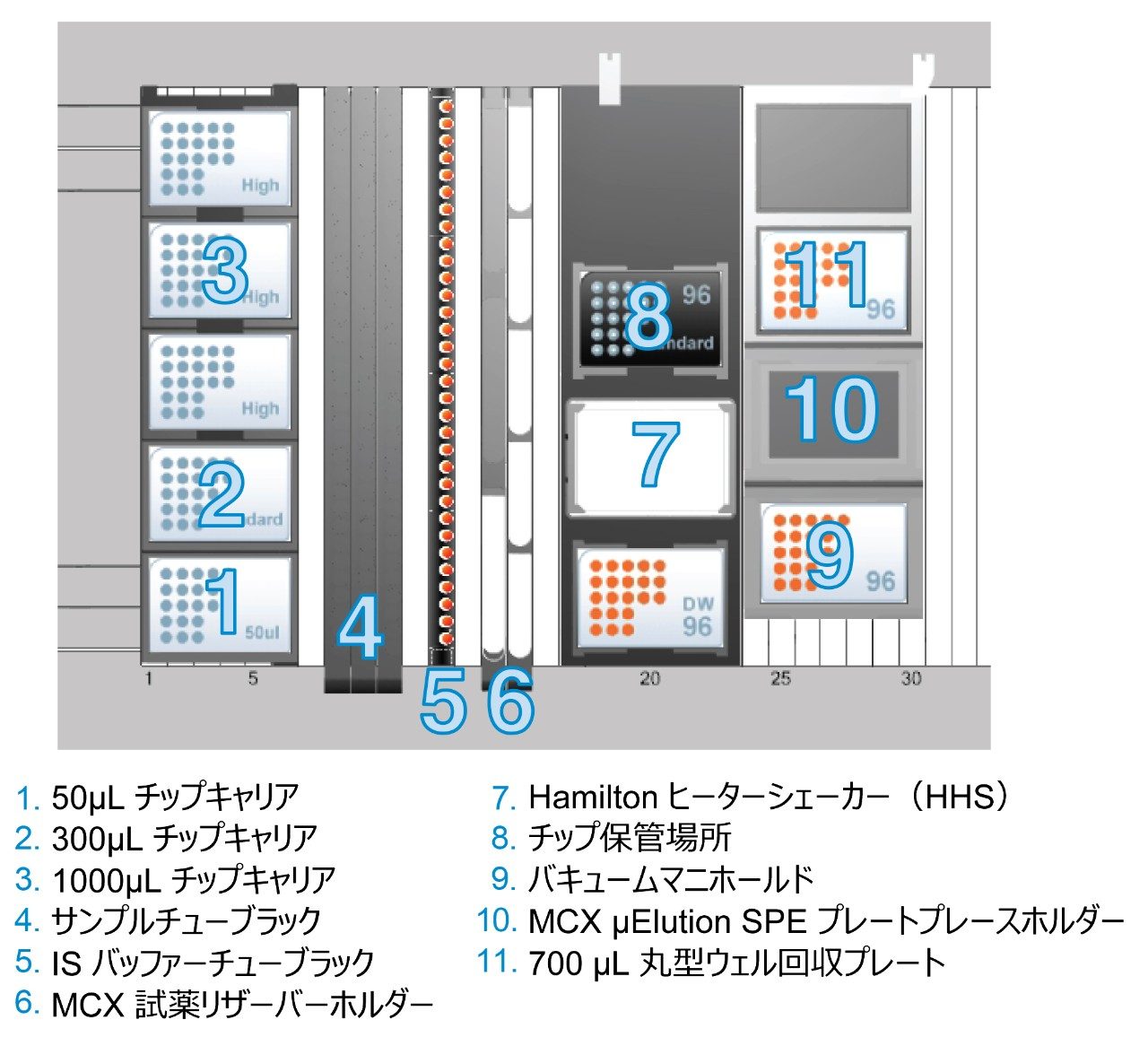

|
LC システム: |
ACQUITY UPLC I-Class(FTN) |
|
検出: |
Xevo TQ-S microESI+ |
|
カラム: |
ACQUITY UPLC BEH C18、1.7 μm、2.1 × 100 mm(製品番号:186002352) |
|
温度: |
40 ℃ |
|
サンプル温度: |
10 ℃ |
|
サンプル注入量: |
5 µL |
|
移動相: |
A:0.1% ギ酸水溶液 B:0.1% ギ酸アセトニトリル溶液 |
|
パージ溶媒: |
50% メタノール水溶液 |
|
洗浄溶媒: |
25:25:25:25 MeOH:H2O:IPA:ACN |
|
時間(分) |
流速(mL/分) |
移動相 A% |
移動相 B% |
|---|---|---|---|
|
0.00 |
0.6 |
98 |
2 |
|
3.33 |
0.6 |
33 |
67 |
|
3.50 |
0.6 |
10 |
90 |
|
3.60 |
0.6 |
98 |
2 |
|
4.00 |
0.6 |
98 |
2 |
|
キャピラリー電圧: |
1.0 kV |
|
脱溶媒温度: |
500 ℃ |
|
コーンガス流量: |
150 L/時間 |
|
脱溶媒ガス流量: |
1000 L/時間 |
取り込み範囲、コーン電圧、MRM トランジション、およびコリジョンエネルギーの各パラメーターは、特定の化合物に対して最適化されています。これらのパラメーターについては、ウォーターズのアプリケーションノート 720006187EN の付録 1 を参照してください。
|
Hamilton コントロールソフトウェア: |
Venus 3 |
|
装置コントロールソフトウェア: |
MassLynx v4.2 |
|
定量ソフトウェア: |
TargetLynx |
定量分析の前に、手動プラットホームと Hamilton Microlab STAR を比較するために分析種回収実験を実施し、自動プラットホームでのバリデーション済みメソッドの頑健性を実証しました。回収の結果は 2 つのプラットホーム間で同等であり、自動サンプル抽出の使用が手動抽出と同等に有効であると考えられます。
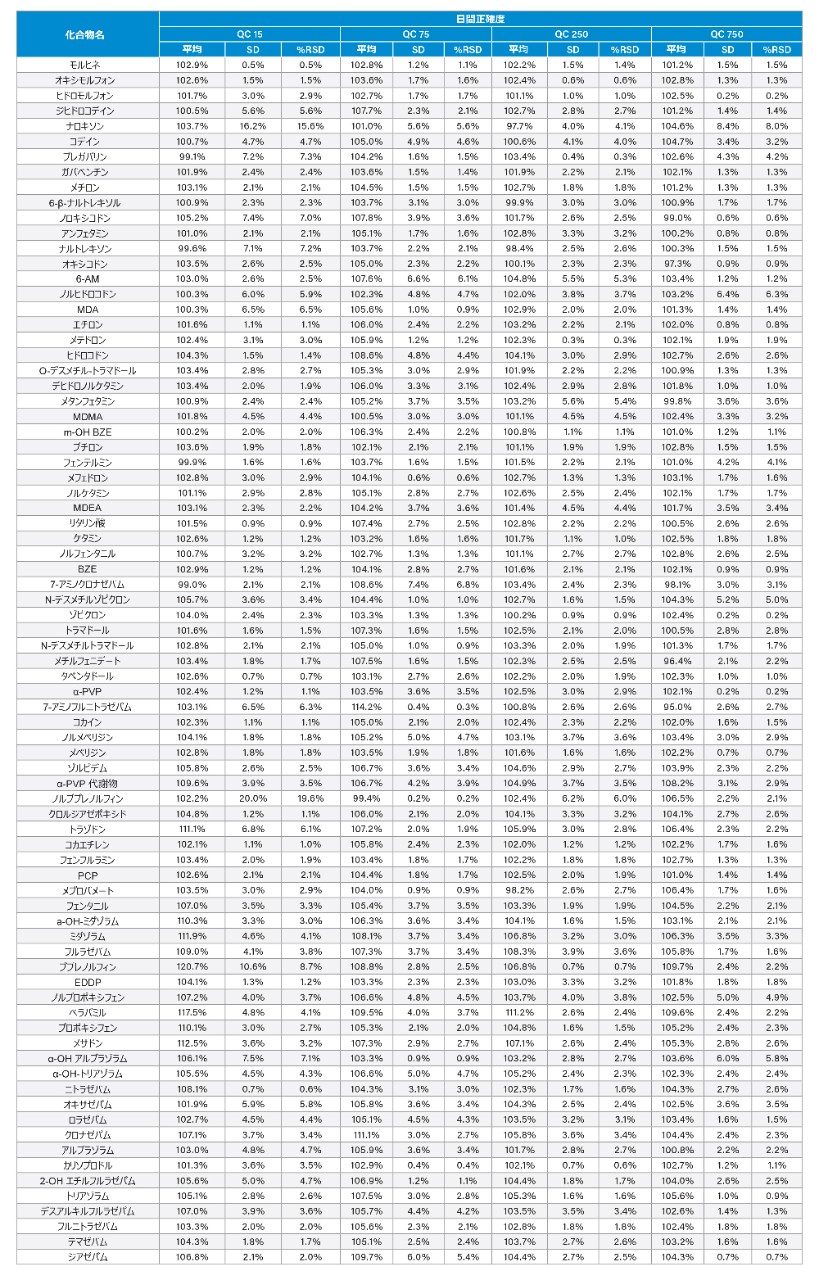
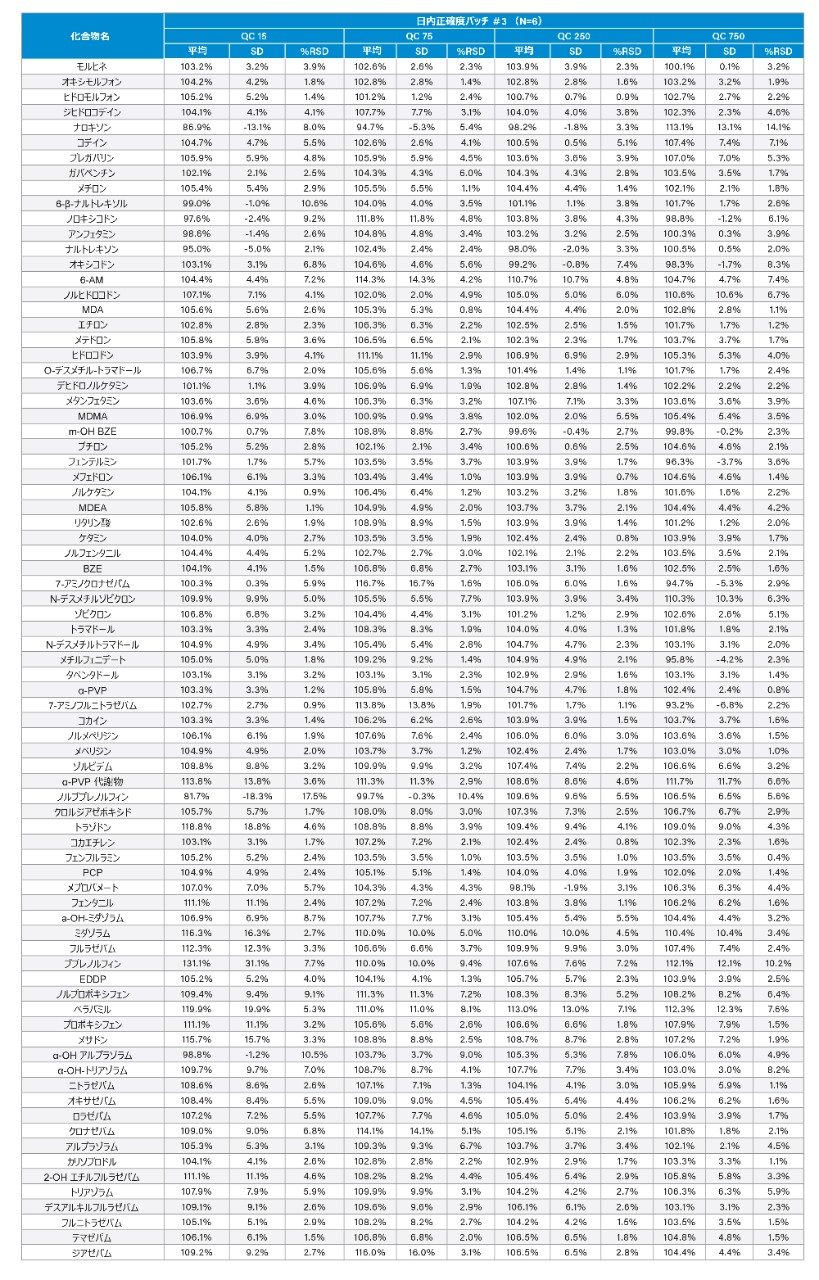
プールした尿サンプルを、3 日間で 3 バッチ抽出しました。7 ポイントからなる検量線を 2 回抽出し、4 つの異なる濃度の品質管理サンプルを 6 回抽出しました。ほとんどの化合物について、品質管理サンプルを 15、75、250、750 ng/mL で調製し、低濃度範囲の化合物は 3、15、50、150 ng/mL で、37.5、高濃度範囲の化合物は 187.5、625、1875 ng/mL で調製しました。各化合物のキャリブレーション範囲については、ウォーターズのアプリケーションノート 720006187EN の表 1 を参照してください。各キャリブレーターの許容基準は、目標値の ±15% 以内でしたが、最低濃度の点については 20% でした。品質管理サンプルの許容基準は 15% 以内でしたが、最低濃度の QC については 20% でした。これらは、SWGTOX ガイドライン7および FDA バイオ分析法のバリデーション要件に準拠しています8。3 バッチにわたる日間の結果のサマリーを付録 1 に記載しています。すべての化合物で上記の基準を満たしており、ほとんどの化合物の %RSD は 5% 未満でした。バッチ #3 の日内の結果のサマリーを付録 2 に記載しています。117% の 7-アミノクロナゼパム、131% のブプレノルフィン、116% のジアゼパムを除き、すべての化合物は %RSD の基準を満たしており、ほとんどの化合物について 5% 未満でした。すべての化合物の R2 値が 0.99 を超えていました。
個々のサンプルはすべて、バッチごとに 2 回抽出しました。各キャリブレーターと品質管理サンプルの 1 アリコートを Hamilton Microlab STAR を使用して処理し、各キャリブレーターと品質管理サンプルの 1 アリコートを手動で処理しました。この目的は、自動プラットホームの信頼性を証明し、期待される許容基準範囲内の正確度と精度が得られるような抽出を実施することにありました。手動と自動でのサンプル前処理の 3 バッチにわたる QC 2 の結果を図 3 に示します。手動サンプル抽出と自動サンプル抽出を比較した場合、STAR での個々の化合物の正確度と %RSD の方が優れているわけではありませんが、同等の結果が得られました。
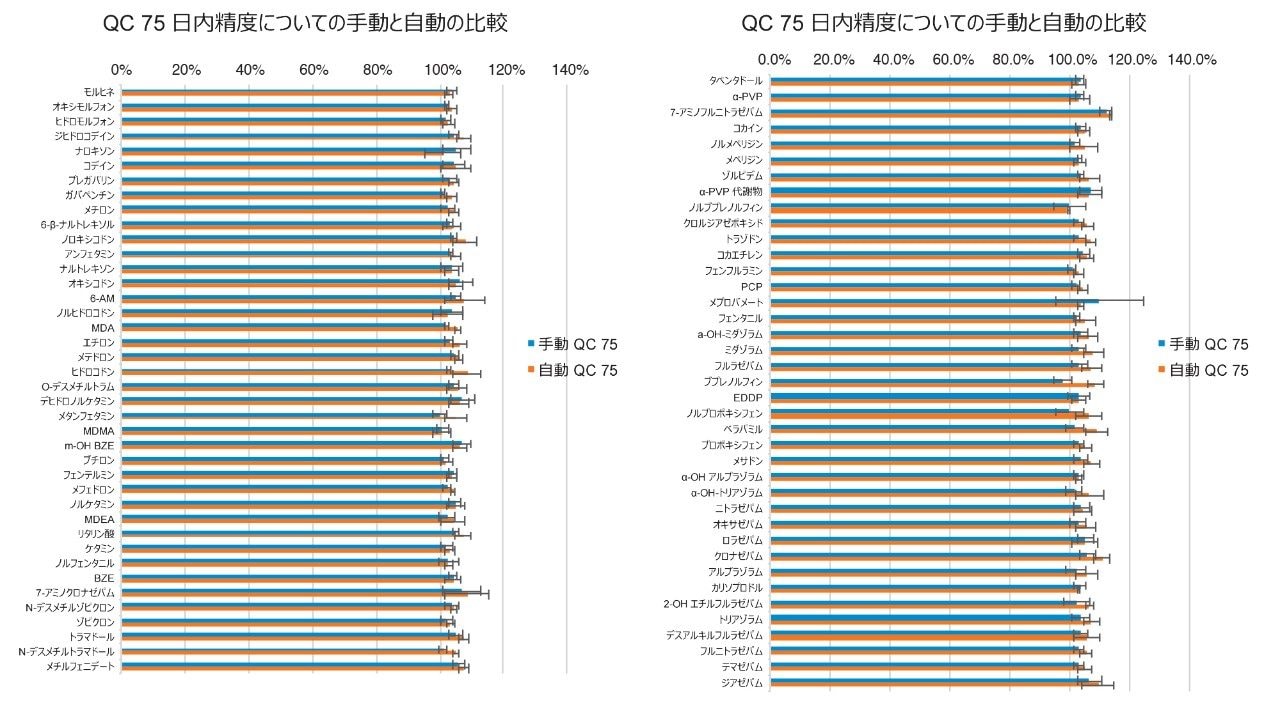
時間がかかるサンプル前処理の問題に対処するために、Hamilton Michrolab STAR を使用して、幅広い尿中の乱用薬物および疼痛管理薬物の前処理とその後の抽出プロセスを自動化することが、非常に有効であることが証明されました。このソリューションは、毒性化合物の包括的な範囲において、シンプルで迅速な SPE プロセスを提供します。バリデーション済みの SPE とメソッドを組み合わせた設定不要なスクリプトにより、プロセス全体の迅速な実装が可能になります。この完全に自動化したサンプル調製法は、R2 値が 0.99 を超え、QC 精度がすべての化合物で 85 ~ 115%(低 QC では 80 ~ 120%)であり、ほとんどの化合物で %RSD が 10% 以内の、頑健で再現性のある定量性能が提供されます。試験者の非一貫性、サンプルの移動、IS の添加、ラベル付けのミスなど、試験者関連のミスを効果的に最小限に抑えます。シンプルでありながらも頑健な完全自動サンプル前処理と SPE プロトコルを使用して、正確な定量を実現しました。
720006984JA、2020 年 8 月