
ACQUITY UPLC PLUS シリーズは特別に再設計することで、UPLC テクノロジーの利便性を強化すると同時に、従来の H-Class および I-Class システム等の ACQUITY UPLC システムと同様の分離性能を保証しています。このアプリケーションノートでは、糖鎖解析、サイズ排除クロマトグラフィー(SEC)、およびペプチドマッピングを含むさまざまなバイオ医薬品アプリケーションにおいて、ACQUITY UPLC PLUS システムの同等性と高い堅牢性を紹介します。
バイオ医薬品は様々な疾患の治療に効果的であり、急速な市場成長を遂げています。現在、費用効率がよく、かつ堅牢性の高い結果を効率的に取得可能な分析装置が必要とされています。コスト、効率、および堅牢性といった課題に対する一つの解決方法は、製品のライフサイクル全体に対応可能な新技術を採用することです。液体クロマトグラフィー (LC) システムは、品質システムにおいて、医薬品パイプライン全体を通じたバイオ医薬品の開発および製造プロセスにおける生産性の向上を可能とする、最新技術の本質的部分である可能性を秘めています。現在では、超高速高分離液体クロマトグラフィー (UPLC) システムは、分析の性能、生産性を大幅に向上させ、またコストを削減できる技術として開発および製造プロセス段階において普及してきました。製薬会社は製品上市の迅速化を図るため、堅牢性とダウンタイムの最小化を可能とする LC システムを必要としています。
ACQUITY UPLC PLUS シリーズは特別に再設計することで、UPLC テクノロジーの利便性を強化すると同時に、従来の H-Class および I-Class システム等の ACQUITY UPLC システムと同様の分離性能を保証しています。既存の ACQUITY UPLC システムのソルベントマネージャーとサンプルマネージャーにおいて多数の機能強化がされました(図 1)。デガッサーハードウェアおよびファームウェアを変更することで、分離の再現性が向上しシステムの稼働時間が最大化しました。一方でサンプルマネージャーを新設計することで、熱の影響を受けやすいサンプルの安定性が改善します。さらに、ニードル外側表面の処理により、バイアルキャップおよびウェルプレートカバーの形状との適合性範囲が広がり、同時にキャリーオーバー性能が大幅に改善しました。システム性能は強化されていますが、同時に ACQUITY UPLC ファミリーで同システムとデュエルボリュームおよび拡散を同一に設計することで、同等の分離プロファイルをシステム間で保証しています。ACQUITY UPLC PLUS シリーズはいずれも、既存の分析法において同等の性能を保証すると同時に、稼働時間を最大化し、使いやすさを向上します。

このアプリケーションノートでは、糖鎖解析、サイズ排除クロマトグラフィー(SEC)、およびペプチドマッピングを含むさまざまなバイオ医薬品アプリケーションにおいて、ACQUITY UPLC PLUS システムの同等性と高い堅牢性を紹介します。ACQUITY UPLC H-Class PLUS Bio システムおよび ACQUITY UPLC I-Class PLUS システムを、ACQUITY UPLC H-Class Bio システムおよび ACQUITY UPLC I-Class システムとそれぞれ比較し、ACQUITY UPLC PLUS システムの性能を評価しました。
糖鎖サンプルは以前報告したアプリケーションノートと同様に調製しました1。 RapiFluor-MS 糖鎖スタンダード (P/N 186007983) を DMF/アセトニトリル/水を混合比 22.5/55.5/22 で混合した溶液 25 µL に溶解しました。LC-MS グレードの水およびアセトニトリルは Fisher Scientific 社から購入しました。50 mM のギ酸アンモニウム溶媒は、Waters Ammonium Formate Solution-Glycan Analysis(P/N 186007081)(1 ボトル (10 mL)) を 1 L の水で希釈して調製しました。
|
LC システム: |
ACQUITY UPLC H-ClassBio ACQUITY UPLC H-Class PLUS Bio |
|
検出器: |
ACQUITY FLR、 10 mm フローセル、λ = 214 nm |
|
LC カラム: |
ACQUITY UPLC Glycan BEH Amide、1.7 μm、 130Å、2.1 mm × 150 mm(製品番号 186004742) |
|
カラム温度: |
60 ℃ |
|
サンプルバイアル: |
12 mm × 32 mm ガラス、 トータルリカバリー (製品番号 600000750cv) |
|
注入量: |
2 µL |
|
移動相 A: |
50 mM ギ酸アンモニウム水溶液、pH4.4 |
|
移動相 B: |
アセトニトリル |
|
時間(分) |
流量(分) |
%A |
%B |
|---|---|---|---|
|
初期条件 |
0.4 |
25 |
75 |
|
35 |
0.4 |
46 |
54 |
|
36.5 |
0.2 |
100 |
0 |
|
39.5 |
0.2 |
100 |
0 |
|
42.5 |
0.2 |
25 |
75 |
|
47.4 |
0.4 |
25 |
75 |
|
55 |
0.4 |
25 |
75 |
以前報告したアプリケーションノートと同様に、2 リン酸一ナトリウム、リン酸二ナトリウム、および塩化ナトリウムを Sigma 社から購入しました。移動相の 20 mM リン酸バッファーは、1.37 g のリン酸一ナトリウム(一水和物)、2.70 g のリン酸二ナトリウム(七水和物)、11.68 g の塩化ナトリウムを 900 mL の水に加え、pH を 6.8 に調整しました。その後、バッファー全体量を 1 L に調製し、移動相として使用しました。BEH200 SEC Protein Standard Mix(製品番号:186006518)は 500 µL の移動相で完全に溶解し、分析に使用しました。
|
LC システム: |
ACQUITY UPLC H-Class Bio ACQUITY UPLC H-Class PLUS Bio |
|
検出器: |
ACQUITY TUV、 10 mm フローセル、λ = 214 nm |
|
LC カラム: |
ACQUITY UPLC Protein BEH SEC、 200Å、1.7 µm、4.6 x 150 mm (製品番号:186005225) |
|
カラム温度: |
室温 |
|
サンプルバイアル: |
12 mm × 32 mm ガラス、 トータルリカバリー (製品番号 600000750cv) |
|
注入量: |
4 µL |
|
移動相: |
20 mM リン酸、 200 M NaCl、pH 6.8 |
|
流量: |
0.885 mL/分 |
トリフルオロ酢酸 (TFA)、LC-MS グレードの水およびアセトニトリルは Fisher Scientific 社から購入しました。Waters MassPREP Enolase Digestion Standard(製品番号 186002325)は 100 µL の移動相 A(0.1% TFA 水溶液)に溶解し、サンプルとして使用しました。
|
LC システム: |
ACQUITY UPLC I-ClassACQUITY UPLC I-Class PLUS |
|
検出器: |
ACQUITY TUV、 10 mm フローセル、λ = 214 nm |
|
LC カラム: |
ACQUITY UPLC BEH C18、 1.7 µm、300 Å、2.1 mm × 100 mm (製品番号 186002350) |
|
カラム温度: |
65 °C |
|
サンプルバイアル: |
12 mm × 32 mm ガラス、 トータルリカバリー (製品番号 600000750cv) |
|
注入量: |
10 µL |
|
移動相 A: |
H2O、0.1% TFA |
|
移動相 B: |
アセトニトリル、0.1% TFA |
|
時間(分) |
流量(分) |
%A |
%B |
|---|---|---|---|
|
初期条件 |
0.200 |
99.0 |
1.0 |
|
3.00 |
0.200 |
99.0 |
1.0 |
|
88.00 |
0.200 |
50.0 |
50.0 |
|
90.00 |
0.200 |
10.0 |
90.0 |
|
100.00 |
0.200 |
10.0 |
90.0 |
|
102.00 |
0.200 |
99.0 |
1.0 |
|
126.00 |
0.200 |
99.0 |
1.0 |
バイオ医薬品開発において、重要品質特性 (CQA) を特定し糖鎖プロファイルを解析しモニタリングすることは、製品の安全性と効能を保証するために欠かせません。糖鎖プロファイリングワークフローの一部においては、遊離糖鎖分析では親水性相互作用クロマトグラフィー(Hydrophilic Interaction Chromatography、HILIC)が広く使用されています。糖鎖プロファイルは複雑なため、長く緩やかなグラジエント分析がしばしば採用されています。そのため、糖鎖プロファイリングでは、堅牢性の高い LC システムが必要です。
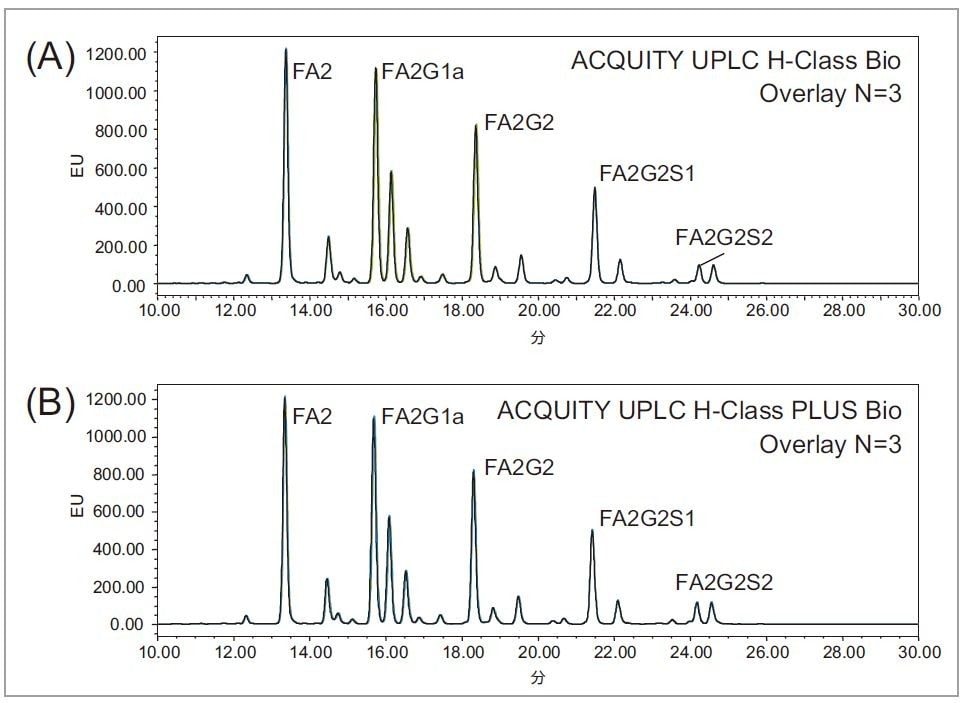
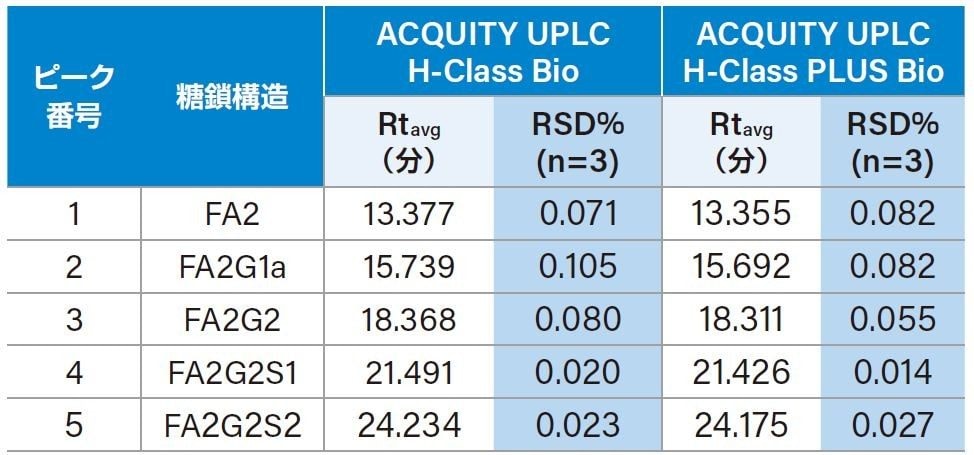
糖鎖分析における ACQUITY UPLC PLUS システムの性能を評価するため、まず従来の ACQUITY UPLC H-Class Bio システムを用いて、RapiFluor-MS Glycan Performance Test Standard を ACQUITY UPLC Glycan BEH Amide カラム (15 cm) で、分離検討を行いました1。 35 分間の 46 ~ 25 % のアセトニトリル グラジエント分析を実施し、すべての糖鎖が 10 分から 30 分の間で溶出し、良好な分離結果が得られました(図 2A)。次に同様の分析を ACQUITY UPLC H-Class PLUS Bio システム で実施、比較しました。結果、同じ分離プロファイルが得られました(図 2B)。表 1 に示した 5 つの主要ピークの保持時間は 2 つの 装置間でほぼ同じであることからも、これらの LC システムが同等であることが分かります。3 回の繰り返し分析の結果から、5 つの主要ピークの保持時間の%RSD(相対標準偏差)を計算し、2 つのシステムの堅牢性を評価しました。ACQUITY UPLC H-Class PLUS Bio システムの保持時間の%RSD(0.082%以下)は、従来の ACQUITY UPLC H-Class Bio システムの %RSD(0.105%以下)よりも全体的に良好な 結果であり(表 1)、アップグレードされた UPLC システムの再現性が向上しています。
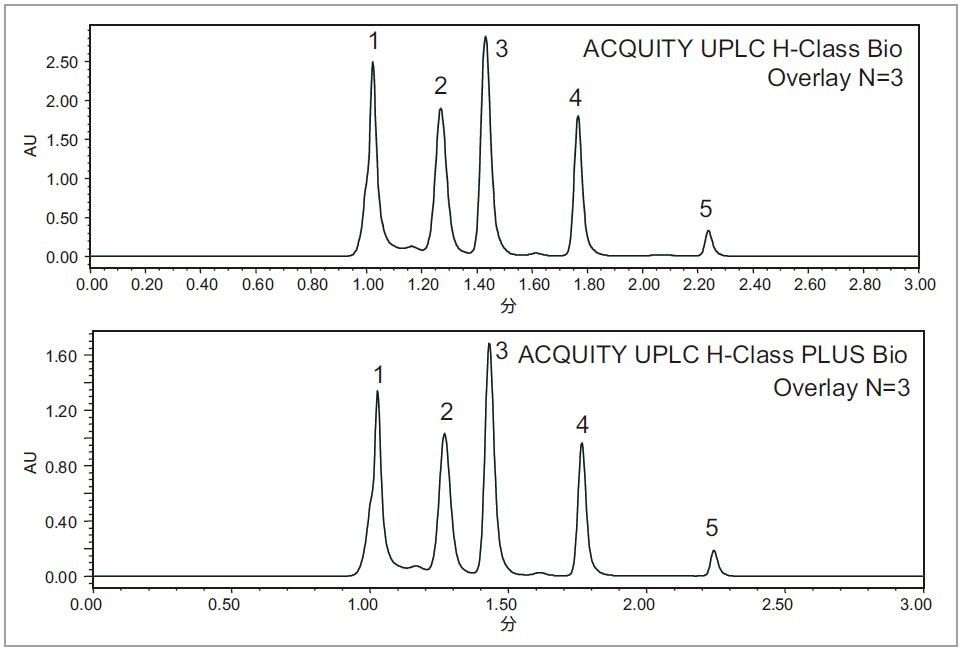
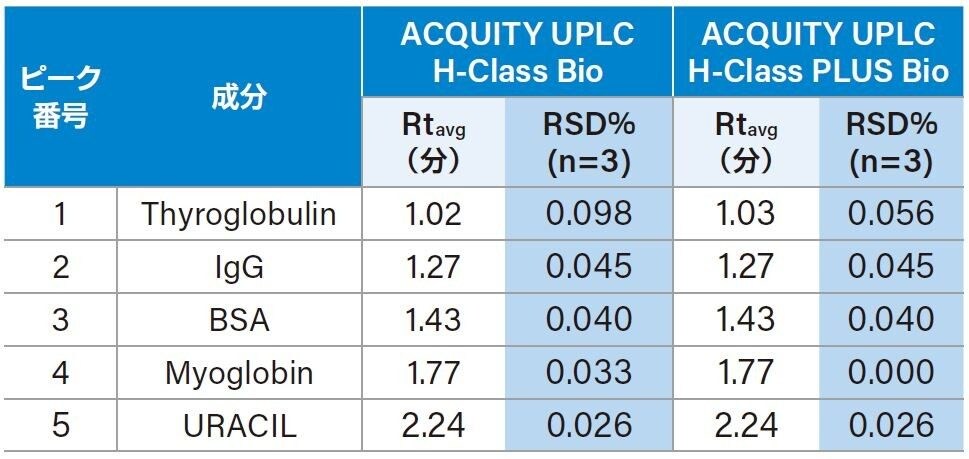
SEC はバイオ医薬品の特性解析とルーチンモニタリングにおいて広く使用されています。SEC における保持時間の再現性は、原薬の凝集および断片化を正確に測定する上で重要です。ACQUITY UPLC H-Class Bio システムと、ACQUITY UPLC H-Class PLUS Bio システムの性能を比較するため、SEC200 タンパク質混合物スタンダードをテストサンプルとして使用し、ACQUITY UPLC Protein BEH SEC カラム (15 cm) で分離しました2。 図 3 の重ね書きクロマトグラム (n=3) に示した通り、5 つの成分が 3 分以内に良好に分離され、各成分について両方の装置でほぼ同一の保持時間が得られたことから(表 2)、2 つのシステムが同等であることが分かります。5 つのピークの保持時間の %RSD の結果(表 2)から SEC アプリケーションにおいても ACQUITY UPLC H-Class PLUS Bio システムの再現性がより高いことが実証されました。
バイオ医薬品の開発において、タンパク質の酵素消化後のペプチドマッピングは、製品の CQA モニタリングや特性解析において、確立されたアプローチです。酵素の切断部位やタンパク質の大きさによって、酵素消化物の分離が困難となることがあります。この場合、近接したピークの共溶出が懸念され、正確なピーク同定と面積算出のためには保持時間の高い再現性が要求されます。
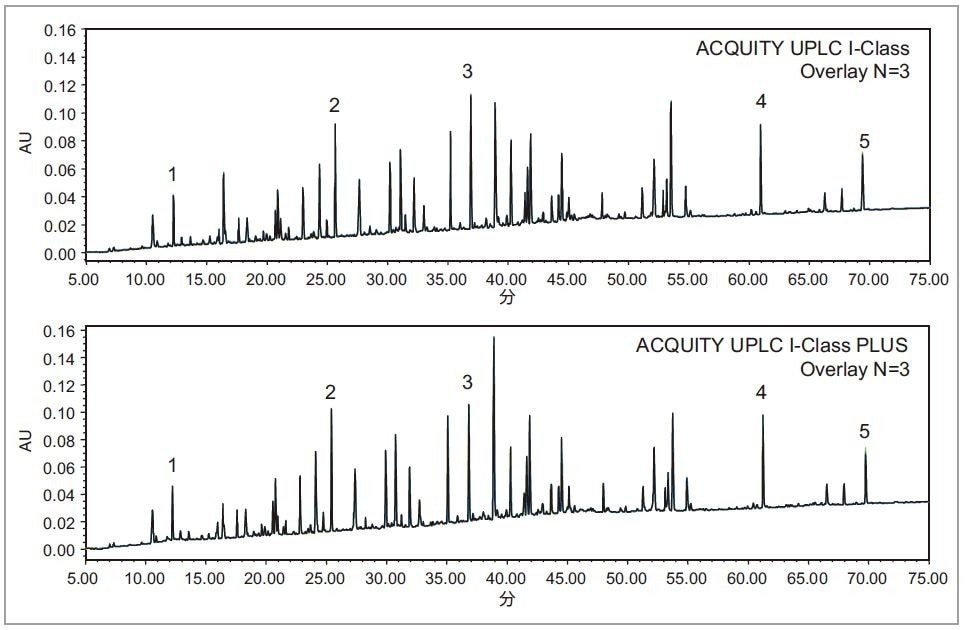
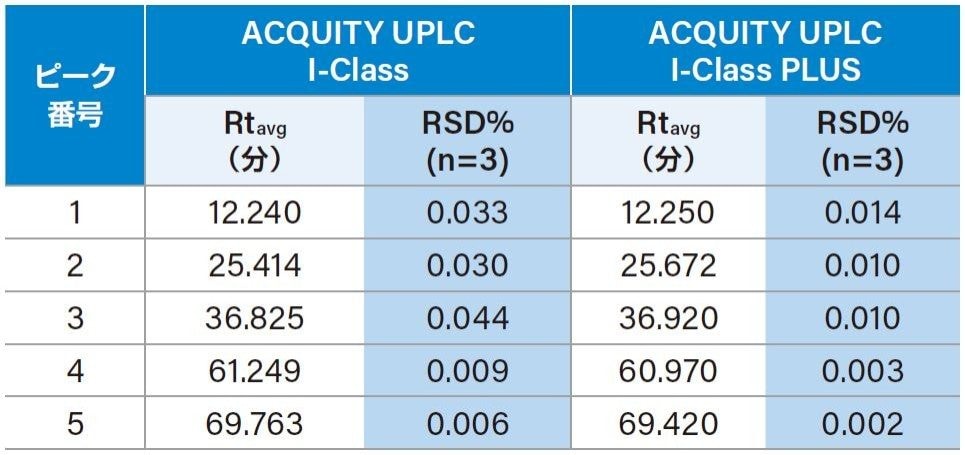
最も再現性の良い結果を得るために、バイナリーポンプと高圧混合方式を搭載した ACQUITY UPLC I-Class システムを用いて、Waters MassPREP Enolase Digestion Standard のペプチドマッピングを行いました。カバレージを最大にするため、75 分間の 1 %~50 %のアセトニトリルグラジエント条件を用いた結果、極性ペプチドを保持した高分離分析を達成しました3。 2 つの装置間でほぼ同等のペプチドマッピングプロファイルが得られたことから(図 4)、ACQUITY UPLC I-Class PLUS システムが従来の ACQUITY UPLC I-Class システムに置き換えることの妥当性が示されました。装置の性能をさらに比較するため、5 つのピークを選択し、グラジエント全体における再現性を検証しました。両装置における平均保持時間は同等でありながら、ACQUITY UPLC I-Class PLUS システムにおける保持時間の %RSD は最大値が 0.044% から 0.014% に大幅に低下しました(表 3)。これらの結果から、ACQUITY UPLC I-Class PLUS システムの分離性能の一貫性と再現性の向上が証明されました。
バイオ医薬品の開発と製造においてよく用いられる技術を例にしてACQUITY UPLC および ACQUITY UPLC PLUS システムの同等性と堅牢性を評価しました。ACQUITY UPLC H-Class PLUS Bio システムは、同等の分離プロファイルを担保しながらも、糖鎖分析と SEC の両分析において低い%RSD 結果が得られました。ACQUITY UPLC I-Class PLUS システムでのペプチドマッピングにおいて、平均保持時間の%RSD が 0.014%以下であり、堅牢性が向上していることも分かりました。ACQUITY UPLC PLUS システムは従来の UPLC システムと同等の分離性能と、バイオ医薬品アプリケーションに有効な高い堅牢性を得ることができます。
720006285JA、2018 年 5 月