Agilent 1100 シリーズLC システムからACQUITY UPLC H-Class システムへHPLC 分析法の移管時における温度の影響について比較検討する。
温度管理は分析法を移管する上で非常に大きな影響力を持ちます。今回はAgilent 1100 シリーズLC システムからシングルカラムコンパートメント搭載ACQUITY UPLC H-Class システムへの分析法移管を問題なく実施することができました。両システムにおいて分離に対する温度の影響は同等でした。しかし、両システムにおいてプレヒーティング機能の使用の有無では異なる分離が得られました。今回の検討では、移動相のプレヒーティング機能の有無にのみ温度における選択性の影響が生じることが分かりました。温度管理における分析法への影響は分析法移管時には検討する必要があります。今回は移動相のプレヒーティング機能の有無両条件において、Agilent1100 シリーズLC システムからシングルカラムコンパートメント(CH-A)搭載ACQUITY UPLC H-Class システムへ問題なく分析法を移管することができました。
原薬(API)及びその類縁化合物の薬剤のライフサイクルにわたり安全性と有効性の検証を HPLC 分析によって実施するケースが多くあります。一般的に規制下のラボにおいて実施されるこれらの分析は、分析法の変更は制限されているか1、許可されていないため、変更する場合は再バリデーションを実施しなければなりません。一方で従来から使用している分析法は旧来の HPLC システムで開発されており、それらの分析法を最新の UHPLC システムに移管するという要望が存在します。その場合は限られたリソースで実施するもしくは完全に UHPLC 法に変更されます。分析法を異なる HPLC/UHPLC システム間で移管する場合、一般的には新しいシステムは以前の分析法/システムと同じ分離を再現し、システム適合性要件に適合しなければいけません1。しかし、各システムの様々な特徴が分析法移管に影響を及ぼします。グラジエント分離を適用している場合、分析法移管はデュエルボリュームの影響を大きく受けます。ミキサー、バルブ、インジェクターに起因するデュエルボリュームは、同じメーカーの製品であっても装置の種類によって異なります。グラジエント分析法の移管においては、システムの特徴を考慮し、グラジエントテーブルを調整する必要があります1。
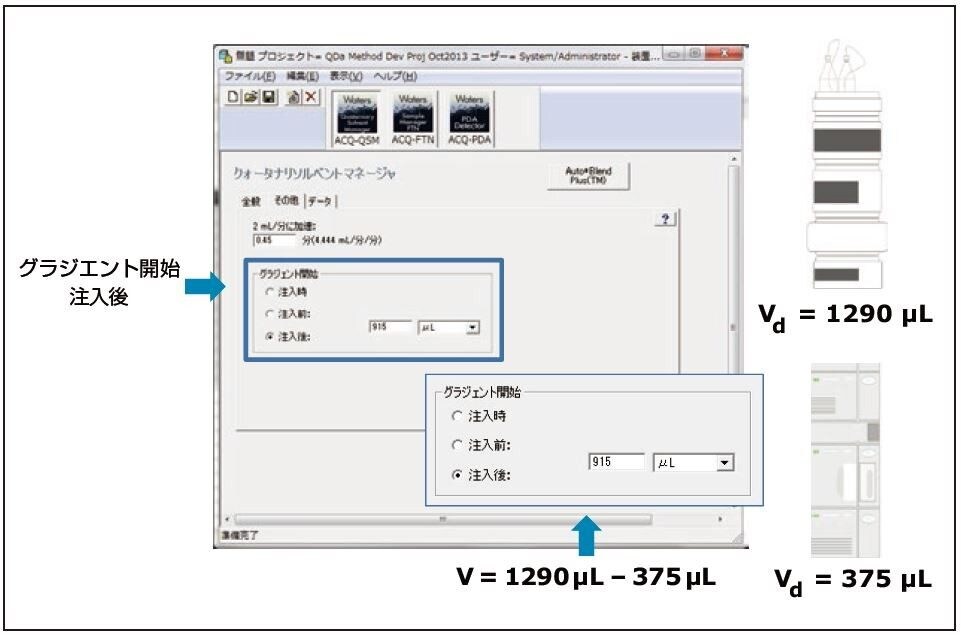
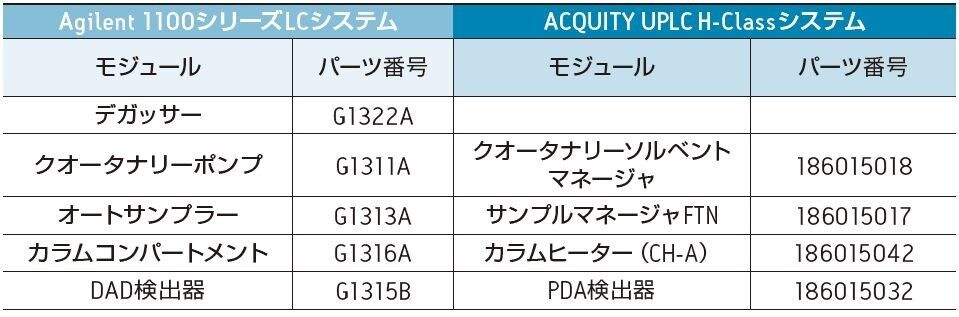
以前報告した Abacavir とその類縁化合物の分析法2を Agilent 1100 シリーズ LC システムから ACQUITY UPLC H-Class システムへ移管しました(表 1)。Agilent 1100 シリーズ LC システムは移動相のパッシブプレヒーター機能(3 µL)を、ACQUITY UPLC H-Class システムはアクティブプレヒーター機能を搭載しています。グラジエントディレイの差を検証するために、両システムの Dwell 容量を測定しました3。 Dwell 容量は Agilent 1100 シリーズ LC システムが大きく、ACQUITY UPLC H-Class システムとの Dwell 容量の違いを補正するために ACQUITY UPLC H-Class システム分析に 915 µL の「注入後」ディレイを使用しました。ディレイはグラジエント SmartStart 機能を用いて装置メソッドに分もしくは µL で直接入力することができます(図 1)4。 分析法開発において Dwell 容量の違いを補正する機能はグラジエントテーブルのマニュアル変更の手間や分析法の再バリデーションを回避することが可能です。容量をグラジエント SmartStart 機能に入力するだけで、分析法の調整を行うことができます。
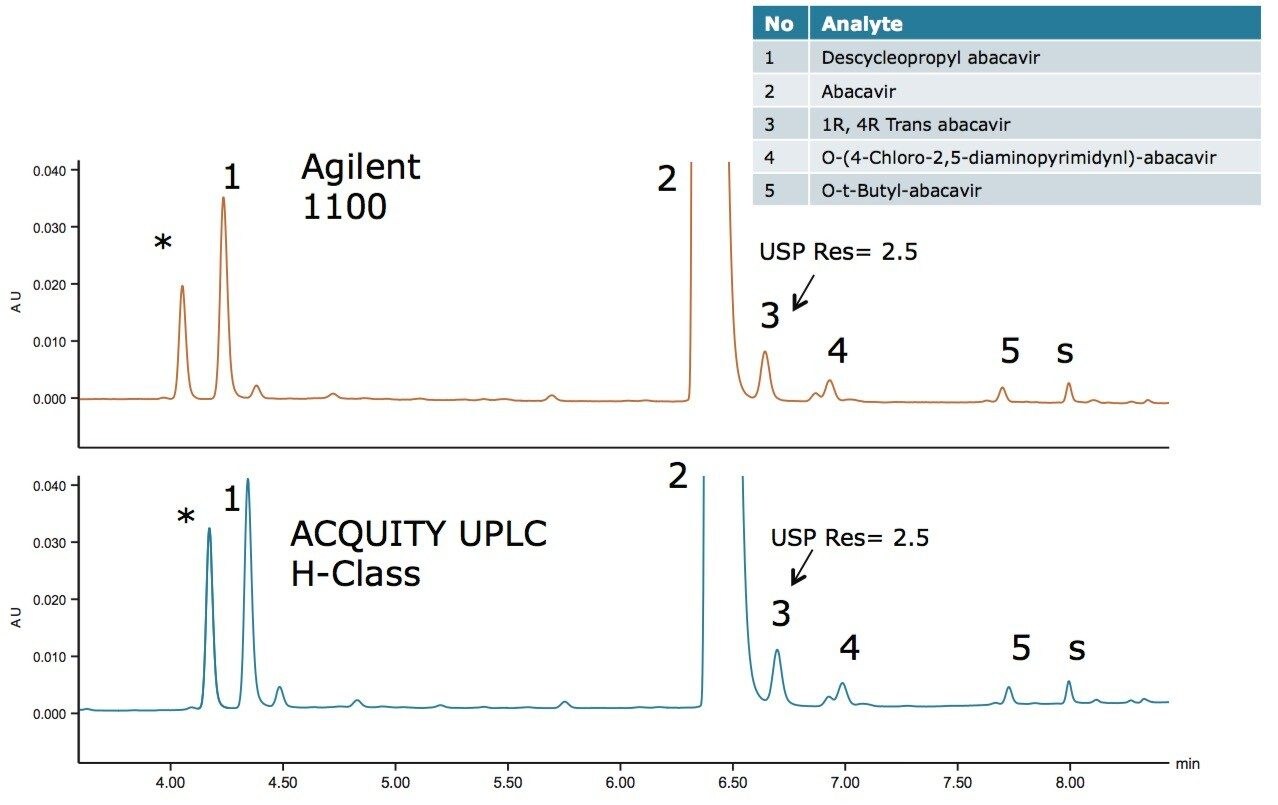
Agilent 1100 シリーズ LC システムと ACQUITY UPLC H-Class システムの両システムにおいて、同等の分離結果を得ることができました(図 2)。Abacavir 及びその類縁化合物は全ての分析種においてシステム間で保持時間が 0.2 分以内もしくは偏差が 3% 以内でした(表 2)。API に対する相対保持時間は類縁化合物において偏差は 0.01% 以内でした。最も重要な API と類縁化合物 3 の USP 分離能は両システムにおいて 2.5 以上で、分析法の移管時に有意な分離能の低下は見られませんでした。両システムにおいて API と各類縁化合物の % 面積の偏差は 0.2% 以内でした。
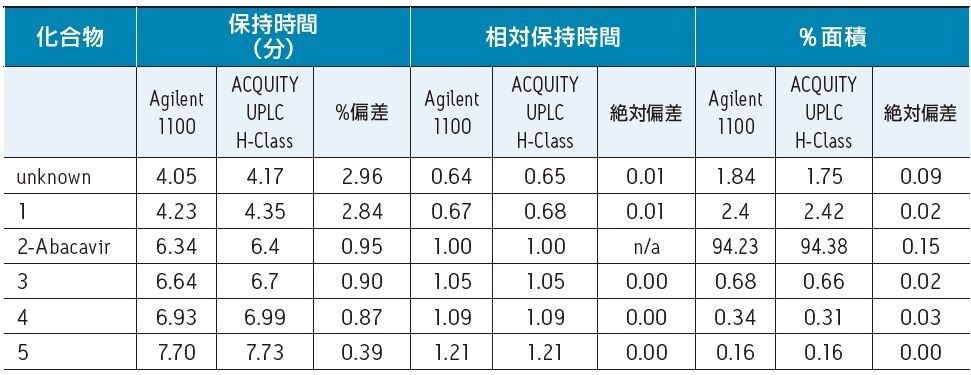
保持時間と相対保持時間は多くの分析法で同定の目的に使用されます5,6。 分析法を別のメーカーの製品に移管する場合、一般的に保持時間の変動の許容値は 3~5% と言われています7。 今回はその許容値に適合する結果が得られました。
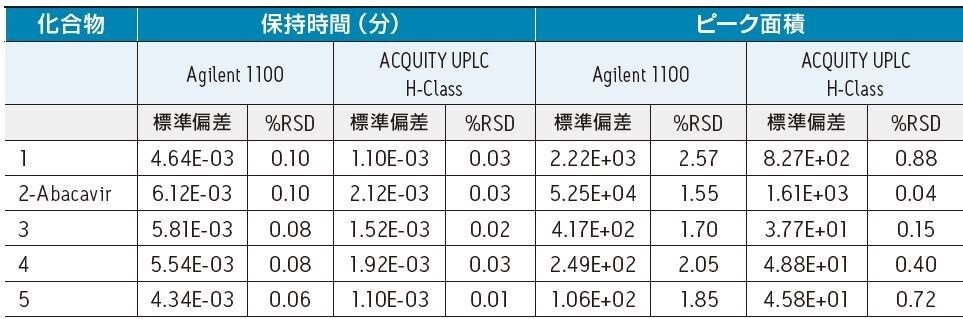
再現性の評価においては、両システムで 5 回の繰り返し分析を実施しました。標準偏差と % 相対標準偏差(%RSD)を計算しました(表 3)。両システムにおいて、すべての既知の分析種において保持時間の %RSD は 0.2% 以下、ピーク面積の %RSD は 3% 以下でした。更に ACQUITY UPLC H-Class システムでは全ての分析種において Agilent 1100 シリーズ LC システムと比較して、より良好なピーク面積 %RSD が得られています。注入再現性においても両システムで許容できる値(RSD < 3%)が得られ、ACQUITY UPLC H-Class システムではピーク面積の %RSD によって Agilent 1100 シリーズ LC システムと比較したインジェクション間のばらつきは若干ですが良好な結果が得られました。
Abacavir およびその類縁化合物の分析において、問題なく Agilent 1100 シリーズ LC システムから ACQUITY UPLC H-Class システムへ分析法を移管することができました。分析法を移管しても分離は維持されており、保持時間、相対保持時間共に 2% 以内でした。今回の検討では、注入再現性の %RSD は Agilent 1100 シリーズ LC システムと比較して ACQUITY UPLC H-Class システムがより良好な結果が得られました。更に装置メソッドのグラジエントSmartStart 機能を利用することでグラジエントテーブルをマニュアルで調整することなく分析法にシステム容量の差を反映することができます。今回の結果より、Agilent 1100 シリーズ LC システムから ACQUITY UPLC H-Class システムへの分析法移管を最小限の分析法/システムの調整で実施可能であることが分かりました。
720005252JA、2014 年 12 月