基于XevoTM MRT液质联用技术增强宿主细胞蛋白的鉴定与定量分析
Jonathan Fox, Malcolm Anderson, Ying Qing Yu, Scott J Berger, Nick Pittman, Laetitia Denbigh
Waters Corporation, United States
发布日期:2025年8月7日
摘要
宿主细胞蛋白(HCP)是生物治疗药物中常见的杂质,由上游和下游生产工艺共同产生。这些低水平内源性蛋白质来自宿主生物,且难以纯化去除或检测。尽管HCP在市售产品中的含量较低(总量通常< 100 ppm),但它可能会影响生物治疗药物的治疗活性和稳定性。因此,在生物制药工艺开发中,对HCP进行表征至关重要,而且在生产和产品放行过程中证明其清除效果对于确保治疗药物的安全性、有效性和质量具有决定性意义。
本应用简报详细介绍了一种新型多反射飞行时间(MRT) Q-ToF质谱仪的使用,用于对NIST单克隆抗体参比品(NIST mAb,RM 8671)样本进行全面的宿主细胞蛋白液相色谱质谱(HCP LCMSE)发现和基于Hi3的定量工作流程。该分析表明,在128 ppm至12 ppb的宽动态范围内,可高置信度检测到101种HCP。
优势
- 可靠地鉴定和定量单个HCP有助于了解产品和工艺、制定有针对性的纯化策略并改善风险评估结果。
- 宽动态范围和高灵敏度有助于尽早鉴定纯化过程中可能持续存在的ppb级HCP,从而促进高效的工艺优化和验证。
- 一致的亚ppm质量误差可实现母离子和碎片离子的可靠归属,支持特定的肽和蛋白质归属,从而实现宿主细胞蛋白质杂质的稳定检测。
- 酶联免疫吸附试验(ELISA)的正交方法:高分辨率质谱(HRMS)不依赖于免疫试剂,可缩短HCP分析的开发时间,拓宽HCP的分析范围,不受免疫试剂特异性限制。HRMS通过提供有关单个HCP的数据来验证ELISA分析的选择性和定量能力。
简介
HCP分析是生物制药工艺开发的重要组成部分,可确保治疗药物的安全性和纯度。传统上,行业一直采用ELISA和免疫分析法测定HCP总浓度,单位为ppm(ng HCP/mg生物药物)。ELISA和免疫分析法具有较高的灵敏度和通量,但1)动态范围有限;2)受限于对免疫试剂的依赖,免疫试剂可能无法识别样品中存在的所有HCP,也无法提供足够的抗体来定量测定特定的HCP;3)可测定总HCP含量,但通常无法定量单个蛋白质。相比之下,基于质谱(MS)的HCP分析已成为一种强大的替代分析方法,它覆盖了整个蛋白质组范围,能够高特异性、高灵敏度地识别和定量单个HCP。随着特定类别的HCP被提示会带来巨大风险,这种方法可以实现更详细的风险评估、更快的工艺优化并符合不断变化的法规要求。
使用生物治疗蛋白质样品的肽酶解物进行MS分析是一种强大的分析方法,可在整个生物治疗药物的开发生命周期中用于监测和定量HCP。随着生物治疗药物管线的扩展,部署更高置信度的自动化方法以准确、一致地表征低水平HCP,对于高效的产品与工艺开发决策变得愈发重要。因此需要稳定、简便易用的分析平台,以便轻松部署到组织内各实验室。
近几十年来,随着LC-MS技术的进步,人们能够更方便、更可靠地发现和定量HCP,同时提高灵敏度并缩短样品分析时间,使得这种方法在生物制药的生产中越来越普及。在先前的研究中,采用纳升级流速和多维LC的复杂方法对于实现鉴定低水平宿主细胞蛋白所需的高灵敏度至关重要1。这些方法执行难度大,而且通量有限,需要经验丰富的分析人员花费数天时间来跨纯化步骤或多个药物批次追踪HCP。向高通量分析型LC-MS分析的转变使该方法的实用性更高,但对MS检测功能的要求也更高。
之所以选择NIST mAb,RM 8671进行分析,是因为它是广受认可的HCP分析基准参比品,可以直接比较不同分析平台和工作流程的方法性能和结果。这种可比性对于展示HCP检测的改进(例如增加的覆盖率、更低的检测限和稳定的定量)尤其重要,同时确保结果在生物制药工艺开发和法规预期这一更广泛的背景下具有意义2,3。
本研究展示了Xevo™ MRT直观的LC-MSE非数据依赖型采集(DIA)模式4如何实现出色的灵敏度、宽动态范围和亚ppm级分析质量精度,从而可靠地鉴定HCP。定量分析通过Hi3定量方法在同一数据集中完成,这是一种基于内部校准、非标记且依赖信号强度的技术。该方法通过平均三种最强胰蛋白酶肽段的MS1信号强度来估算蛋白质丰度,从而能够对复杂生物样品进行准确、可重现的定量。
总体而言,由waters_connect™信息学平台控制并采用ProteinLynx Global Server进行数据处理的Waters™ Xevo MRT质谱仪系统为HCP的质谱发现与定量提供了全面解决方案。该系统通过高置信度的自动化方法增强产品和工艺开发能力,支持更加安全的生物治疗药物研发。
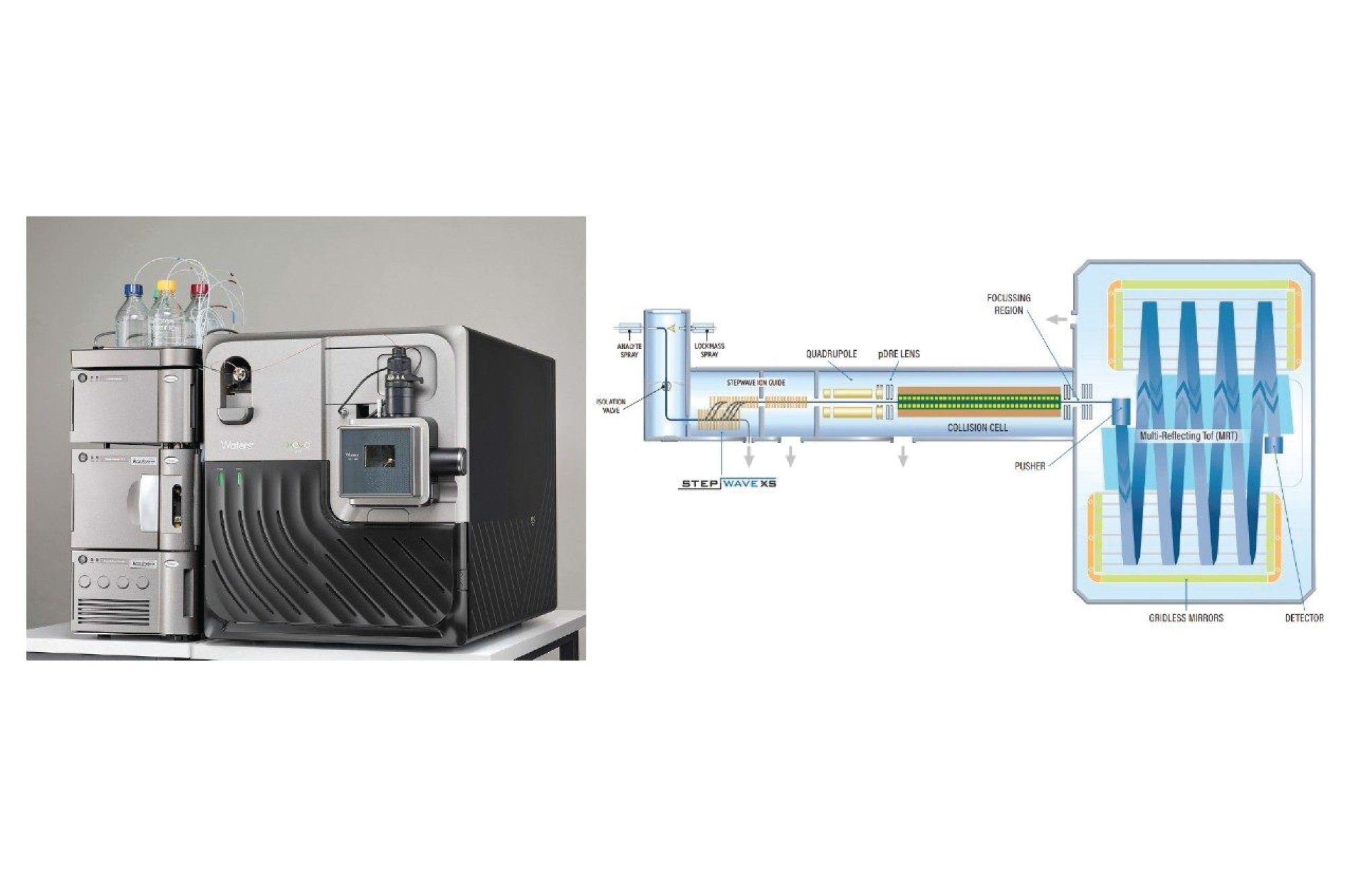
实验
样品前处理采用Huang等人2先前描述的优化非变性酶解方案。在非变性条件下的单抗(mAb)酶解提供了一种简单且稳定的样品前处理方法,可优先酶解HCP并大幅减少高丰度的治疗性单抗蛋白。这种方法可实现富集,并有助于通过分析级LC-MS分析鉴定较低丰度的HCP。
使用Xevo MRT质谱仪和LC-MSE (DIA)采集模式对胰蛋白酶酶解的NIST mAb样品(参考的Lily方法)进行分析。数据使用PLGS 3.0.3处理。
非变性单克隆抗体(mAb)酶解方案:
试剂和材料:
- NISTmAb人源化IgG1k单克隆抗体标准品NIST® SRM® 8671购自Merck,由一个装有800 µL 10 mg/mL NIST IgG1κ单克隆抗体(NISTmAb)(总计8 mg)的冷冻瓶组成。
- RapiZyme™:40 µL (0.5 µg/µL)
- Tris/CaCl₂缓冲液(100 mM/10 mM):80 µL
- 二巯基苏糖醇(DTT):350 mM
- Waters 质谱制备标准品:磷酸化酶B (p/n: 186002326), BSA (p/n: 186002329), ADH (p/n: 186002328) 和烯醇酶 (p/n: 186002325)
- 甲酸:10%溶液
步骤:
1. 酶解:
- 将800 µL mAb (8 mg)与40 µL Rapizyme (0.5 µg/µL)及80 µL 100 mM Tris/CaCl₂缓冲液混合于Waters QuanRecovery™ MaxPeak™ HPS样品瓶中。
- 以400:1的底物/酶比率,将混合物置于37 °C孵育16小时。
2. 还原:
- 向酶解液中加入15.7 µL 350 mM DTT。
- 涡旋混合后在90 °C下孵育15 min。可能会形成混浊的悬浮液。
3. 离心:
- 将混合物在12,000 × g下以软加速和软减速设置离心5 min。
- 小心收集上清液(~800 µL)。
4. 质谱制备标准品加标:
- 取上清液,加入以下标准品:
- BSA:28.96 µL的1 pmol/µL溶液(最终浓度:250 ppm)
- 磷酸化酶B:8.24 µL的1 pmol/µL溶液(100 ppm)
- ADH:10.88 µL的1 pmol/µL溶液(50 ppm)
- 烯醇酶:34.16 µL的100 fmol/µL溶液(20 ppm)
5. pH调节:
- 加入4 µL 10%甲酸调节pH。
液相色谱条件
|
液相色谱系统: |
Waters ACQUITY™ Premier UPLC™系统(二元) |
|
样品瓶: |
Waters QuanRecovery MaxPeak HPS 12 × 32 mm螺纹口样品瓶(p/n:186009186) |
|
色谱柱: |
ACQUITY Premier CSH C18肽分析专用柱, 130 Å, 1.7 µm, 2.1 × 150 mm(p/n:186009489) |
|
柱温: |
60.0 °C |
|
样品盘温度: |
6.0 °C |
|
进样体积: |
100 µL |
|
流速: |
0.200 mL/min |
|
流动相A: |
0.1%甲酸的水溶液 |
|
流动相B: |
0.1%甲酸的乙腈溶液 |
梯度表
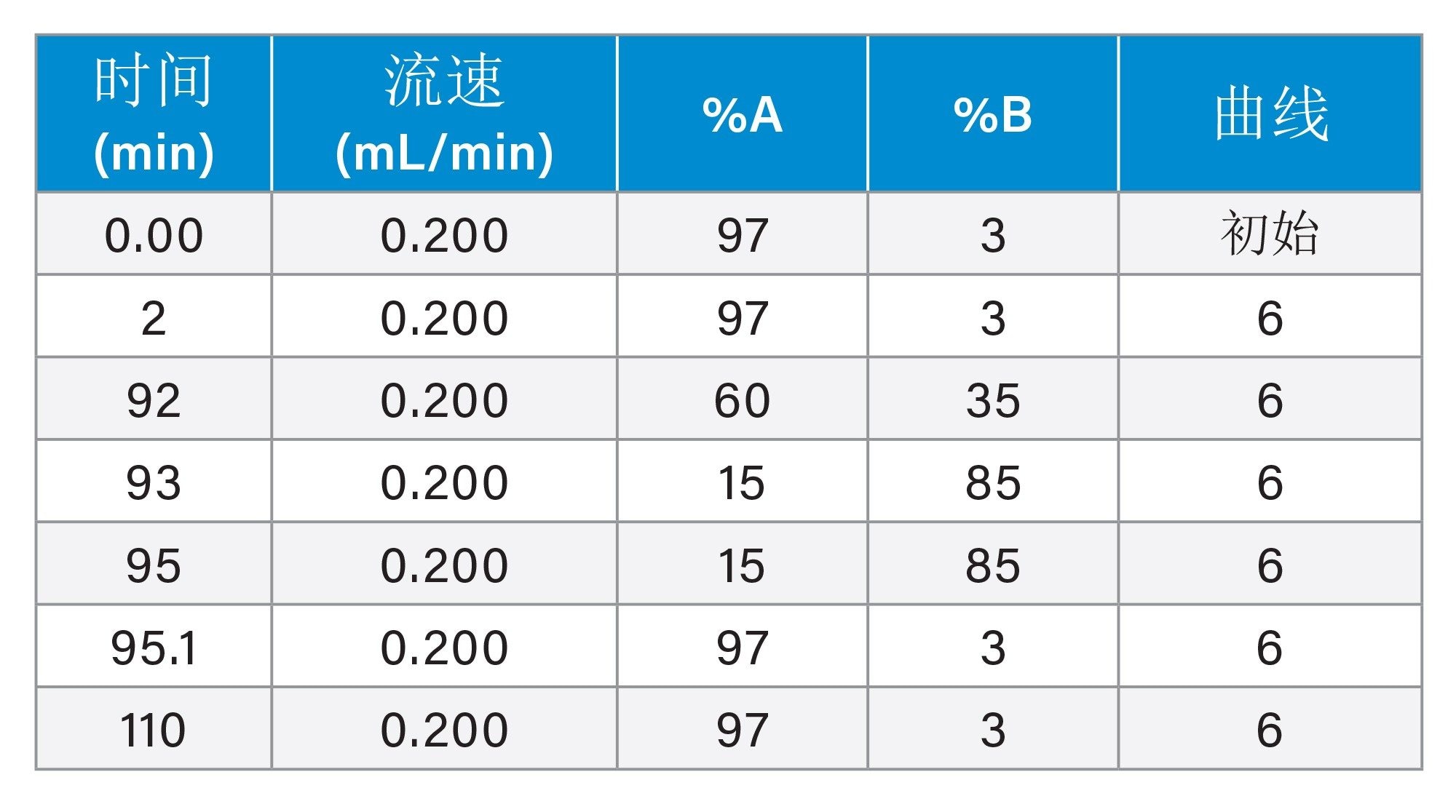
质谱条件
|
质谱系统: |
Waters Xevo MRT质谱仪 |
|
模式: |
MSE碎裂模式下的全扫描 |
|
质量范围: |
50–2000 m/z |
|
极性: |
正 |
|
扫描速率: |
2 Hz |
|
锥孔电压: |
15 V |
|
碎裂碰撞能量梯度: |
20–45 V |
|
源温度: |
120 °C |
|
脱溶剂气温度: |
450 °C |
|
脱溶剂气流速: |
800 L/h |
|
毛细管电压: |
0.5 kV |
数据分析
使用ProteinLynx Global Server 3.03(PLGS)处理MSE数据,并在经过审查且随机化的UniProt小鼠数据库(其中附加有mAb及内标物种)中进行搜索。肽鉴定标准包括1 ppm的质量精度阈值和每种蛋白质至少需要两种肽的要求。
结果与讨论
MSE (DIA)方法可同时进行蛋白质定性鉴定和非标记Hi3定量分析4,从而报告加标有标准蛋白质(已知浓度)的样品中检出的HCP蛋白质绝对含量。通过无预选地碎裂所有母离子,MSE技术实现了全面的肽段和碎片离子覆盖,可为低丰度蛋白质的检测提供高灵敏度。
HCP的鉴定基于以下搜库标准:每个蛋白需匹配两个或更多个肽,肽MS1容差为1 ppm,碎片离子MS2容差为3 ppm,检索数据库为UniProt审查的小鼠数据库(附加Waters MassPREP™标准品及mAb序列)。利用此搜索标准,鉴定了101种HCP(图2),达到约10 ppb的检测下限,总HCP含量为420 ng/mg。图2摘录了已鉴定和定量超过4个数量级的HCP。
根据NIST mAb参比物质鉴定出的101种HCP
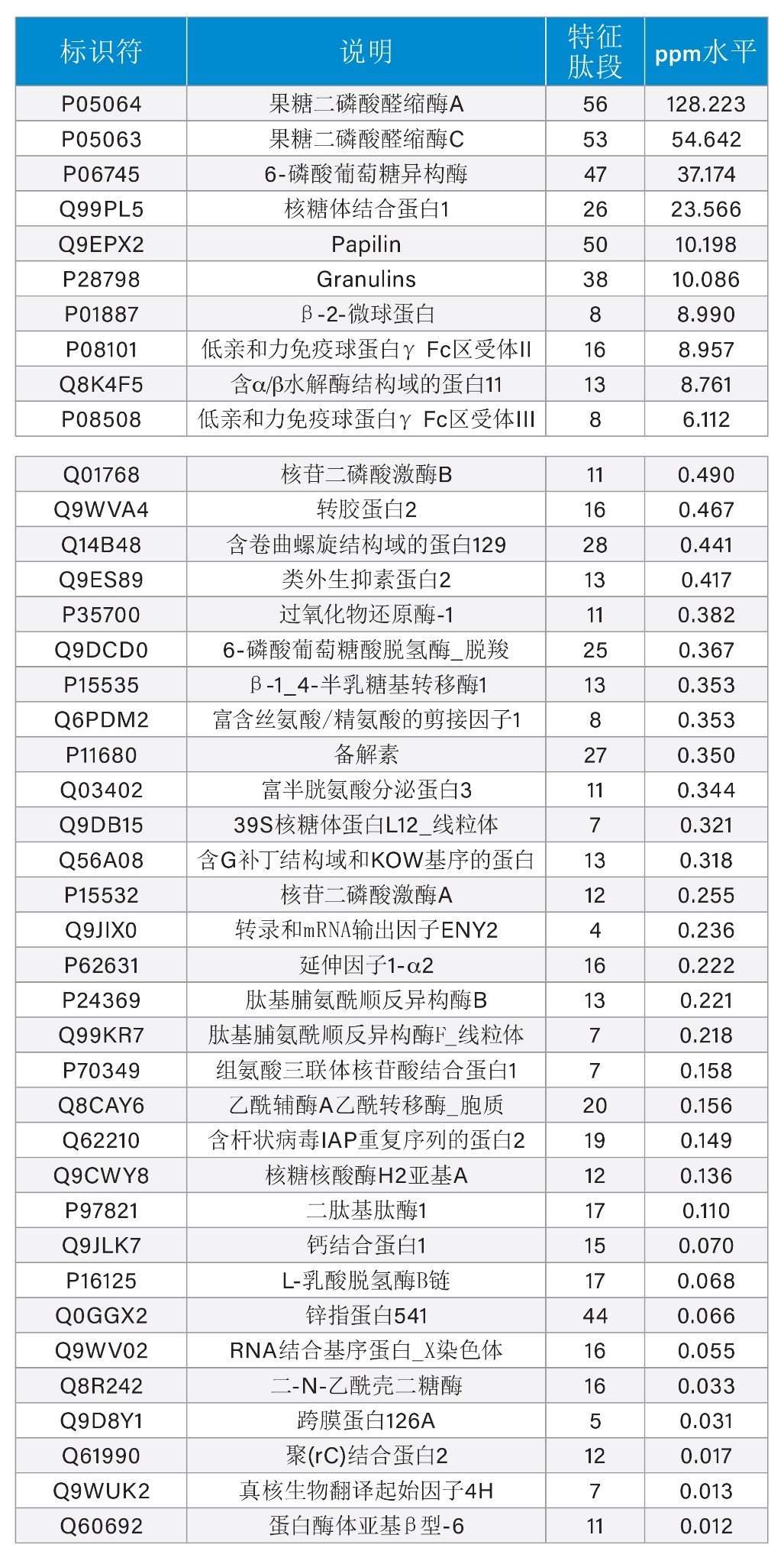
在NIST mAb样品中鉴定出的101种HCP里,有58种在亚ppm级水平下被准确定量,这充分展示了Xevo MRT质谱仪的高灵敏度(图3)。使用MSE进行分析可为HCP鉴定提供全面的数据集。该方法基于精确质量数碎片数据和MS1峰积分的精准定量,通过单次进样即可实现高序列覆盖率。MSE方法能够一致、可重现地生成母离子和碎片离子数据,使其成为跨处理步骤进行比较研究以及跨批次和处理条件进行趋势分析的理想选择。MSE分析的无偏倚特性确保了即使低丰度HCP肽也能通过特征碎片离子和特征肽得到确认,从而提升了HCP表征的深度与重现性。
NIST mAb参比物质中的HCP定量
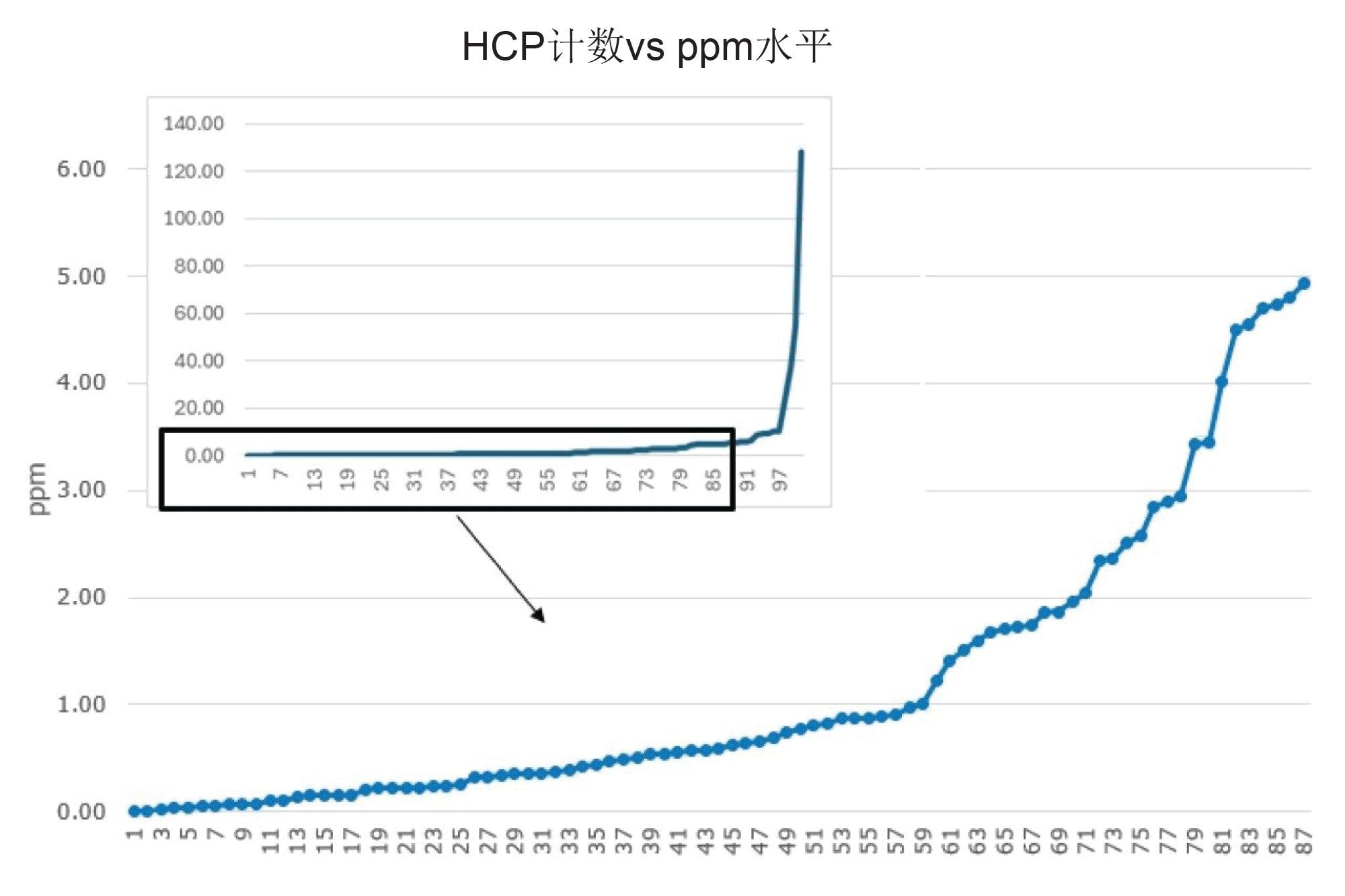
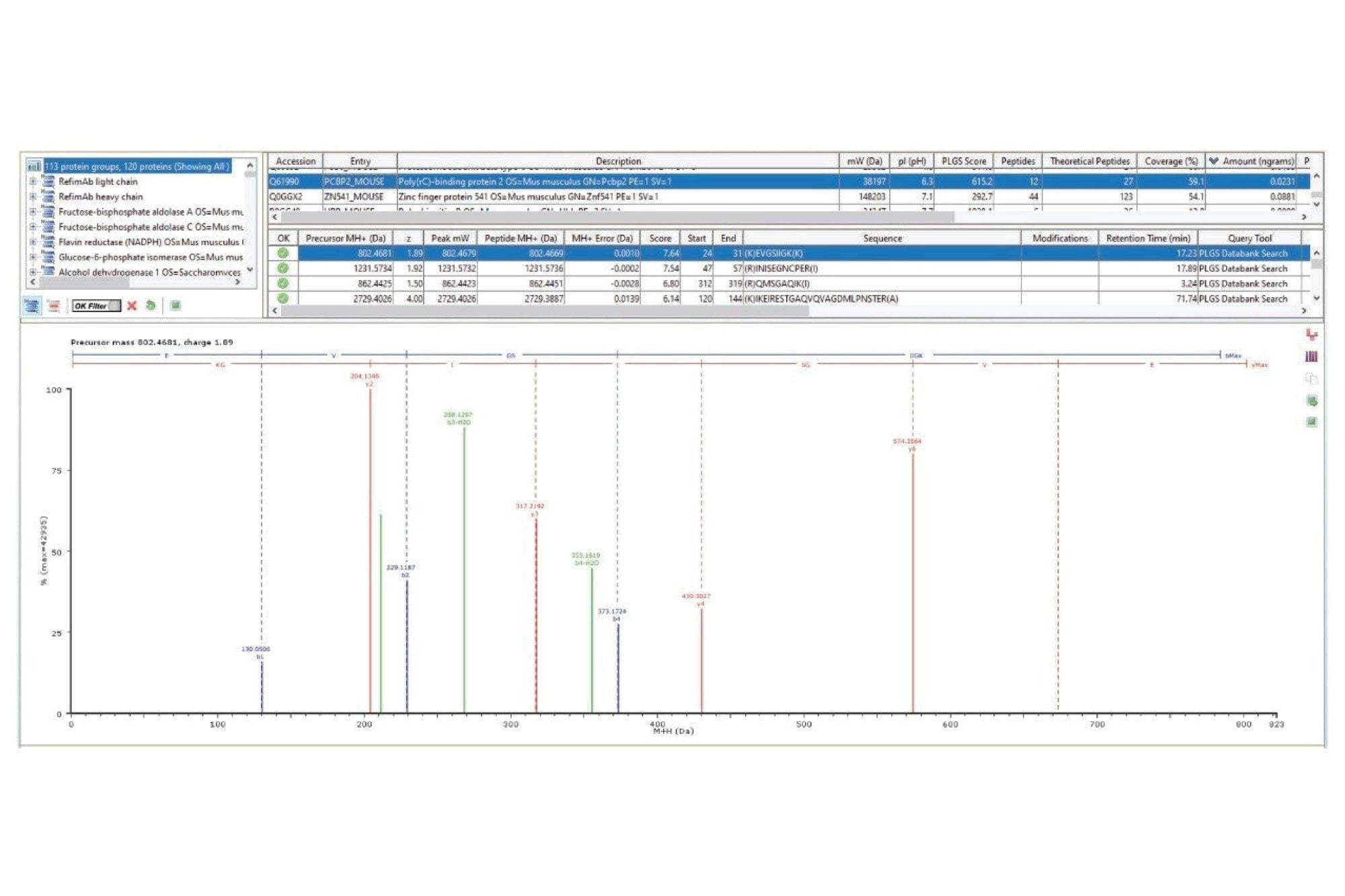
如图4所示,定量检测到一种约16 ppb的HCP(Q61990,多聚(rc)结合蛋白2)(),其肽碎片覆盖率高且匹配到大量特征肽段(12个),蛋白质的肽序列覆盖率达到59%。
蛋白质、肽和碎片离子归属
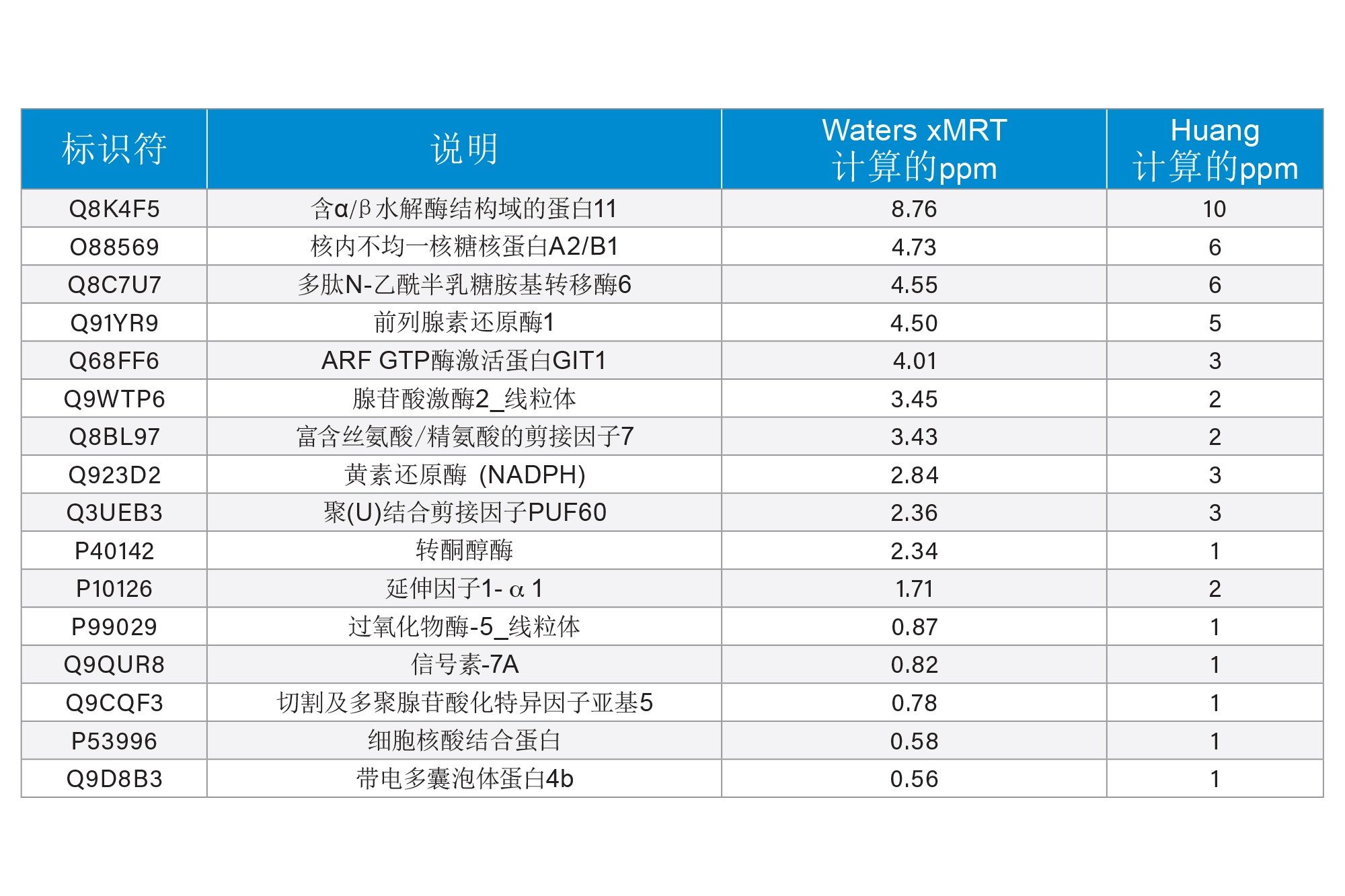
尽管本研究中分析的NIST mAb样品与文献报道(Huang等)的生产批次不同,但在共同检测到的蛋白质相对定量(ppm)结果中仍观察到高度相关性,如图5所示。
定量结果:与Huang等人的比较
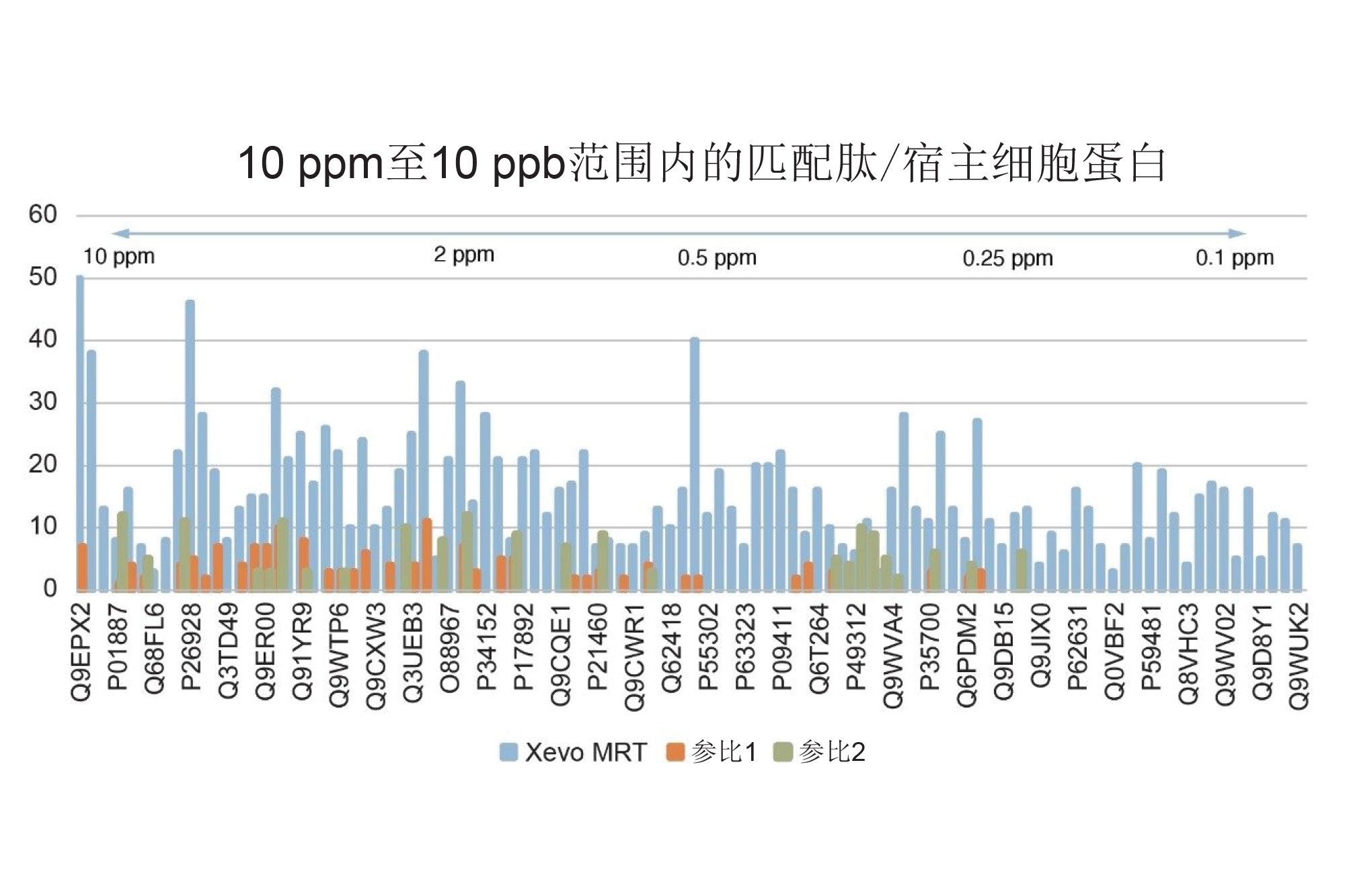
Xevo MRT质谱仪的分析结果显示,相较于既往研究(图6),该系统能够鉴定出更多HCP的特征肽段,有效提升HCP蛋白质鉴定与定量的可靠性。此外,图6显示,在HCP的整个动态浓度范围内(包括低至ppb水平的HCP),每个蛋白质均能稳定检测到大量肽段。这种广泛的肽段覆盖率对于实现稳定且可靠的HCP发现与定量至关重要,尤其是在低丰度水平下,同时凸显了LC-MS工作流程(包括样品前处理、分析、分离/检测和数据分析)的高灵敏度。
结论
Waters Xevo MRT质谱仪通过分析级LC-MS实验,在小鼠源NIST mAb样品中实现了从较高ppm至约10 ppb水平的HCP发现与定量。
- 通过LC-MSE DIA分析和Hi3定量方法,对NIST mAb参比样品的分析实现了101种HCP的鉴定与定量,动态范围跨越4个数量级(128 ppm至12 ppb)。
- 定量结果与此前针对该样品发布的HCP分析基准数据一致,验证了方法的准确度。
- 与既往研究相比,该方法大幅提升了每个HCP蛋白匹配的肽段数量,且在低至ppb水平的条件下仍能维持更高的肽段鉴定量及丰富的碎片离子归属。
综上所述,采用Waters Xevo MRT质谱仪的分析型LC-MS工作流程,使生物治疗药物开发者能够以比既往研究更高的灵敏度和准确度检测并定量宿主细胞蛋白,从而提升产品安全性,并支持快速可靠的工艺开发决策。
参考资料
- Doneanu, C. E., Gomes, A., Williams, B. J., Yu, Y. Q., & Chen, W. (2015). Enhanced detection of low-abundance host cell protein impurities in high-purity monoclonal antibodies down to 1 ppm using ion mobility mass spectrometry coupled with multidimensional liquid chromatography. Analytical Chemistry, 87(20), 10283–10291.
- Huang, L., Wang, N., Mitchell, C. E., Brownlee, T. J., Maple, S. R., & De Felippis, M. R. (2017). A Novel Sample Preparation for Shotgun Proteomics Characterization of HCPs in Antibodies. Analytical Chemistry, 89(10), 5436–5444.
- Claydon, A., Widdowson, P., & Williamson, A. (2020). Residual Host Cell Protein Analysis of NISTmAb: From Simplified Sample Preparation to Reliable Results (Application Note AN73412). Thermo Fisher Scientific.
- Wang H, Hanash S. Mass spectrometry-based proteomics for absolute quantification of proteins from tumor cells. Methods. 2015 Jun 15;81:34-40. doi: 10.1016/j.ymeth.2015.03.007. Epub 2015 Mar 17. PMID: 25794949; PMCID: PMC4678004.
720008961ZH, 2025年7月