使用多反射TOF MS技术进行先进的单克隆抗体肽图分析
摘要
肽图分析是表征和监测生物治疗药物的主要方法,尤其在单克隆抗体(mAb)等生物制药的开发中具有关键作用。该方法可在肽水平实现详细的蛋白质鉴定和序列分析,并能定位可能影响功能的预测修饰或产品相关杂质。此外,对已充分表征的生物治疗药物进行肽图分析,可作为工艺监测及后期开发产品商业化的重要工具。
在本应用简报中,我们展示了将ACQUITY™ Premier UPLC系统与采用新型多反射飞行时间技术的Xevo™ MRT多反射飞行时间(MRT)质谱仪联用,分析沃特世mAb胰蛋白酶酶解标准品的方法。在waters_connect UNIFI™应用程序中使用肽图分析工作流程执行表征。结果表明,Xevo MRT MS平台具有高灵敏度、高质量分辨率及一致的亚ppm级质量精度,结合waters_connect的一体化数据采集与处理功能,有助于我们实现高度可靠的表征能力,更快制定更优的产品与工艺开发决策。
优势
- 灵敏度高,有助于深入表征mAb以及检测低水平PTM和肽属性
- 动态范围达5个数量级,适用于复杂样品分析,轻松识别产品变体及降解物等低丰度成分
- 质量数误差始终低于1 ppm,确保产品和杂质鉴定的可靠性
简介
单克隆抗体(mAb)的肽酶解物水平分析是贯穿治疗性mAb生命周期的主要分析方法,用于确保产品质量和一致性。随着生物治疗药物产品管线的扩展,部署高可信度的自动化方法以准确、稳定地表征低水平mAb修饰变得愈发重要,这将助力高效制定产品与工艺开发决策。因此需要稳定、简便易用的分析平台,以便轻松部署到组织内各实验室1。
Xevo MRT MS系统正是此类平台的典范。该系统采用创新的四极杆-多反射飞行时间设计,通过延长离子飞行路径,在50 Hz扫描速率下实现高达100K的质量分辨率,并配备双增益ADC检测器,可提供更高的灵敏度、动态范围及亚ppm级质量精度,确保可靠的肽图分析。合规的waters_connect软件与UNIFI应用程序实现了自动化数据采集、处理及报告,而一体化的自动工作流程进一步提升了LC-MS分析的可及性,使分子研究能够突破传统MS核心实验室的限制,覆盖从早期到扩展阶段的产品表征。

实验
样品
沃特世mAb胰蛋白酶酶解标准品(P/N:186009126)用于在执行肽水平蛋白质分析时进行LC-MS性能基准测试并确保系统适用性。此冻干标准品含有NIST参比物质8671(NIST mAb,一种由鼠细胞系表达的人源IgG1κ)的还原和烷基化胰蛋白酶酶解物。
为制备mAb样品,向含40 µg酶解物的样品瓶中加入200 µL超纯Milli-Q水,得到浓度为200 ng/µL的溶液。随后将该样品稀释成一系列浓度,以评估色谱柱载样范围在2000 ng至0.002 ng之间的性能表现。
液相色谱条件
|
液相色谱系统: |
ACQUITY Premier UPLC系统(二元系统) |
|
检测: |
UV 280 nm |
|
样品瓶: |
TruView™ LCMS认证12×32 mm螺纹口全回收样品瓶,配有瓶盖和预切割PTFE/硅胶隔垫(P/N:186005663CV) |
|
色谱柱: |
ACQUITY Premier BEH™ C18, 1.7 µm 2.1 mm x 100 mm(P/N:186009453) |
|
柱温: |
40.0 °C |
|
样品温度: |
6.0 °C |
|
进样体积: |
0.2~10 µL |
|
流速: |
0.250 mL/min |
|
流动相A: |
0.1%甲酸的水溶液 |
|
流动相B: |
0.1%甲酸的乙腈溶液 |
梯度表
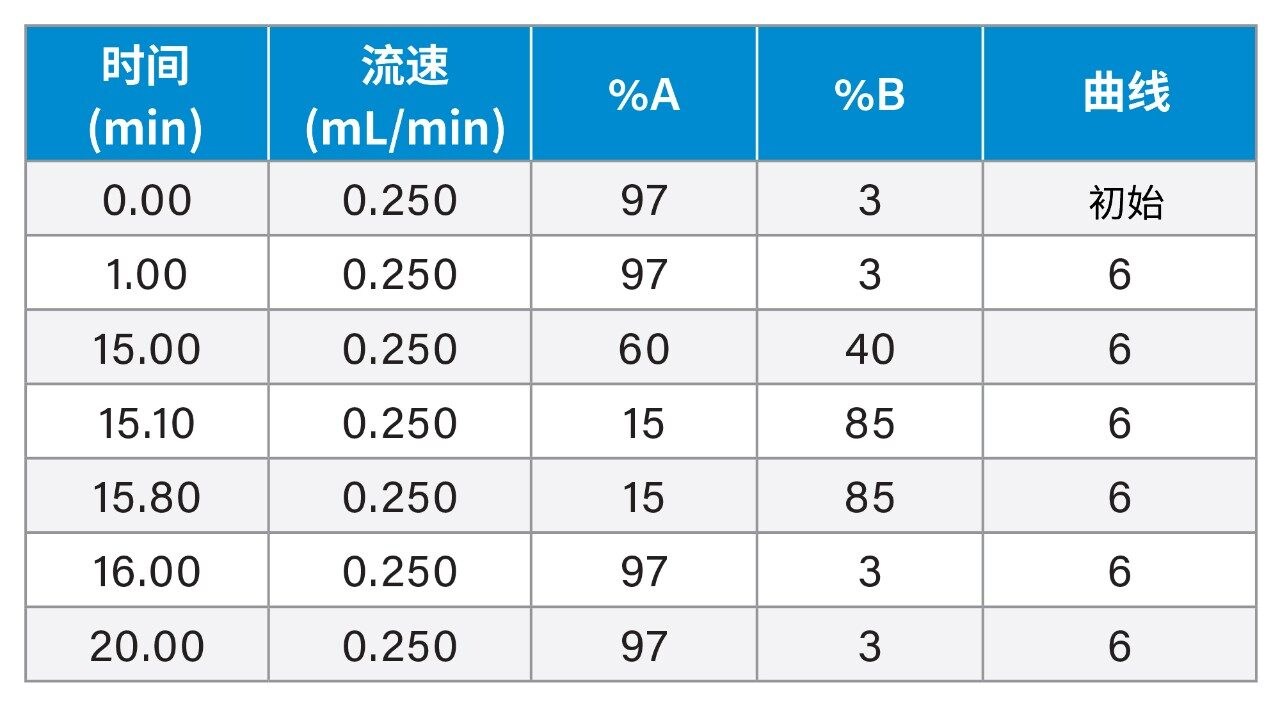
质谱条件
|
质谱系统: |
Xevo MRT MS |
|
模式: |
MSE碎裂模式下的全扫描 |
|
质量范围: |
50~2000 m/z |
|
极性: |
+ve |
|
扫描速率: |
2 Hz |
|
锥孔电压: |
25 V |
|
碎裂碰撞能量梯度: |
25~50 V |
|
离子源温度: |
120 °C |
|
脱溶剂气温度: |
400 °C |
|
脱溶剂气流速: |
800 L/h |
|
毛细管电压: |
3.00 kV |
结果与讨论
本研究在UPLC-Xevo MRT MS系统上采集NIST mAb酶解标准品的肽图分析数据,旨在评估整体工作流程性能并报告特定的仪器功能(质量精度、质量分辨率和灵敏度)。在MSE数据非依赖型碎裂模式下采集数据,以分配肽并定位所分配修饰的位点。
使用waters_connect UNIFI应用程序的肽图分析工作流程进行自动化数据处理,轻链和重链均实现了高序列覆盖率(96% LC,98% HC),质量数误差容差小于1 ppm。图2、图3和图4展示了肽图分析实验的输出结果。
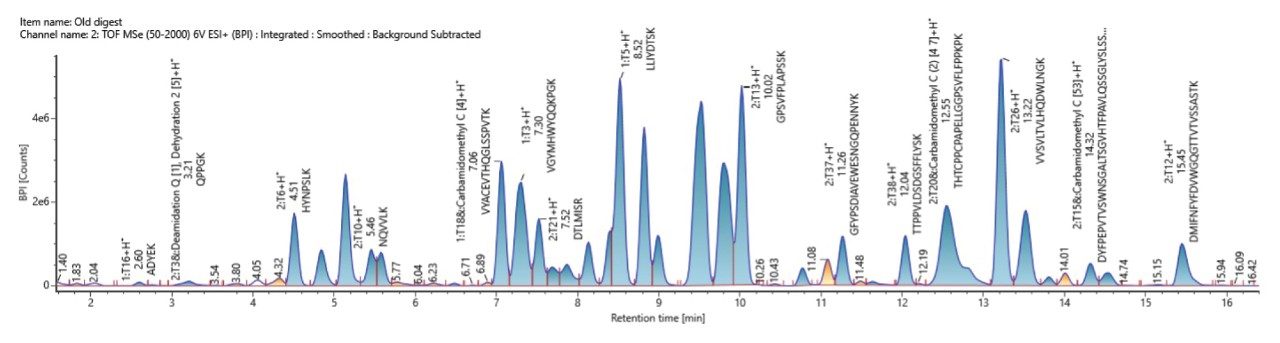

通过与NIST mAb的计算机模拟酶解结果比对,同时考虑方法中定义的修饰,生成的分配肽列表如图4所示。此列表可以按强度、质量数容差和匹配碎片离子的数量进行筛选和排序。高排名的分配肽段均具有小于1 ppm的质量数误差,并通过数据非依赖型MSE碎裂获得的大量b/y碎片离子进一步确认2,3,4。
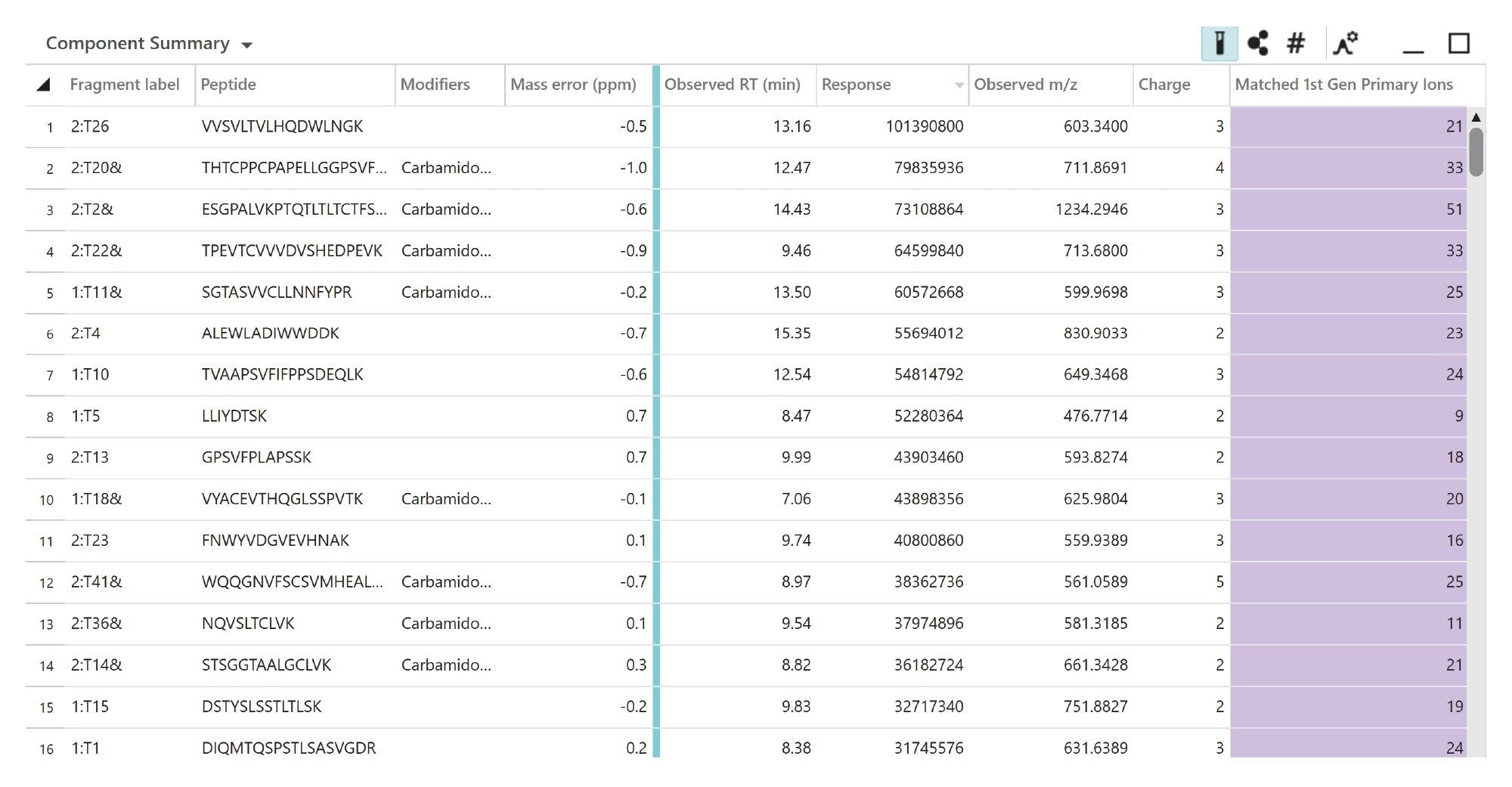
利用MSE进行肽图分析可以为蛋白质表征提供全面的数据集。与传统的数据依赖型采集方法不同,MSE采用数据非依赖型采集,可在单次运行中捕获所有MS1肽离子对应的MS2碎片离子。该方法通过精确质量数碎片离子数据实现高序列覆盖率,并通过MS1峰定量实现准确定量,且仅需单次进样。MSE方法能够常规、可重现地生成母离子和碎片离子数据,使其成为蛋白质药物产品或原料药中肽离子分配、产品相关异构体和杂质相对定量的理想选择。MSE的无偏倚特性甚至可对低丰度肽进行特征碎片确认,提升mAb表征的深度与重现性。
图5展示了DTLMISR肽的分析结果,其天然肽段与氧化变体均以亚ppm级质量精度检出。DTLMISR肽的氧化变体洗脱时间较早(保留时间6.48分钟),而未修饰肽段为7.52分钟。高质量的MSE碎片离子谱图显示,y4、y5及母离子均出现+15.9949 Da的质量数漂移,表明甲硫氨酸残基发生了氧化。
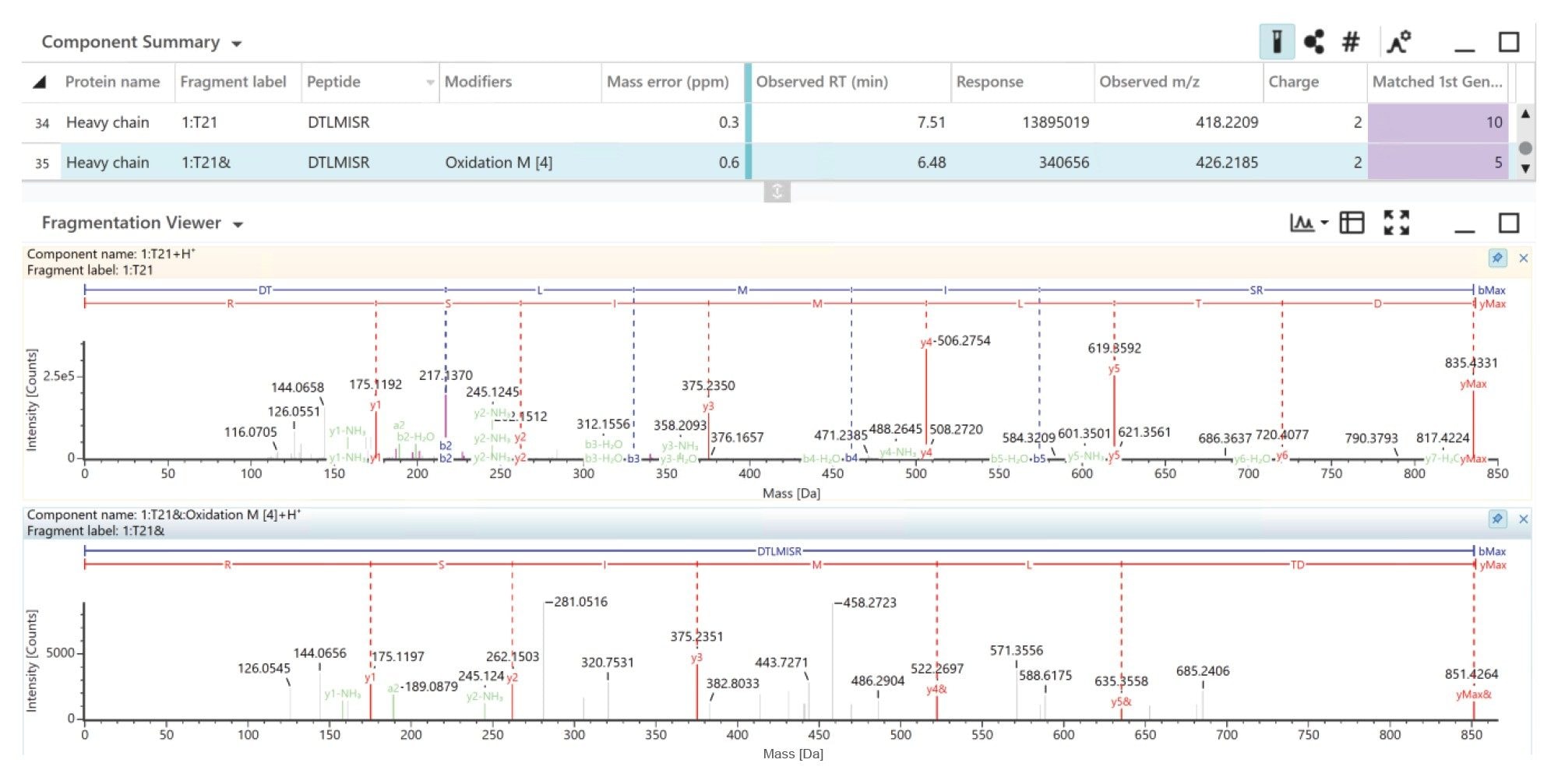
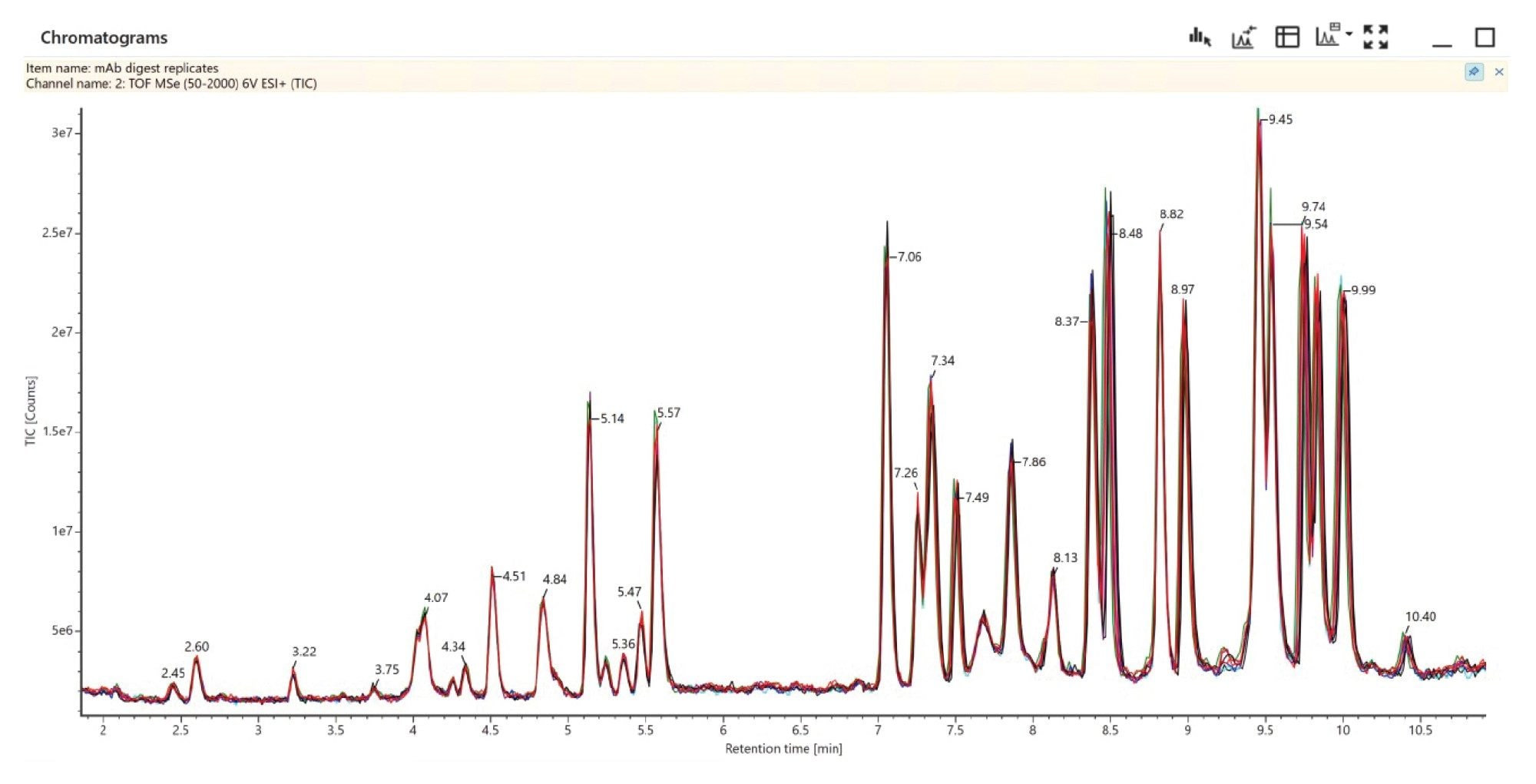
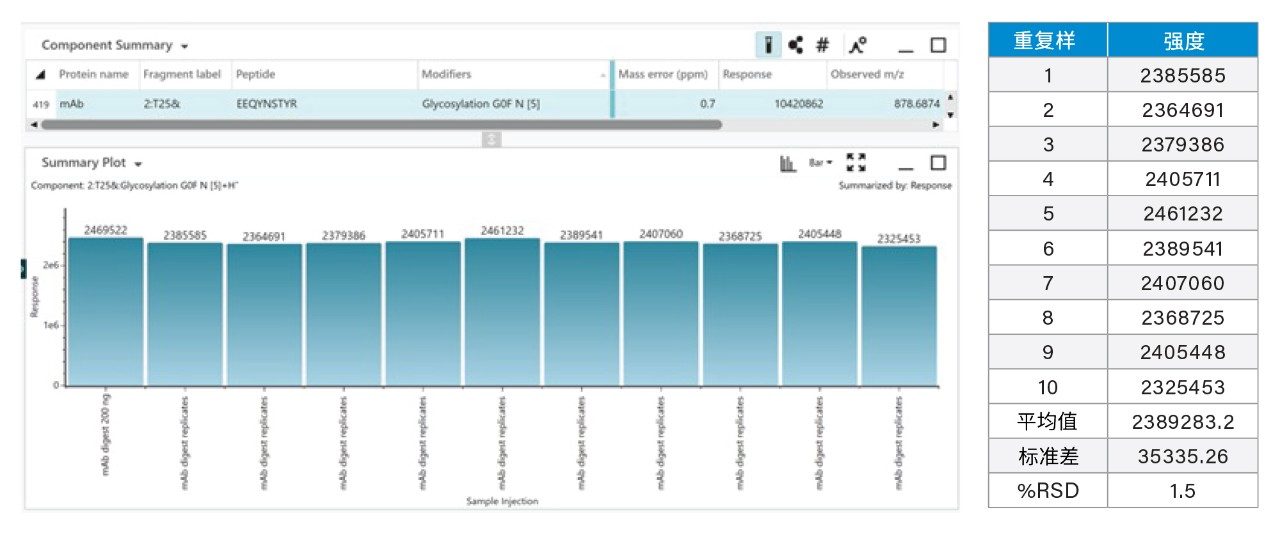
图6展示了10次重复进样中T25糖肽(G0F)的响应叠加色谱图,色谱峰高度重叠,证明数据非依赖型LC-MSE肽图分析方法与生俱来的重现性。色谱图显示10次进样中的UPLC色谱分离结果及LC-MS检测响应保持一致。图7进一步展示了HC T25糖肽G0F在重复进样中的MS1总响应,强度RSD为1.5%。
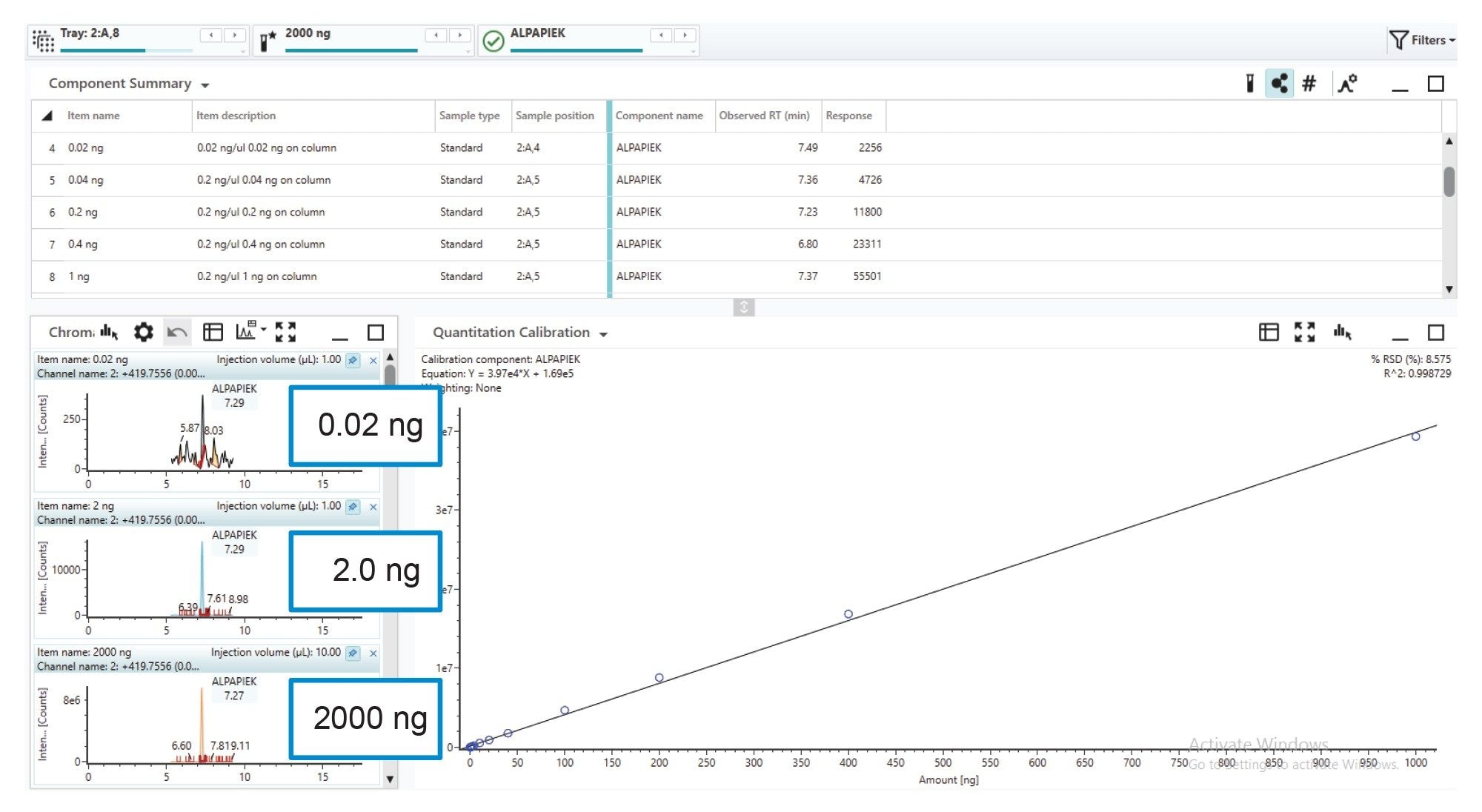
全面的蛋白质杂质分析至少需要四个数量级的动态范围,以满足胰蛋白酶解肽的不同电离势,并在较宽的相对浓度范围内检测和定量修饰肽。图8的稀释系列显示了mAb酶解标准品在色谱柱载样为2000 ng、2 ng和0.02 ng(五个数量级)酶解物时,选定肽的提取离子流色谱图及线性MS1响应(1000 ng~0.02 ng范围内呈线性)。
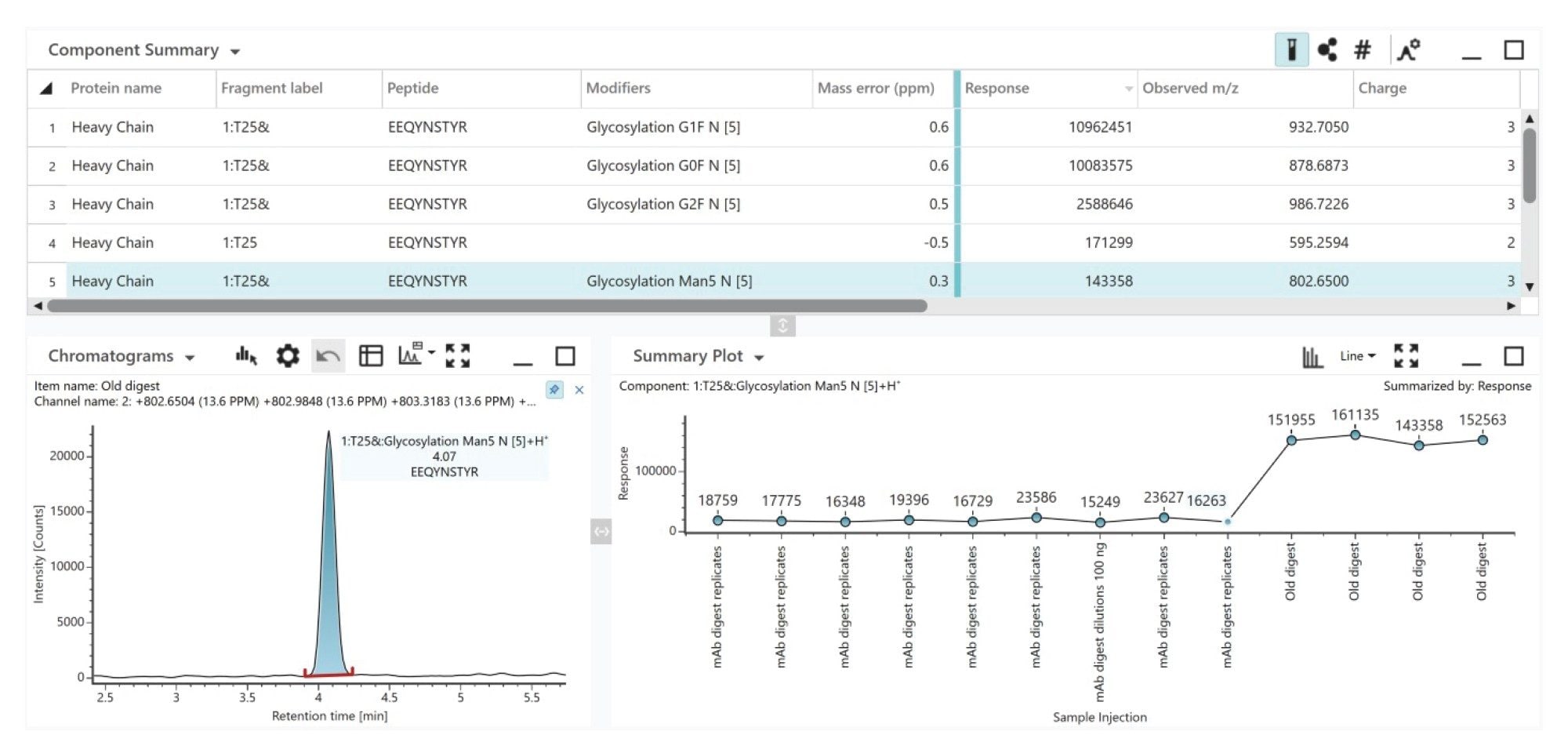
定位和分析糖基化位点对于了解单克隆抗体(mAb)的生物活性、安全性和治疗效果至关重要。本文展示了Xevo MRT MS系统的肽图分析工作流程如何为NIST mAb标准品提供一致的糖肽MS响应,如图9所示,分配糖肽的质量数误差小于1 ppm。这种一致性使我们能够观察到两个mAb批次间目标T25 Man5糖肽的不良Man5水平趋势变化。
结论
Xevo MRT质谱仪能够为肽类生物治疗药物的表征提供诸多优势,对产物变体及杂质实现高置信度的序列确认和分配。其高性能的多反射飞行时间(MRT)技术可提供亚ppm级质量精度,确保利用母离子和碎片离子数据实现可靠的肽段分配;同时,其检测肽离子的有效质量分辨率接近100,000 FWHM,且不受扫描速度和m/z值影响,从而确保在整个图谱范围内实现精准、可靠的分析物鉴定。
这种出色的MS检测性能辅以waters_connect信息学平台上UNIFI应用程序内简化的自动化合规工作流程,支持一体化数据采集、处理、审查和报告,可从单个样品采集肽图分析数据,并涵盖更大样品组的汇总分析。
总体而言,Xevo MRT质谱仪可提供一个稳定高效的平台,能够提供可靠的实验结果,助力生物制药分析人员在生物治疗药物的开发与商业化方面做出自信的决策。
如需了解更多信息,敬请访问Xevo MRT质谱仪。
参考资料
- European Medicines Agency (EMA). (2016). Guideline on development, production, characterisation and specification for monoclonal antibodies and related products. EMA/CHMP/BWP/532517/2008.EMA website.
- Nilini Ranbaduge, Henry Shion, Ying Qing Yu.使用BioAccord系统进行常规肽图分析.沃特世应用纪要, 720006466ZH.2019年.
- Kellen DeLaney, Samantha Ippoliti, Lisa Reid, Owen Cornwell, Ying Qing Yu, Emma Harry, Mark Towers.在Xevo™ G3 QTof平台上应用肽图分析和多属性方法(MAM)工作流程执行mAb药品的生物类似药比较. 沃特世应用纪要720007632ZH.2022年.
- Vera B. Ivleva, Ying Qing Yu, Scott J. Berger, Weibin Chen.Generating Automated and Efficient LC-MS Peptide Mapping Results with the Biopharmaceutical Platform Solution with UNIFI Waters Application Note 720004620.2013.
720008737ZH,2025年3月