将方法从ACQUITY™ UPLC™“经典”系统迁移至ACQUITY Premier系统(FL)
摘要
在药品生命周期管理中,建议通过发现改进机会来提高药品安全性并且不断扩展药品生产知识体系。本研究展示了如何将肽图分析方法从传统系统(ACQUITY UPLC“经典”系统)成功迁移到采用MaxPeak™高性能表面(HPS)的ACQUITY Premier系统(固定定量环设计)。减少分析物/表面吸附干扰有助于减少峰拖尾并提高关键质量属性的回收率,从而更好地管理生物治疗药品的生命周期。
优势
ACQUITY Premier系统的固定定量环设计具有以下优势:
- 性能一致且可靠,能够提供可重现的结果
- 从传统ACQUITY UPLC“经典”系统实现无缝方法迁移
- MaxPeak HPS技术可减少峰拖尾并提高金属敏感分析物的回收率
简介
生命周期管理在药品生产中发挥着关键作用。
作为该过程的一部分,ICH指南建议以反馈/前馈方式识别和评估改善药物安全性的机会,以不断扩展药品生产的知识体系1。 这个过程可以应用于过时的分析方法和仪器。新技术带来了更快速、更稳定、更灵敏的分析能力,无论是制造商还是消费者,都能从更高的结果可信度和效率中获益。最近,沃特世公司推出了采用MaxPeak HPS的ACQUITY Premier系统,该系统进一步改善了Waters LC产品组合的色谱性能。MaxPeak HPS经过精心设计,可减少分析物/表面相互作用,从而减少峰拖尾和分析物回收率降低等吸附干扰。作为该产品的一部分,ACQUITY Premier系统现在采用固定定量环设计,通过将这种创新的表面技术运用于产品线中,供科学家充分利用。
本研究的目的是证明采用固定定量环设计的ACQUITY Premier系统可以成功迁移ACQUITY UPLC“经典”系统等传统系统的肽图分析方法,同时利用MaxPeak HPS技术提供额外的色谱性能优势。
实验
MS级水和乙腈购自Honeywell Burdick and Jackson。MS级甲酸购自Thermo Scientific™。使用购自沃特世公司的mAb胰蛋白酶酶解标准品(P/N:186009126),用0.1%甲酸水溶液制备浓度为0.8 mg/mL的样品。
液相色谱条件
|
液相色谱系统: |
ACQUITY Premier系统(BSM-FL变式) ACQUITY UPLC系统 |
|
检测: |
ACQUITY TUV, FC=Ti 5 mm, λ=214 nm |
|
样品瓶: |
QuantRecovery™ MaxPeak样品瓶(P/N:186009186) |
|
色谱柱: |
ACQUITY UPLC CSH™ C18色谱柱, 130 Å, 1.7 µm, 2.1 x 100 mm, (P/N:186005297) ACQUITY Premier CSH C18, 130 Å, 1.7 µm, 2.1×100 mm肽分析专用柱(P/N:186009488) |
|
柱温: |
60 °C |
|
样品温度: |
10 °C |
|
进样模式: |
PLUNO |
|
进样定量环: |
10 µL |
|
进样体积: |
5 µL |
|
弱清洗溶剂体积: |
600 µL |
|
强清洗溶剂体积: |
200 µL |
|
流速: |
0.200 mL/min |
|
流动相A: |
水,0.1%甲酸 |
|
流动相B: |
乙腈(0.1%甲酸) |
|
弱清洗液: |
50:50 乙腈:水 |
|
强清洗液: |
50:50 乙腈:水 |
|
密封清洗液: |
20:80 乙腈:水 |
梯度
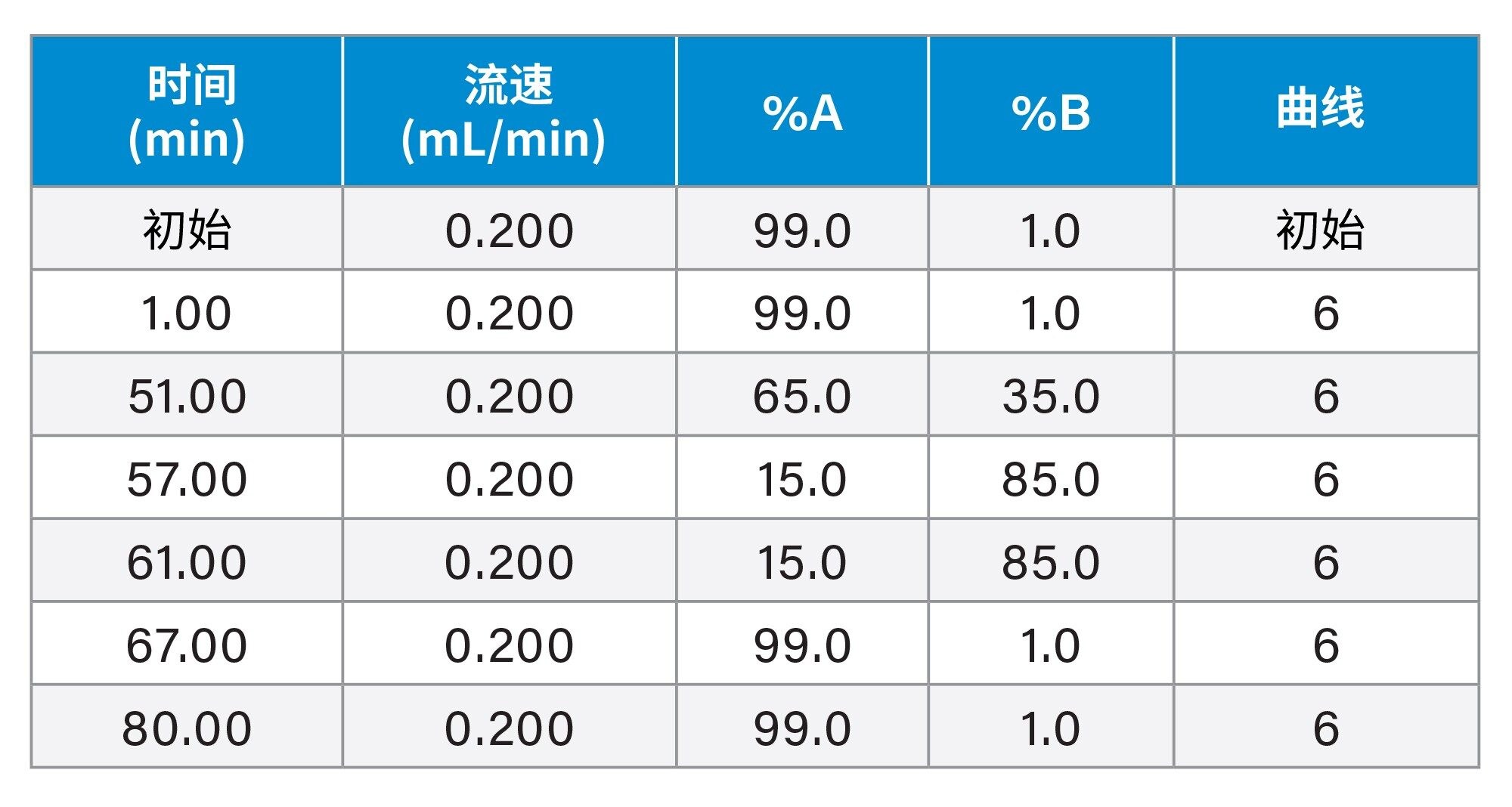
质谱条件
|
MS系统: |
ACQUITY QDa™质谱检测器 |
|
扫描模式: |
阳性,全扫描 |
|
扫描范围: |
350-1250 m/z |
|
采集速率: |
5 Hz |
|
探头温度: |
600 °C |
|
毛细管电压: |
1.5 kV |
|
锥孔电压: |
15 V |
数据管理
|
色谱软件: |
Empower™ 3, FR4 |
结果与讨论
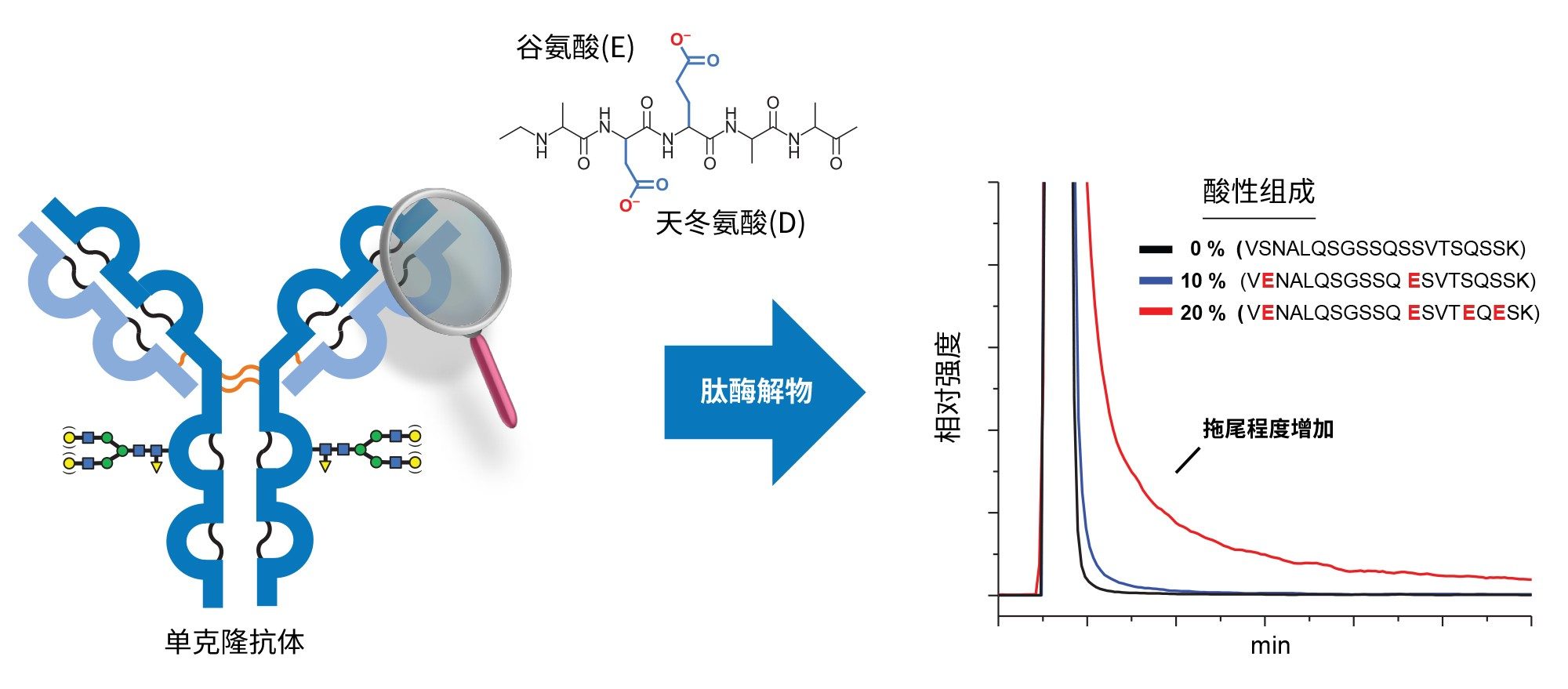
在本方法迁移研究中,我们选择单克隆抗体酶解物的肽图分析作为代表性方法,旨在考验该系统是否能以较低的流速为复杂样品提供准确的梯度组成。选择肽图分析的原因不仅仅是因为其分离难度,还因为肽分析在蛋白类治疗药物的表征和质量控制中非常常见。在这方面,肽图分析可作为一种替代方法,证明ACQUITY Premier能够广泛应用于产品的开发和生产流程。最后,对于蛋白类治疗药物的主要组成部分 — 酸性氨基酸而言,MaxPeak HPS技术有一种固有的优势。蛋白质中天然存在的酸性残基(例如谷氨酸或天冬氨酸)可能带负电荷,这会导致肽吸附到金属表面从而发生峰拖尾,如图1所示。其在生物治疗方面的重要性在于,天冬酰胺脱酰胺化形成天冬氨酸和异天冬氨酸,是单克隆抗体(mAb)中常见的翻译后修饰,与药物疗效相关。鉴于此,本案例研究不仅要证明方法等效性,还要证明MaxPeak HPS技术在这些分析中的价值,即减少不良吸附干扰从而改善药品生命周期管理。
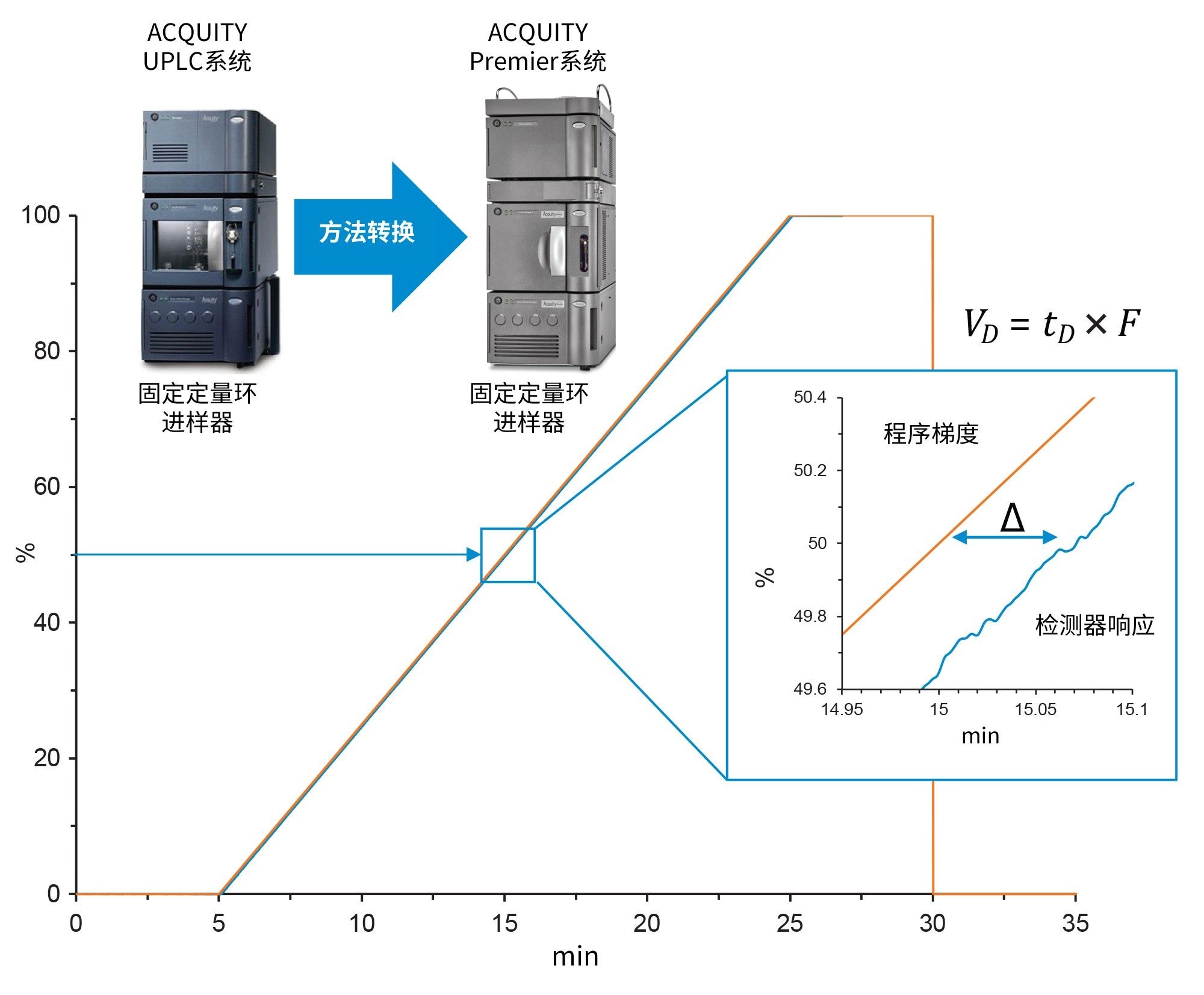
就后者而言,配备固定定量环样品管理器的ACQUITY Premier系统经过专门设计,其进样针设计和系统延迟体积与之前的ACQUITY UPLC“经典”系统非常接近,有助于更轻松地迁移传统方法。如图2所示,两个系统均采用简单的梯度,在25 min内将流动相B从5%增加至95%,并使用咖啡因测定系统延迟体积2。 利用插图中所示的检测器响应与程序梯度之间的差异,确定ACQUITY Premier系统的延迟体积(158.8 µL)与ACQUITY UPLC系统的延迟体积(149.4 µL)相差不超过10 µL。这种接近等效的结果意味着,在系统之间迁移方法时,几乎不需要改变梯度即可获得相同的分离效果。为突出这一优势,图3显示了在两套系统上使用相同的色谱柱和方法运行的mAb胰蛋白酶酶解标准品的肽图。如图所示,在不修改方法的情况下,在整个色谱图中选择的22个肽峰的肽图谱在峰保留时间和相对强度方面非常一致。
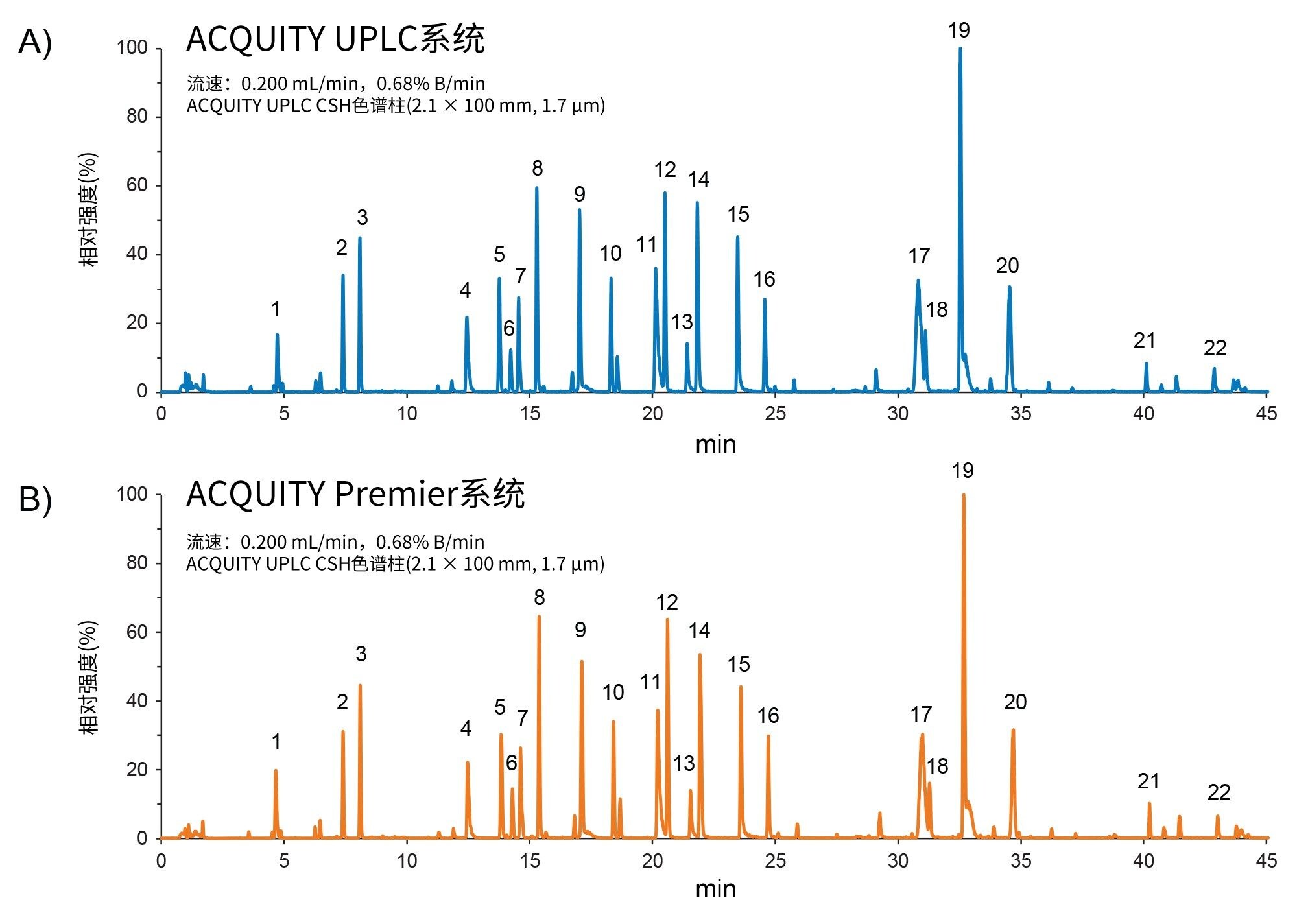
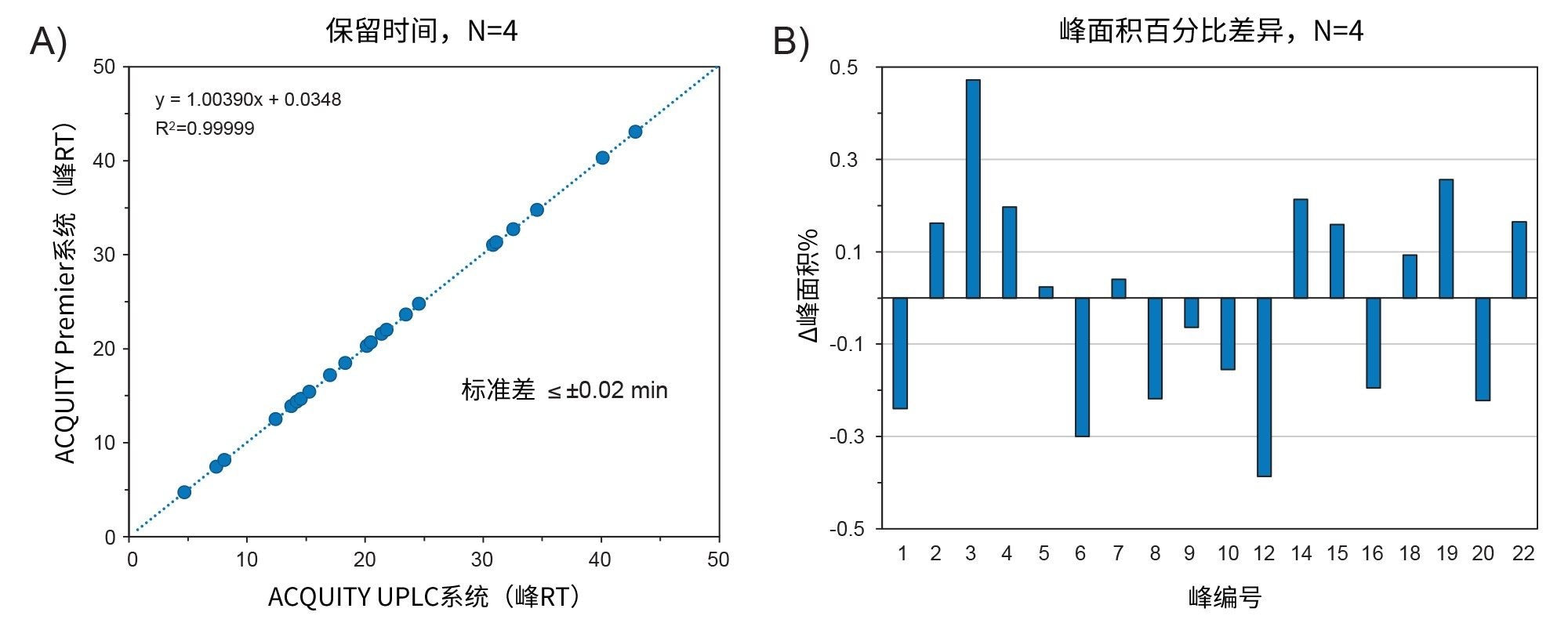
为评估方法等效性,使用通过两套系统获得的数据绘制了所示22个峰的保留时间正交图。如图4A所示,正交图表现出线性响应,斜率约为1.00,y轴截距接近零(0.003),表明ACQUITY Premier系统能够重现与ACQUITY UPLC系统相同的选择性和保留时间。此外,如图4B所示,系统之间的峰面积保持不变,相对峰面积差异在0.5%以内。这些结果表明,ACQUITY Premier系统能够可靠地重现ACQUITY UPLC系统的传统方法,促进方法的无缝迁移。
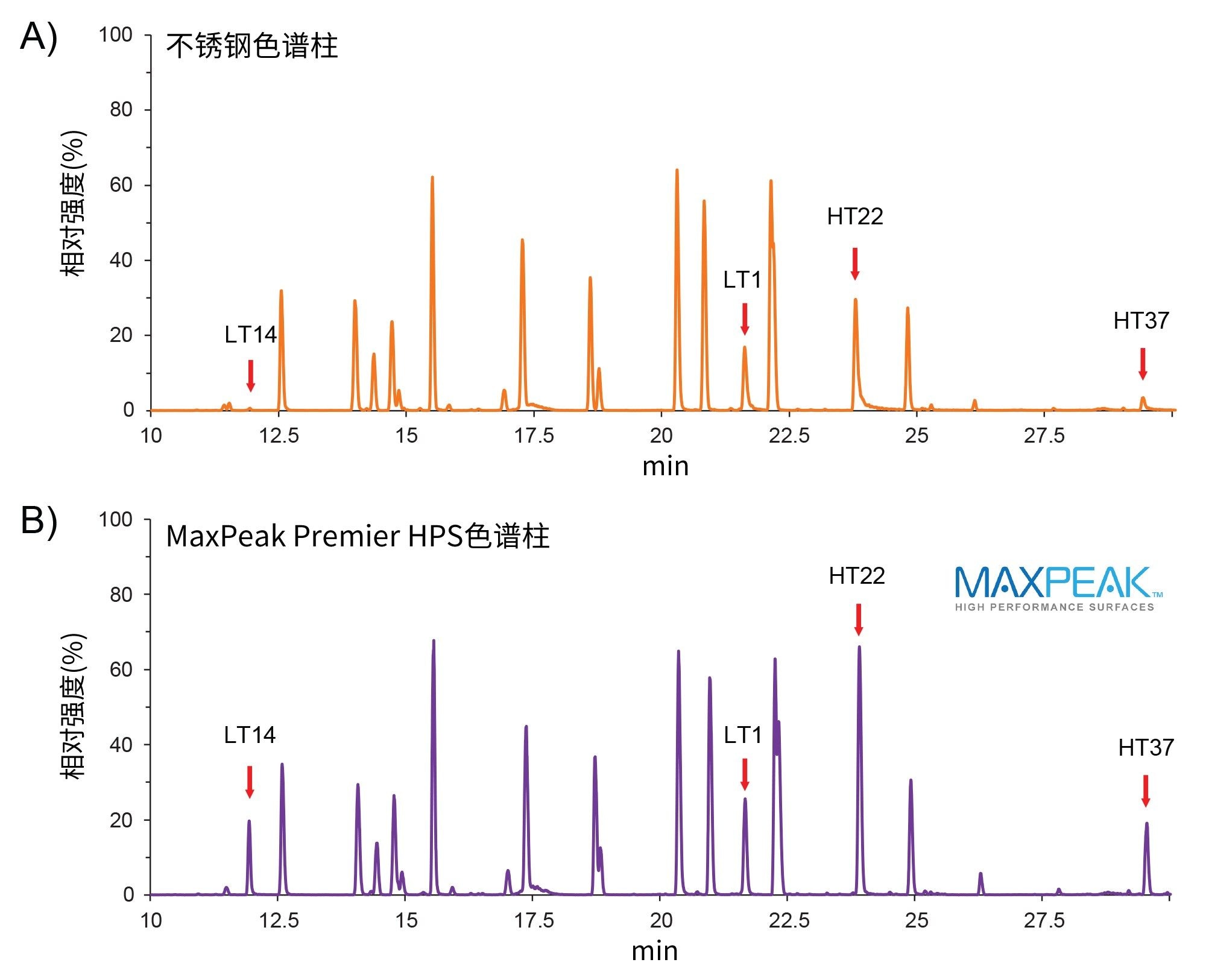
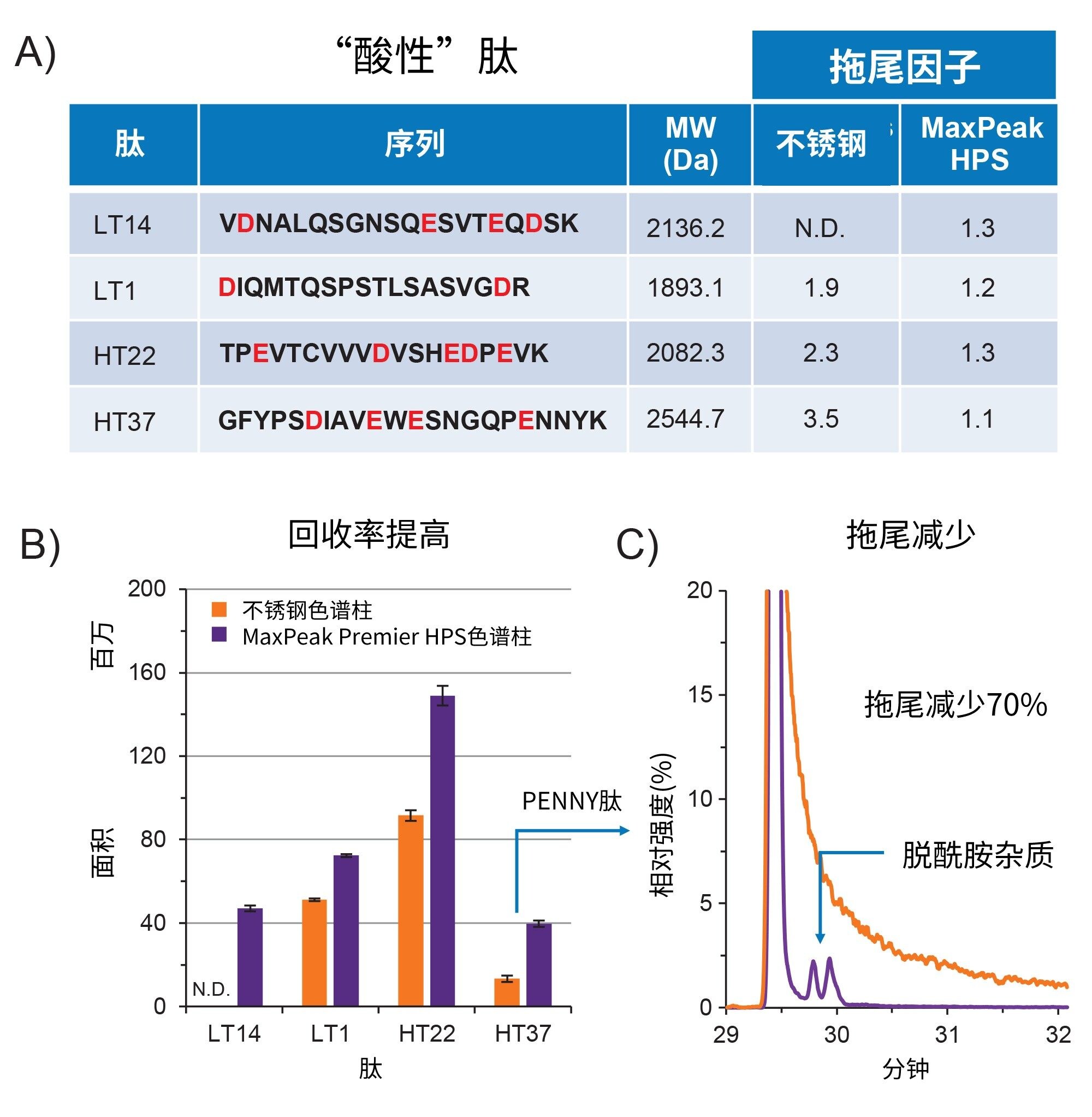
在确立系统之间的可比性后,下一个问题是确定MaxPeak HPS技术是否能为肽图分析提供额外的优势。本实验分别使用采用和未采用MaxPeak HPS技术的CSH色谱柱在ACQUITY Premier系统上执行相同的肽图分析。如图5所示,使用搭载MaxPeak HPS技术的色谱柱时,有四个肽峰的峰拖尾明显改善。进一步研究发现,这4个肽峰包含2–4个“酸性”氨基酸残基,如图6A表格中的序列所示。如条形图所示(图6B),在所有四个峰中均观察到峰拖尾减少,峰面积回收率得以提高。最值得注意的是,使用不锈钢色谱柱时,LT14肽片段的回收率低于检测阈值。此外,酸性肽的拖尾减少且回收率更高,有助于鉴别与关键质量属性相关的杂质。图6C所示的与关键质量属性相关的“penny”肽(一种已知会影响mAb药物产品疗效的肽)的脱酰胺物质证明了这一点3。 在本例中,观察到原型峰的峰拖尾减少70%,从而能够检测到相关的脱酰胺杂质。这些结果证明了MaxPeak高性能表面在肽图分析中的价值及其在改善生物药物生命周期管理方面的潜力。
结论
在药品生命周期管理中,建议通过发现改进机会来提高药品安全性并且不断扩展药品生产知识体系。采用MaxPeak HPS的ACQUITY Premier系统能够减少分析物/表面相互作用并改善色谱性能,这是分离科学的一次创新性飞跃。通过在ACQUITY Premier系统产品组合中引入固定定量环设计,科学家现在可以充分利用这种创新的表面技术对传统方法进行现代化改进,开发出更快速、更稳定、更灵敏的分析方法,从而更好地保护药品的消费者安全。
参考资料
- Guidance for industry Q10 pharmaceutical quality system.ICH, 2009.
- P. Bigos, R. Birdsall, Y. Yu.使用Waters方法转换计算器通过自动方法缩放获得等效的IEX色谱性能.沃特世应用纪要, 720007807ZH.2022年.
- Chelius D, Rehder DS, Bondarenko PV.Identification and Characterization of Deamidation Sites in the Conserved Regions of Human Immunoglobulin Gamma Antibodies. Anal. Chem. 77: 6004 2005.
720007935ZH,2023年7月