在临床研究中使用Xevo™ TQ Absolute搭配Capitainer® B设备对全血中的免疫抑制药物进行LC-MS/MS分析
仅供研究使用,不适用于诊断。
摘要
本文介绍了一种从干血斑(收集移液的少量人全血而得)中进行液液萃取的临床研究方法。
优势
- 在小体积样品分析中使用Xevo TQ Absolute具有良好的分析灵敏度
- 色谱和质谱检测具有良好的分析选择性,分析运行时间更短,并且能够同时分析四种分析物
- Capitainer B设备的样品体积小,可提供良好的精密度和准确度
简介
Deprez等人之前已经展示了一种准确、可重现的LC-MS/MS方法,分析少量全血样品中的环孢霉素、依维莫司、西罗莫司和他克莫司,方法是将样品移液到Capitainer B设备的入口处,即可生成已知体积的干血斑1。
本文介绍了一种从干血斑(收集移液的少量人全血而得)中进行液液萃取的临床研究方法。在Waters ACQUITY UPLC I-Class PLUS上使用Waters™ ACQUITY™ UPLC™ HSS C18 SB色谱柱,可在1.5分钟内完成色谱洗脱。同时分析所有四种分析物,然后使用Xevo TQ Absolute质谱仪(图1)进行检测,进样间隔时间为2.2分钟。

实验
样品前处理
使用含有环孢霉素、依维莫司、西罗莫司和他克莫司的全血MassTrak免疫抑制剂标准曲线样品和质控品套装。分别使用2H12-环孢霉素、13C22H4-依维莫司、2H3-西罗莫司和子囊霉素作为内标。
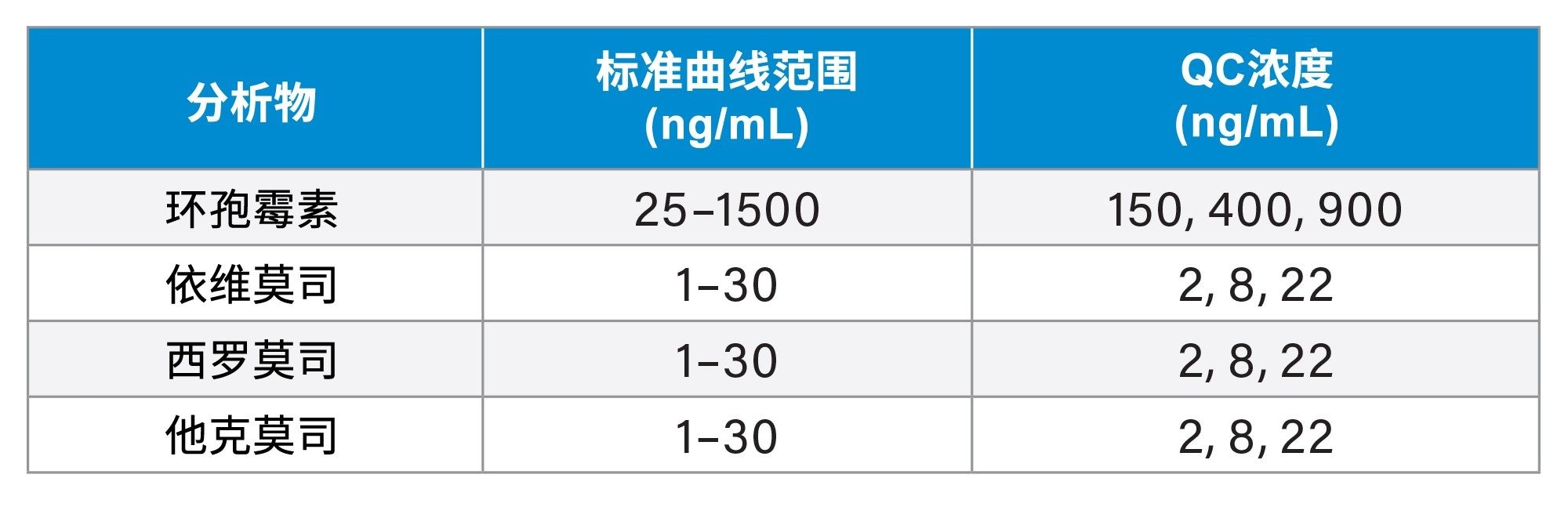
标准曲线样品和QC样品浓度(低浓度、中浓度和高浓度)详见表1。
样品萃取
移取30 μL样品至设备入口,检查是否形成了可用的10 μL干血斑,然后放置过夜,等待其干燥。将干血斑转移到微量离心管中,加入200 μL工作内标溶液,然后在多管涡旋混合器中混合(2500 rpm,30分钟),超声处理(20分钟),最后再涡旋混合(2500 rpm,10分钟)。加入10 μL 0.05 M盐酸和1 mL甲基叔丁基醚。在多管涡旋混合器中混合(2500 rpm,3分钟),然后在25155 g下离心2分钟。将850 μL上层液体转移到全回收样品瓶(P/N:186005669CV)中,在40 °C氮气流下蒸干。用200 μL流动相A:流动相B 50:50 (v:v)溶液复溶。
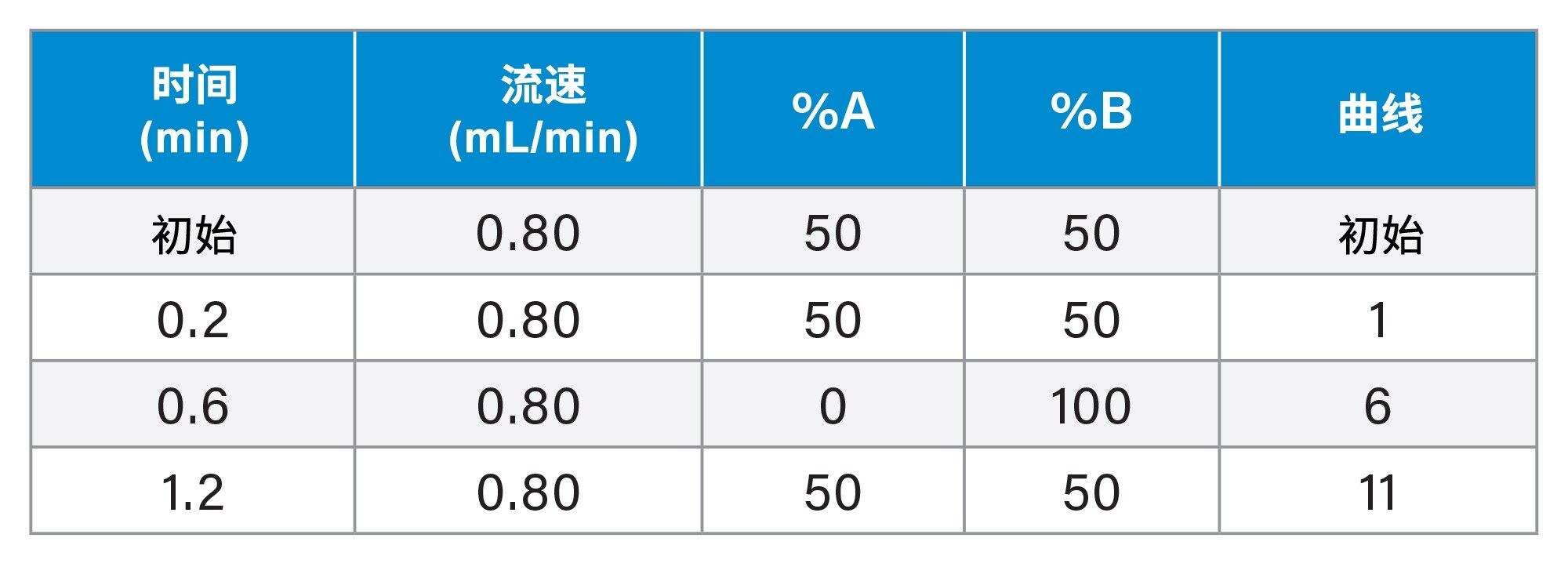
UPLC条件
|
系统: |
ACQUITY UPLC I-Class PLUS(配备FL) |
|
针: |
20 µL |
|
定量环: |
50 µL |
|
色谱柱: |
ACQUITY UPLC HSS C18 SB色谱柱;1.8 µm, 2.1 × 30 mm (P/N: 186004117) |
|
柱温: |
55 °C |
|
样品温度: |
10 °C |
|
进样体积: |
20 µL |
|
进样模式: |
部分环,禁用“预加载”功能 |
|
流动相A: |
0.05 mM氟化铵水溶液 |
|
流动相B: |
0.05 mM氟化铵甲醇溶液 |
|
弱清洗液: |
水:甲醇95:5 (v:v),600 µL |
|
强清洗液: |
水:甲醇:乙腈:IPA 25:25:25:25 (v:v:v:v),200 µL |
|
密封清洗液: |
水:甲醇80:20 (v:v) |
|
运行时间: |
1.5分钟(2.2 分钟) |
MS条件
|
系统: |
Xevo TQ Absolute |
|
分辨率: |
MS1 (0.7 FWHM) MS2 (0.7 FWHM) |
|
采集模式: |
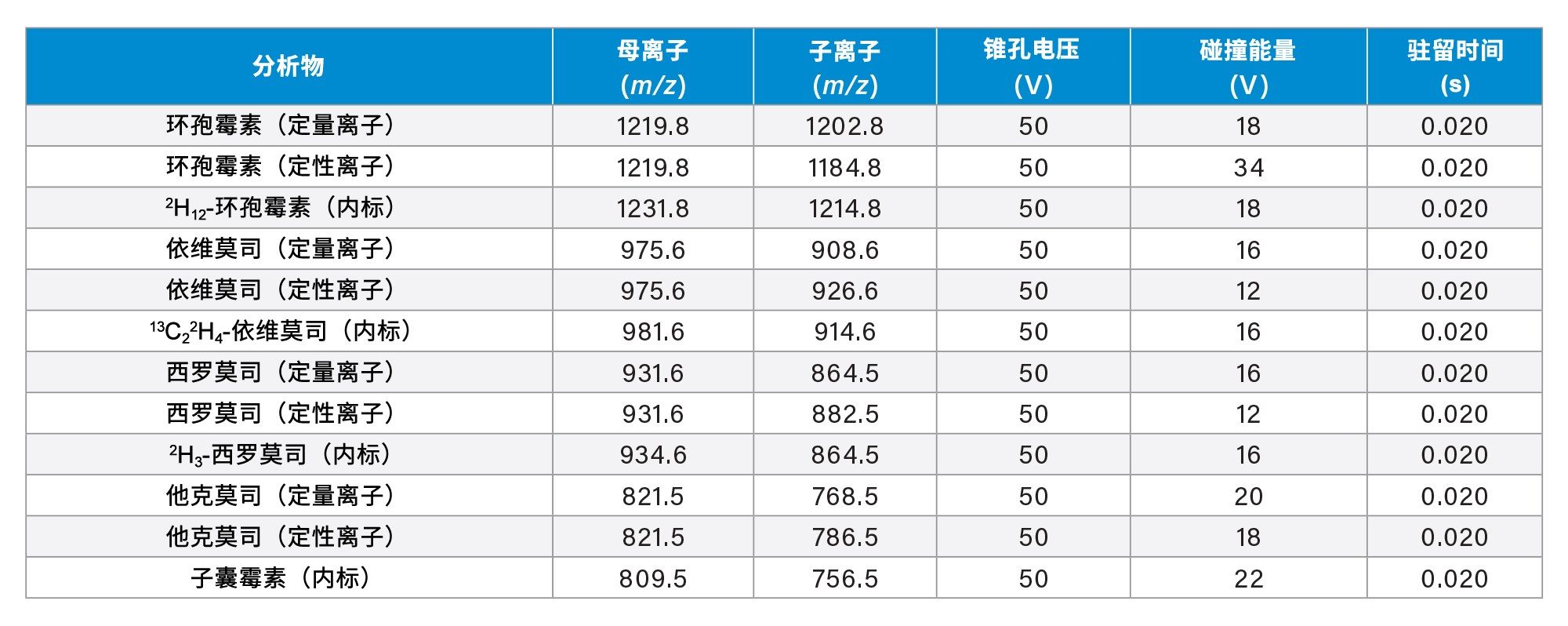
多反应监测(MRM)(详见表3) |
|
极性: |
ESI正离子电离(ESI+) |
|
毛细管电压: |
1.0 kV |
|
离子源温度: |
120 °C |
|
脱溶剂气温度: |
400 °C |
|
扫描间延迟时间: |
0.003 s |
|
通道间隔延迟时间: |
0.02 s |
数据管理
带TargetLynx™应用管理软件的MassLynxTM v4.2
结果与讨论
该方法运行了五次分析。
图2展示了标准曲线样品1(含25 ng/mL环孢霉素以及1 ng/mL依维莫司、西罗莫司和他克莫司)的示例色谱图。
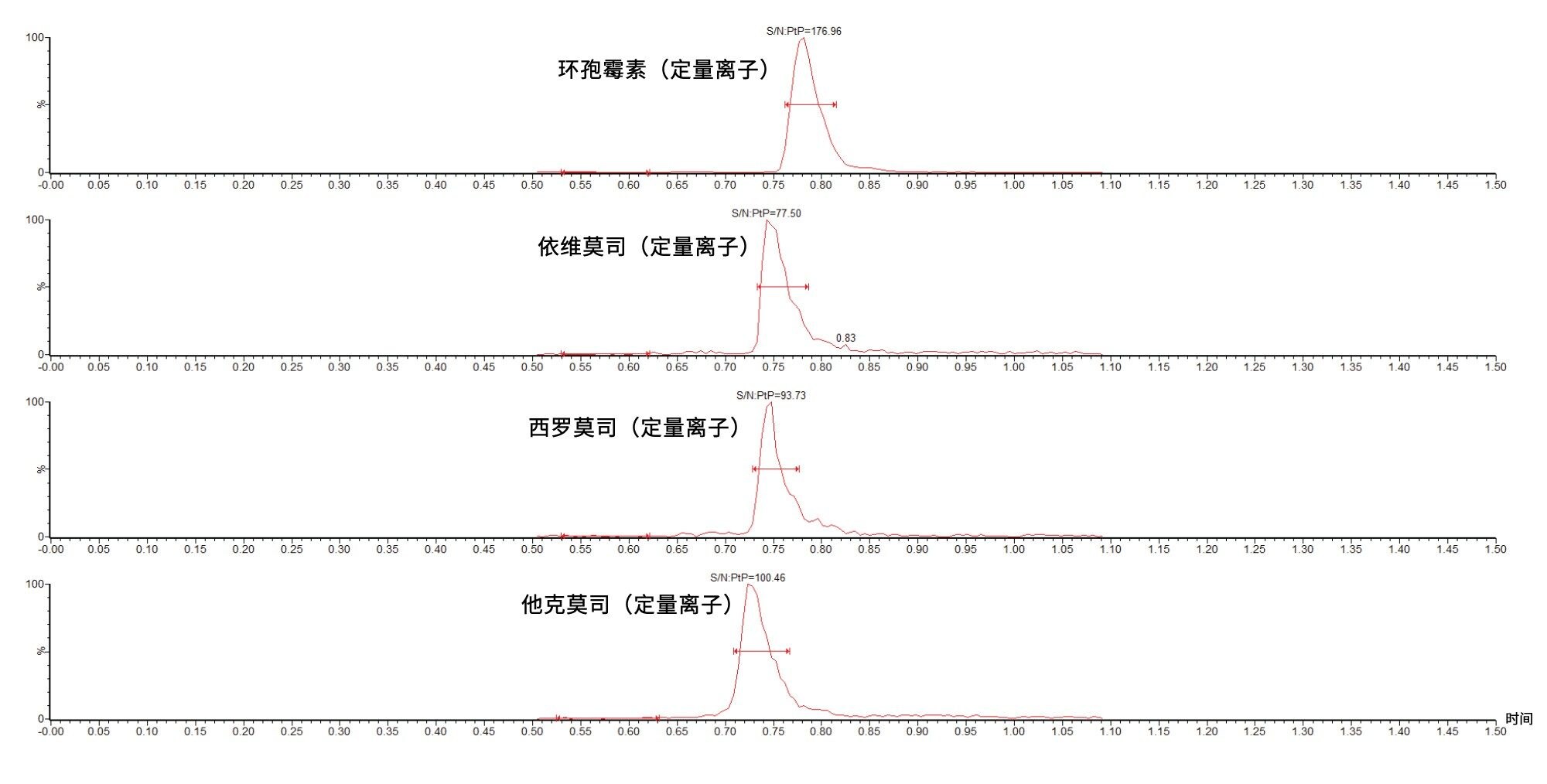
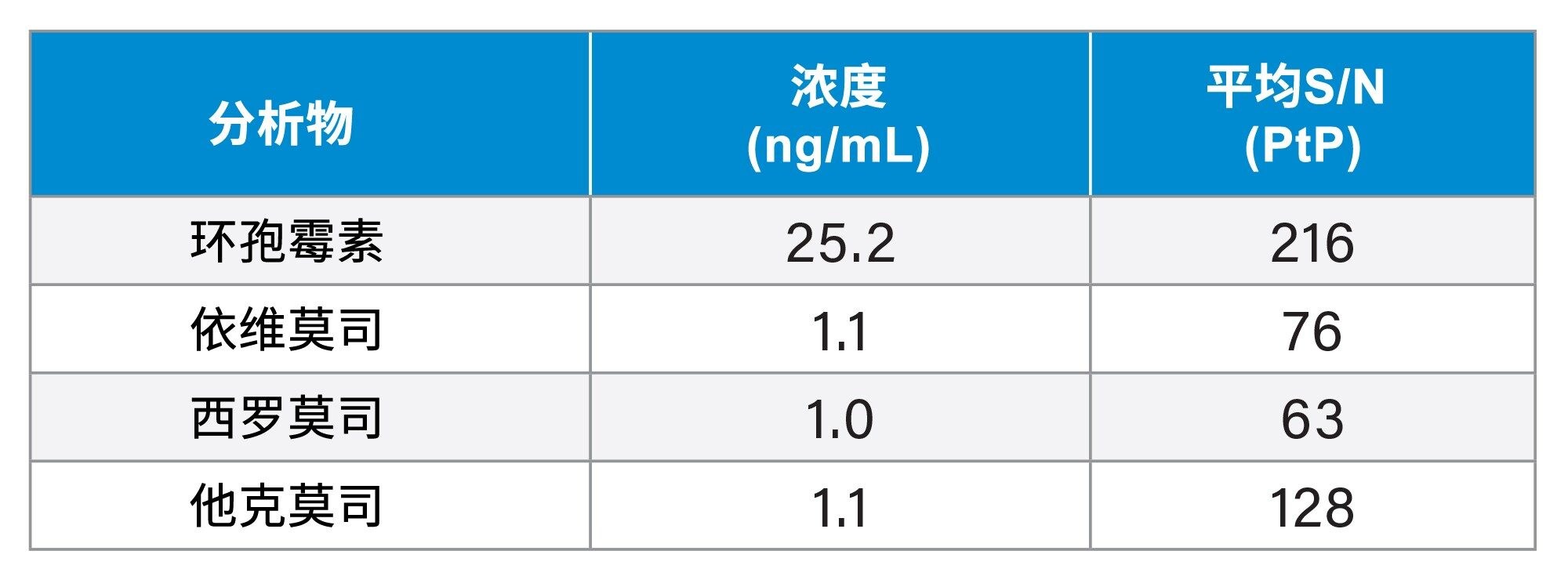
五次分析运行中最低浓度标准曲线样品的分析灵敏度为S/N (PtP) > 10:1(表4)。
每次运行标准曲线样品6之后运行的空白样品,显示环孢霉素、依维莫司、西罗莫司和他克莫司未观察到系统残留。
五次分析运行得到的标准曲线均呈线性,每种免疫抑制剂在其标准曲线范围内的r2 均大于等于0.99(如表1所示)。
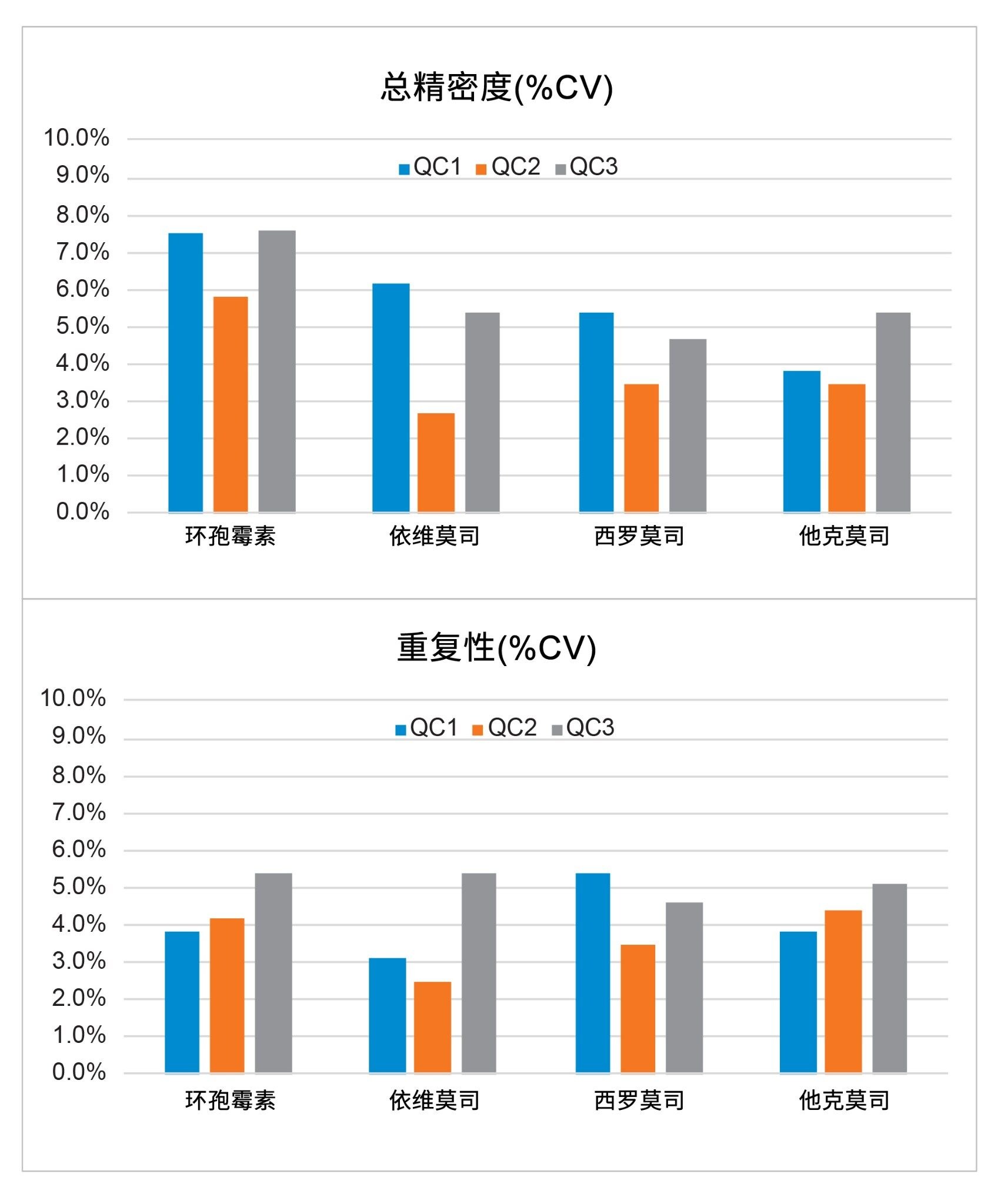
在五天内每天萃取和定量分析三个浓度的全血样品(每个浓度五个重复样,n = 25),以此确定方法的总精密度。环孢霉素除外,分析时间为四天(n=20)。研究中分析了各QC水平的五个重复样,以此评估方法的重复性。图3显示了这些实验的结果,测得三个浓度水平下的总精密度和重复性为RSD≤7.6%。
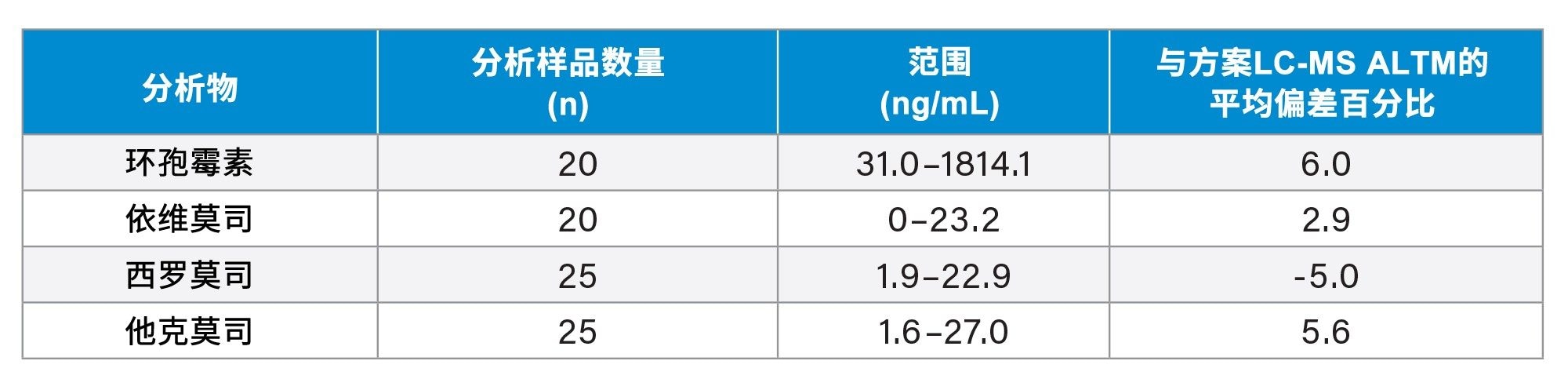
使用购自LGC(英国伯里)的全血外部质量保证样品进行分析,评估方法的准确度。表5中展示了汇总结果。
结论
在短短两分多一点的单次分析时间内(进样间隔),使用少量全血和Capitainer B设备来生成干血斑,即可同时分析免疫抑制药物环孢霉素、依维莫司、西罗莫司和他克莫司。
本方法的性能特点证明了本方法在所有分析物和测试浓度中都具有良好的分析灵敏度、总精密度和重复性(≤7.6% RSD)。
最后,在分析外部质量保证样品时获得了良好的一致性,进一步印证了本方法的准确度。
致谢
感谢Capitainer为支持本研究提供的Capitainer B设备。
1Deprez S, Van Uytfanghe K and Stove CP.Liquid chromatography-tandem mass spectrometry for therapeutic drug monitoring of immunosuppressants and creatinine from a single dried blood spot using the Capitainer qDBS device.Analytica Chimica Acta. 1242 (2023) 340797.
720007893ZH,2023年3月