比较ELSD和CAD定量英夫利昔单抗药物中聚山梨酯的性能
摘要
本应用纪要介绍了Empower 3中的基线扣除处理方法,使用蒸发光散射检测器(ELSD)在聚山梨酯分析中实现了0.01 mg/mL的检测限(LOD)。修改先前报道的洗脱梯度后成功定量了四种英夫利昔单抗药品(原研药和三种生物类似药)中的聚山梨酯浓度。使用相同的方法评估了电雾式检测器(CAD),其检测限和动态范围与ELSD相当。
优势
- 基线扣除改善了ELSD技术对完整聚山梨酯分析的检测限
- ELSD能够在生物制药的制剂水平上定量完整的聚山梨酯
- Empower控制的ELSD为用户提供了一个无缝集成的、易于使用的平台以及强大的数据处理解决方案
- ELSD在聚山梨酯分析中拥有与CAD相当的性能
简介
聚山梨酯(PS)由于具有低毒性和生物兼容性而被广泛用作药品的常见辅料:小分子药物的乳化剂和增溶剂;药物递送纳米颗粒的涂层;防止生物制药中的蛋白质发生变性、聚集和吸附损失的稳定剂。作为辅料,PS可通过氧化、水解和/或酶促等方式在制剂药品中降解1-3。 为确保含有PS的药品在保质期内安全有效,需要对PS进行准确定量。
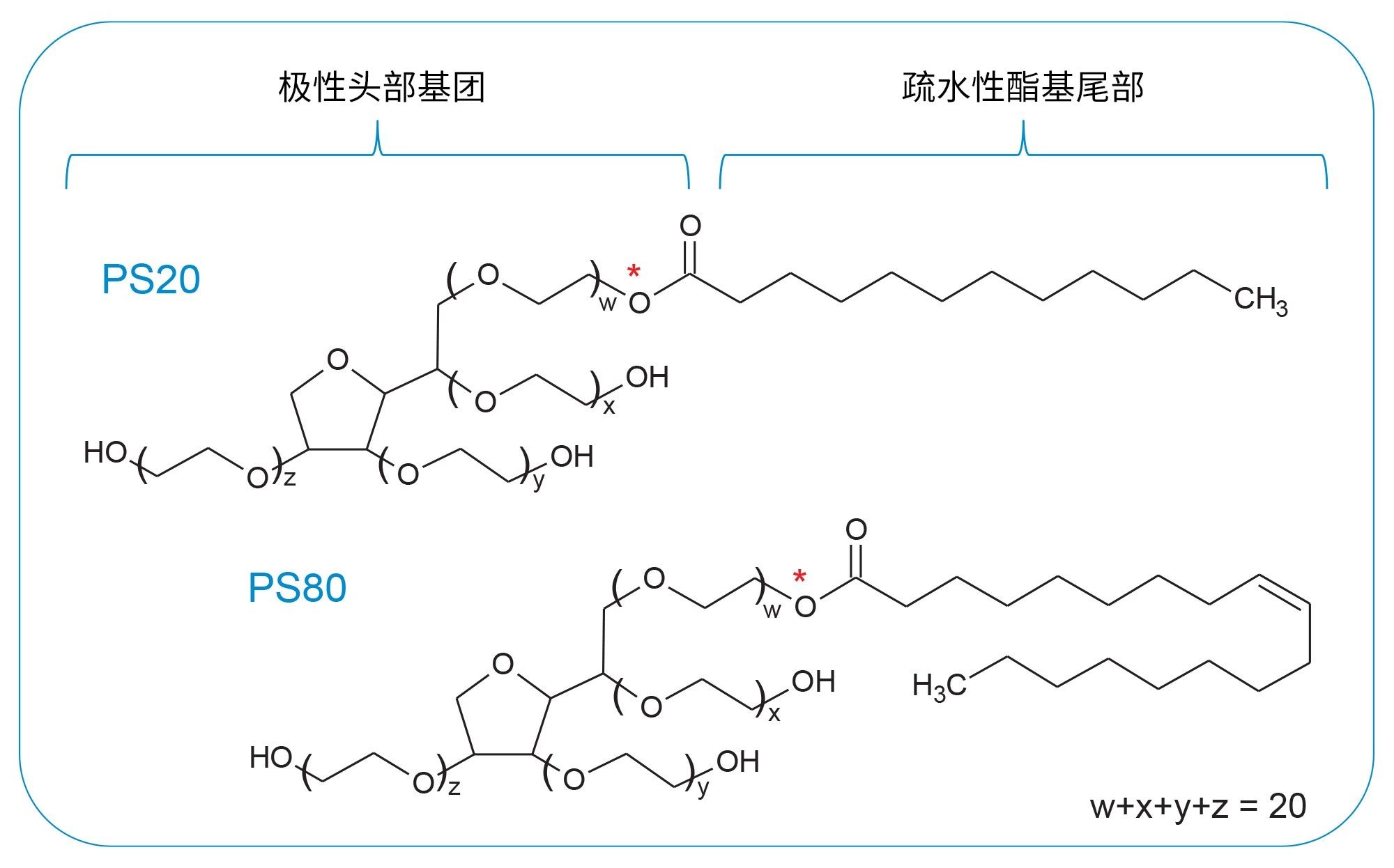
聚氧乙烯脱水山梨醇单油酸酯(PS-80)和聚氧乙烯脱水山梨醇单月桂酸酯(PS-20)是生物药物中常用的两种聚山梨酯(图1)。这两种聚山梨酯都具有乙氧基化脱水山梨醇碱基结构的极性头部基团,不同之处在于每种类型的疏水酯尾(PS80 =油酸酯尾,PS20 =月桂酸酯尾)。由于PS的分子结构中没有能够对紫外可见吸光度检测有效响应的发色团,导致完整水平的分析有一定难度。研究证明,可以改用水解法通过质谱(MS)成功检测游离脂肪酸。虽然这些方法提供了高度的专属性和灵敏度,但它们可能并不一定适用于生产环境,在这类环境中,质谱易用性有限且通量是保持生产力的关键因素4。 在这方面,需要使用替代检测技术,使PS80的分析更加容易,以支持生物制药的生产过程。
对于不含紫外吸收发色团的分析物(例如糖、醇),ELSD是一种常用选择。ELSD是一种气雾式检测技术,先用氮气雾化洗脱液,随后加热液滴以蒸发流动相。监测剩余的干燥分析物颗粒的散射光量5。 CAD是指另一种气雾式检测技术。与ELSD类似,CAD从流动相进入雾化器开始,在氮气流作用下形成气溶胶液滴。这些液滴随后进入蒸发室,去除溶剂,只留下干燥的分析物颗粒。带正电的氮离子将电荷转移到干燥颗粒上,产生与分析物含量成比例的信号,可以使用静电计测量。
为加快在工业环境中部署这些检测器,以一致的方式准确检测并报告治疗水平的分析物非常重要。在这项研究中,由Waters Empower 3色谱数据系统控制的ELSD和CAD均在优化条件和相同的色谱方法下,评估了它们检测和准确报告以治疗剂量水平制备的四种治疗药物中聚山梨酯浓度的能力。
实验
样品前处理
PS80购自Sigma Aldrich。使用水配制浓度为1 mg/mL的PS80储备液。用水将储备液稀释至0.01、0.03、0.05、0.07、0.1、0.3、0.5、0.7和1 mg/mL,制备PS80标样。英夫利昔单抗药品、原研药Remicade和三种生物类似药Avsola、Inflectra和Renflexis购自Amerisource Bergen,按照制造商说明制成剂量浓度(10 mg/mL)。ELSD和CAD在实验开始之前进行了维护,以确保两种检测器均在制造商的规格范围内运行。CAD通过制造商提供的SII软件与Empower 3连接。
液相色谱条件
|
液相色谱系统: |
ACQUITY UPLC H-Class PLUS Bio系统 |
|
样品瓶: |
Waters TruView(部件号:186005662CV) |
|
色谱柱: |
Oasis MAX, 30 µm, 2.1×20 mm(部件号:186002052) |
|
柱温: |
30 °C |
|
样品温度: |
5 °C |
|
进样体积: |
10 µL |
|
流速: |
1 mL/min |
|
流动相A: |
水(MS级),含2%甲酸,v/v |
|
流动相B: |
异丙醇(MS级)。含2%甲酸,v/v |
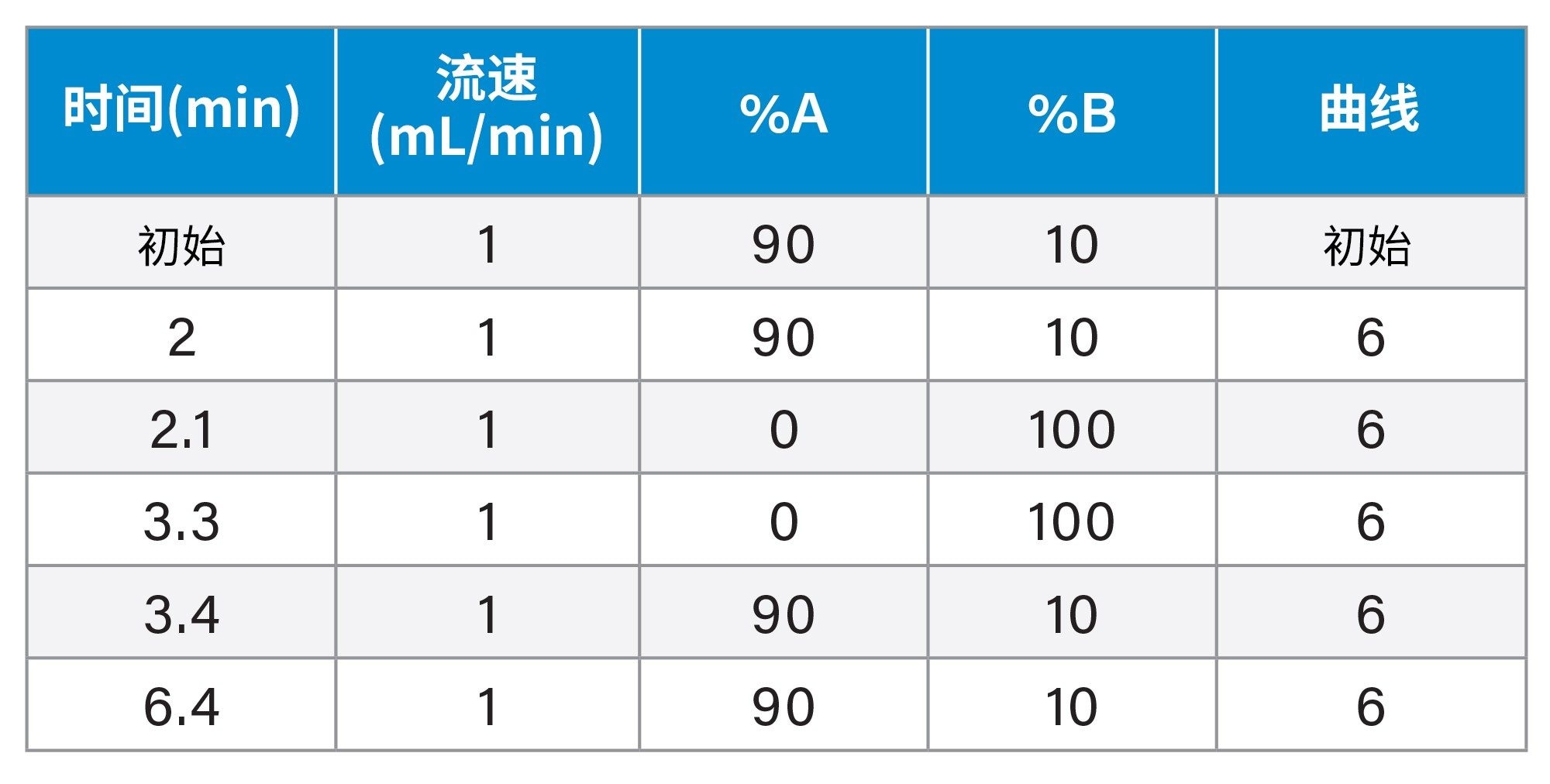
梯度表
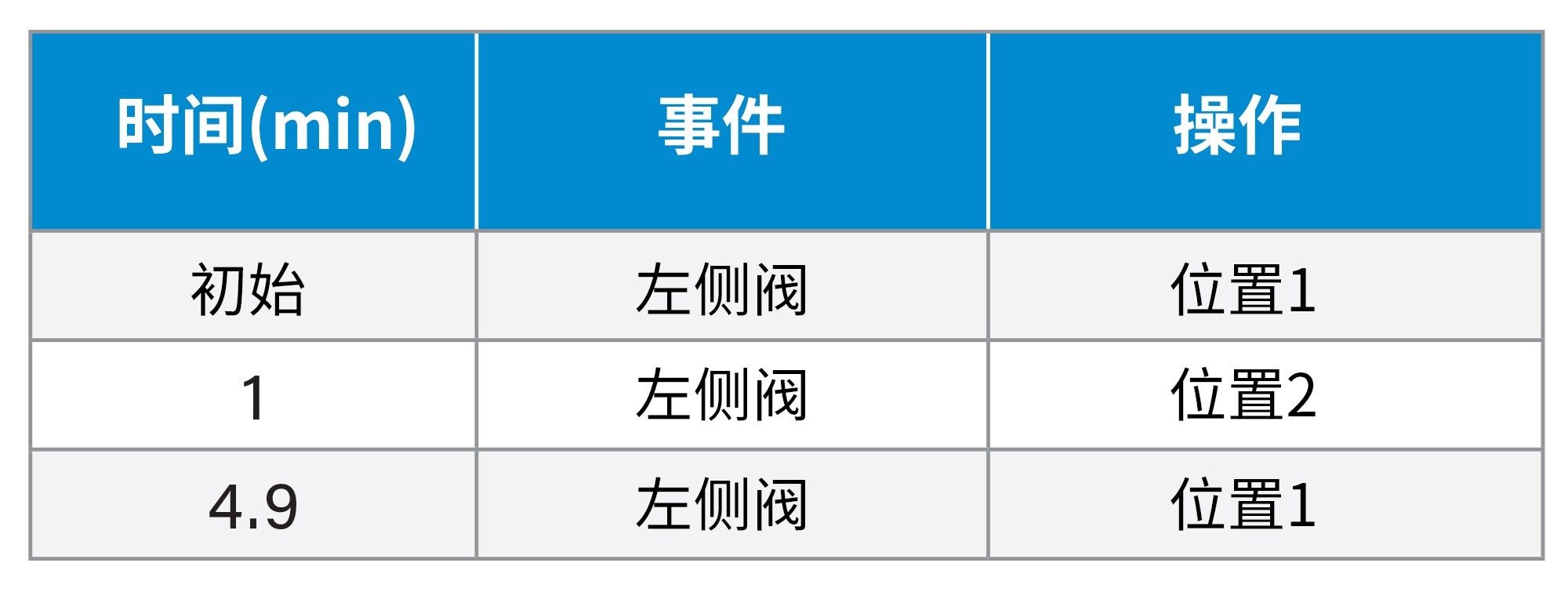
CM-A事件
ELSD设置
|
增益: |
100 |
|
数据采集速率: |
2 Hz |
|
时间常数: |
慢 |
|
模式: |
加热 |
|
功率级: |
75% |
|
漂移管温度: |
80 °C |
|
气体压力: |
20 psi |
CAD(电晕针Veo)设置
|
幂函数: |
1.2 |
|
蒸发温度: |
低 |
|
数据采集速率: |
2 Hz |
结果与讨论
之前的研究表明,使用ELSD,可以在添加了蛋白质的PS溶液中监测完整水平的聚山梨酯6。 简而言之,使用配置有2位6口阀的沃特世色谱柱管理器(CM-A)开发了“富集/洗脱”方案(图2)。在这种配置中,PS在低pH条件下被吸附到Oasis MAX色谱柱的固定相(阴离子交换和反相吸附剂)上,而未保留的蛋白质和剩余的辅料会被导入废液中(图2A)。完成吸附步骤后,切换阀位置,使用有机溶剂将PS洗脱到ELSD中(图2B)。绘制双对数坐标图后,这项概念验证工作显示该方法在峰面积和PS浓度之间存在线性关系。本次评估中使用了这种稳健且快速的方法。
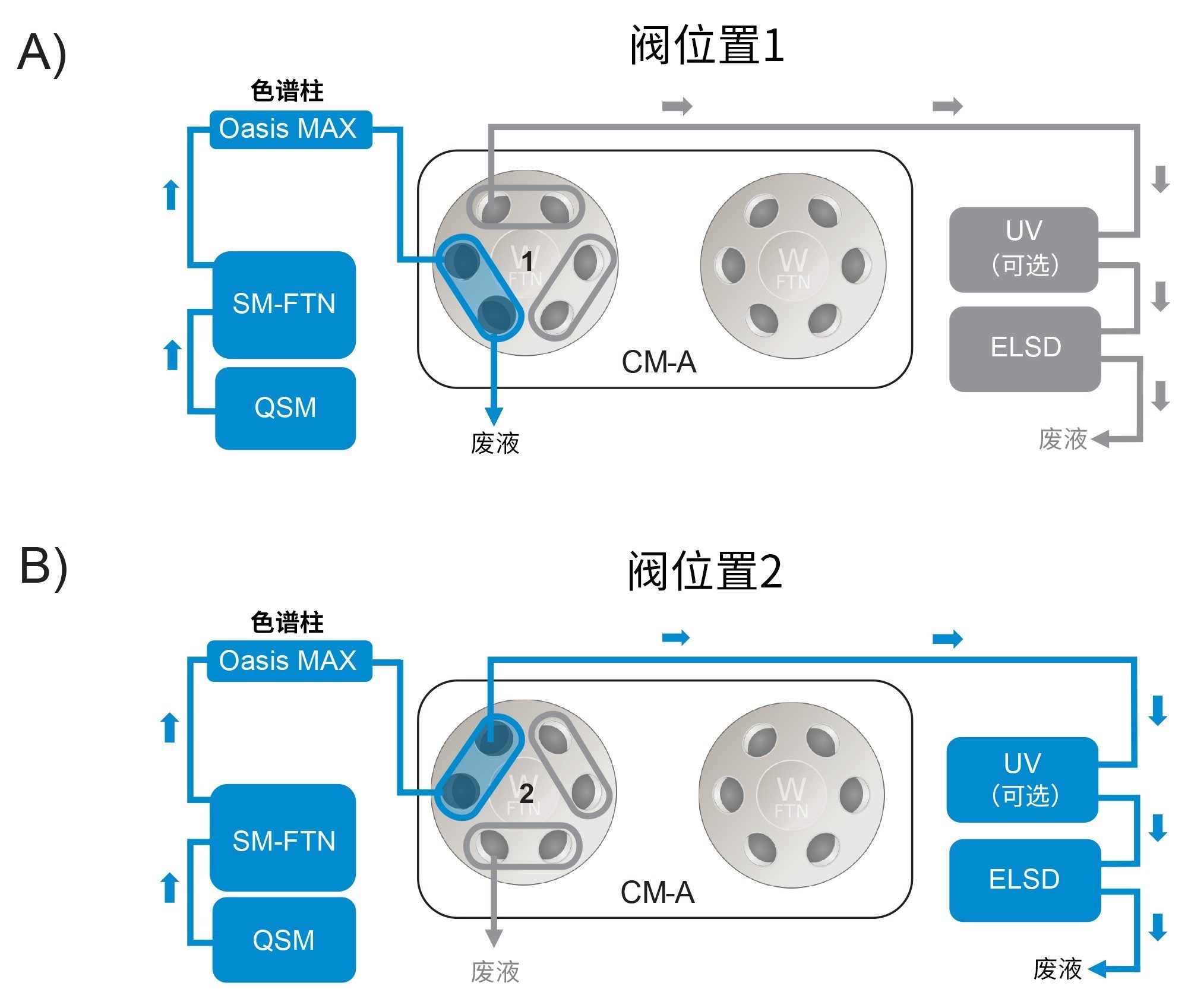
A)在位置1,聚山梨酯被吸附到色谱柱上,未保留的蛋白质和剩余的辅料被导入废液中。
B)然后将阀切换到位置2,将洗脱的PS导至ELSD进行定量。
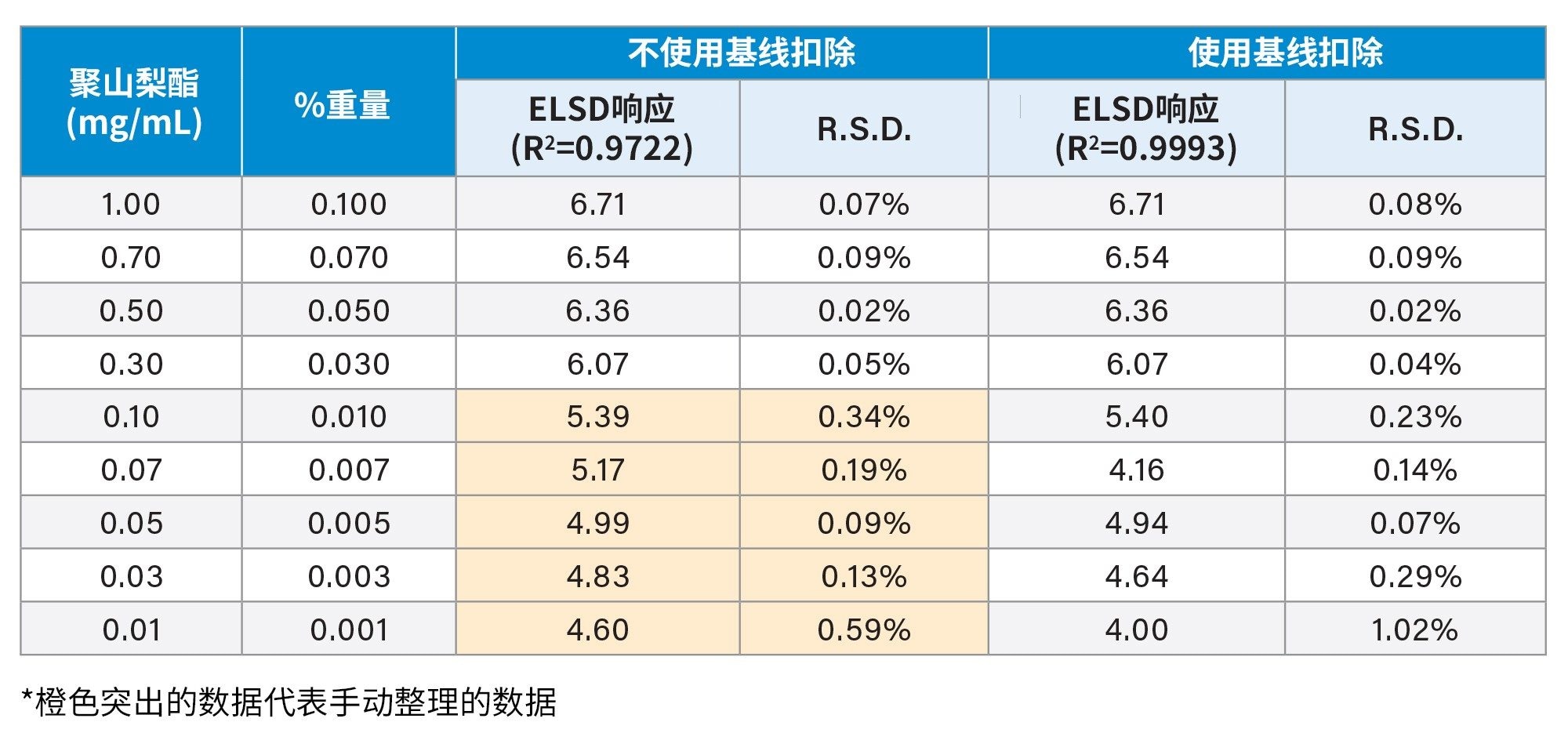
为促进该方法在生物制药制剂(PS浓度可能低至0.003% w/v (0.03 mg/mL))中的应用,必须考虑方法和检测器响应。稳定的基线在确保低浓度水平下准确、一致的检测方面起着重要作用。这在“富集/洗脱”配置中尤其具有挑战性,其中与“阶梯”洗脱梯度(图3A,橙色迹线)相关的快速变化的流动相组成会由于基线上升(图3A,蓝色迹线)而阻碍分析物的准确检测和积分。为了进一步说明基线的影响,将10 µg PS80 (10µL, 1 mg/mL)进样至Oasis Max色谱柱中,并使用分级梯度进行洗脱(见实验)。在10 µg的高载样量下,观察到检测器响应足以实现准确积分(图3B),三次重复进样的峰面积RSD计算为0.08%。然而,当载样量降低到低于1 µg PS80 (10 µL, 0.1 mg/mL)的浓度时,由于基线上升干扰,需要手动处理数据。示例见图3C,其中基线上升是载样量为0.1 µg (10 µL, 0.01 mg/mL)时的主要响应,并且被检测为聚山梨酯峰的一部分。为了提高低浓度下积分的准确度和检测器响应线性,采用基线扣除来减轻与洗脱步骤相关的基线上升影响。如图3D所示,当使用基线扣除时,能够可靠地检测聚山梨酯峰,无需使用相同的处理方法手动整理数据,溶液中浓度为0.01 mg/mL,峰面积RSD值为1.02%。使用这种基线扣除方法,ELSD的线性范围提高了一个数量级(0.01–1 mg/mL),如表1所示。
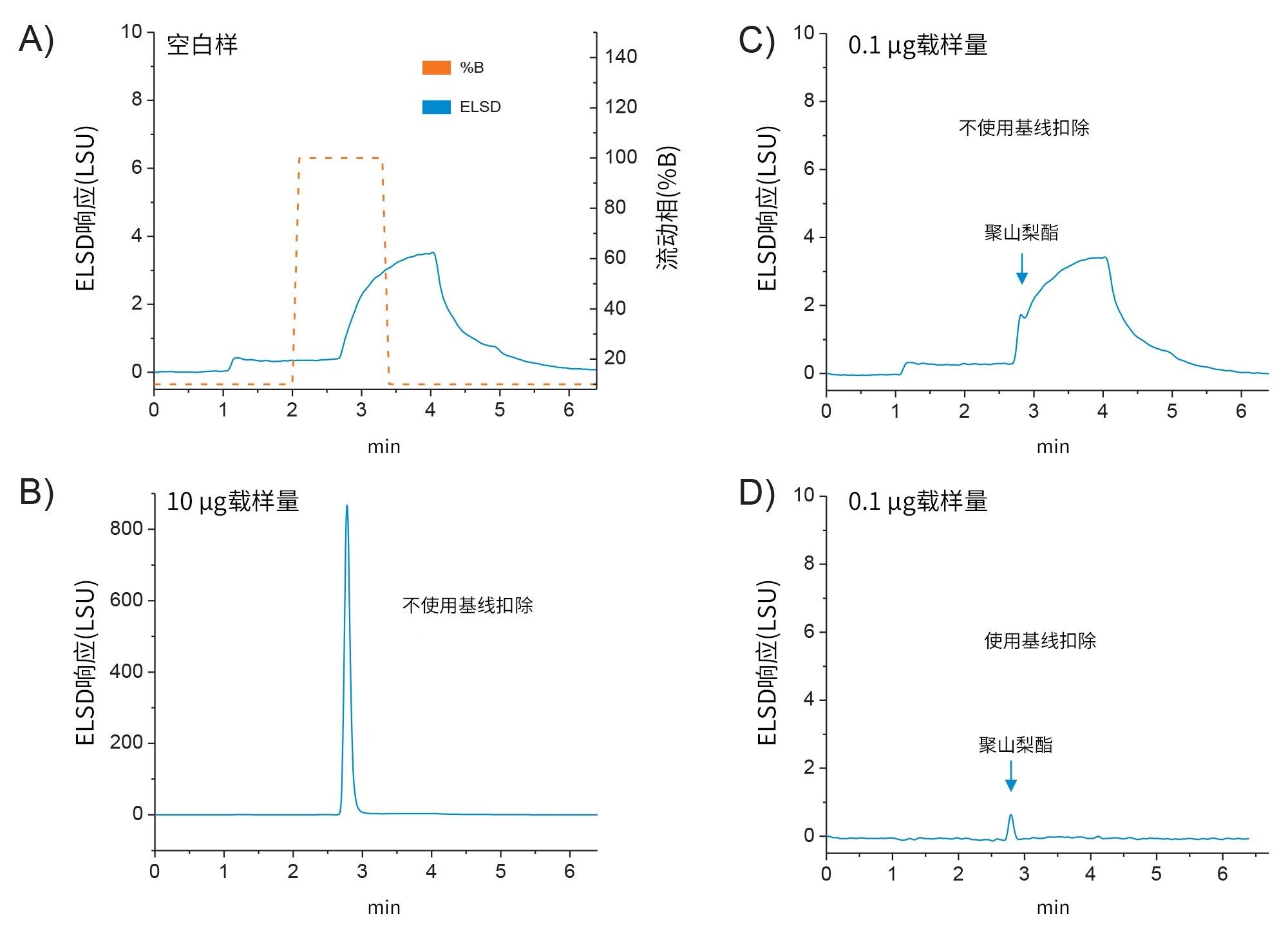
A)“富集/洗脱”配置中有机流动相的基线响应(蓝色迹线)和梯度(橙色迹线)。
B)高载样量(10 µg)的ELSD响应。基线上升不影响积分处理方法。
C)低载样量(0.1 µg)的ELSD响应。基线上升需要手动管理数据。
D)基线扣除后低载样量(0.1 µg)的ELSD响应。聚山梨酯峰不受基线影响,能够可靠地检测并用处理方法积分。
为了评估此优化方法的适用性,对四种含PS的英夫利昔单抗药品进行了完整聚山梨酯分析,包括原研药(Remicade)和三种生物类似药(Avsola、Inflectra和Renflexis)。使用优化方法生成9点校准曲线。如图4A所示,观察到ELSD在选定的浓度范围(0.01–1 mg/mL)内具有良好的线性(R2=0.993)。这些样品列出的PS80浓度均为0.05 mg/mL,完全在ELSD方法的动态范围内。对复溶溶液进行了三次重复进样,并使用校准曲线确定了PS80浓度(图4A,橙色数据点)。如图4B所示,ELSD方法显示出良好的分析一致性,计算的RSD在1%–2.5%之间。对于Remicade、Avsola、Inflectra和Renflexis,计算得出的PS80浓度分别为0.045、0.045、0.044和0.042 mg/mL。实测PS80与预期PS80之间存在微小差异,部分原因可能是治疗样品和校准标准品所用PS80原材料的差异。数据表明,在优化条件下,ELSD能够可靠且一致地检测治疗样品中剂量水平的完整聚山梨酯。
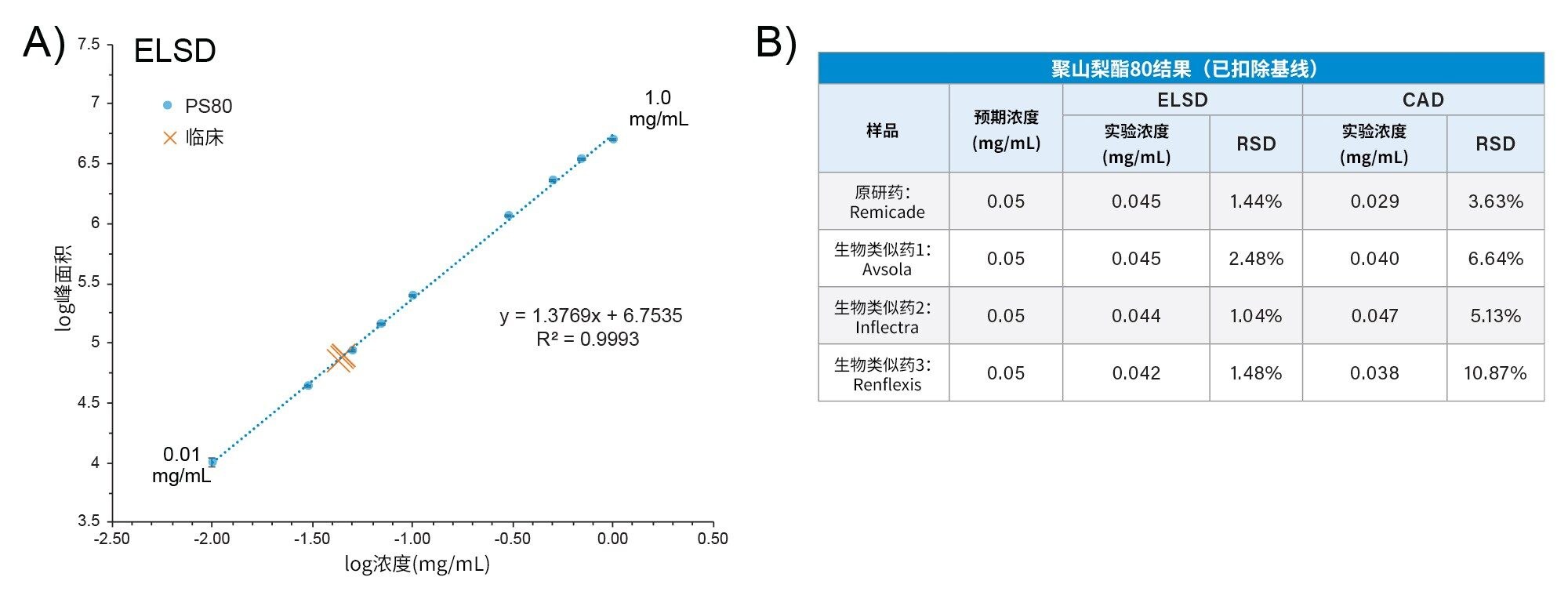
A) ELSD在0.01~1 mg/mL范围内表现出线性响应。
B)通过ELSD和CAD测量的四种英夫利昔单抗药品中的PS80浓度。
为了进一步评估ELSD在检测和定量治疗药品中PS的适用性,使用与替代检测器相同的系统和方法评估了电雾式检测器。为便于比较,CAD响应针对蒸发温度和幂函数进行了优化。观察到蒸发温度设置为“低”时,PS的检测器响应更高。使用此设置,根据制造商说明分别在1、1.2、1.4和1.6评估CAD的幂函数7。 使用PS的5点校准曲线,发现1.2的幂函数具有最高的线性响应,因此用作优化设置7。 作为优化方法的一部分,使用优化设置评估了LOD以确定动态范围。有趣的是,在这项聚山梨酯研究中,与ELSD相比,CAD只能额外产生一个数据点(0.005 mg/mL)。然而,在此浓度水平下,与CAD相关的基线噪声增加会对积分准确度(RSD高达29%)产生负面影响,由此确定这款检测器不适合在生产环境中进行分析。因此,对于拟定的PS分析,CAD与ELSD的有效范围相同,定量下限的浓度为0.01 mg/mL,如图5所示。
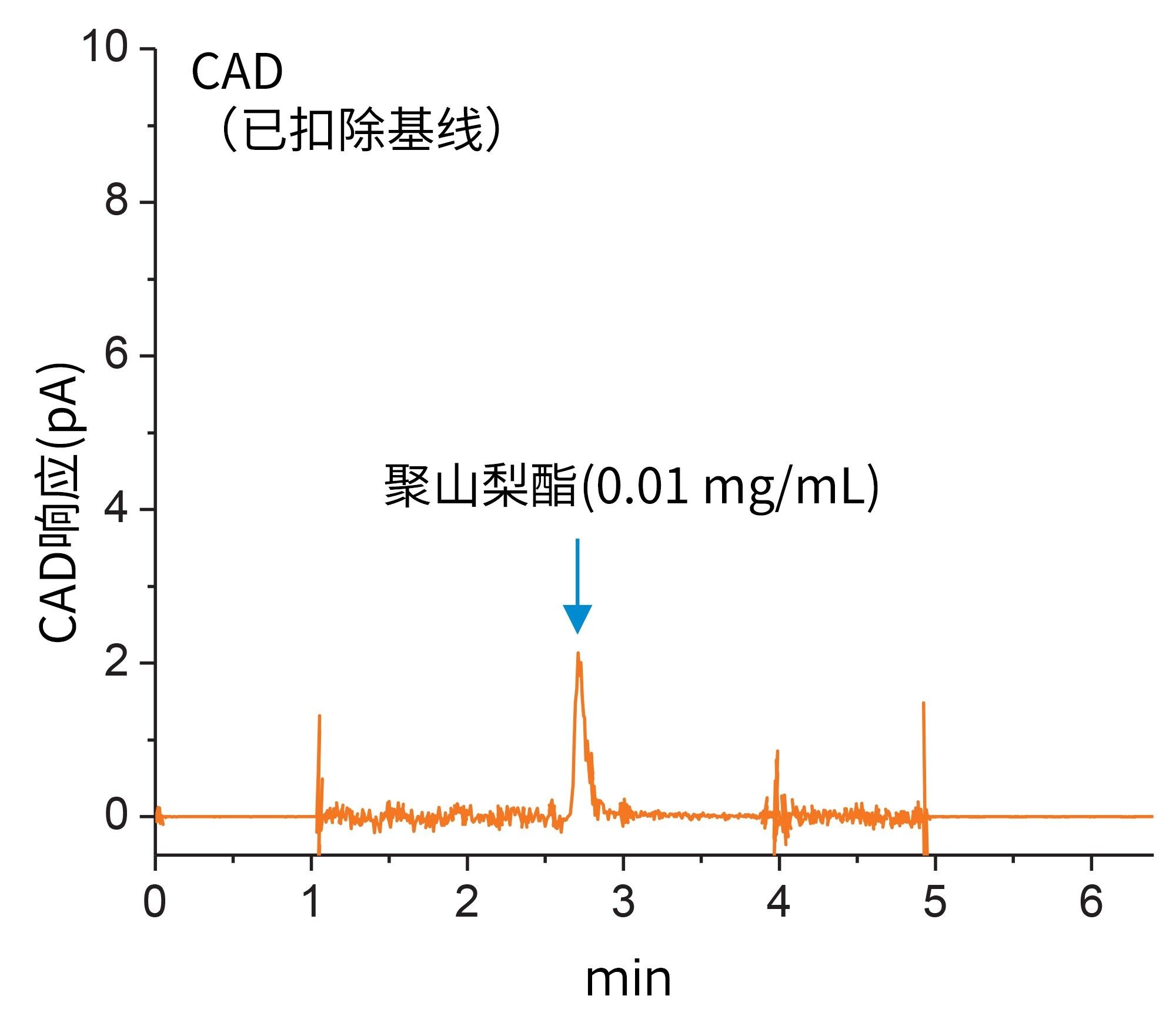
使用与之前相同的方法,使用面积与浓度的9点校准曲线,在优化的CAD设置下定量英夫利昔单抗临床样本中的PS80含量。使用线性拟合,生成趋势线(y=18.285x + 0.2144, R2 = 0.9991)用于定量。为便于与ELSD方法进行比较,CAD数据也使用了基线扣除。应该注意的是,在Empower 3控制下从CAD输出的数据无法分配衍生通道来执行基线扣除。为此,必须使用外部电子表格手动整理CAD数据,执行基线扣除和峰积分,导致临床样本中的RSD值更高(介于4%–11%之间),并降低了分析准确度,如图4B所示。为保证本研究中不存在偏差,以相同方式处理ELSD数据,确定准确度(RSD值)的影响可忽略不计。
比较ELSD与CAD的结果时,数据表明在优化条件下,ELSD能够可靠地检测治疗样品中的完整聚山梨酯,与CAD的结果相近。有趣的是,两种检测器在优化条件下对聚山梨酯80都具有相同的有效工作范围和LOD。Waters ELSD模块通过使用Empower 3 CDS中内置的自动峰值处理方法和基线扣除功能,在完整聚山梨酯的分析中可获得更高的准确度和一致性。这是使用CAD模块无法完全实现的功能。总之,作为Empower 3控制下的集成解决方案,Waters ELSD检测器为聚山梨酯的分析提供了一种有效的解决方案,可以轻松部署在生物治疗药物的开发和生产中。
结论
作为一种气雾式检测方法,沃特世ELSD非常适合分析治疗药品中的完整聚山梨酯。本研究表明,基于ELSD的方法能够可靠且一致地检测浓度范围为0.01–1.0 mg/mL的完整聚山梨酯。此外,Waters ELSD与Empower 3的集成功能使其成为在生产环境中部署的理想解决方案,在这些环境中易用性、自动化能力和通量对于保持生产力至关重要。
参考资料
- Kerwin, B. Polysorbate 20 and 80 Used in the Formulation of Protein Biotherapeutics: Structure and Degradation Pathways.Journal of Pharmaceutical Sciences. 2007.97(8):2924–2935.
- Honemann, M. et al.Monitoring Polysorbate Hydrolysis in Biopharmaceuticals Using a QC-Ready Free Fatty Acid Quantification Method.Journal of Chromatography B. 2019 Mar; 1116 (2019)1–8.
- Labrenz, S. Ester Hydrolysis of Polysorbate 80 in mAb Drug Product: Evidence in Support of the Hypothesized Risk After the Observation of Visible Particulate in mAb Formulations.Journal of Pharmaceutical Sciences 2014 May.103:2268–2277.
- Birdsall, R. et al. 使用基于“一锅法”RPLC-MS的平台方法定量分析蛋白类生物治疗药物中的聚山梨酯20/80.沃特世应用纪要, 2021.720007249ZH.
- Magnussona, L. et al.Aerosol-based detectors for liquid chromatography Journal of Chromatography A1421 (2015) 68–81.
- McCarthy, S. Quantification of Polysorbate Using the ACQUITY UPLC H-Class Bio System with ELS Detection.Waters Application Note, 2015.720005323EN.
- Gamache, P. et al. Charged Aerosol Detection-Use of the Power Function and Robust Calibration Practices to Achieve the Best Quantitative Results.Thermo Scientific Technical Note, 2019.73299.
720007501ZH,2022年1月