考察色谱柱重现性:使用三个历史批次的1.8 µm HSS T3固定相分析人尿液中的内源性咖啡因和代谢物
摘要
使用液相色谱-质谱(LC-MS)和液相色谱-串联质谱(LC-MS/MS)技术进行尿液分析是临床和代谢组学市场中的一种常规检测手段1-3。 针对给定的一组分析物开发的单一分析可以对数千个样本进行检测,其结果对患者健康以及药物开发和发现都有重要意义。因此,分析条件以及色谱柱的可靠性极为重要。通过在方法开发过程中检查色谱柱的重现性,可以进一步确保所开发的方法在使用期间内始终保持适用。本研究对尿液中的尿咖啡因代谢物进行了LC-MS/MS分析,结果表明HSS T3固定相是一种可靠的固定相,其在五年内的三个批次获得的结果相当。
优势
- 三个历史批次的HSS T3材料的批次间性能相当
- 与稀释-上样法相比,固相萃取改善了信号和检测结果
简介
使用高质量产品,尤其是液相色谱固定相和色谱柱,能够确保生成的分析数据在长时间内始终准确且可重现。液相色谱固定相的质量可以通过给定分析的批次间重现性测试来评估,确保生产的每批材料性能相近。大多数批次间测试是使用在一段时间内生产的三批材料进行的,例如方法验证包中的材料。这些验证包虽然好用,但它们可能只能对产品的整体质量提供大致了解。为获取全面了解,应测试不同历史批次的材料,才能提供更全面的整体产品质量信息。
ACQUITY™ HSS T3固定相是一种常用的C18键合相,采用了全多孔硅胶颗粒。相比传统C18,该固定相可以更好地保留极性分析物,并且由于其键合相密度更低,因此不会影响疏水化合物的分离效果。较低的键合相密度增加了与基质颗粒的相互作用,同时与100%水性流动相兼容。许多应用和出版刊物中都使用该固定相进行分离,从小分子药物制剂到生物分析应用均有涉及4–6。为证明HSS T3材料的质量,用不同批次的材料分别填充三根色谱柱。这些材料的生产时间相隔五年(2016年~2021年)。然后,在进行固相萃取(SPE)和稀释-上样样品制备后,使用这三根色谱柱来分离人尿液中的内源性咖啡因和代谢物。
实验
样品描述
在进样前用水1:1稀释人尿液,用于进行稀释-上样实验。对于SPE,将样品上样到Oasis™ HLB 1 cc 30 mg小柱(部件号:WAT094225)并用1 mL水冲洗两次,然后用0.5 mL 100%乙腈洗脱两次。洗脱液于60 °C氮气环境中干燥,然后用100 µL Milli-Q水复溶留待分析。
方法条件
|
液相色谱条件 |
|
|
液相色谱系统: |
ACQUITY UPLC™ I-Class Plus,配备二元溶剂管理器(BSM)、流通针式样品管理器(SM-FTN)和PDA检测器 |
|
检测条件: |
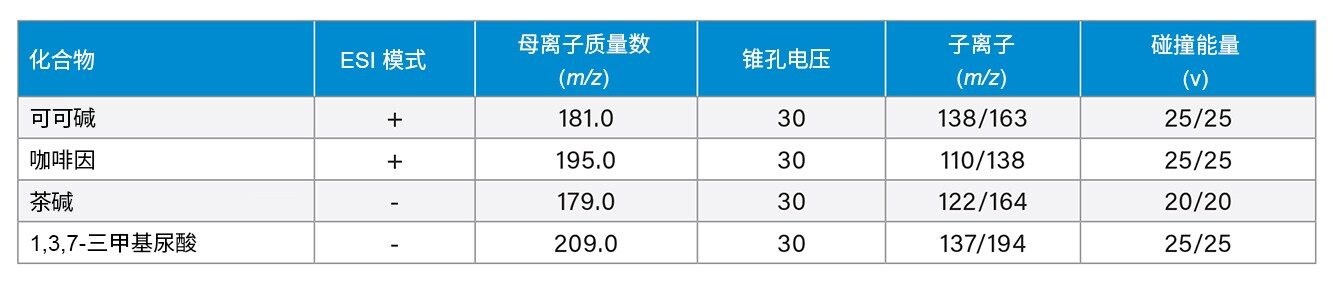
咖啡因代谢物的MRM见表1 |
|
色谱柱: |
ACQUITY UPLC HSS T3 1.8 μm, 2.1 x 50 mm(部件号:186009467) 三批材料: 188 – 2016年10月生产 233 – 2019年11月生产 270 – 2021年11月生产 |
|
柱温: |
30 °C |
|
样品温度: |
10 °C |
|
进样体积: |
5.0 µL |
|
流速: |
0.6 mL/min |
|
流动相A: |
含0.1%甲酸的Milli-Q水溶液 |
|
流动相B: |
0.1%甲酸的乙腈溶液 |
|
梯度曲线: |
流动相B在2.5 min内从2%增加到25%,并在25%流动相B条件下保持0.5 min |
质谱条件
|
质谱系统: |
Xevo™ TQ-S micro |
|
电离模式: |
ESI+,ESI- |
|
采集范围: |
MRM见表1 |
|
毛细管电压: |
3.0 kV |
|
锥孔电压: |
依具体分析物而定(表1) |
|
脱溶剂气温度: |
500 °C |
|
脱溶剂气流速: |
500 L/h |
|
锥孔气流速: |
10 L/h |
数据管理
|
色谱软件: |
Masslynx™ V4.1 |
结果与讨论
在进行柱间重现性测试之前,先评估了两种不同的样品制备技术。典型的稀释-上样法是尿液分析中常用的一种样品制备技术,因为尿液中存在磷脂等内源性化合物的可能性较低。因为尿液中可能含有高浓度的盐,会影响分析物的保留,特别是对于极性分析物,所以仍需要进行样品稀释。相比之下,SPE更常用于血浆和血清基质以去除磷脂。SPE还可以浓缩样品中的分析物。而且由于尿样中某些分析物的浓度非常低,因此证明这种浓缩效应对尿液分析来说也十分有益。图1显示了使用SPE以及稀释-上样法制备样品后,通过MS/MS检测到的四种分析物的叠加图。
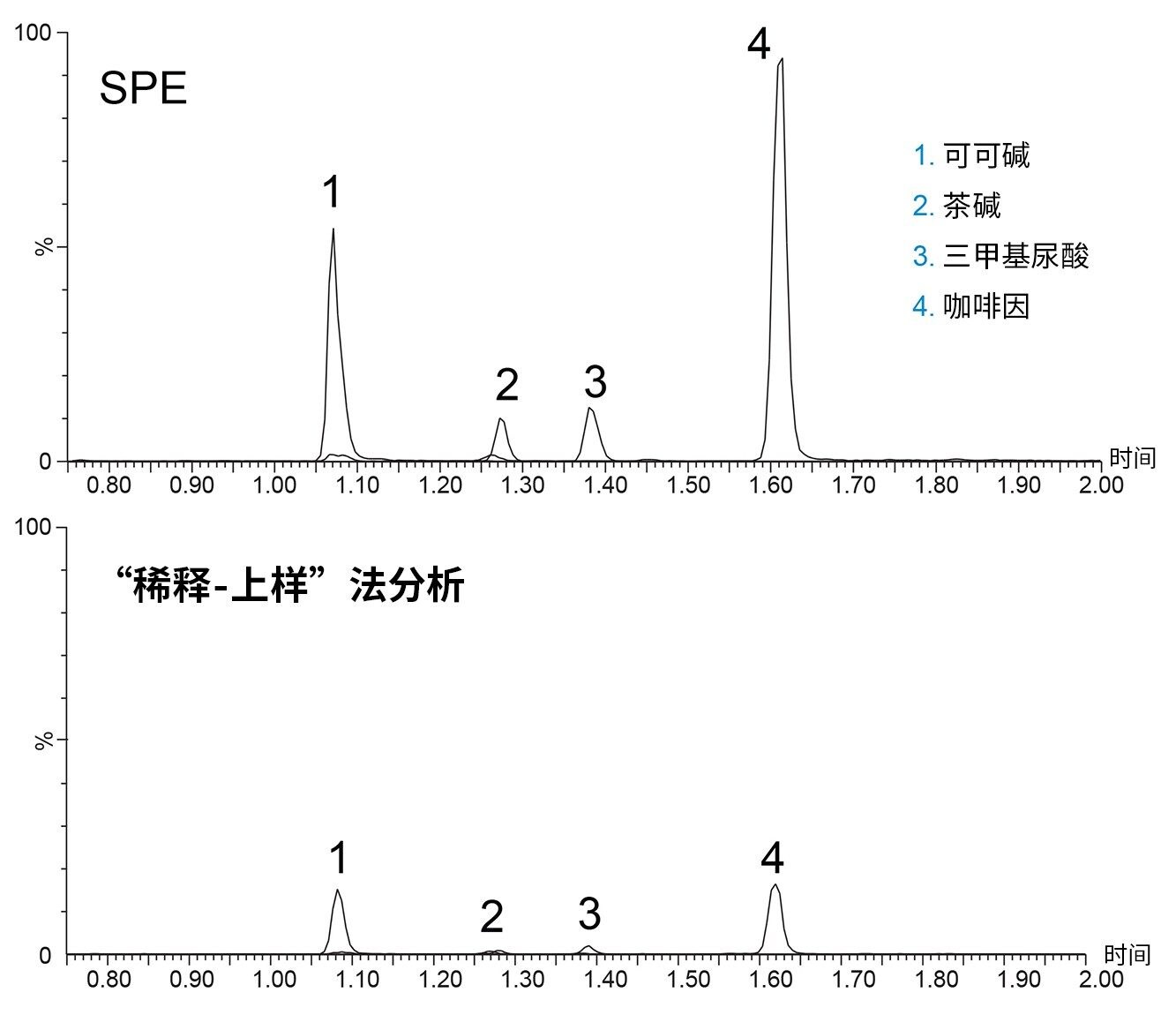
与稀释相比,使用SPE的四种分析物的强度要高得多。强度的提高可能是由于SPE的浓缩效应,或者是由于样品更纯净而提高了电离效率。信号强度的提升意味着能够降低检测限和定量限,使方法获得更宽的动态范围。因此,批次间评估使用了SPE。
将三个批次的ACQUITY UPLC HSS T3吸附剂填充到不锈钢硬件中,用于分析人尿液中的咖啡因及其主要代谢物。用于填充色谱柱的材料批次生产时间跨度为五年,并且都符合沃特世针对所有产品制定的严格质量控制方案。图2显示了咖啡因及其三种主要代谢物可可碱、茶碱和1, 3, 7-三甲基尿酸在三个批次HSS T3色谱柱上的色谱图。
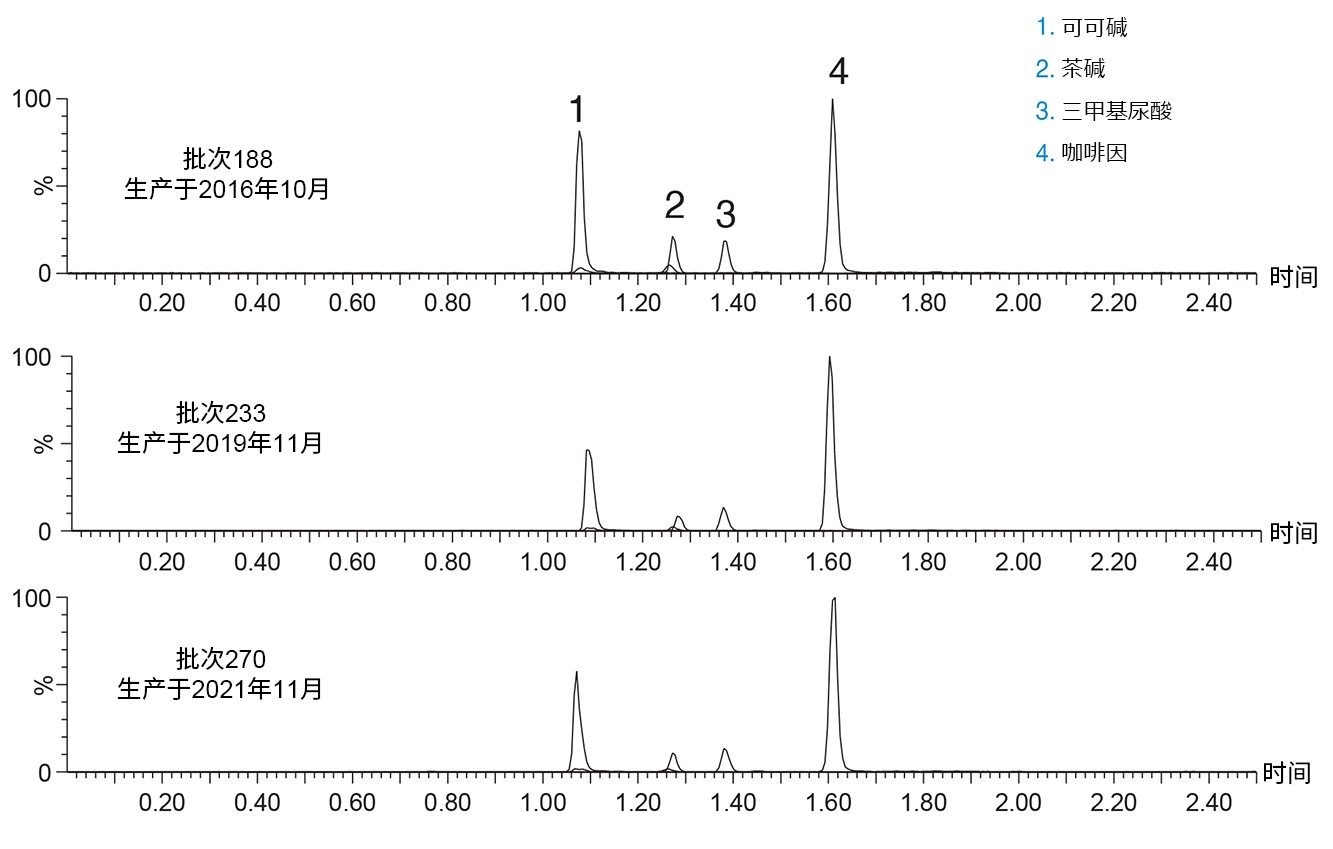
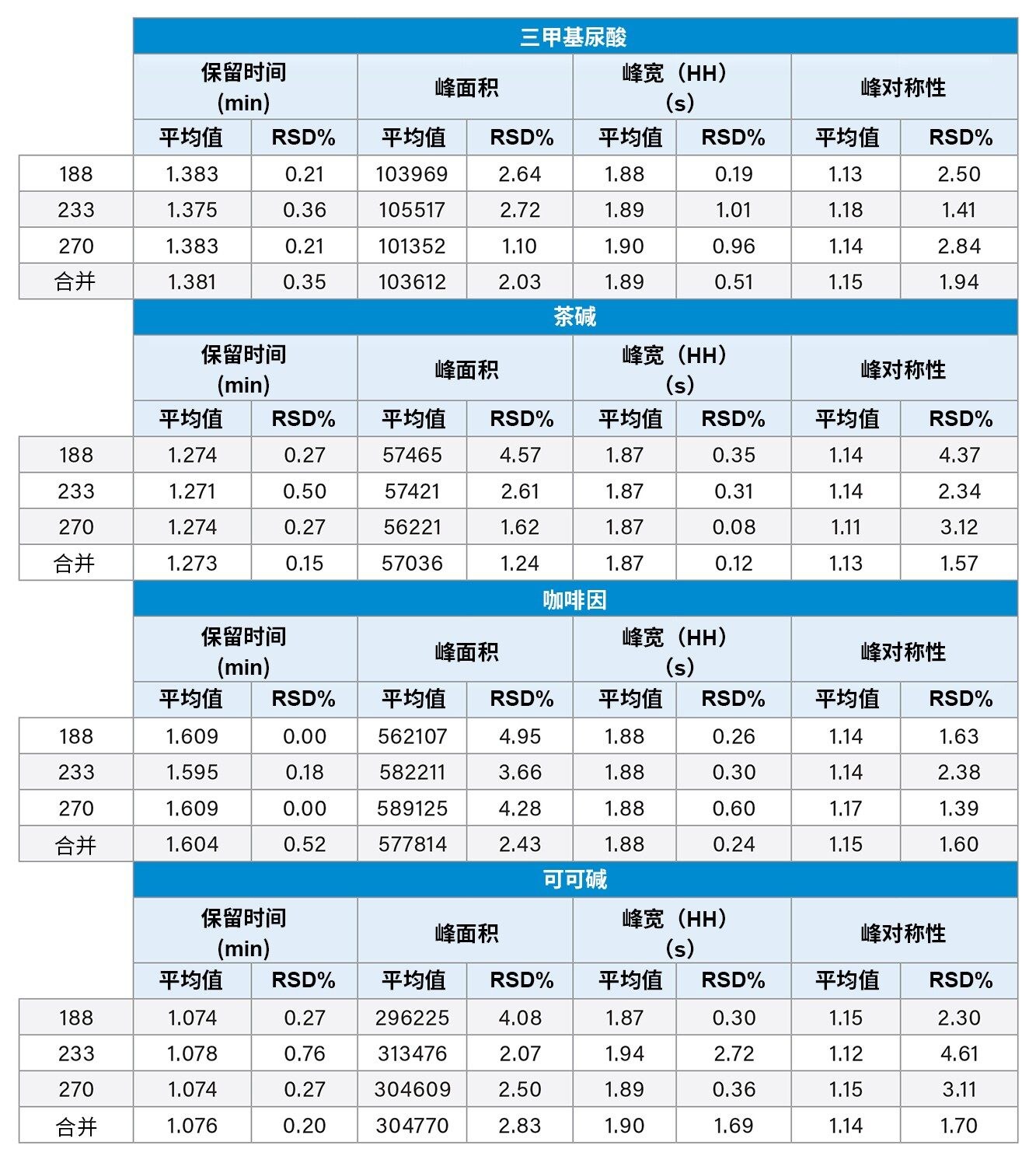
三根色谱柱对所有四种分析物均显示出相似的保留性和选择性。峰面积、峰对称性和峰宽等参数在三种色谱柱上均得到了可重现结果。如表2所示,对于给定的色谱柱和合并数据集,峰保留时间、峰面积、半高峰宽和峰对称性的%RSD均低于5%。
结论
为证明沃特世颗粒和色谱柱生产工艺的质量,我们使用在五年间生产的三批ACQUITY HSS T3固定相来分离人尿液中的内源性咖啡因和代谢物。鉴于稀释法无法提供充足的结果,重现性测试的所有样品制备都使用SPE。
这三个批次展示出可重现的色谱性能。每根色谱柱以及合并数据集(n=9)的保留时间%RSD值均<1%。此外,每种检测到的分析物的峰面积、峰宽和峰对称性的%RSD均<5%。实验结果表明,即使所用材料的生产时间相隔五年,仍然可以生成相同质量的数据。这有助于保证数据质量常年保持稳定,对开发新方法非常有用。如果确定选择的固定相能在不同生产批次以及不同生产年份中发挥相同性能,就能延长实验有效期,且无需额外进行重新验证。
参考资料
- Wong GF, Lee WM, Li CK.Qualitative Screening of Amphetamine- and Ketamine-type Abuse Drugs in Urine Employing Dual Mode Extraction Column by Liquid Chromatography-Tandem Mass Spectrometry (LC-MS/MS).Journal of Analytical Toxicology.(2022).
- Peng KW, Klotz A, Guven A, Gray K, Friss T, et.al. Multiplexed LC-MS/MS Analysis of Methylsuccinic Acid, Ethylmalonic Acid, and Glutaric Acid in Plasma and Urine. Analytical Biochemistry. (2022).
- Jacyna J, Kordalewska M, Artymowicz M, Markuszewski M, Matuszewski M, Markuszewski M. Pre- and Post-Resection Urine Metabolic Profiles of Bladder Cancer Patients: Results of Preliminary Studies on Time Series Metabolomics Analysis.Cancers.(2022) 1210.
- New LS, Chan ECY.Evaluation of BEH C18, BEH HILIC and HSS T3 (C18) Column Chemistries for the UPLC-MS/MS Analysis of Glutathione, Glutathione Disulfide, and Ophthalmic Acid in Mouse Liver and Human Plasma.Journal of Chromatographic Science.(2008).209–214.
- Mohamed, M. Stability Indicating New RP-UPLC Method for Simultaneous Determination of a Quaternary Mixture of Paracetamol, Pseudoephedrine, Chlorpheniramine, and Sodium Benzoate in (Cold-Flu) Syrup Dosage Form.Journal of AOAC International.(2022).
- Sottani C, Grignani E, Cottica D, et.al. Development and Validation of a Bioanalytical UHPLC-MS/MS Method Applied to Murine Liver Tissue for the Determination of Indocyanine Green Loaded in H-Ferritin Nanoparticles. Frontiers in Chemistry 2022.
- Thorn C, Aklillu E, McDonagh E, Klein T, Altman R. PharmGKB summary: Caffeine Pathway.Pharmacogenet Genomics.(2012) 389–395.
- Caffeine and Caffeine Metabolites – Urine Lab Procedure.Method UHPLC-ESI-MS/MS.Method number 4063.08. https://wwwn.cdc.gov/nchs/data/nhanes/2011-2012/labmethods/CAFE_G_MET.pdf Access 14-March-2022.
720007605ZH,2022年4月