由分析物/表面非特异性吸附引起的样品损失给获取准确且可重现的数据带来了挑战。分析物本身的理化特性进一步加剧了这个问题,这些分析物会表现出疏水和/或离子特性,可以增强或抑制吸附现象。样品瓶表面在方法优化过程中经常被忽视。样品瓶表面材料的组成和纯度可能会有所不同,导致吸附活性以及样品变性或聚集方面的稳定性受到影响。携带电荷的物质尤其易受影响,例如唾液酸化或磷酸化糖,此类物质会表现出高吸附活性,且容易在样品基质中沉淀。本研究介绍了如何在游离寡糖的HILIC-FLR/MS分析中使用配置MaxPeak高性能表面(HPS)技术的QuanRecovery样品瓶提高棘手分析物的回收率和稳定性。
提高样品回收率,从而提高游离寡糖的HILIC-FLR/MS分析准确度
糖基化通常被指定为生物治疗药物的关键质量属性(CQA),因为它会影响药物安全性和有效性。因此,在整个开发过程中需要准确表征和监测糖基化,确保产品质量和一致性。通过释放并标记糖基随后进行亲水作用色谱(HILIC)结合荧光(FLR)和/或MS检测的方法可获得糖谱,提供糖基鉴定和相对丰度信息。然而,HILIC-FLR/MS分析可能会出现峰回收率低或不一致的问题,部分原因是在工作台和LC系统上制备和分离样品时分析物与表面发生非特异性吸附。采用MaxPeak HPS技术的ACQUITY Premier LC系统和色谱柱最近的成功经验表明,我们正致力于尽可能减少LC流路和色谱柱的非特异性吸附作用,但LC样品瓶也是方法开发中常遭忽视的样品损失原因之一。样品损失会随着样品在队列中等待分析的时间推移而增加,因此需要可以在实验室轻松部署并与现有方法兼容的解决方案。本应用简报证明,使用配置MaxPeak HPS技术的QuanRecovery样品瓶能够减少样品损失,并改善游离寡糖分析的数据质量。
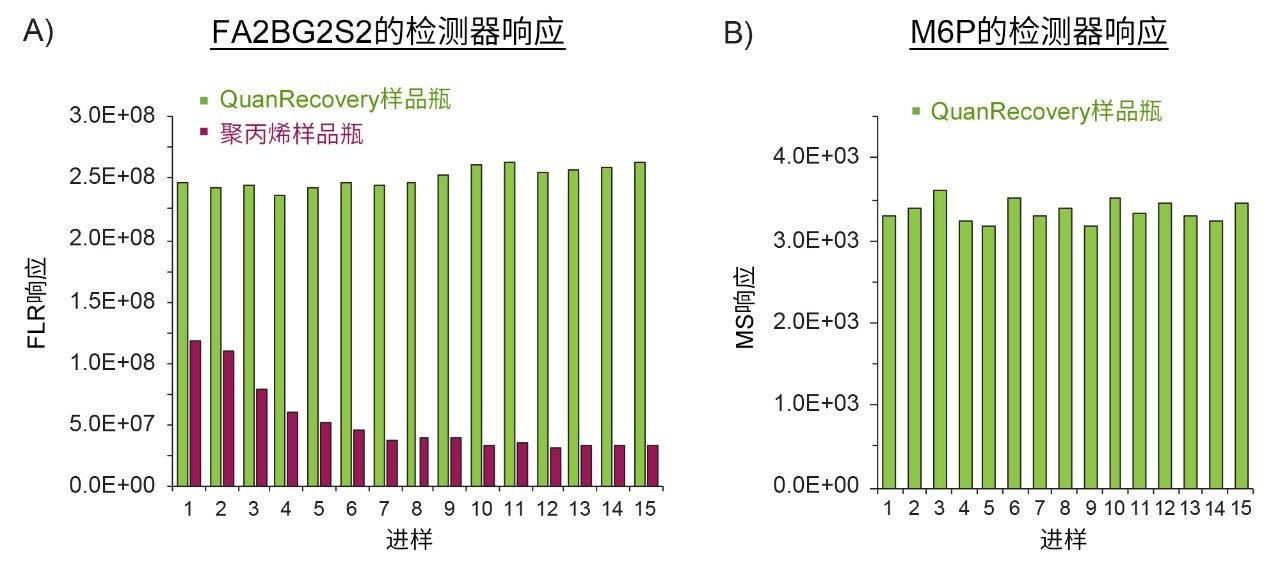
在LC进样之前,游离寡糖样品通常储存在自动进样器内的进样瓶中,因此游离寡糖在溶液中的稳定性对于获取一致且可重现的数据至关重要。本文介绍了一种集成的解决方案:使用QuanRecovery样品瓶结合BioAccord LC-MS系统和ACQUITY Premier BEH Amide糖基分析柱尽可能地减少分析物/表面非特异性相互作用,大幅提高HILIC-FLR/MS分析中游离寡糖的回收率。以糖基性能测试标准品(部件号:186007983)为例,将重复进样的FLR响应一致性作为游离寡糖回收率和溶液中稳定性的衡量标准进行评估。在原有容器(聚丙烯样品瓶)中复溶样品,然后立即将一半的复溶样品转移到QuanRecovery样品瓶中。图1A显示了唾液酸化糖FA2BG2S2(F = 岩藻糖,A = 天线,B = 二等分,G = 半乳糖,S = 唾液酸)连续15次进样后的FLR响应。与原有的聚丙烯样品瓶相比,使用QuanRecovery样品瓶获得的FLR响应高出近1倍且结果更一致,表明MaxPeak HPS技术可提高唾液酸化糖的回收率和溶液中稳定性。实验还评估了带有磷酸聚糖的蛋白质组织蛋白酶D中游离寡糖回收率的一致性,该蛋白质的甘露糖-6-磷酸(M6P)在溶酶体贮积症的治疗中起着重要的作用。已有研究表明,磷酸化糖由于丰度较低且容易吸附到LC系统上,因此难以从HILIC分析中回收。最近的研究表明,ACQUITY Premier系统与ACQUITY Premier BEH Amide色谱柱结合使用,可提高甘露糖7-磷酸寡糖的回收率1。 本研究利用QuanRecovery样品瓶进一步提高检测器(FLR和MS)响应的一致性。如图1B所示,15次进样获得了一致的M6P MS响应,表明QuanRecovery样品瓶作为集成解决方案的一部分,可帮助分析人员提高难回收游离寡糖的回收率,并在游离寡糖分析中获得更一致的数据。
本应用简报展示了使用配置MaxPeak高性能表面(HPS)技术的QuanRecovery样品瓶对游离寡糖进行HILIC-FLR/MS分析的优势。对于糖基性能测试标准品和磷酸聚糖,可观察到游离寡糖的一致性和回收率有所增加,这可能是因为分析物/表面非特异性相互作用减少,而这类相互作用在过去常用的聚丙烯样品瓶中时有发生。将HILIC-FLR/MS分析与ACQUITY Premier解决方案相结合,可以对游离寡糖进行更准确、更一致的分析,提高方法稳定性,将方法轻松地部署到生物治疗药物的开发和制造中。
720007308ZH,2021年7月