
本研究旨在证明一种直接进样测定饮用水中氯酸盐、高氯酸盐、溴酸盐和亚氯酸盐的方法优于2020年新版欧盟饮用水指令的要求。方法性能研究采用ACQUITY UPLC I-Class PLUS与Xevo TQ-XS联用系统以及阴离子型极性农药分析色谱柱完成。方法性能的评估方式为:将所研究的每种水质类型分为2批,使用3种加标浓度(氯酸盐和高氯酸盐:20、50、100 µg/L,溴酸盐:2、5、10 µg/L,亚氯酸盐:100、250和500 µg/L),每种浓度的样品重复测定22次。研究的水质类型有矿泉水、软质饮用水和硬质饮用水。在软水和硬水中检出氯酸盐残留,通过标准加入法定量测得浓度分别为54.3 µg/L和12.0 µg/L,明显低于欧盟饮用水指令中列出的参数值。就方法性能而言,所有水质类型的加标浓度测得的平均正确度值为:高氯酸盐96.2~100.3%、氯酸盐(仅包含矿泉水数据)98.1~100.5%、溴酸盐92.2~102.1%、亚氯酸盐84.1~114.1%。除亚氯酸盐在部分水样中观察到较高的RSD以外,其他化合物的RSD均明显低于10%。利用所有方法性能研究批次及另外的重复性研究考察保留时间重复性,结果表明,所有分析物在550次进样中获得的保留时间RSD均小于1%。
溴酸盐、亚氯酸盐和氯酸盐是水处理过程中形成的消毒副产物。氯酸盐和亚氯酸盐在使用高氯酸盐进行消毒的过程中形成,而溴酸盐在水的臭氧化处理过程中形成。水中的高氯酸盐可能是天然存在或人为引入的,例如从使用天然肥料的土地径流汇入水体。高氯酸盐也可能是次氯酸钠降解、水消毒以及各种工业制程中形成的副产物1。 据了解,高氯酸盐、氯酸盐和亚氯酸盐会危害人体健康,溴酸盐被归类为可能的人类致癌物1。 监测水中存在的这些化合物对于公众健康至关重要。
使用快速、高效的方法测定饮用水中的含氧阴离子非常重要,因为我们需要识别并管控饮用水源中与化学污染相关的风险。世界卫生组织(WHO)于2017年更新了饮用水指南2,欧盟也在新版欧盟饮用水指令中设立了化学污染的新标准3。新指令增加了亚氯酸盐(新参数值为250 µg/L),氯酸盐和溴酸盐的监测要求保持不变,参数值依旧分别为250 µg/L和10 µg/L。WHO对高氯酸盐设立了额外的指导原则(浓度限值为70 µg/L),并对氯酸盐和亚氯酸盐提出了更高的浓度限值(700 µg/L)。美国国家环境保护局(US EPA)在《国家饮用水基本条例》(National Primary Drinking Water Regulations)中纳入溴酸盐(MCL 0.01 mg/L)和氯酸盐(MCL 1 mg/L)4。
分析含氧阴离子的常用方法需要使用抑制型电导检测进行离子色谱分离。有时,为使溴酸盐达到要求的检测限,通常需要柱后衍生(PCD)处理5,再进行UV检测。我们利用阴离子型极性农药分析色谱柱开发出一种快速、小体积直接进样方法。此法采用串联四极杆质谱仪,这款仪器正成为分析这些化合物的常用工具,可以在5 min内快速分析4种含氧阴离子。这项技术的优势在于,通过多重反应监测(MRM)实现分析物可靠定量,无需PCD或专用色谱仪即可检测饮用水中的所有4种含氧阴离子。
从软水(英国威姆斯洛)和硬水(英国约克)地区收集多份1 L自来水样品,运输到应用实验室(英国威姆斯洛)。在英国购得多份1 L普通矿泉水样品用作基质空白。
在实验室收到饮用水样品后,将其分为50 mL等份试样,装入Falcon塑料试管中。然后将样品储存于4 °C冰箱中以待分析。
在分析之前,将样品转移到LC样品瓶中,然后添加同位素标记的内标(样品中Cl18O3-和Cl18O2-的加标浓度为100 µg/L,Br18O3-的加标浓度为10 µg/L),以测定含氧阴离子。仅亚氯酸盐未经内标校准,因为该分析物未鉴定出合适的内标。
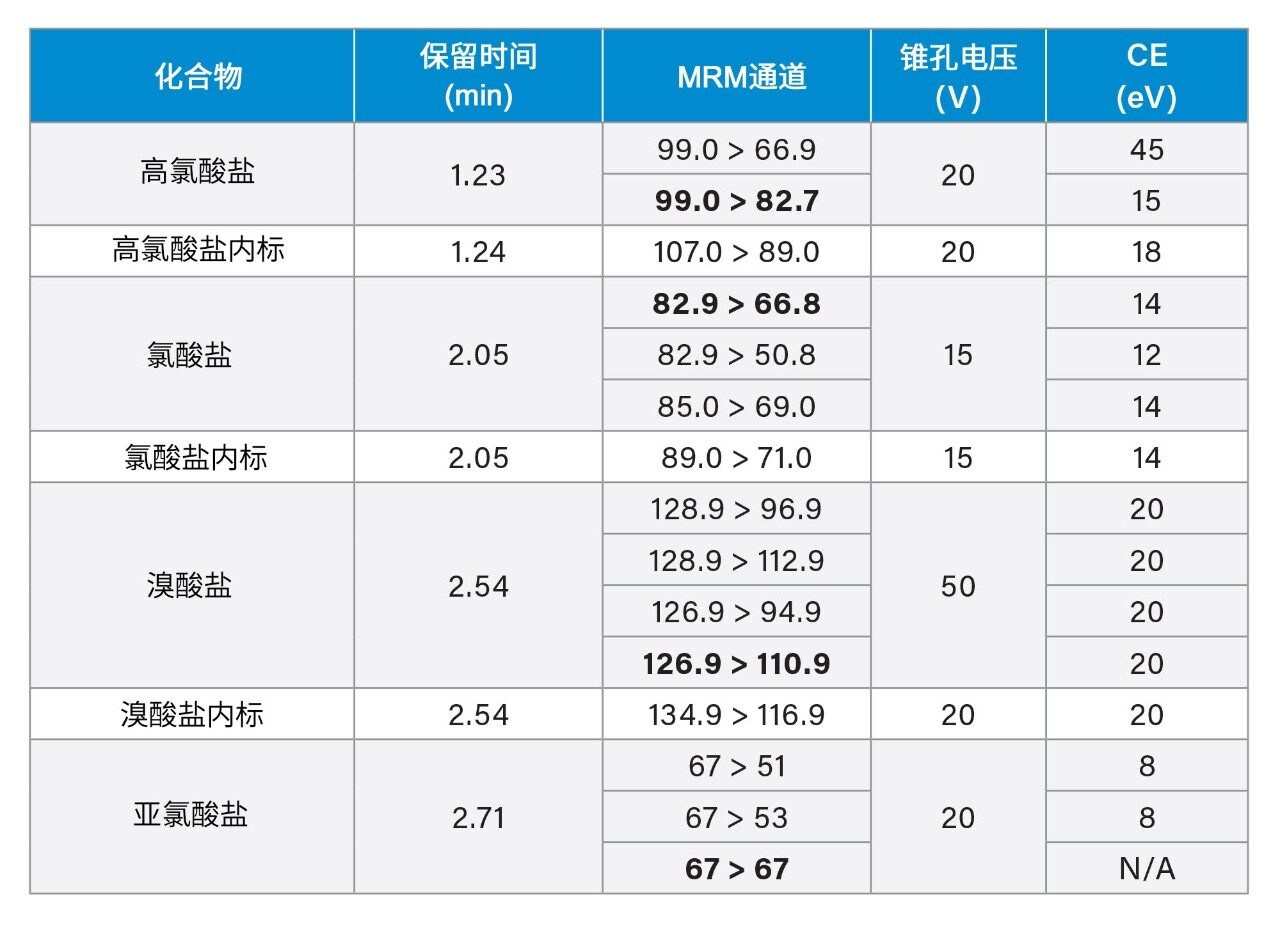
完成方法开发阶段后,使用矿泉水、软水和硬水进行方法性能研究:每种水质类型分为2个批次,每个批次包含33个加标水样,以指定的低、中和高浓度(溴酸盐加标浓度为2、5和10 µg/L,氯酸盐和高氯酸盐加标浓度为20、50和100 µg/L,亚氯酸盐加标浓度为100、250和500 µg/L)加标的样品各11个。表1中列出的MRM突出显示了本研究在定量并确认含氧阴离子时所用的优化离子通道。
|
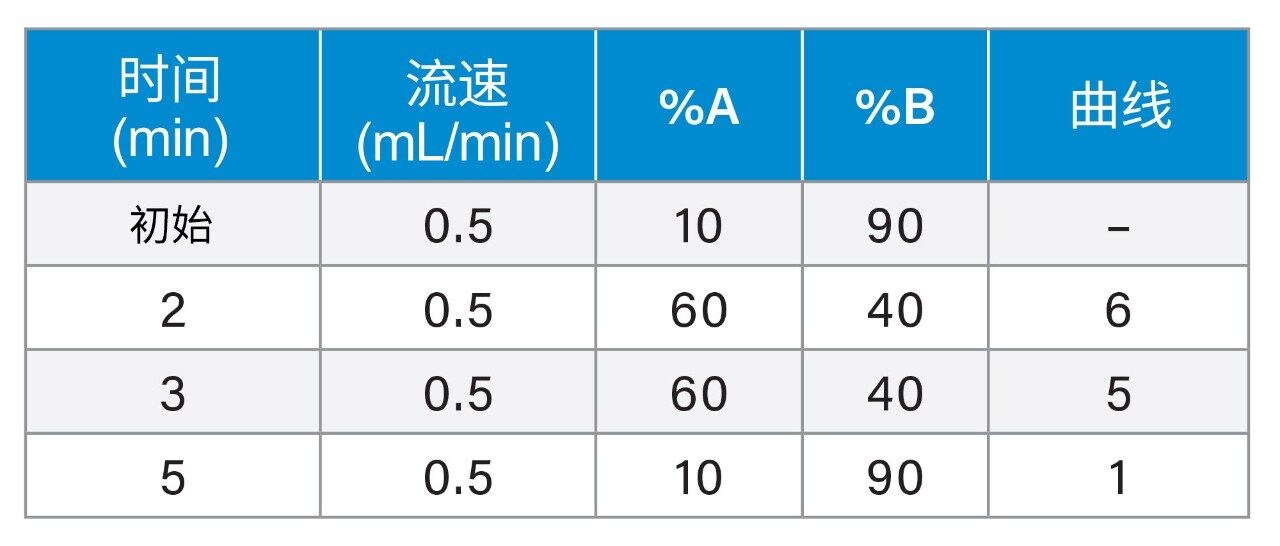
液相色谱系统: |
ACQUITY UPLC I-Class PLUS系统(FL) |
|
检测器: |
串联四极杆质谱仪 |
|
样品瓶: |
Waters TruView LCMS认证透明玻璃螺纹颈口样品瓶,12 × 32 mm (186005666CV) |
|
色谱柱: |
沃特世阴离子型极性农药分析色谱柱, 5 µm, 2.1 × 50 mm (186009286) |
|
柱温: |
50 °C |
|
样品温度: |
10 °C |
|
进样体积: |
5 µL |
|
流速: |
0.5 mL/min |
|
流动相A: |
含0.9%甲酸和50 mM甲酸铵的水溶液(LC-MS级) |
|
流动相B: |
0.9%甲酸的乙腈溶液(LC-MS级) |
|
质谱系统: |
Xevo TQ-XS |
|
电离模式: |
ESI- |
|
采集范围: |
MRM |
|
毛细管电压: |
0.5 kV |
|
锥孔气流速: |
150 L/h |
|
脱溶剂气温度: |
400 °C |
|
脱溶剂气流速: |
800 L/h |
|
离子源温度: |
150 °C |
|
信息学软件: |
MassLynx 4.2版 |
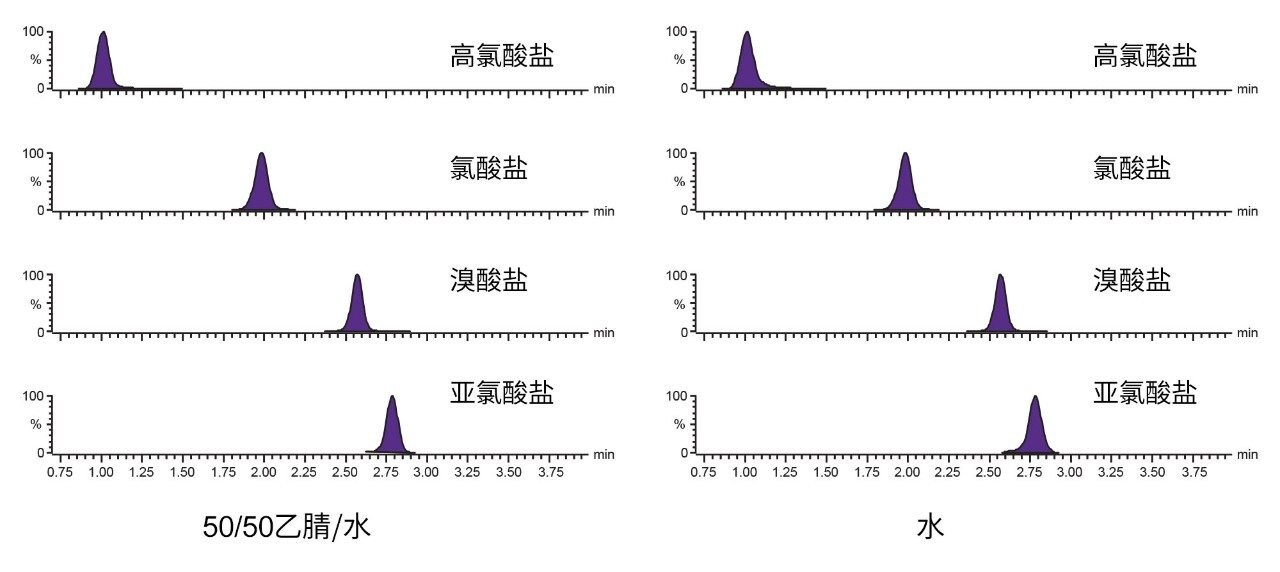
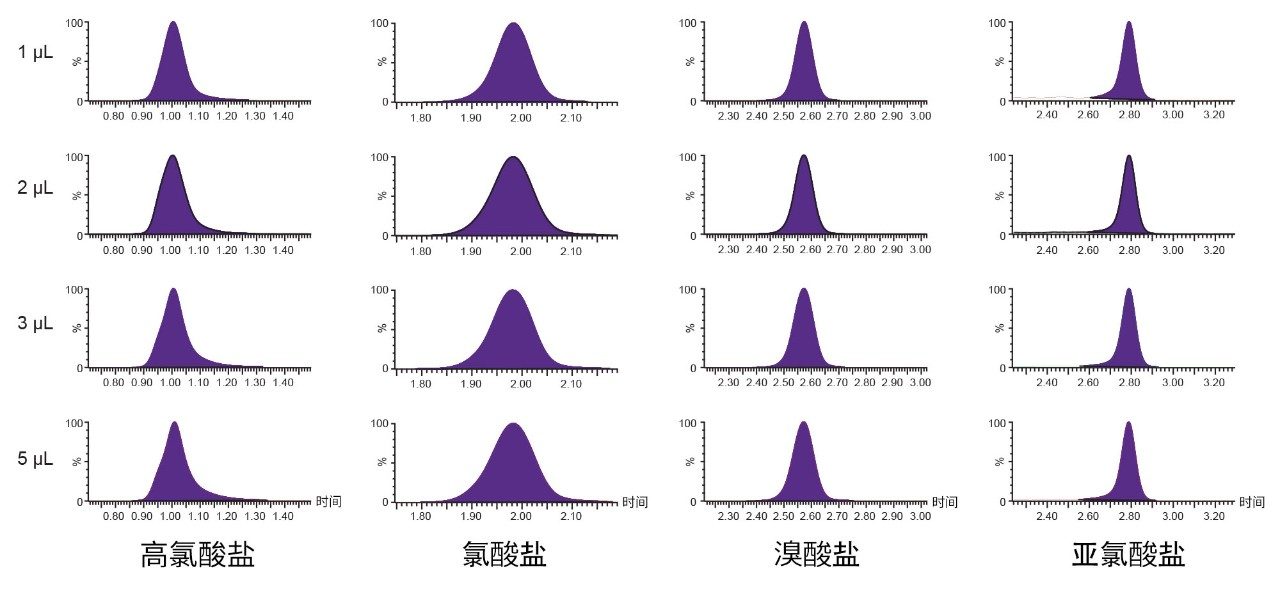
本研究在方法开发阶段考察了进样稀释剂。为确保HILIC色谱柱提供良好峰形,考察了添加乙腈的要求。图1所示的结果证实,注入未经稀释的水与含有50%乙腈的标准水样相比,峰完整性无明显损失。研究还考察了进样体积,以便提高灵敏度(如果需要)。图2所示的结果证实,将未经稀释的水样注入色谱柱1 µL与5 µL相比,峰完整性无明显损失。由这些初步研究得出以下结论:可以将5 µL未经稀释的水注入阴离子型极性农药分析色谱柱中,峰完整性无明显损失,然后利用该规格进行方法性能研究以改善方法定量限。
在开始方法性能研究之前,先对采集的饮用水和矿泉水样品进行含氧阴离子筛查。在矿泉水中未检出含氧阴离子;在硬水和软水中检出氯酸盐,其浓度虽明显低于法定限值,但会干扰方法性能研究。利用标准加入法(n=6)计算氯酸盐残留浓度,结果参见表2所示的方法性能数据,其明显低于参数限值。
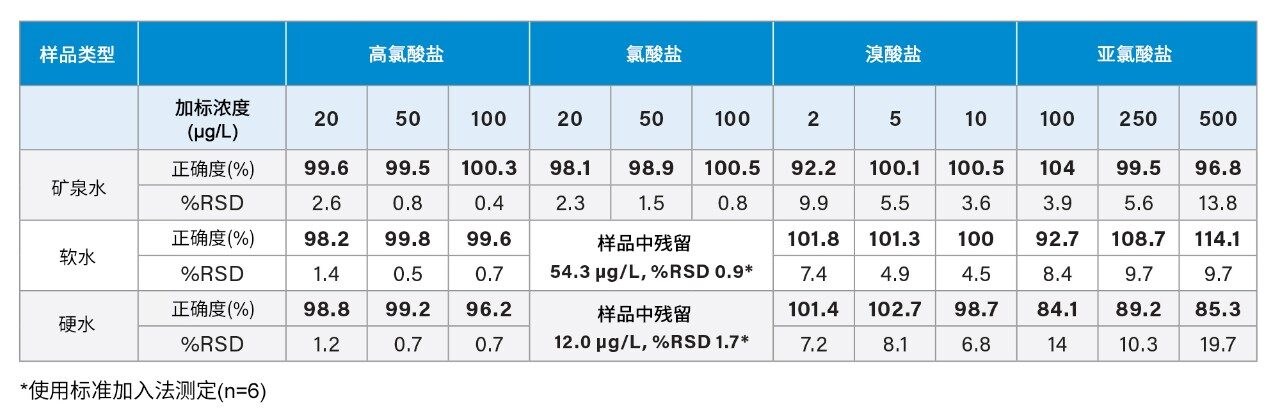
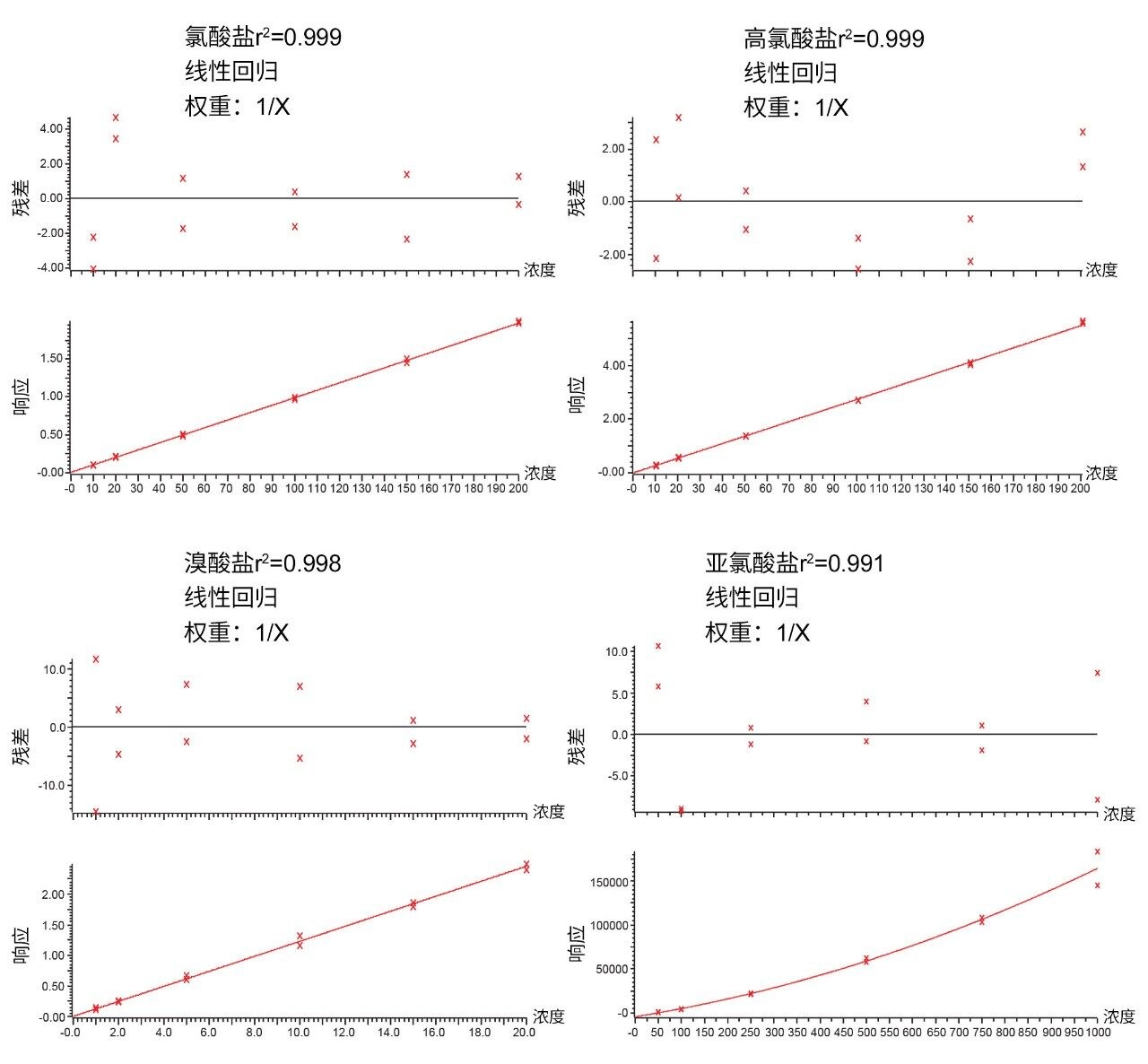
本研究对每种水质类型使用2个分析批次评估方法性能,每个批次各包含33个加标样品,以指定的低、中和高浓度各含氧阴离子加标的样品各11个。排除软水和硬水类型的氯酸盐结果,因为这些样品中存在氯酸盐残留。利用矿泉水评估该方法分析氯酸盐的性能。所有方法性能研究批次均使用了基质匹配校准标样。在制得的校准溶液中,高氯酸盐和氯酸盐浓度范围为10~200 µg/L,溴酸盐浓度范围为1~20 µg/L,亚氯酸盐浓度范围为100~1000 µg/L。图3展示了该方法的预期校准曲线。对于氯酸盐、高氯酸盐和溴酸盐,决定系数为0.995或更高;对于氯酸盐,决定系数为0.99或更高。高氯酸盐和氯酸盐残差均低于10%,溴酸盐残差低于12%,亚氯酸盐残差则为10%或更低。
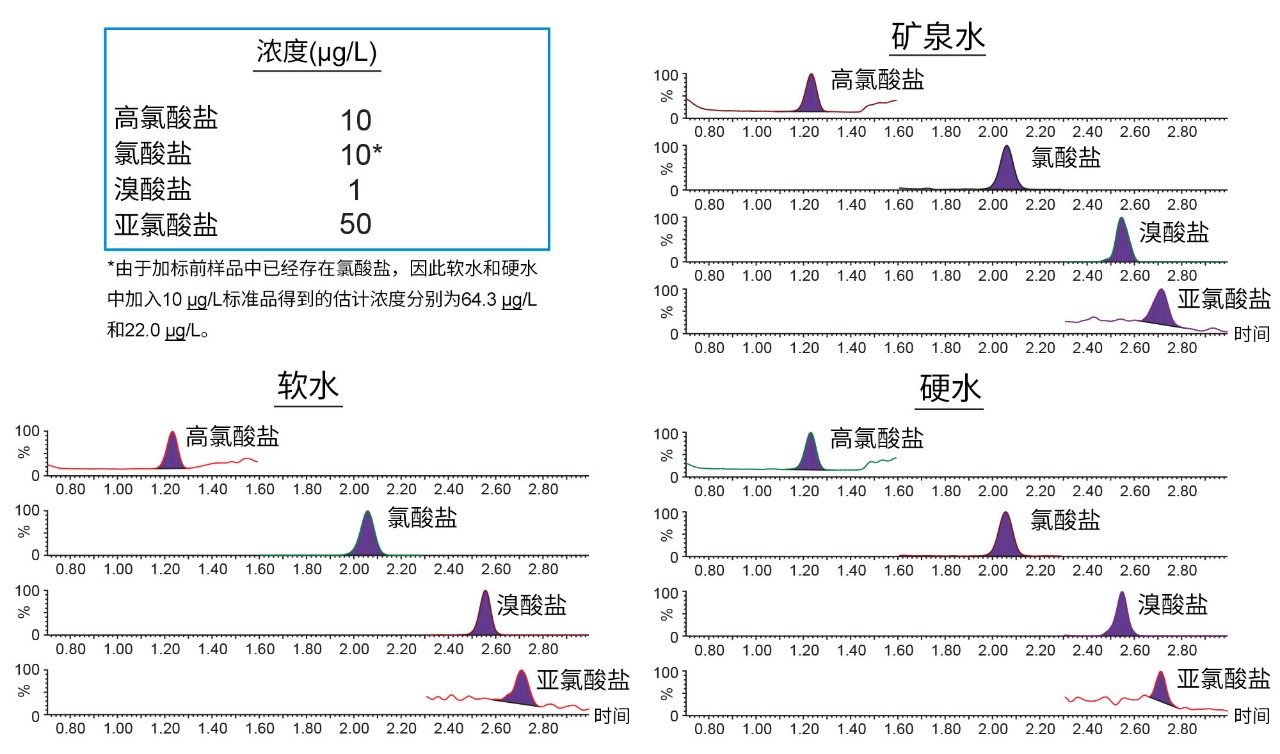
该方法的色谱性能在整个性能研究期间始终保持一致。图4展示了分析软水、硬水和矿泉水校准系列中最低浓度校准标样获得的色谱图示例。在研究的三种不同水质类型中,峰形无明显变化。表2列出了6个方法性能研究批次的加标样品定量结果。所有6个批次的高氯酸盐和溴酸盐结果均表现出一致的方法性能;矿泉水批次的氯酸盐结果表现出一致的方法性能。硬水批次的亚氯酸盐结果表现出较大变化。
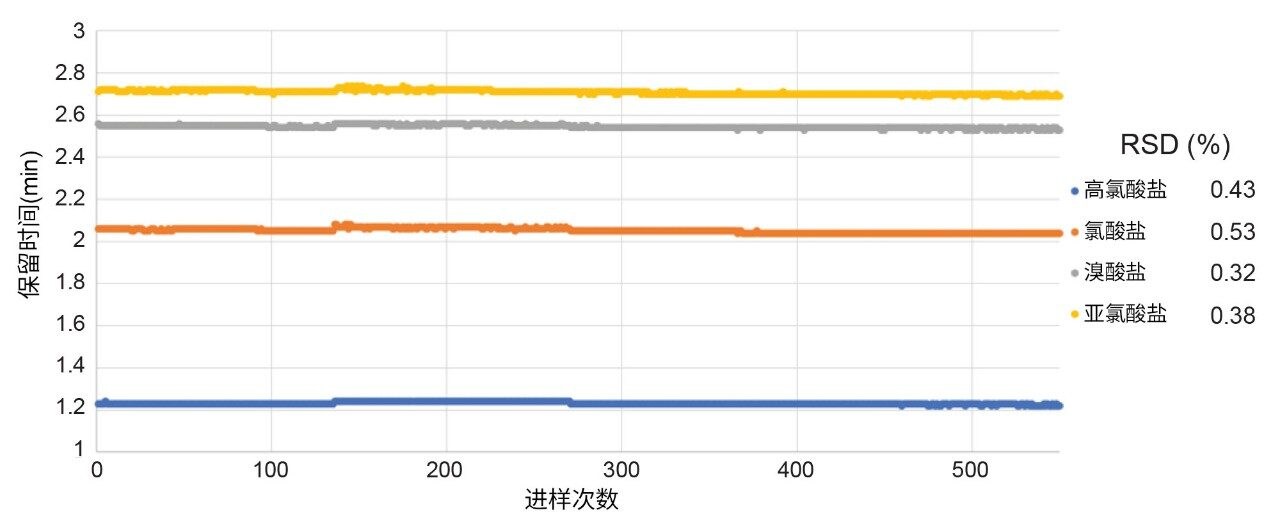
保留时间稳定性是方法性能研究中考察的一项重要因素。为考察此性能,将软水、硬水及矿泉水标准品交替进样300次,实施重复性研究。6个方法性能研究批次及保留时间稳定性研究得到的所有保留时间汇总图见图5。在整个方法性能研究和重复性研究期间,保留时间未见明显变化,所有4种含氧阴离子的RSD均低于1%。
方法性能研究数据证明,将水样直接进样至ACQUITY UPLC I-Class PLUS与Xevo TQ-XS联用系统上装配的阴离子型极性农药分析色谱柱来测定含氧阴离子的分析方法非常稳定耐用。本研究所用方法的性能优于2020年末生效的欧盟饮用水指令(EU DWD)最新要求3、现行WHO饮用水指南2和US EPA《国家饮用水基本条例》4的规定。氯酸盐和高氯酸盐的定量限为20 µg/L,溴酸盐的定量限为2 µg/L,亚氯酸盐的定量限为100 µg/L。对于氯酸盐,此定量限比EU DWD最新拟定限值低11.5倍;对于溴酸盐,比规定的限值低4倍;对于亚氯酸盐,比规定的限值低1.5倍。高氯酸盐的定量限比WHO建议的浓度限值低1.5倍。在研究过程中证明了保留时间稳定性:在所有6个方法性能研究批次和保留时间稳定性研究中,4种含氧阴离子的RSD均低于1%。此直接进样方法只需5 min即可完成分析,有助于提高样品通量。
科学家必须在其实验室内验证分析方法,证明方法性能适合预期用途,并且满足相关分析控制保证体系的要求。
720007112ZH,2021年1月