仅适用于法医毒理学应用。
过去十年来,使用毛发作为法医毒理学检测的生物基质越来越受欢迎,实验室根据国际毛发检测协会(SoHT)或欧洲工作场所药物检测协会(EWDTS)等机构的建议对一组药物进行检测1,2。 我们开发出一套稳定的样品制备工作流程和灵敏的UPLC-MS/MS方法,使用户可以测定毛发中该组药物的滥用情况,以符合指南的要求。该工作流程使用户可利用一个毛发样本测定多类药物,例如阿片类、安非他命类、可卡因、氯胺酮、丁丙诺啡、苯二氮卓类及其代谢物以及四氢大麻酚(THC)及其代谢物羧基-THC (cTHC)。在市售提取缓冲液中进行温育后,使用OASIS PRiME MCX 96孔板通过单一固相萃取(SPE)法将分析物与剩余的毛发基质分离。使用ACQUITY UPLC I-Class/Xevo TQ-S micro联用系统开发出两种LC-MS/MS方法;一种用于测量29种“碱性药物”,另一种用于测量THC、大麻二酚和大麻酚。需要使用不同的样品制备方法(使用剩余的温育混合物)以及新型LC-MS/MS方法来测量羧基-THC,以确认存在THC3。 该工作流程能够定量浓度低于两大协会推荐截止值的所有分析物,每个样品只需不到10分钟,因此可以在短时间内分析大量样品。
之前,我们讨论了在法医毒理学检测中使用毛发作为生物基质的优势,并介绍了一种高灵敏度羧基-THC(THC的一种代谢物,可用于明确证明大麻的有效使用)分析方法3。 该方法使用M3试剂从20 mg毛发基质中提取药物,然后使用OASIS PRiME HLB进行样品净化,再用ACQUITY UPLC I-Class系统/Xevo TQ-S micro质谱仪联用的LC-MS/MS方法进行分析。
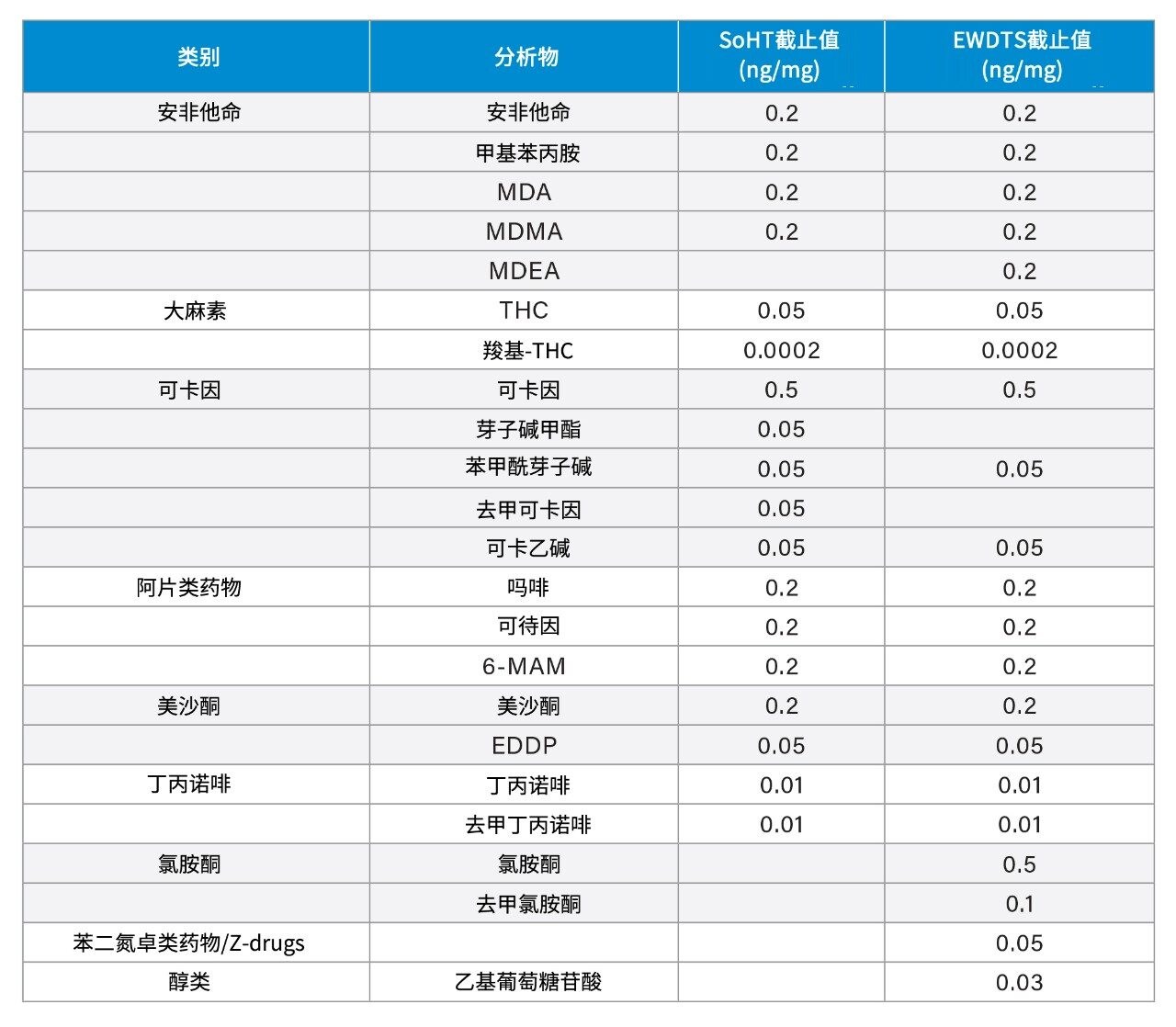
但是,在常规实践中,有大量药物需要常规分析,并且已被纳入SoHT或EWDTS等协会推荐的指南中(见表1),cTHC只是其中一种化合物。这些药物包括阿片类、安非他命类、可卡因、氯胺酮、丁丙诺啡、苯二氮卓类及其代谢物以及四氢大麻酚(THC)。每类药物的推荐截止值不同,其中一些分析物的推荐截止值非常低。因此,一些实验室应用多种不同的程序来确保该药物组中的所有分析物都在检测范围内。在实践中,这可能涉及使用不同的提取程序、单独的样品净化方案,甚至针对同一样本应用不同的后续分析方法,以确保不同药物类别获得适当的灵敏度。除应用多种方案带来的不便以外,还潜在地增加了所需样品的数量,这一点比较麻烦,因为可用的毛发数量通常有限。因此,需要一种更简化的方法;利用简单的样品制备工作流程提高实验室效率,并以快速、稳定且灵敏的分析方法对毛发中的这些分析物进行定量分析。工作流程必须能够容纳大量检测工作,同时符合SoHT和EWDTS等协会推荐的指南。
从志愿者身上采集对照毛发样品,用二氯甲烷、甲醇和二乙醚进行连续去污处理,然后剪成1~2 mm的小段。M3试剂由Comedical(意大利特伦托,http://www.comedical.biz/)提供。
称取对照毛发(10~20 mg)加入带有密封盖的玻璃离心管中,加入一组滥用药物,加标浓度范围为截止浓度的0.5倍至截止浓度的200倍。加入浓度为1 ng/mg的内标(ISTD)混合物以及M3试剂。将样品在培养箱中于100℃下加热60 min,冷却后,取100 µL样品用磷酸稀释,然后上样至OASIS PRiME MCX 30 mg 96孔板(部件号:186008916)。依次用2%甲酸和50%甲醇冲洗样品。用含氨的乙腈/甲醇(9:1 v/v)溶液洗脱分析物。取25 µL SPE洗脱液等分试样以分析“碱性药物”,再取25 µL等分试样分析THC。
采用FTN(流通针式)设计的ACQUITY UPLC I-Class系统配备30 µL进样针,能够分析15 µL样品。使用ACQUITY UPLC BEH C18色谱柱(部件号:186002350)以甲酸铵/乙腈梯度分离复溶后的样品,两种样品分别采用两种不同的进样方法,但使用相同的流动相。监测每种分析物的两个MRM通道以及每种内标的一个MRM通道。两种LC-MS/MS方法的总运行时间为10 min。
图1所示色谱图为“碱性药物”的分离结果,这些药物以SoHT和EWDTS推荐的确认截止浓度加入10 mg毛发中,显示了29种分析物的定量MRM迹线。在该药物组中,丁丙诺啡和去甲丁丙诺啡的推荐截止浓度非常低。图2所示为丁丙诺啡以0.005 ng/mg~2 ng/mg的浓度范围加入20 mg毛发中获得的校准曲线和残差图。
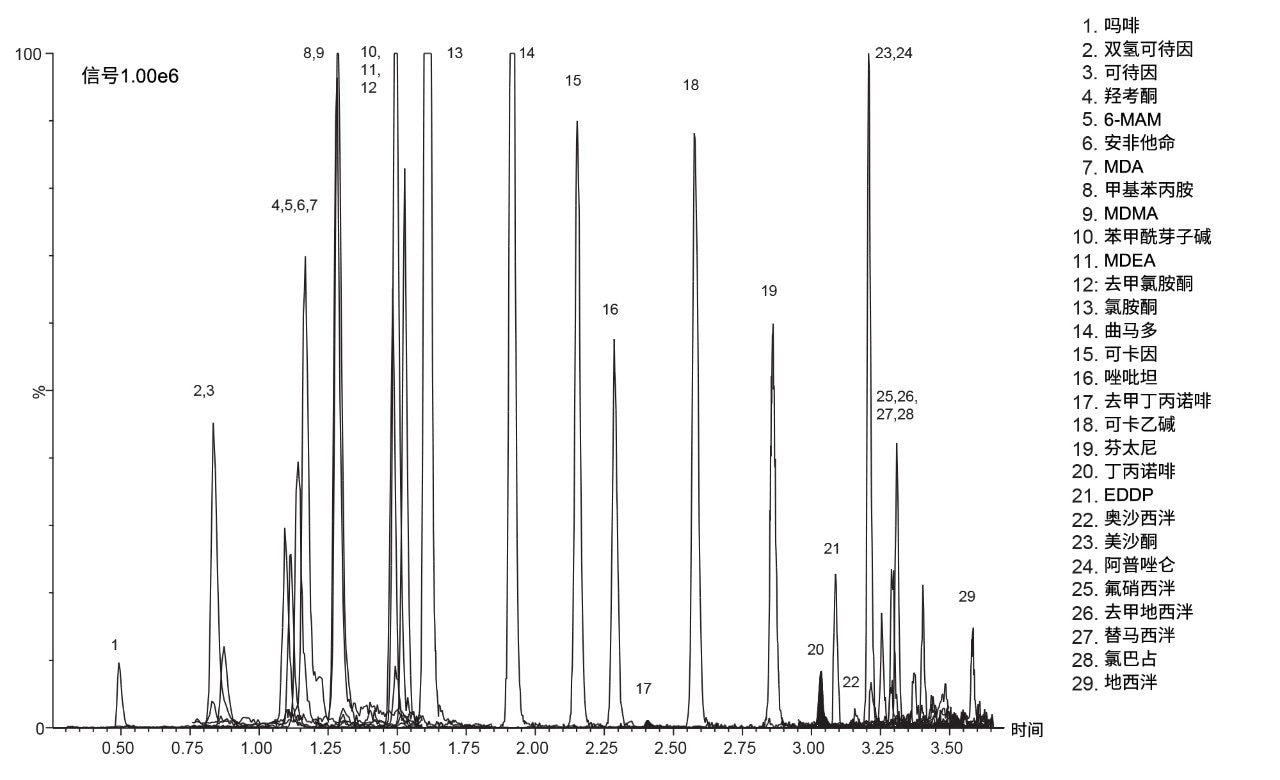
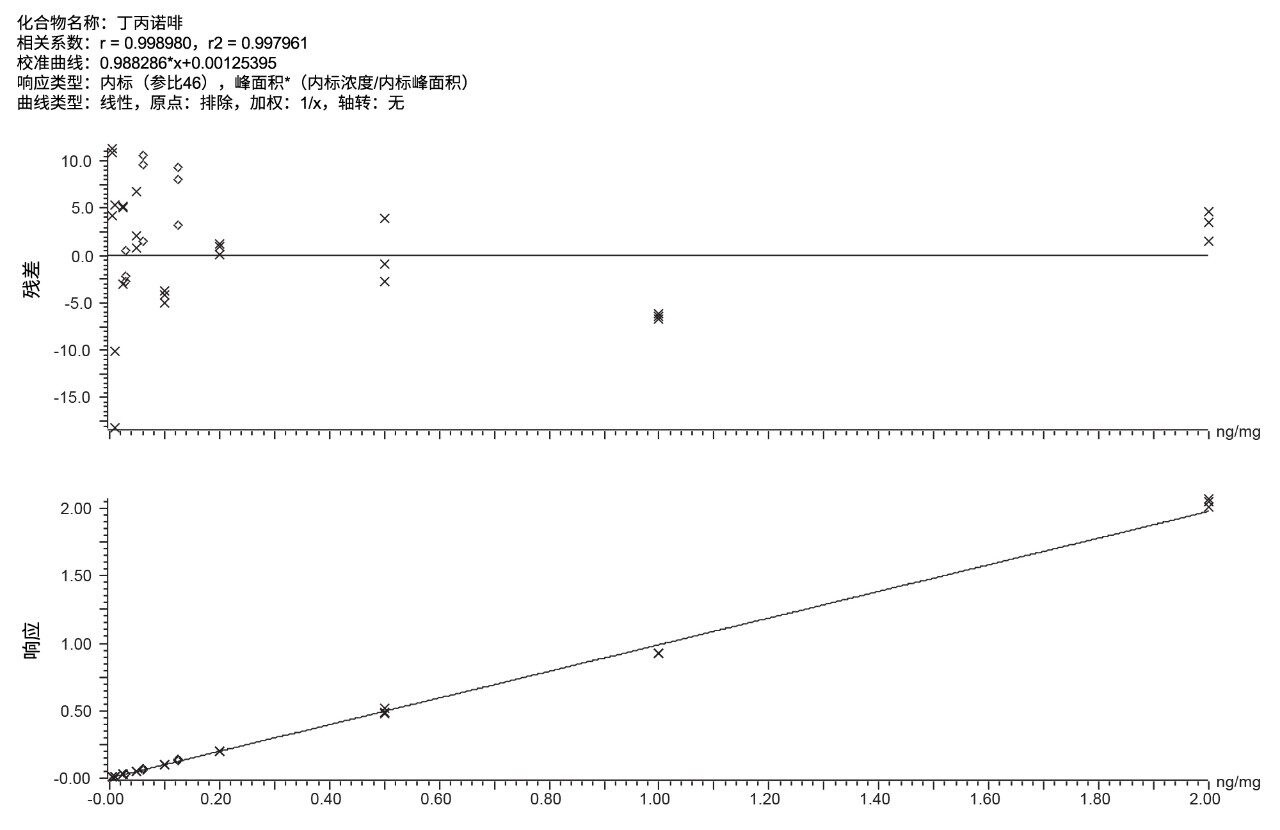
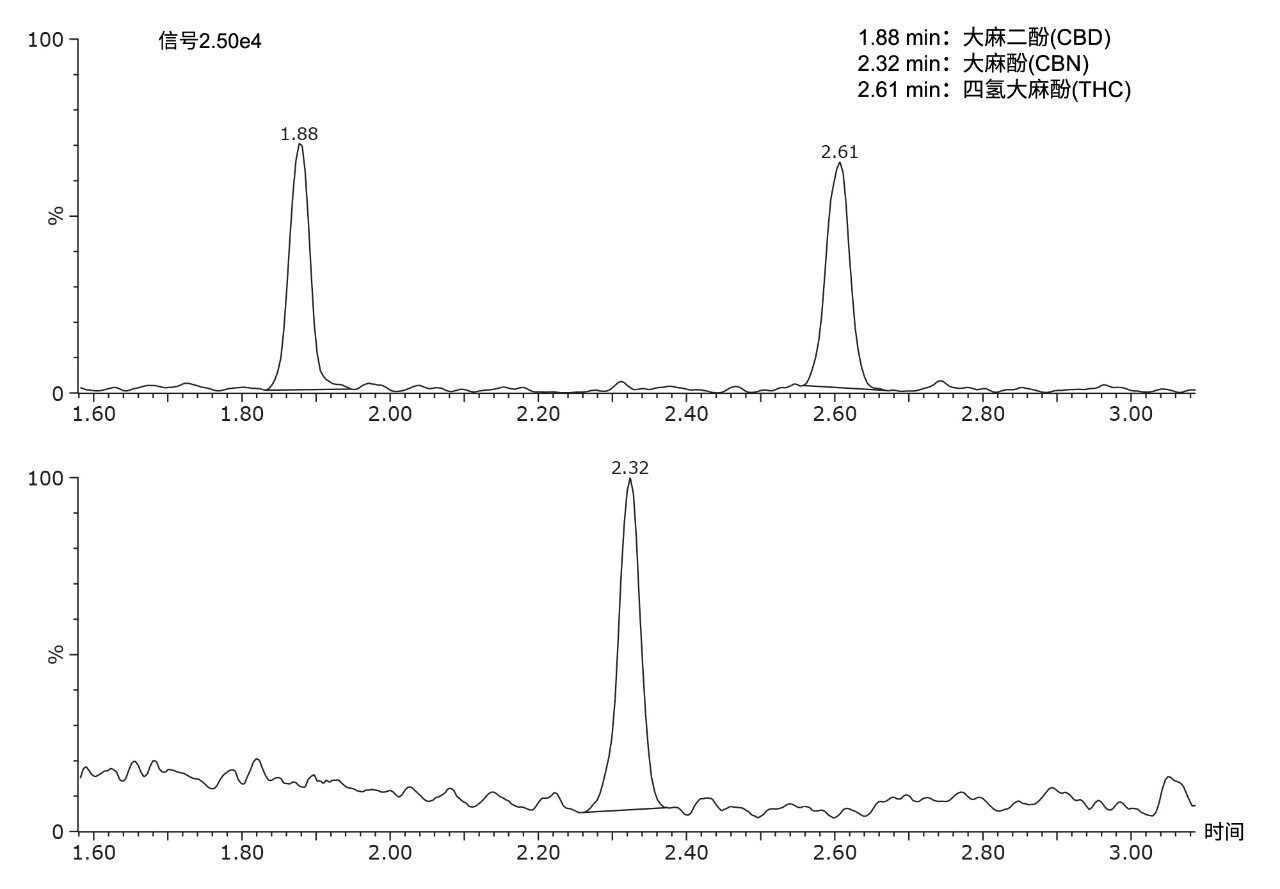
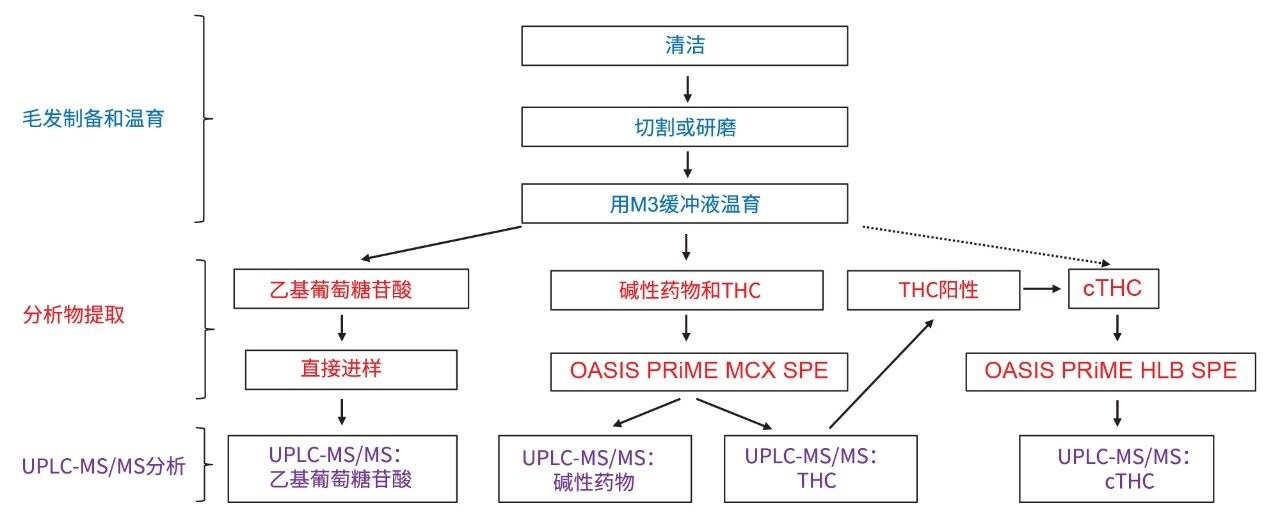
图3显示了THC、大麻二酚和大麻酚以0.05 ng/mg的浓度加入毛发中获得的定量MRM迹线。为确认样品中存在THC,利用之前报道的另一种分析方法检测剩余温育混合物中的cTHC。可以按照Joya等人介绍的方法,测量M3温育混合物中的醇类生物标志物乙基葡萄糖苷酸4。 潜在的完整工作流程示意图见图4。
随着毛发在药物检测中的运用越来越多,亟需使用快速、准确、可靠、耐用的方法对浓度非常低的滥用药物进行定量分析。本文详细介绍了一套工作流程,使用市售的提取缓冲液和OASIS PRiME MCX 96孔板,根据SoHT和EWDTS推荐的截止浓度定量分析单个毛发样本中的一组药物。将ACQUITY UPLC I-Class系统与Xevo TQ-S micro质谱仪联用,能够定量分析大量低浓度化合物,确保获得高样品通量。
720006989ZH,2020年10月修订