仅供研究使用,不适用于诊断。
本研究为使用Xevo TQ-XS质谱仪分析血浆醛固酮开发了一种高灵敏度、高选择性的临床研究方法。
醛固酮是一种属于盐皮质激素的类固醇激素,在调节血压方面发挥着重要作用。过去,人们一直采用放射免疫分析法来分析醛固酮。然而,此类方法需要使用危险的放射性同位素。此外,由于结构相似的类固醇激素和代谢物会发生交叉反应,这些方法往往缺乏专属性,而这会极大地影响检测的精密度和准确度。为了尽可能解决专属性问题,放射免疫分析法需采用耗时的手动提取方案。LC-MS/MS与具备样品追踪功能的自动化样品前处理流程相结合,为临床研究中的醛固酮分析提供了一种替代方法。这种集成工作流程解决方案有助于实现高选择性、高灵敏度的醛固酮表征,同时还能缩短样品处理时间。
本文介绍了一种使用Oasis MAX μElution提取板技术从血浆中提取醛固酮的临床研究方法,且该方法已在Tecan Freedom Evo 100/4液体处理器上实现了自动化。在ACQUITY UPLC I-Class系统上使用CORTECS C18, 2.7 μm色谱柱进行色谱分离,然后在Xevo TQ-XS串联四极杆质谱仪上进行检测,这种方法能够定量分析极低生理浓度的醛固酮(图1)。

|
系统: |
带柱温箱(CH)的ACQUITY UPLC I-Class (FTN) |
|
进样针: |
30 μL |
|
色谱柱: |
CORTECS C18, 2.7 μm, 2.1 × 100 mm(部件号:186007367) |
|
保护柱: |
带有CORTECS C18 2.7 μm VanGuard小柱(部件号:186007682)的VanGuard小柱卡套(部件号:186007949) |
|
流动相A: |
0.05 mM氟化铵水溶液 |
|
流动相B: |
甲醇 |
|
进样针清洗溶剂: |
甲醇 |
|
清洗时间: |
6 s |
|
清除溶剂: |
35%甲醇水溶液 |
|
柱温: |
45 °C |
|
进样体积: |
25 μL |
|
流速: |
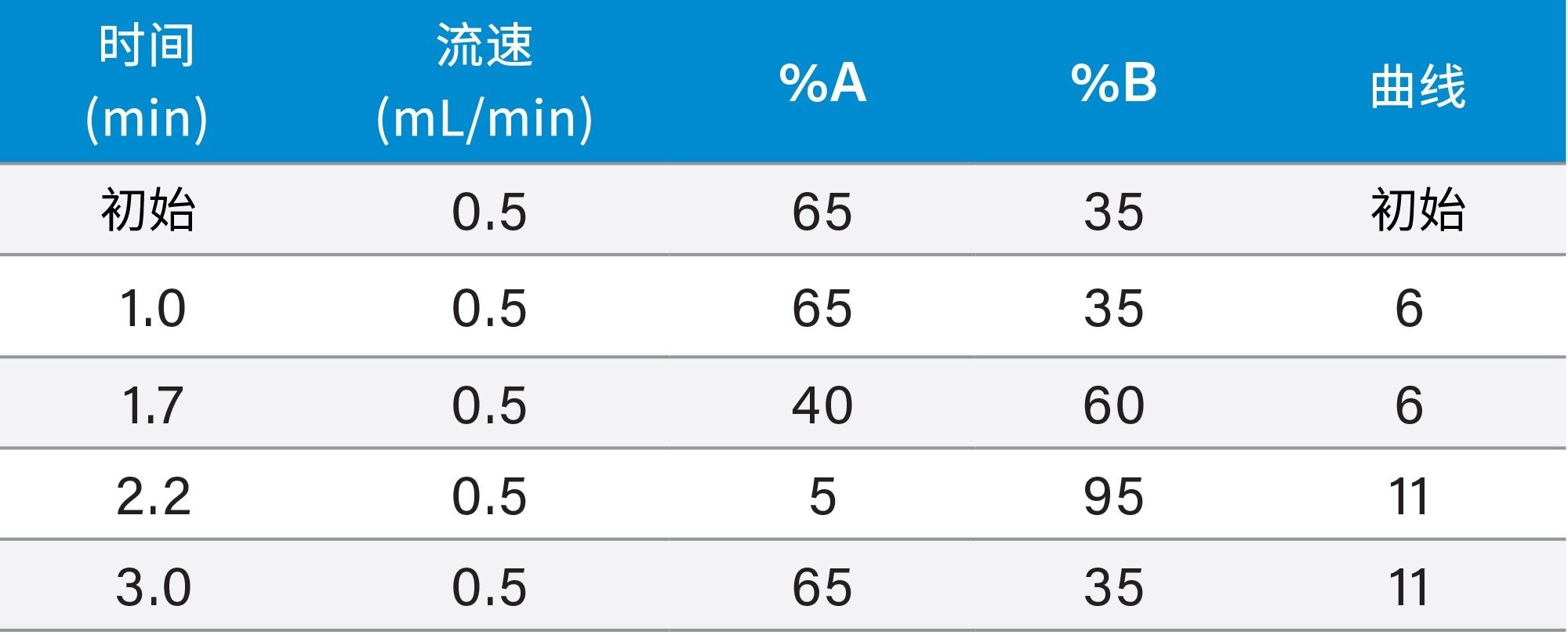
见表1 |
|
梯度: |
见表1 |
|
运行时间: |
3.5 min |
|
系统: |
Xevo TQ-XS |
|
分辨率: |
MS1 (0.75 FWHM) MS2 (0.5 FWHM) |
|
采集模式: |
多重反应监测(MRM)(详见表2) |
|
极性: |
ESI- |
|
毛细管电压: |
2.75 kV |
|
离子源温度: |
150 °C |
|
脱溶剂气温度: |
600 °C |
|
扫描间延迟时间: |
自动 |
|
通道间延迟时间: |
自动 |

带TargetLynx定量应用软件的MassLynx软件4.2版
醛固酮认证参比溶液和醛固酮 – 2H4稳定标记内标购自Sigma Aldrich(英国普尔)。
在MSG4000经处理的血清(Golden West Biologicals,美国)中制备标曲溶液,在混合人血浆(BioIVT,英国)中制备质量控制样品(QC)。制备浓度范围为8~4162 pmol/L的醛固酮标曲溶液,以及浓度为36 pmol/L、286 pmol/L和2932 pmol/L的QC样品。
醛固酮浓度数据除以2.774可将SI单位转换为传统的质量单位(pmol/L转换为pg/mL)。
使用液体移取器进行样品提取,提取前先将样品在4000 g转速下离心5 min。向200 μL样品中加入25 μL内标溶液(5550 pmol/L醛固酮-2H4)、200 μL 70/30 (v/v)甲醇/0.1 M硫酸锌和500 μL水,每次添加试剂之后充分混合。最后将样品在4000 g转速下离心5 min。
先后使用150 µL甲醇和水活化和平衡Oasis MAX µElution提取板(部件号:186001829)。从每份预处理的样品中取600 µL上样至Oasis MAX µElution提取板的各个孔中,使样品缓慢通过板孔。接下来,分别使用50 µL含1% (v/v)甲酸的10% (v/v)乙腈水溶液*、50 µL含1% (v/v)氨水的10% (v/v)乙腈水溶液*连续清洗,除去潜在的干扰物质。然后,使用30 µL 60%乙腈水溶液洗脱分析物,最后在洗脱样品中加入35 µL水。*每周配制。
当单独检查与醛固酮极性类似的其他结构相关化合物(皮质醇、可的松、18-羟基皮质酮、皮质酮、11-脱氧皮质醇、21-脱氧皮质醇、强的松和强的松龙)时,在醛固酮的保留时间内未观察到显著干扰(回收率偏差在±15%范围内)。分析其他内源性化合物(白蛋白、胆红素、尿酸、脂肪乳剂、甘油三酯和胆固醇)时,未观察到显著干扰(回收率偏差在±15%范围内)。
分析高浓度样品之后,在后续的空白进样中未观察到明显的系统残留污染(小于最低浓度标曲溶液的20%)。将高浓度样品成功稀释5倍后,醛固酮的平均准确度为100%,RSD为2.2%。
使用加标到经处理的血清中的醛固酮在校准范围内和校准范围以下进行了四次进样(每个浓度水平n = 40),以此评估分析方法的灵敏度。该方法使2.8 pmol/L醛固酮的定量结果也具有较高精密度(<20% RSD)。在8.3 pmol/L浓度下的信噪比(PtP)高于10。
我们在五天内每天对三个浓度的QC样品进行一次萃取和定量分析(每个浓度五个重复样品,n = 25),以此确定该方法的总精密度。每个QC水平设置五个重复样,以评估方法的重复性。醛固酮的低、中、高浓度分别为36、286和2932 pmol/L。
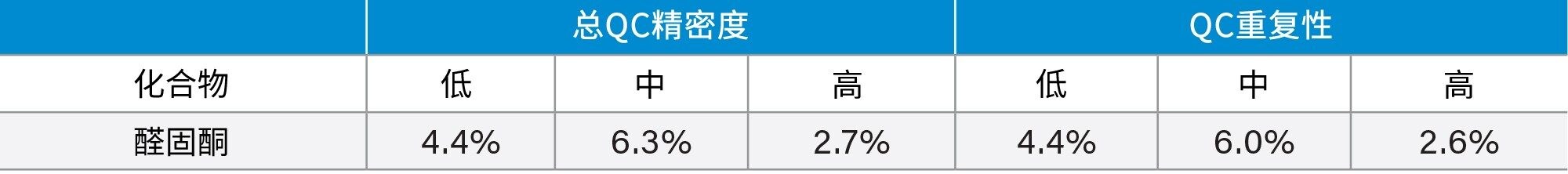
将不同比例的高浓度和低浓度分析物混合样品组合进行分析的结果表明,该方法在醛固酮浓度范围6.7–4994 pmol/L内呈线性。此外,在所有分析中,加标经处理的血清样品的校准曲线均呈线性,且决定系数(r2) > 0.995。
使用单个供体血浆样品(n = 6)研究了醛固酮的基质效应。基质因子计算结果如表4所示。基于分析物:内标响应比率计算归一化的基质因子,结果表明内标可以补偿观察到的所有离子抑制效应。
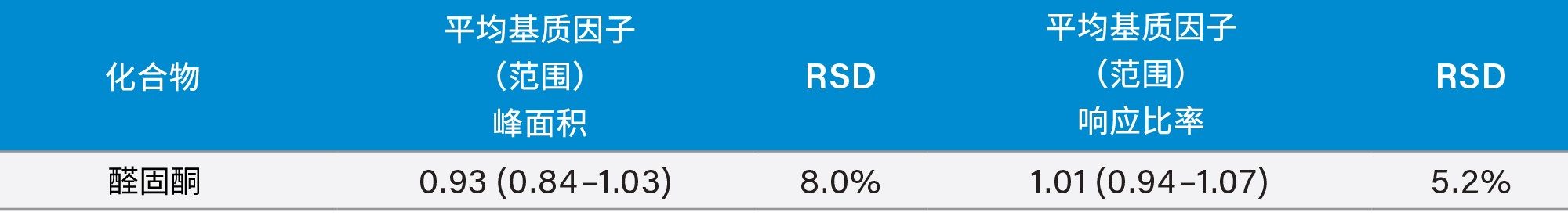
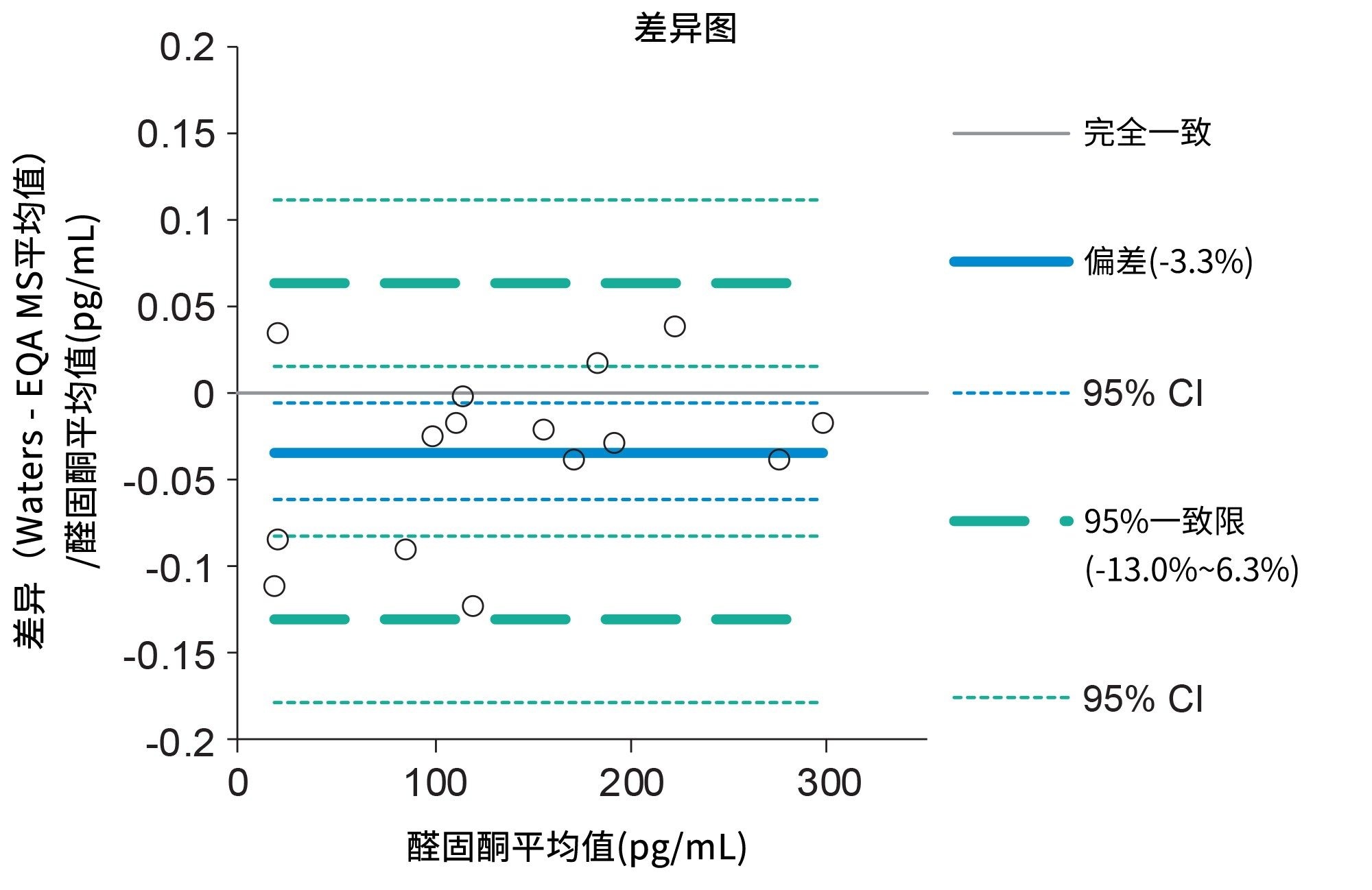
通过分析英国NEQAS的EQA样品评估醛固酮的分析偏差。将所得结果与这些样品的质谱法平均结果进行比较,并进行Deming回归分析(表5)。醛固酮的Altman-Bland一致性分析结果表明,平均方法偏差为-3.3%,与EQA质谱法分析醛固酮的平均值非常一致(图2)。

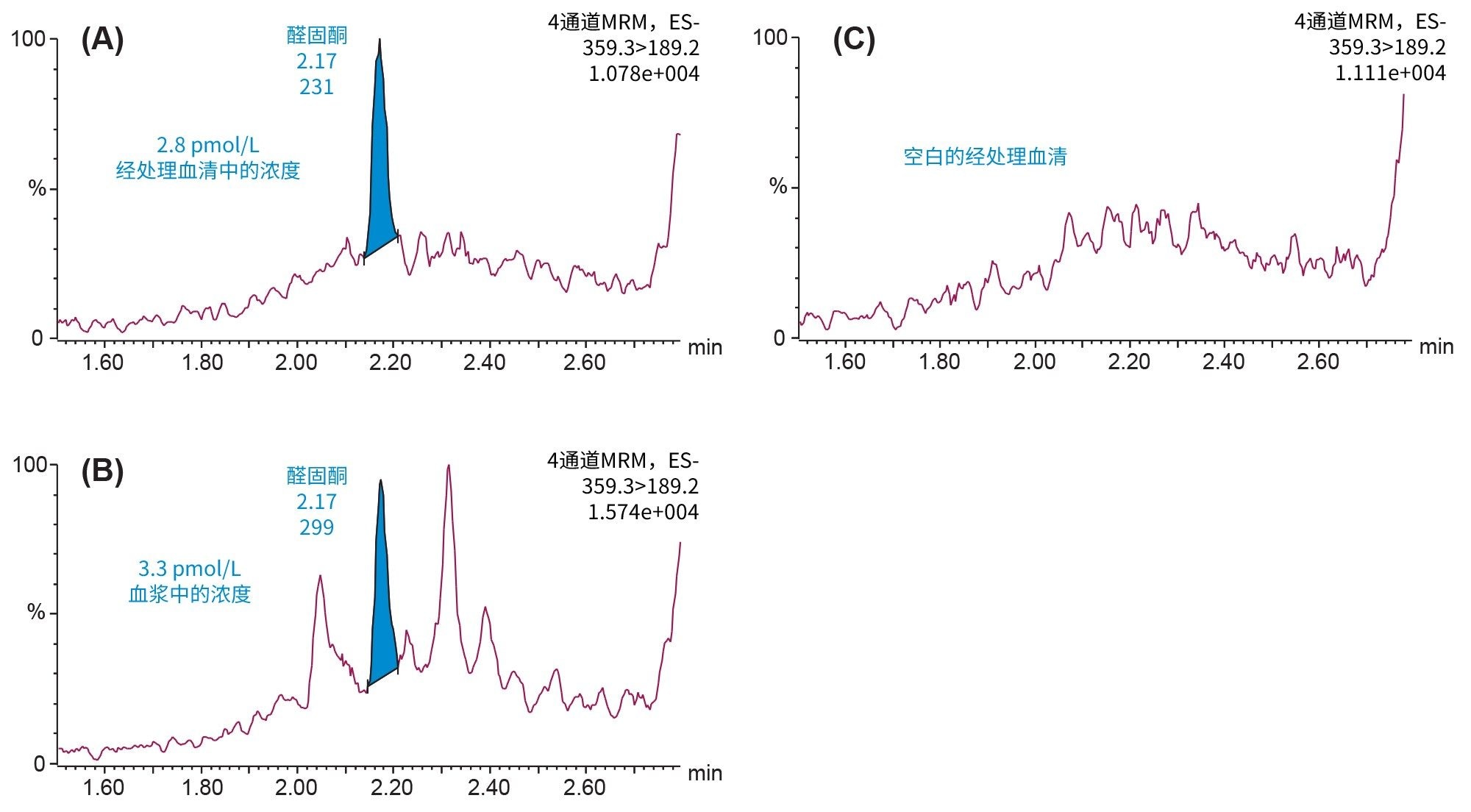
用低浓度血浆样品评估分析灵敏度和选择性,比较纯样品与用于校准的经处理血清加标样品。图3所示为该方法的分析灵敏度,从图中可以看出,该方法在血浆和经处理血清中检出醛固酮峰的浓度分别为3.3 pmol/L (1.2 pg/mL)和2.8 pmol/L (1 pg/mL)。
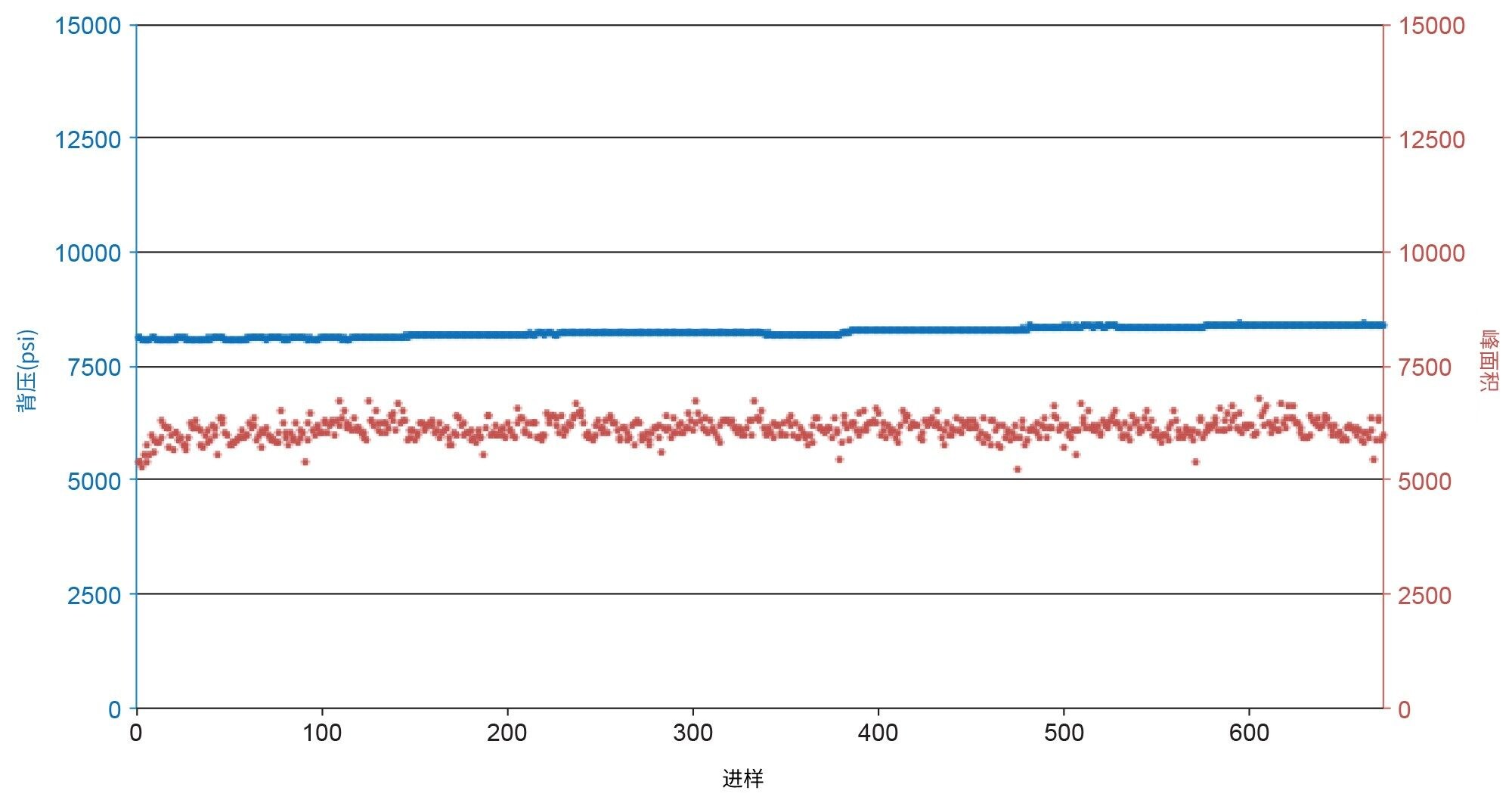
在48小时内连续分析672份提取的血浆样品,评估方法稳健性。图4显示了柱压的微小变化,整个分析过程中柱压增加380 psi(平均值= 8247 psi,RSD = 1.3%),醛固酮峰面积偏差非常小(平均值= 6122,RSD = 3.6%),表明醛固酮的分析方法具有很高的稳健性。
本研究为使用Xevo TQ-XS质谱仪分析血浆醛固酮开发了一种高灵敏度、高选择性的临床研究方法。
Xevo TQ-XS能够仅用200 μL的样品体积分析低至8 pmol/L的低生理水平醛固酮。该方法在线性范围内表现出良好的精密度。EQA样品的准确度评估结果表明,该方法分析醛固酮的结果与参比值具有良好的一致性。利用Tecan文件转换器和MassLynx LIMS Interface,可以将方法自动化的优势与液体处理器的样品追踪功能相结合,从而改进实验室工作流程并减少样品处理工作量,有效避免潜在的操作人员失误。
感谢Wythenshawe医院的Brian Keevil教授及其同事们提供用于评估的样品。
720006677ZH,2019年9月