
仅供研究使用,不适用于诊断。
本研究为血清中25OHD3、25OHD2、C3-epi-25OHD3和24,25(OH)2D3的LC-MS/MS分析成功开发出了一种临床研究方法。研究证明,Oasis PRiME HLB可去除磷脂的优势对于维生素D代谢物分析很有帮助,其具有以下优势:
开发一种用于分析25-羟基维生素D3 (25OHD3)、25-羟基维生素D2 (25OHD2)、24,25-二羟基维生素D3 (24,25(OH)2D3)和C3-epi-25-羟基维生素D3 (C3-epi-25OHD3)的LC-MS/MS方法。本方法采用Xevo TQ-S micro质谱仪进行检测,并使用Waters Oasis® PRiME HLB最大限度减少磷脂干扰物和提高分析灵敏度。
使用LC-MS/MS测定血清中的维生素D代谢物含量时,基质干扰物质会带来挑战。其中,疏水性与25-羟基维生素D (25OHD)相似的溶血磷脂酰胆碱(LysoPCs 16:0、18:1和18:0)尤为棘手,已有研究表明,在质谱分析过程中,这类物质会产生离子抑制。尽管LysoPCs的结构各不相同,但研究表明它们很难通过样品制备过程去除,也很难与维生素D代谢物实现色谱分离。
本文介绍了一种使用Oasis PRiME HLB μElution固相萃取(SPE)板(图1)的优化方法,评估了该方法相较于Oasis HLB SPE和蛋白质沉淀法的LysoPCs去除性能。本研究使用Waters ACQUITY UPLC HSS PFP色谱柱分离三种样品萃取方法所得萃取物中的25OHD2、25OHD3、24,25(OH)2D3和C3-epi-25OHD3,并将峰面积与萃取物中目标LysoPCs(16:0、18:1和18:0,母离子为m/z 496、m/z 522和m/z 524,子离子为m/z 184)的峰面积进行了对比。使用Waters ACQUITY UPLC I-Class (FTN)/Xevo TQ-S micro系统评估了优化后的萃取方法的性能。
将稳定的标记内标加入100 μL校准品、QC样品和测试样品中,使用甲醇/硫酸锌(水溶液)进行蛋白质沉淀。
离心之后,将上清液转移到Oasis PRiME HLB µElution板孔内。使不同浓度的乙腈(水溶液)(0–100%)通过SPE吸附剂以洗脱分析物,使用每种浓度的洗脱溶液制备三个重复样,然后分析所得洗脱液,得到洗脱曲线。
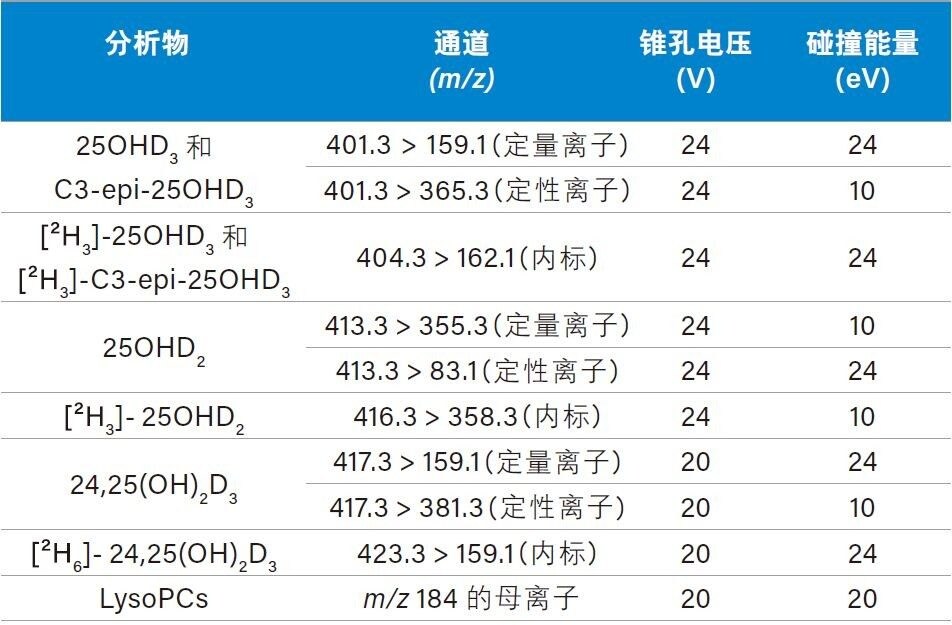
使用配备2.1 x 100 mm ACQUITY UPLC HSS PFP色谱柱的ACQUITY UPLC I-Class系统,以水、甲醇、醋酸铵和甲酸为流动相,梯度分离经过稀释的洗脱液,并在Xevo TQD上采用表1所列的MRM通道和母离子扫描参数进行检测。
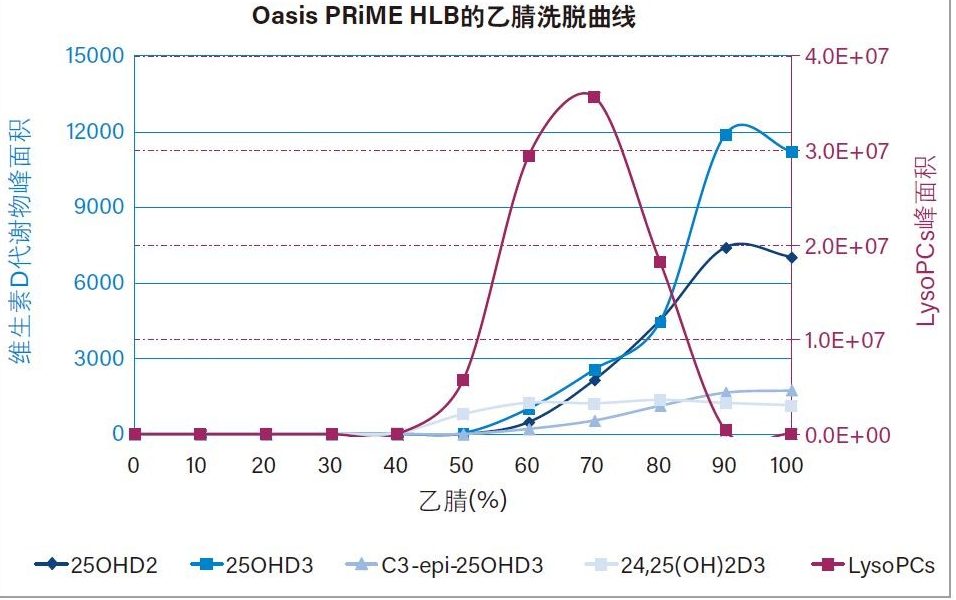
将三个重复样中每种目标维生素D代谢物和LysoPCs的平均峰面积绘制成散点图,得到其洗脱曲线(图2)。
通过洗脱曲线可以看出,LysoPCs开始从Oasis PRiME HLB吸附剂中洗脱出来时的有机溶剂浓度与维生素D代谢物开始洗脱出来时的有机溶剂浓度接近,这是因为它们的疏水性相似。但是,当乙腈(水溶液)的浓度> 90%时,几乎所有LysoPCs都保留在了Oasis PRiME HLB SPE吸附剂上,而维生素D代谢物成功洗脱。因此,优化方法选择以25%乙腈(水溶液)作为清洗溶液,以100%乙腈作为洗脱溶液。
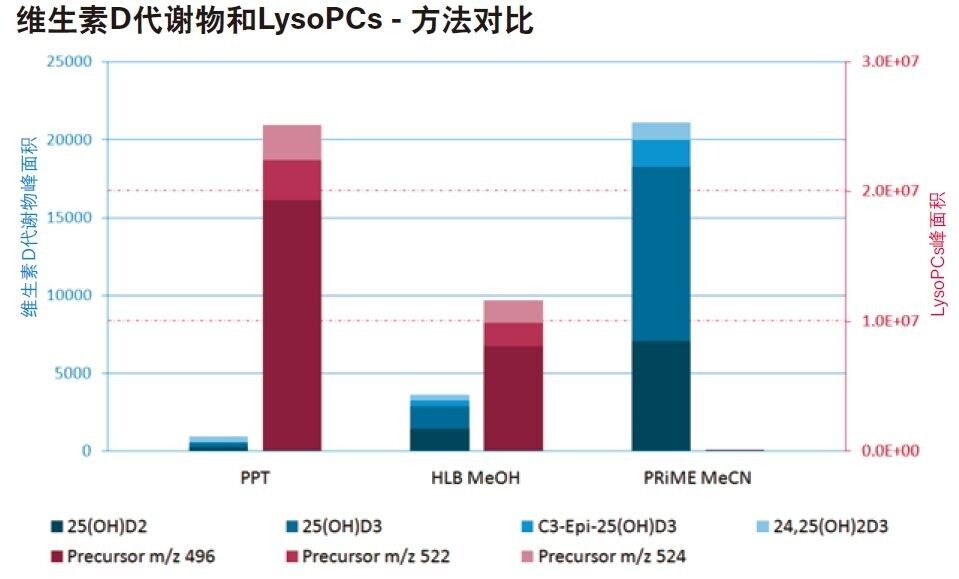
我们对比了优化Oasis PRiME HLB方法、使用甲醇/硫酸锌(水溶液)的简单蛋白质沉淀萃取法,以及使用甲醇作为洗脱溶剂的优化Oasis HLB方法这三种方法得到的LysoPCs和维生素D代谢物平均峰面积。结果汇总于图3。
与使用甲醇的Oasis HLB方法和蛋白质沉淀法相比,使用乙腈的Oasis PRiME HLB方法去除了99%以上的目标LysoPCs。因此,使用该方法得到的维生素D代谢物峰面积比Oasis HLB方法增加了5倍,比蛋白质沉淀方案增加了10倍。
我们使用ACQUITY UPLC I-Class/Xevo TQ-S micro系统评估了优化后的萃取方法的性能。连续五天的实验结果显示,25OHD3、25OHD2、C3-epi-25OHD3和24,25(OH)2D3在下列浓度范围内(表2)的所有校准曲线相关系数(r²)均> 0.99,表中还列出了nmol/L到ng/mL的换算系数。
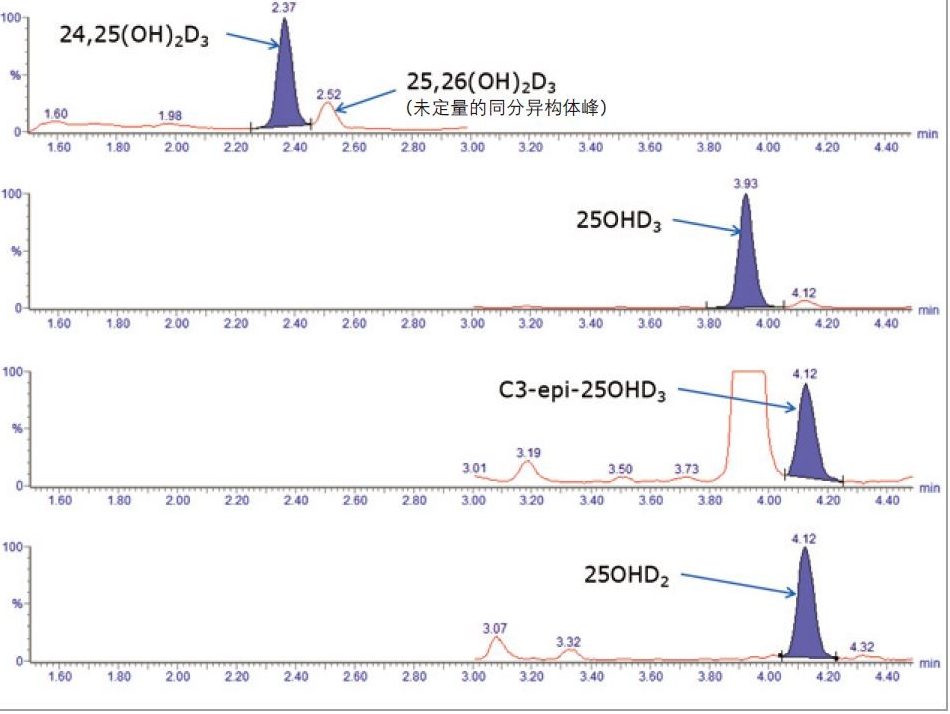
ACQUITY UPLC HSS PFP色谱柱成功分离了C3-epi-25OHD与25OHD(包括25OHD2和25OHD3)。24,25(OH)2D3定量和定性通道中均存在的一个同分异构体峰也分离了出来,经确认为25,26(OH)2D3。图4所示为示例色谱图,表明进样之间的运行时间< 8 min。
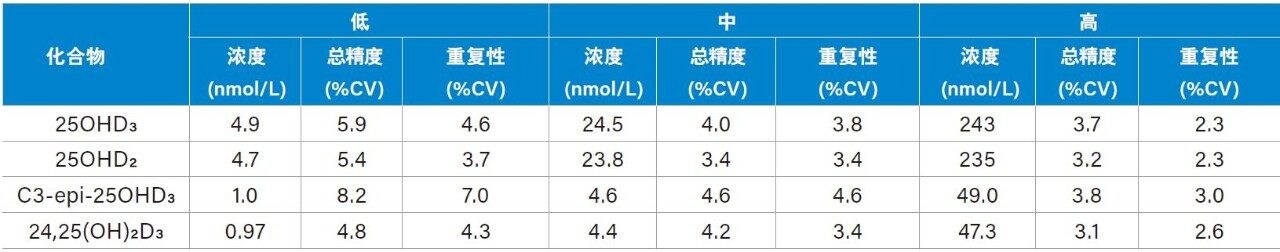
连续五天萃取低、中、高浓度的血清样品(每个浓度制备五个重复样,n=25)并进行定量分析,以评估方法的总精度和重复性。如表3所示,所有结果均≤ 8.2%CV。
通过分析DEQAS(维生素D外部质量评估计划)样品和NIST SRM972a(美国国家标准技术研究所(NIST)标准参比物质972a)评估方法的准确性,然后将计算所得的浓度与NIST指定值对比。25OHD3的Deming回归方程为y=1.02x-1.09,Altman Bland分析结果表明其一致性良好(最小偏差仅为-0.1%)。25OHD2只有七个数据点可用,与NIST指定值对比得出的总体平均百分比偏差为-0.9%(在-9.7%~10.0%范围内)。虽然对于C3-epi-25OHD3 DEQAS样品的结果呈现明显的分散趋势,但其结果与NIST SRM972a参比标准物质对比呈现出良好的一致性,所有被测样品的偏差都在±6.7%以内(使用含有C3-epi-25OHD3的三个样品制备三个重复样)。对比DEQAS试验性研究得出的LC-MS/MS ALTM值评估15个样品的24,25(OH)2D3分析结果,同样观察到结果呈现明显的分散趋势(NIST没有指定值)。LC-MS/MS ALTM值仅来源于六个实验室,参与实验室返回的结果之间的标准偏差较大。

分三天在经过处理的血清样品中加标低、中、高浓度的分析物并进行样品萃取(每个浓度制备10个重复样,n=30),根据分析结果评估分析灵敏度。加标浓度为1 nmol/L时的25OHD3和25OHD2分析结果,以及加标浓度为0.5 nmol/L时的24,25(OH)2D3和C3-epi-25OHD3分析结果均达到了< 20%CV的精度,且S:N (ptp) > 10:1。
本研究为血清中25OHD3、25OHD2、C3-epi-25OHD3和24,25(OH)2D3的LC-MS/MS分析成功开发出了一种临床研究方法。研究证明,Oasis PRiME HLB可去除磷脂的优势对于维生素D代谢物分析很有帮助,其具有以下优势:
720005965ZH,2017年5月