仅供研究使用,不适用于诊断。
本文介绍了一种临床研究方法,该方法在添内标(5-氟尿嘧啶-13C15N2)之后,对血浆样品进行液液萃取。
5-氟尿嘧啶是一种抗肿瘤制剂,通过干扰脱氧核糖核酸(DNA)合成以及小范围抑制核糖核酸(RNA)形成抑制肿瘤生长。由于5-氟尿嘧啶代谢的个体差异非常大1,灵敏度和选择性俱佳的测定方法将有助于5-氟尿嘧啶的药代动力学和药效动力学临床研究。
本文介绍了一种临床研究方法,该方法在添内标(5-氟尿嘧啶-13C15N2)之后,对血浆样品进行液液萃取。然后使用配备Waters ACQUITY UPLC HSS PFP色谱柱(2.1 × 100 mm, 1.8 µm)的ACQUITY UPLC I-Class系统进行色谱分离,所需时间仅为3 min,最后在Xevo TQD质谱仪上进行检测(图1)。

样品前处理:5-氟尿嘧啶认证参比标准品及其稳定标记内标(13C15N2)购自Toronto Research Chemicals(加拿大安大略省多伦多)。使用购自Golden West Biologicals(美国加利福尼亚州特曼库拉)的混合血浆作为替代基质制备标准曲线样品品。5-氟尿嘧啶的标准曲线范围为20~2000 ng/mL。使用相同的混合血浆分别制备浓度为40、350、750和1500 ng/mL的QC样品。
样品萃取:向50 µL样品中添加5 µL 10 µg/mL溶于甲醇的内标(ISTD),旋涡混合30 s。加入500 µL含0.1%甲酸(体积比)的乙酸乙酯溶液,旋涡混合30 s,然后以16,100 g的离心力离心2 min。取400 µL上清液在40 ℃下氮气吹干。用75 µL 0.1%甲酸水溶液复溶后,在UPLC-MS/MS上分析。
|
系统: |
ACQUITY UPLC I-Class (FTN) |
|
进样针: |
30 μL |
|
色谱柱: |
ACQUITY UPLC HSS PFP色谱柱 |
|
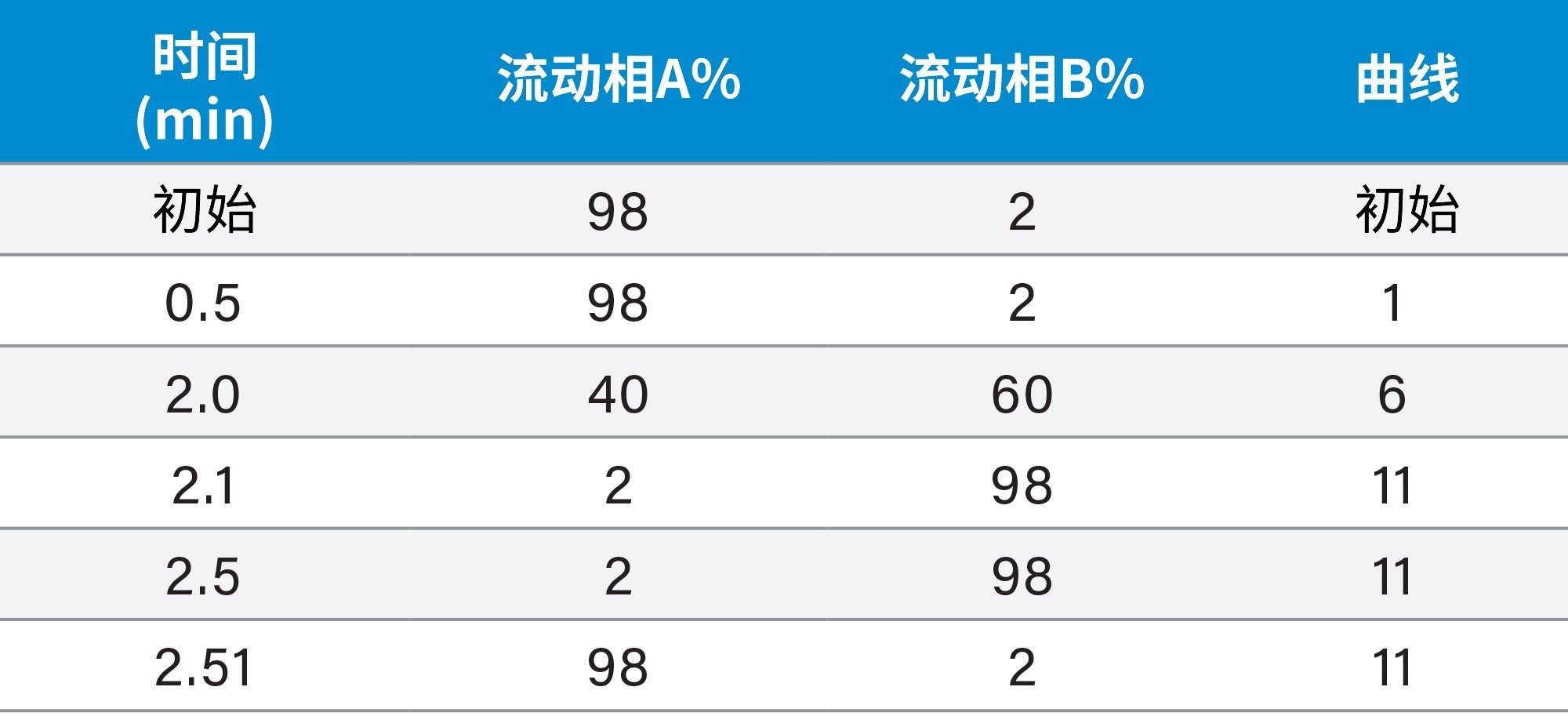
流动相A: |
水 |
|
流动相B: |
乙腈 |
|
进样针清洗溶剂: |
80%甲醇水溶液+0.1%甲酸 |
|
清除溶剂: |
流动相A |
|
密封清洗液: |
20%甲醇水溶液 |
|
柱温: |
35 °C |
|
进样体积: |
20 μL |
|
流速: |
0.40 mL/min |
|
运行时间: |
3.0 min(进样之间间隔约 3.5 min) |
|
系统: |
Xevo TQD |
|
分辨率: |
MS1 (0.7 FWHM) MS2 (0.7 FWHM) |
|
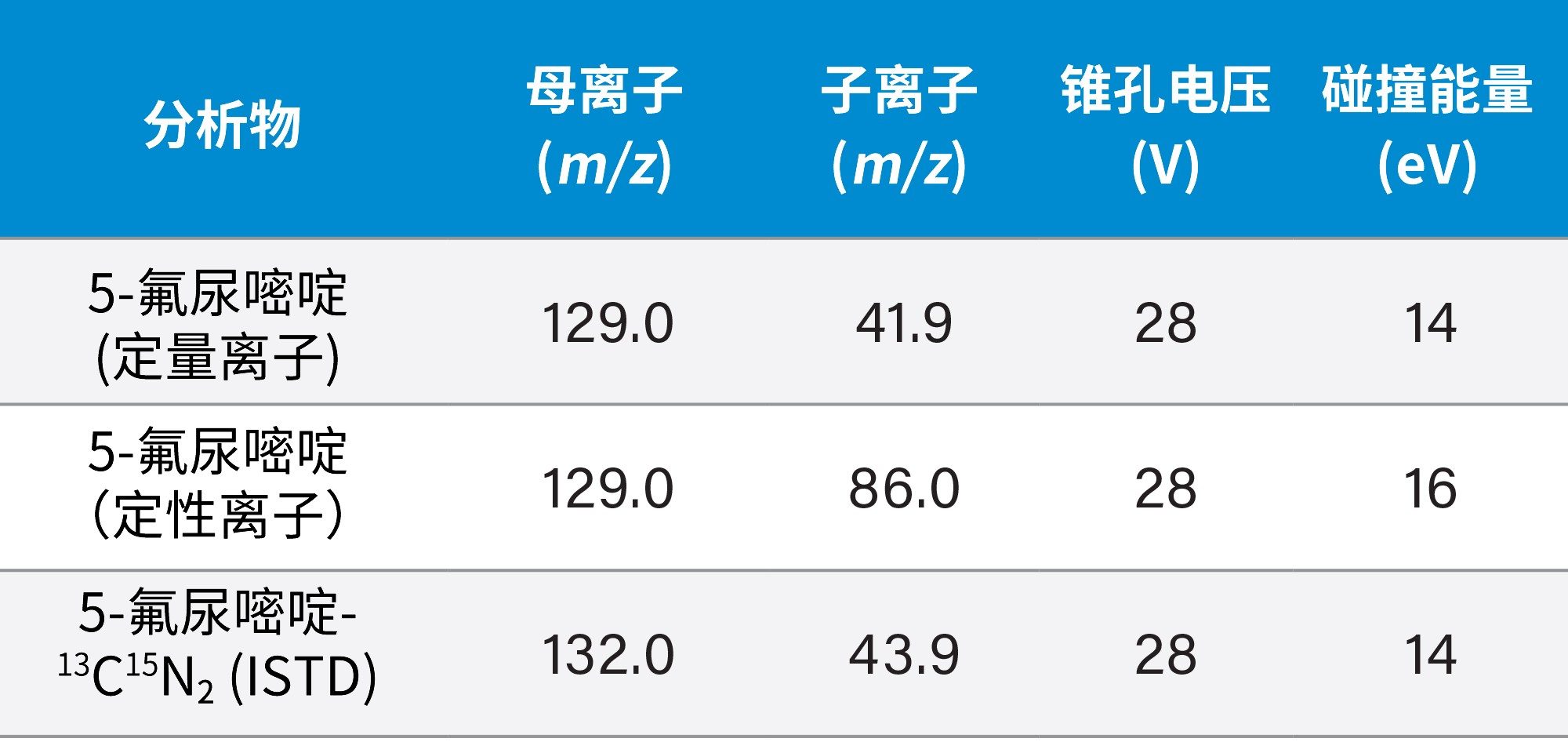
采集模式: |
多重反应监测(MRM)(详见表2) |
|
极性: |
ESI负离子模式 |
|
毛细管电压: |
3.0 kV |
|
离子源温度: |
140 °C |
|
脱溶剂气温度: |
450 °C |
|
驻留时间: |
0.05 s(5-氟尿嘧啶),0.015 s(内标) |
|
扫描间延迟时间: |
0.02 s |
|
通道间延迟时间: |
0.01 s |
带TargetLynx应用管理软件的MassLynx软件4.1版
在上述色谱条件下,5-氟尿嘧啶与血浆中萃取出的同分异构干扰物(大约在1.1 min处洗脱)实现了分离。5-氟尿嘧啶的保留时间约为1.18 min。
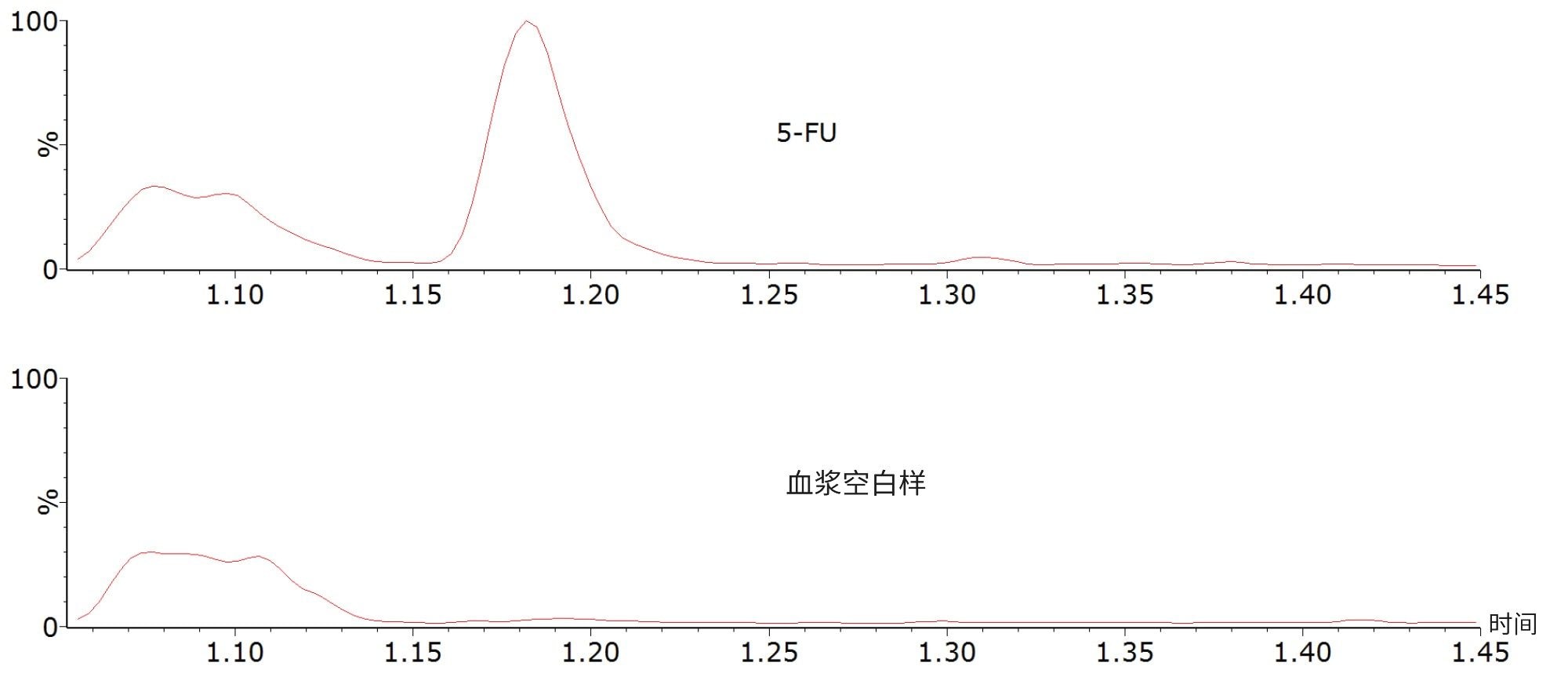
在分析5-氟尿嘧啶浓度高达10,000 ng/mL的血浆样品之后,未观察到系统残留。
分析灵敏度研究结果表明,该方法5-氟尿嘧啶的定量限为7.5 ng/mL(RSD < 20%,偏差< 15%)。
精度评估试验设计为五天内每天萃取并定量分析四个不同浓度的QC样品(每个浓度五个重复样,n = 25)。研究中分析了各QC水平的五个重复样,以此评估方法的重复性。表3显示了四个浓度水平的5-氟尿嘧啶的总精度和重现性的RSD均小于9.0%。
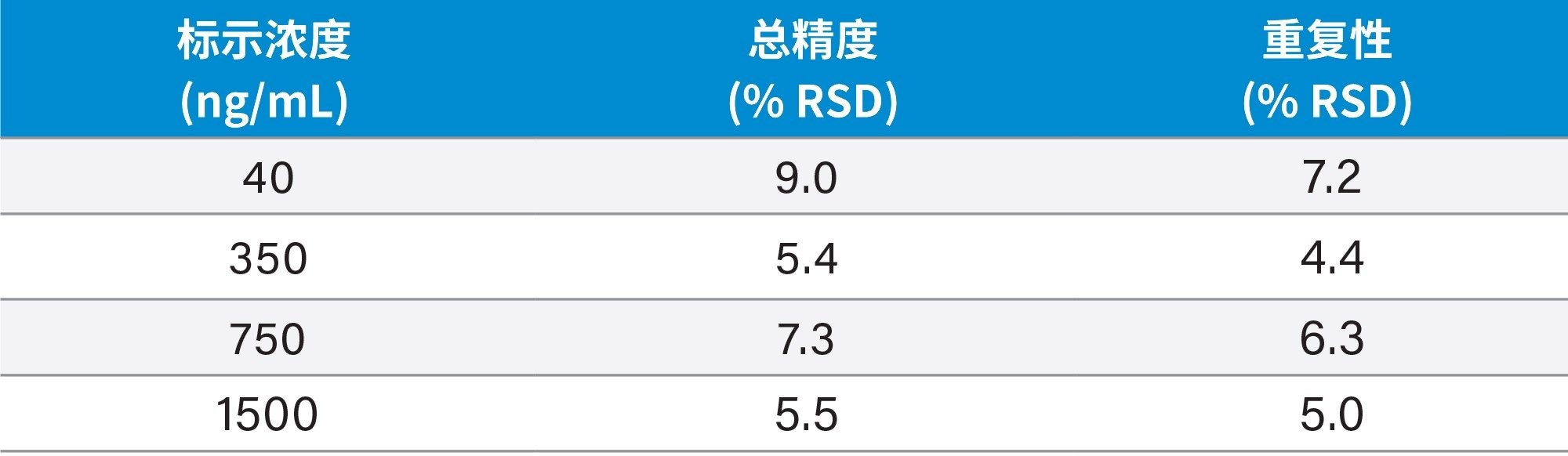
将高浓度和低浓度5-氟尿嘧啶混合样品按不同比例混合并进行分析,结果表明该方法在14~2600 ng/mL的范围内呈线性。
本研究评价了血浆中含有低浓度(40 ng/mL)和高浓度(1500 ng/mL)5-氟尿嘧啶时的基质效应(n = 6)。低浓度下的基质效应因子为0.62~0.69(平均值0.66),高浓度下的基质因子为0.46~0.75(平均为0.65)。使用同位素标记的5-氟尿嘧啶内标可补偿观察到的基质效应,得到低浓度和高浓度下的基质因子分别为0.94~0.98(平均值0.96)和0.96~1.05(平均值1.02)。
通过测定添加了高浓度的内源性化合物(白蛋白、胆红素、胆固醇、甘油三酸酯和尿酸)和外源性物质20%脂肪乳剂)的混合血浆样品中5-氟尿嘧啶高/低加标(40 ng/mL和1500 ng/mL)的回收率(n = 3),评估了这些物质可能对分析造成的干扰。所得回收率范围为90.5%~110.6%。评估对乙酰氨基酚、氟康唑、5,6-二氢-5-氟尿嘧啶、酮康唑、伊曲康唑、甲氨蝶呤、苯妥英、泊沙康唑、尿嘧啶和伏立康唑对分析的干扰作用,得到回收率范围为91.8%~108.0%。导致回收率超出85%~115%范围的物质被视为干扰物。
血清外部质量保证样品(n = 6,范围100~2000 ng/mL)购自Asqualab(法国巴黎)。结果处于该方案的可接受范围内,平均偏差为2.6%。
720006049ZH,2017年7月