
USP和AOAC等机构已建立分析膳食补充剂中异黄酮的标准方法。这些方法采用配备C18色谱柱以及紫外和可见光(UV-Vis)光谱的反相LC进行分离和定量。由于这些化合物具有结构相似性,因此这些方法的色谱运行时间通常会超过70 min。因此,十分有必要开发更快速的异黄酮分析方法。
本应用纪要(第1篇,共3篇)介绍了USP方法到ACQUITY Arc UHPLC系统的方法转换。采用ACQUITY Arc系统的分析时间仅为18 min,其中包括色谱柱清洗和平衡时间。使用ACQUITY QDa质谱检测器可加快本研究所述的方法转换。
此方法的优势包括:
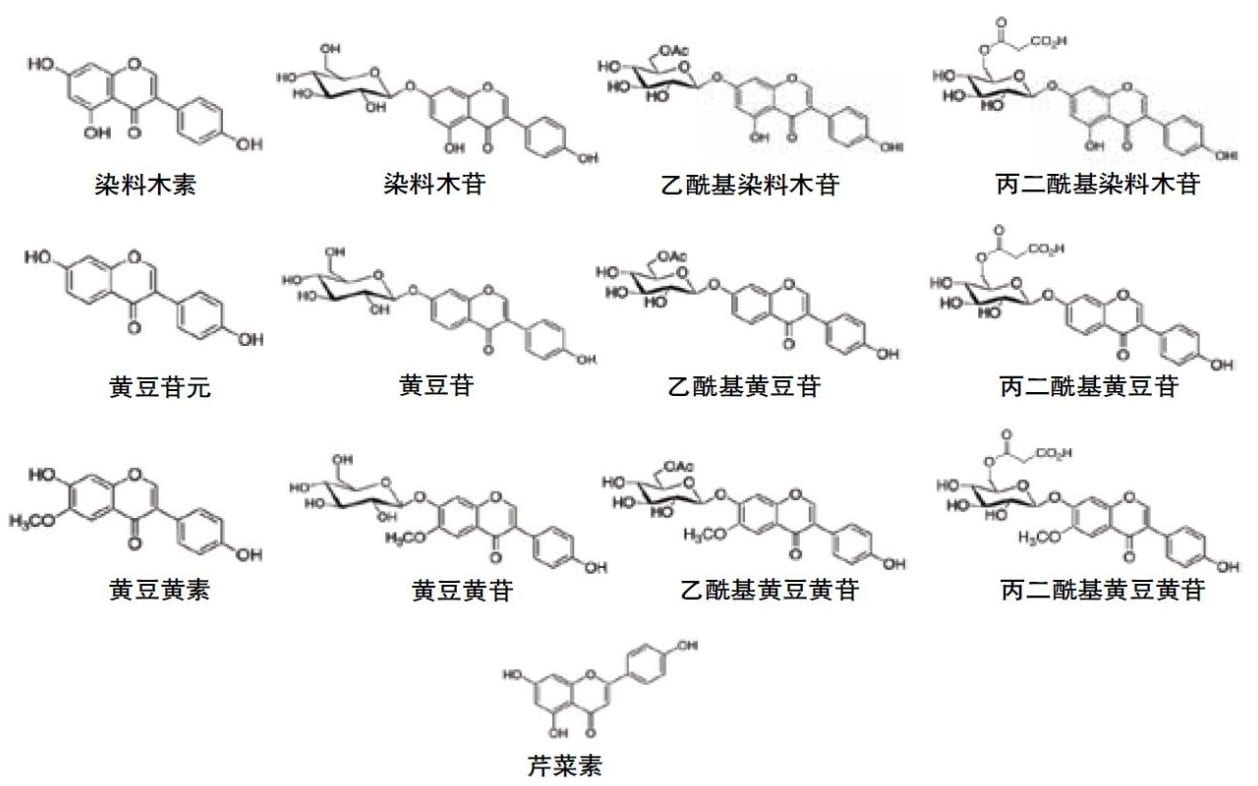
异黄酮主要存在于大豆(Glycine max)、红三叶草(Trifolium pretense)以及葛根(Pueraria lobata)的植物中。这些植物中发现的12种主要异黄酮为黄豆苷元、黄豆黄素、染料木素及其各自的葡萄糖苷以及丙二酰基和乙酰基葡萄糖苷衍生物。12种异黄酮以及内标芹菜素的结构如图1所示。这些类激素化合物通常作为补救措施用于减轻绝经期和绝经后症状。它们甚至还可降低亚洲的乳腺癌发病率,并减缓阿尔茨海默病的进展。
USP1和AOAC2等机构已建立分析膳食补充剂中异黄酮的标准方法。这些方法采用配备C18色谱柱以及紫外和可见光(UV-Vis)光谱的反相LC进行分离和定量。由于这些化合物具有结构相似性,因此这些方法的色谱运行时间通常会超过70 min。因此,十分有必要开发更快速的异黄酮分析方法。
本应用纪要介绍了USP方法到Waters ACQUITY Arc UHPLC系统的方法转换。采用ACQUITY Arc系统的分析时间仅为18 min,其中包括色谱柱清洗和平衡时间。使用Waters ACQUITY QDa质谱检测器可加快本研究所述的方法转换,同时也突出说明了质谱检测对谱峰鉴定和方法开发的优势。
样品前处理
标准品、黄豆苷、黄豆黄苷、染料木苷、黄豆苷元、黄豆黄素、染料木素以及芹菜素购自ChromaDex(加利福利亚州欧文)和INDOFINE Chemical(新泽西州希尔斯伯勒)。脱脂大豆粉RS购自美国药典公司(马里兰州罗克维尔)。NIST SRM 3238购自NIST(马里兰州盖瑟斯堡)。主要品牌的异黄酮膳食补充剂样品通过网上零售商店购得。
USP异黄酮方法中采用相同方式制备标准品溶液和样品溶液1。 使用乙腈水混合物(2/3,体积比)将样品溶液进一步稀释至满足校准范围的不同浓度。内标浓度始终保持为4 ppm不变。
|
UHPLC系统 |
ACQUITY Arc |
|
检测器 |
2998 PDA |
|
软件 |
Empower 3 |
|
色谱柱 |
CORTECS C18 2.7 μm, 3.0 x 100 mm |
|
柱温 |
30 °C |
|
流动相A |
0.1%甲酸的水溶液 |
|
流动相B |
0.1%甲酸的乙腈溶液 |
|
进样体积 |
2.0 μL |
|
流速 |
1.08 mL/min |
|
运行时间 |
18.0 min |
|
UV检测条件 |
260 nm |
|
UV分辨率 |
1.2 nm |
|
|
时间(min) |
流速(mL/min) |
%A |
曲线 |
|---|---|---|---|---|
|
1 |
初始 |
1.08 |
90 |
6 |
|
2 |
14.40 |
1.08 |
70 |
6 |
|
3 |
14.50 |
1.08 |
10 |
6 |
|
4 |
15.20 |
1.08 |
10 |
6 |
|
5 |
15.40 |
1.08 |
90 |
6 |
|
6 |
18.00 |
1.08 |
90 |
6 |
|
MS系统 |
ACQUITY QDa (Performance) |
|
电离模式 |
ESI+ |
|
毛细管电压 |
0.8 kV |
|
锥孔电压 |
15 V |
|
探头温度 |
600 °C |
|
SIR质量数 |
如下所示 |
将USP方法(异黄酮粉末提取物)1转换至配备CORTECS C18色谱柱(2.7 µm, 3 x 100 mm,部件号:186007372)的ACQUITY Arc UHPLC系统。CORTECS色谱柱的2.7μm填料为实心核颗粒,与同等粒径的全多孔颗粒色谱柱相比可提升分离效率并降低柱压。使用Waters ACQUITY UPLC色谱柱计算器将USP方法梯度洗脱程序转换为新的梯度洗脱程序3。将USP方法中的色谱柱参数(5 μm, 3.0×250 mm)、CORTECS C18色谱柱参数(2.7 μm, 3.0×100 mm)以及USP方法的74 min梯度洗脱程序输入色谱柱计算器,计算与USP方法等效的18 min梯度洗脱程序。流动相添加剂从0.05%磷酸变为0.1%甲酸,得到兼容MS的添加剂。
采用ACQUITY QDa质谱检测器的出厂默认仪器参数进行分析,未经任何修改。最初尝试了40°C的柱温,后优化为30°C以满足USP适应性标准中分离度的要求。图2所示为未加热和加热状态下USP脱脂大豆粉RS的色谱图,及使用ACQUITY QDa质谱检测器获得的分子量信息。利用质谱检测来鉴定谱峰。

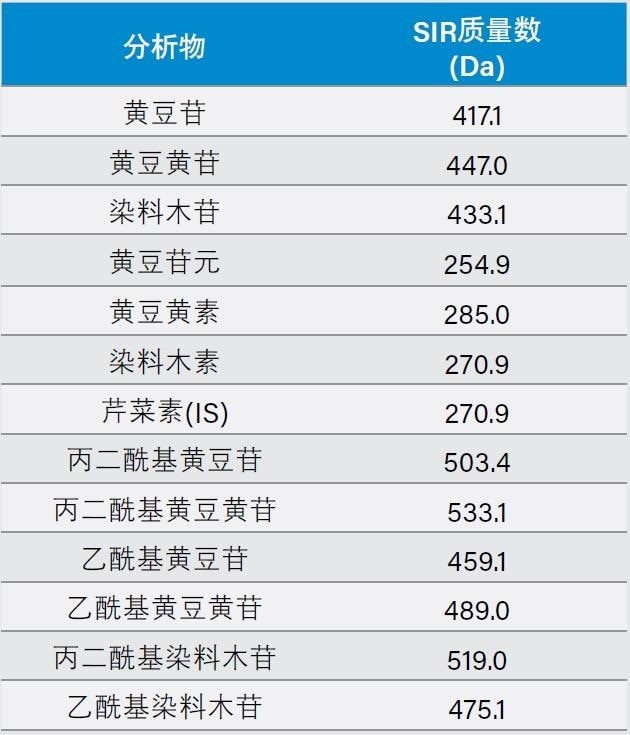
由于乙酰基和丙二酰基异黄酮标准品无法购买,因此USP标准中使用所述的参比标准品和分布匹配方法对这些化合物进行谱峰分配。对脱脂大豆(DFS)进行热处理可将丙二酰形式转化为乙酰形式。通过比较未加热DFS和加热DFS的色谱图及其参比色谱图,可为乙酰基和丙二酰基异黄酮分配峰ID。然而,这种分布匹配方法并不可靠,当色谱柱、流动相添加剂等LC条件或LC系统发生变化时更是如此。ACQUITY QDa可检出以单位质量分辨率(0.7 Da)在电喷雾电离(ESI)下形成的离子。表1列出了这些异黄酮的分子离子。利用质谱检测可选择性地检出这些化合物,并消除邻近洗脱化合物的所有可能干扰。
染料木素和芹菜素的质量数相同,但是它们的峰通过色谱法实现了良好分离(见图2)。添加质谱检测(ACQUITY QDa质谱检测器)后,无需借助单独标准品即可将峰ID明确匹配至正确的乙酰基和丙二酰基异黄酮。
ACQUITY QDa质谱检测器还可加快方法优化,因为我们可以借助每种化合物的选择性检测高度可靠地对所有化合物的保留时间(RT)变化进行同时监测。此举极大减少了方法优化中的进样次数。关于QDa质谱检测器如何有利于方法转换的更多详细信息将在单独的应用纪要中进行讨论4。
表2所示为标准品的UV校准结果。芹菜素用作所有化合物的校准和定量内标。所有化合物的相对响应(峰面积比)和溶液中标准品浓度(ppm)之间相关系数(R2)的平方均大于0.999。所有化合物的保留时间相对标准偏差均小于0.12%。
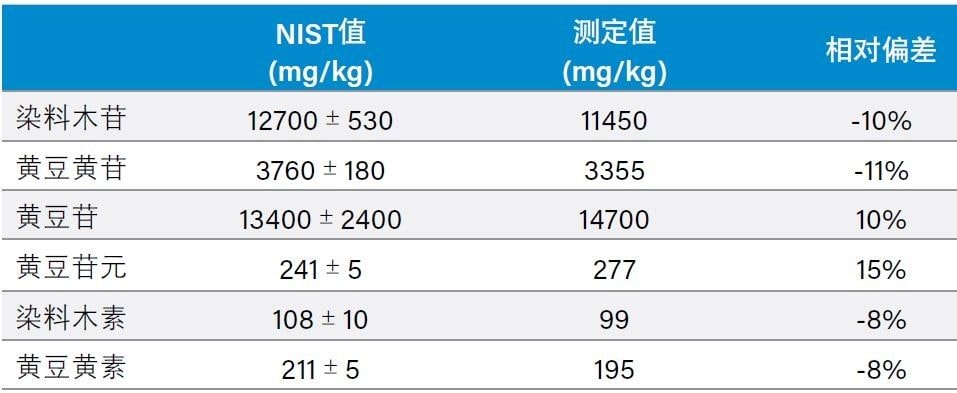
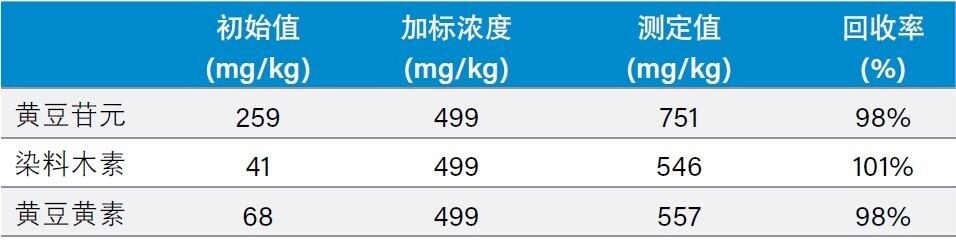
表3所示为NIST 3238 SRM的异黄酮结果及其与认证值和参比值的比较。获得的染料木苷、黄豆黄苷、黄豆苷、染料木素和黄豆黄素的相对偏差<11%。黄豆苷元的结果比NIST值大15%。文献检索发现,其它文献报道的黄豆苷元值同样较高5。 此外还通过加标实验评估了黄豆苷元、染料木素和黄豆黄素的精度(表4)。这些化合物的回收率为98%~101%。

通过上述快速18 min UHPLC-UV方法测定四种异黄酮膳食补充剂样品中的异黄酮含量。样品类型包括片剂、胶囊和大豆粉。数据处理遵循USP校准和定量方案1。
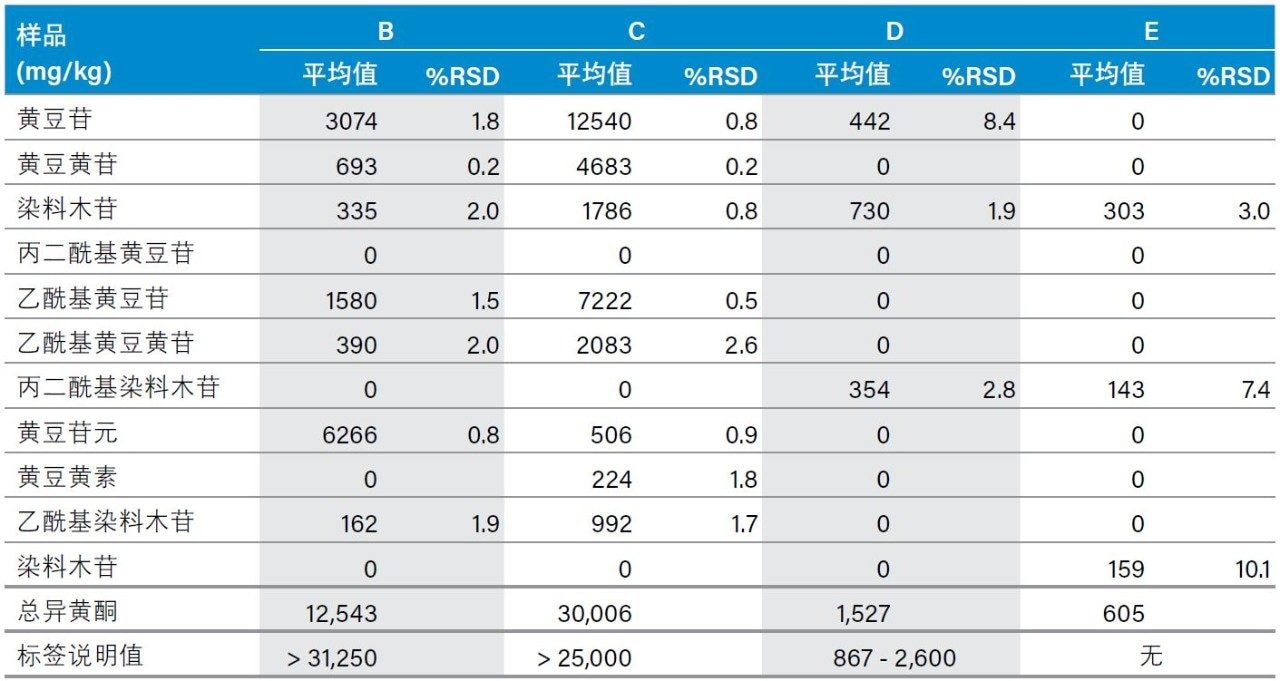
分析中使用的换算系数与USP HPLC-UV方法中规定的乙酰基和丙二酰基衍生物的系数相同。表5所示为单个异黄酮和总异黄酮的测定含量以及标签说明的总异黄酮含量。为便于比较,将标签说明值换算为浓度(mg/kg)。三份样品(C和D)中有两份的测定值与其标签说明值具有较高的一致性,而另一份样品(B)的总异黄酮测定含量比其标签说明值小得多。总异黄酮含量如此低的原因尚不明确。
异黄酮的USP方法可成功转换至配备2998 PDA检测器的ACQUITY Arc UHPLC系统。UHPLC系统上每次进样的总分析时间为18 min,与USP方法的74 min相比,分析时间显著缩短。这使分析通量增加了三倍,所用溶剂成本节省了75%。ACQUITY QDa质谱检测器具有出色的检测选择性,这是方法转换和开发,以及对未知物和潜在干扰风险较高的棘手样品中异黄酮分析的一大优势。三种膳食补充剂中异黄酮的分析表明两种样品的标签说明符合法规要求。在三份测试样品中发现其中一份样品的异黄酮含量较低,具体原因未知。
720005858ZH,2016年12月